文档内容
重难点 12 实验探究综合题
本题考查实验方案的设计与分析,清楚原理是解答的关键,注意对题目信息的应用,是对学生实验综合能
力的考查。在高考中,化学实验所占分值较高,主要考查化学实验基础知识、涉及物质的分离提纯、仪器
的使用基本操作、、产率计算等实验数据分析和处理、实验方案的设计、完善与评价等。从近几年高考试
题的命题趋势来看,题目的难度先增加,又有所下降,预计2024年总体难度会保持稳定。
一、实验综合题注意的问题与易错点
1.掌握定量测定实验题的解题思路
常见的定量测定实验包括混合物成分的测定、物质纯度的测定等。该类试题常涉及物质的称量、物质的分
离与提纯、中和滴定等实验操作。实验过程中要特别注意以下几个问题:
(1)气体体积的测定是考查的重点,对于气体体积的测量,读数时要特别注意消除“压强差”,保持液
面相平,还要注意视线与液面最低处相平。
(2)测定实验中还要注意消除干扰气体的影响,如可利用“惰性”气体将装置中的干扰气体排出。
(3)要使被测量气体全部被测量,反应结束后可继续向装置中通入“惰性”气体以使被测量气体全部被
吸收剂吸收。
(4)许多实验中的数据处理,都是对多次测定的结果求取平均值,但对于“离群”数据(指与其他测定数
据有很大差异的数据)要舍弃。
2. 记住物质制备实验操作中应注意的四个问题
(1)实验操作顺序。如与气体有关实验的操作为:装置选择与连接→气密性检验→装固体药品→加液体
药品→开始实验(按程序)→拆卸仪器→其他处理等。
(2)加热操作的要求。主体实验加热前一般应先用原料气赶走空气后,再点燃酒精灯,其目的一是防止
爆炸,如H 还原CuO、CO还原Fe O ;二是保证产品纯度,如制备MgN 、CuCl 等。反应结束时,应先
2 2 3 3 2 2
熄灭酒精灯,继续通原料气直到冷却为止。
(3)尾气处理方法。有毒气体常采用溶液(或固体)吸收或将之点燃,无毒气体直接排放。
(4)特殊的实验装置。(1)制取在空气中易吸水、潮解以及易水解的物质(如Al S 、AlCl 、MgN 等)及
2 3 3 3 2
易受潮的物质时,往往在装置末端再接一个干燥装置,以防止空气中水蒸气进入。(2)用碱石灰吸收测
定实验中生成CO 的质量时,前面要干燥,末端要防止空气中的水蒸气和CO 进入。
2 2
3.避免气体制备中的常见易错点
(1)制备气体时误认为先加药品后检查装置的气密性,为了避免浪费,应该先检查装置气密性后加药品。
(2)无水氯化钙是中性干燥剂,误认为可以干燥任何气体,其实CaCl 不能干燥氨气。
2
(3)实验室里用大理石和稀盐酸反应制取CO,而不能用大理石和稀硫酸反应制取。
2(4)实验室里用MnO 和浓盐酸加热制取Cl,错误认为MnO 和稀盐酸加热也能发生反应。
2 2 2
(5)SO 具有还原性,浓HSO 具有强氧化性,错误认为SO 不能用浓硫酸干燥,其实不然。
2 2 4 2
(6)误认为倒扣的漏斗一定能防止倒吸。如图装置不能防倒吸。
4.避免物质制备和实验设计中的易错点
净化、吸收气体及熄灭酒精灯时要防止液体倒吸。 进行某些易燃易爆实验时要防爆炸(如H 还原CuO应
2
先通H ,气体点燃前先验纯等);防氧化(如H 还原CuO后要“先灭灯再停氢”,白磷切割宜在水中进行
2 2
等)。防吸水(实验取用和制取易吸水、潮解、水解的物质宜采取必要措施,以保证达到实验目的。如
NaOH固体应放在烧杯等玻璃器皿中称量);冷凝回流:有些反应中,为减少易挥发液体反应物的损耗和充
分利用原料,需在反应装置上加装冷凝回流装置(如长玻璃管、冷凝管等);易挥发液体产物(导出时可为蒸
气)的及时冷却。
仪器拆卸的科学性与安全性(也从防污染、防氧化、防倒吸、防爆炸、防泄漏等角度考虑)。其他,如实验
操作顺序,试剂加入顺序等。
二、实验规范语言表述
1.性质实验设计
从实验原理出发(含性质),按操作过程(或方法)、实验现象、实验结论顺序来表述答案
液体:取少量液体试剂于试管中→滴入某某试剂→描述现象→得出结论
固体: 取少量固体试剂于试管中,加水 ( 酸或某溶液 ) 配成溶液 ( 说成溶解也行 )→滴入某某试剂→描述现象→
得出结论。
气体:将气体通入某某溶液中→描述现象→得出结论
(1)水蒸气最先检验;
(2)有干扰的气体先检验:例如,气体甲对气体乙检验有干扰,检验思路:检验气体甲→除去气体甲→确定
气体甲除尽(比如SO 和CO 混合、CO和CO 混合)→检验气体乙。
2 2 2
核心思想是不能有干扰物质的出现,出现即除之。
2.定量实验误差分析
对于定量实验,要采用措施减小误差。减小误差从以下角度考虑:
(1)装置气密性良好;(2)排除装置中原有干扰气体;(3)减少副反应;(4)避免气体带杂质(如测定水的质量,
气体必须干燥);(5)防止空气中二氧化碳和水进入装置等。(6)反应后需要赶气,将需要吸收的气体赶至吸
收装置吸收。
燃烧法定量测定实验一般设计思路:气体发生装置→气体干燥装置→主反应装置→吸收产物(1)→吸收产物
(2)→干燥装置→尾气处理装置。
所有习题中实验题的不足之处:未防倒吸、未处理尾气、未处理残留在装置中的有毒气体、未将装置中残
留气体赶至某装置中吸收 ( 定量分析 ) 等 。所有习题中含有冰水浴或液态氮气或冰盐水等低温物质的装置:冷凝收集易挥发的液态产物或易升华的固
体产物或作为需要低温发生的反应装置(故反应方程式是有必要落实的)。
所有习题中含有热水浴或直接加热等非低温物质的装置:使液体挥发为液体、制取水蒸气(乙醇气发生催化
氧化)等。
所有习题中已知信息的运用:遇到易水解物质(前防水后防水,比如金属氢化物CaH、SiCl 、SiHCl 、金
2 4 3
属氮化物MgN、Ca N、某某其它物质)、遇到给熔沸点的物质(创造低温环境冷凝收集或蒸馏分离提纯),
3 2 3 2
已知信息必考。
温度计的位置:a、蒸馏时,水银球与支管口处相平 b、反应液以下(比如乙醇的消去反应)
c、水浴温度,温度计放置在反应装置外。
玻璃液封管的作用:吸收残留的或剩余的尾气
3.某试剂的作用:得分点及关键词:
(1)作用类:“除去”、“防止”、“抑制”、“使……”等,回答要准确。
(2)作用—目的类:作用+目的
“作用”是“……”,“目的”是“……”。
如调节容液的pH:
①目的: 使溶液中的……金属阳离子形成氢氧化物完全沉淀下来而除去
②需要的物质: 含主要阳离子的难溶性氧化物或氢氧化物或碳酸盐,即能与 H + 反应,是 H 增大的物质 如
P
用MgO、Mg(OH) 等等。
2
③原理: 加入的物质能与溶液中的 H + 反应,降低了 H + 的浓度,增大 pH ,促使某某水解沉淀 。
④pH控制的范围:大于除去离子的完全沉淀值,小于主要离子的开始沉淀的pH
如作氧化剂或还原剂:HO:氧化剂、还原剂、复分解类型(制备过氧化钡等提供过氧键而已)
2 2
还原性试剂:除去(反应)氧化性物质 玻璃纤维:固定固体,防止粉末被气流带走
玻璃液封管的作用:吸收残留的或剩余的尾气
4.原因、理由类
“有理”——化学原理,“有据”——事实依据,可采取以下两种方式:
(1)“正说”——“直接原因+根本目的” (2)“反说”——“如果……就……”
某反应温度不高于××℃(或在某个反应温度范围内、或在此温度下转化率最大等)的原因:(1)(低温速率较
慢)适当加快反应速率;(2)若有催化剂则考虑催化剂的催化活性;(3)但温度过高会造成反应物(如浓硝酸)挥
发或分解(如HO、NH HCO 、NH HO等);还要考虑温度过高,平衡移动的问题。(4)成本问题。某条件
2 2 4 3 3 2
下,转化率已经很高,若再改变条件,转化率提高不大,生产成本增加,得不偿失。
5.理论型简答题
……存在……(书写可逆反应)平衡,……(条件)使平衡向……(方向)移动,……(结论)比如为何电
解时,阴极的碱性增大了,从平衡移动角度解析:溶液中存在 平衡,氢离子阴极放电,
氢离子浓度降低,促使平衡向右移动,氢氧根浓度增大,故碱性增强。
6.沉淀的洗涤与洗涤是否干净实验操作简答题
(1)沉淀洗涤的目的:除去沉淀表面附着或沉淀中包夹的可溶性离子。
(2)洗涤方法:向漏斗内加 …… ( 蒸馏水 ) 至浸没沉淀,待水自然流出后,重复操作2~3次。(3)①凡是涉及冰水(或冷水)洗涤的目的:洗去晶体表面的杂质离子并降低被洗涤物质的溶解度,减少其在
洗涤过程中的溶解损耗,最终提高产品产率。
②若用特殊溶剂洗涤,例如乙醇(丙酮)洗涤的目的: a 、 降低被洗涤物质的溶解度,减少其在洗涤过程中的
溶解损耗 ; b 、除去固体表面吸附的杂质; c 、乙醇挥发带出水分,使固体易干燥 。
再如用沉淀的饱和溶液洗涤:减小沉淀的溶解。
③乙酸乙酯制备中精除杂时饱和碳酸钠溶液的作用:a、溶解乙醇;b、反应乙酸;c、减小乙酸乙酯在水中
的溶解度。
(4)误差分析:若沉淀不洗涤或洗涤不干净,则使沉淀的质量偏高。若沉淀洗涤次数过多,则会使部分沉淀
溶解而使其质量偏低。
(5)沉淀剂是否过量的判断方法
答题模板
(1)加沉淀剂:静置,向上层清液中继续滴加少量沉淀剂,若无沉淀产生,则证明沉淀剂已过量。
(2)加入与沉淀剂反应的试剂:静置,取适量上层清液于另一洁净试管中,向其中加入少量与沉淀剂作用产
生沉淀的试剂,若产生沉淀,证明沉淀剂已过量 。
注意:若需称量沉淀的质量而进行有关定量计算时则只能选用方法(1)。
(6)判断沉淀是否洗净的操作
取最后一次洗涤液,滴加……(试剂),若没有……现象,证明沉淀已洗净(一般是现象明显的优先检验
比如Fe3+、Cl-、SO 2-等)
4
1. (2023江苏卷)实验室模拟“镁法工业烟气脱硫”并制备 ,其实验过程可表示为
(1)在搅拌下向氧化镁浆料中匀速缓慢通入 气体,生成 ,反应为
,其平衡常数K与 、 、
、 的代数关系式为 ___________;下列实验操作一定能提高氧化镁浆料吸
收 效率的有___________(填序号)。
A.水浴加热氧化镁浆料
B.加快搅拌速率
C.降低通入 气体的速率
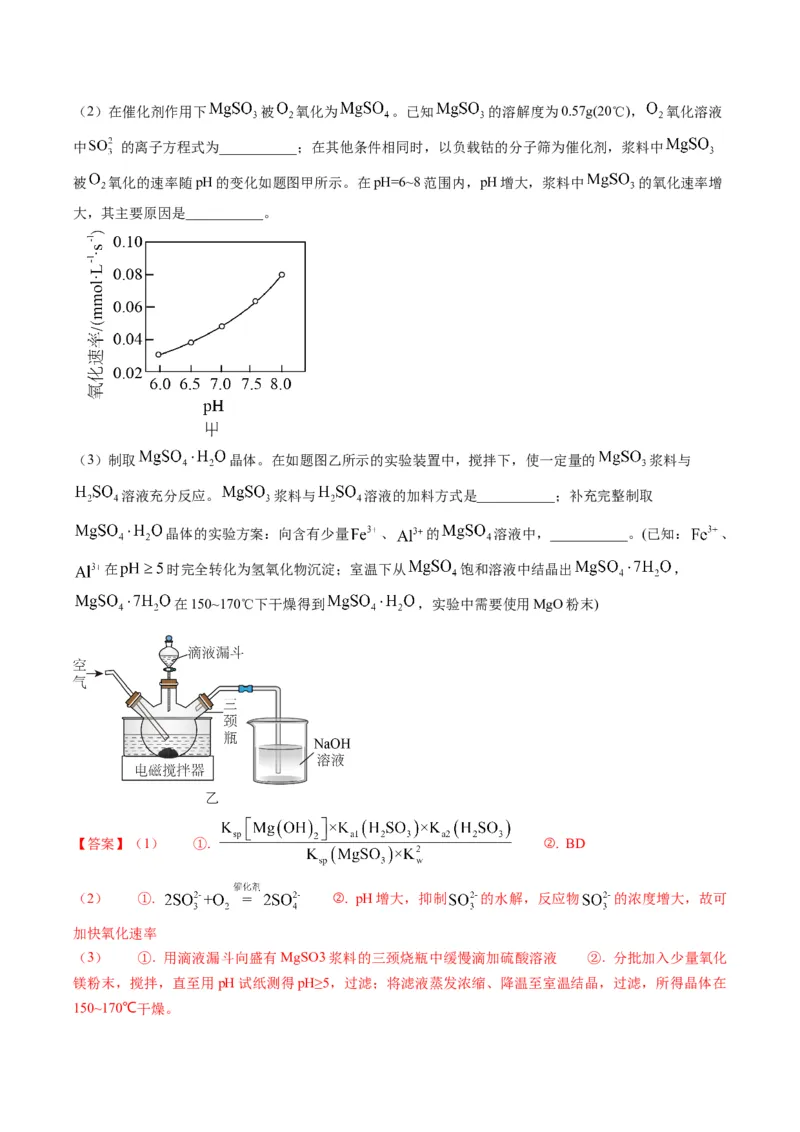
D.通过多孔球泡向氧化镁浆料中通(2)在催化剂作用下 被 氧化为 。已知 的溶解度为0.57g(20℃), 氧化溶液
中 的离子方程式为___________;在其他条件相同时,以负载钴的分子筛为催化剂,浆料中
被 氧化的速率随pH的变化如题图甲所示。在pH=6~8范围内,pH增大,浆料中 的氧化速率增
大,其主要原因是___________。
(3)制取 晶体。在如题图乙所示的实验装置中,搅拌下,使一定量的 浆料与
溶液充分反应。 浆料与 溶液的加料方式是___________;补充完整制取
晶体的实验方案:向含有少量 、 的 溶液中,___________。(已知: 、
在 时完全转化为氢氧化物沉淀;室温下从 饱和溶液中结晶出 ,
在150~170℃下干燥得到 ,实验中需要使用MgO粉末)
【答案】(1) ①. ②. BD
(2) ①. ②. pH增大,抑制 的水解,反应物 的浓度增大,故可
加快氧化速率
(3) ①. 用滴液漏斗向盛有MgSO3浆料的三颈烧瓶中缓慢滴加硫酸溶液 ②. 分批加入少量氧化
镁粉末,搅拌,直至用pH试纸测得pH≥5,过滤;将滤液蒸发浓缩、降温至室温结晶,过滤,所得晶体在
150~170℃干燥。【解析】本实验的目的是为了制取 ,首先在搅拌下向氧化镁浆料中匀速缓慢通入 气体,
生成 ,然后使一定量的 浆料与 溶液充分反应生成硫酸镁,在硫酸镁的溶液中加入
氧化镁调节溶液的 pH除去三价铁和三价铝,将滤液蒸发浓缩、降温至室温结晶,过滤,所得晶体在
150~170℃干燥即可得到 ;
(1)已知下列反应:
① K
②
③
④
⑤
⑥
根据盖斯定律,①=②-③+④+⑤-⑥ ,故K= ;
A.加热可加快反应速率,但温度升高,SO 在水中溶解度降低,且会导致HSO 受热分解,不一定能提高
2 2 3
吸收SO 效率,A错误;
2
B.加快搅拌速率,可以使反应物充分接触,提高吸收SO 效率,B正确;
2
C.降低通入SO 气体的速率,SO 可与MgO浆料充分接触,但会降低反应速率,不一定能提高吸收SO
2 2 2
效率,C错误;
D.多孔球泡可以让SO 与MgO浆料充分接触,能提高吸收SO 效率,D正确;
2 2
故选BD。
(2)根据题意,O 氧化溶液中的 , 被氧化为 ,1molO 氧化2mol ,故 氧化溶液中
2 2
的离子方程式为: ;
pH增大,抑制 的水解,反应物 的浓度增大,故可加快氧化速率;
(3)在进行含固体物质的反应物与液体反应的实验时,应将含固体物质的反应物放在三颈瓶中,通过滴
液漏斗滴加液体,HSO 溶液的滴加速率要慢,以免HSO 过量;
2 4 2 4
根据题意,首先需要调节pH≥5以除去Fe3+、Al3+杂质,需要用到的试剂为MgO粉末,操作细节为分批加
入少量MgO粉末,以免pH过高,不断搅拌进行反应直至检测到pH≥5,然后过滤除去氢氧化铁、氢氧化
铝沉淀;接着需要从溶液中得到 ,根据题目信息,室温下结晶只能得到 ,
因此需要在150~170℃下干燥得到 ,操作细节为将滤液蒸发浓缩、降温至室温结晶,过滤,
所得晶体在150~170℃干燥。2.(2022年江苏卷)实验室以二氧化铈( )废渣为原料制备 含量少的 ,其部分实验过
程如下:
(1)“酸浸”时 与 反应生成 并放出 ,该反应的离子方程式为_______。
(2)pH约为7的 溶液与 溶液反应可生成 沉淀,该沉淀中 含量与加料方
式有关。得到含 量较少的 的加料方式为_______(填序号)。
A.将 溶液滴加到 溶液中 B.将 溶液滴加到 溶液中
(3)通过中和、萃取、反萃取、沉淀等过程,可制备 含量少的 。已知 能被有机萃取
剂(简称HA)萃取,其萃取原理可表示为
(水层)+3HA(有机层) (有机层)+ (水层)
①加氨水“中和”去除过量盐酸,使溶液接近中性。去除过量盐酸的目的是_______。
②反萃取的目的是将有机层 转移到水层。使 尽可能多地发生上述转移,应选择的实验条件或采
取的实验操作有_______(填两项)。
③与“反萃取”得到的水溶液比较,过滤 溶液的滤液中,物质的量减小的离子有_______(填化学
式)。
(4)实验中需要测定溶液中 的含量。已知水溶液中 可用准确浓度的 溶液滴
定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为
。请补充完整实验方案:①准确量取 溶液[ 约为
],加氧化剂将 完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到
容量瓶中后定容;②按规定操作分别将 和待测 溶液装入
如图所示的滴定管中:③_______。【答案】(1)2CeO+H O+6H+=2Ce3++O ↑+4H O
2 2 2 2 2
(2)B (3) ①. 减少氢离子,使萃取的过程右移,促进Ce3+被萃取
②. 酸性条件,多次萃取 ③.
(4)从左侧滴定管中放出一定体积的待测 溶液,加入指示剂苯代邻氨基苯甲酸,用
来滴定,当滴入最后半滴标准液时,溶液由紫红色变为亮黄色,即达
到滴定终点,记录标准液的体积
【解析】
【分析】首先用稀盐酸和过氧化氢溶液酸浸二氧化铈废渣,得到三价铈,加入氨水调节pH后用萃取剂萃
取其中的三价铈,增大三价铈浓度,之后加入稀硝酸反萃取其中的三价铈,再加入氨水和碳酸氢铵制备产
物,以此解题。
(1)根据信息反应物为 与 ,产物为 和 ,根据电荷守恒和元素守恒可知其离子方程式
为:2CeO+H O+6H+=2Ce3++O ↑+4H O;
2 2 2 2 2
(2)反应过程中保持 少量即可得到含 量较少的 ,故选B;
(3)①减少氢离子,使萃取的过程右移,促进Ce3+被萃取,故答案为:减少氢离子,使萃取的过程右移,
促进Ce3+被萃取;
②根据萃取原理可知,应选择的实验条件是酸性条件,为了使 尽可能多地发生上述转移,可以采用多
次萃取;
③“反萃取”得到的水溶液中含有浓度较大的 ,过滤后溶液中 离子浓度较小,故答案为: ;
(4)应该用标准液滴定待测 溶液,用苯代邻氨基苯甲酸作指示剂,故答案为:从左侧滴定管中放出
一定体积的待测 溶液,加入指示剂苯代邻氨基苯甲酸,用 来滴定,
当滴入最后半滴标准液时,溶液由紫红色变为亮黄色,即达到滴定终点,记录标准液的体积。
(建议用时:45分钟)
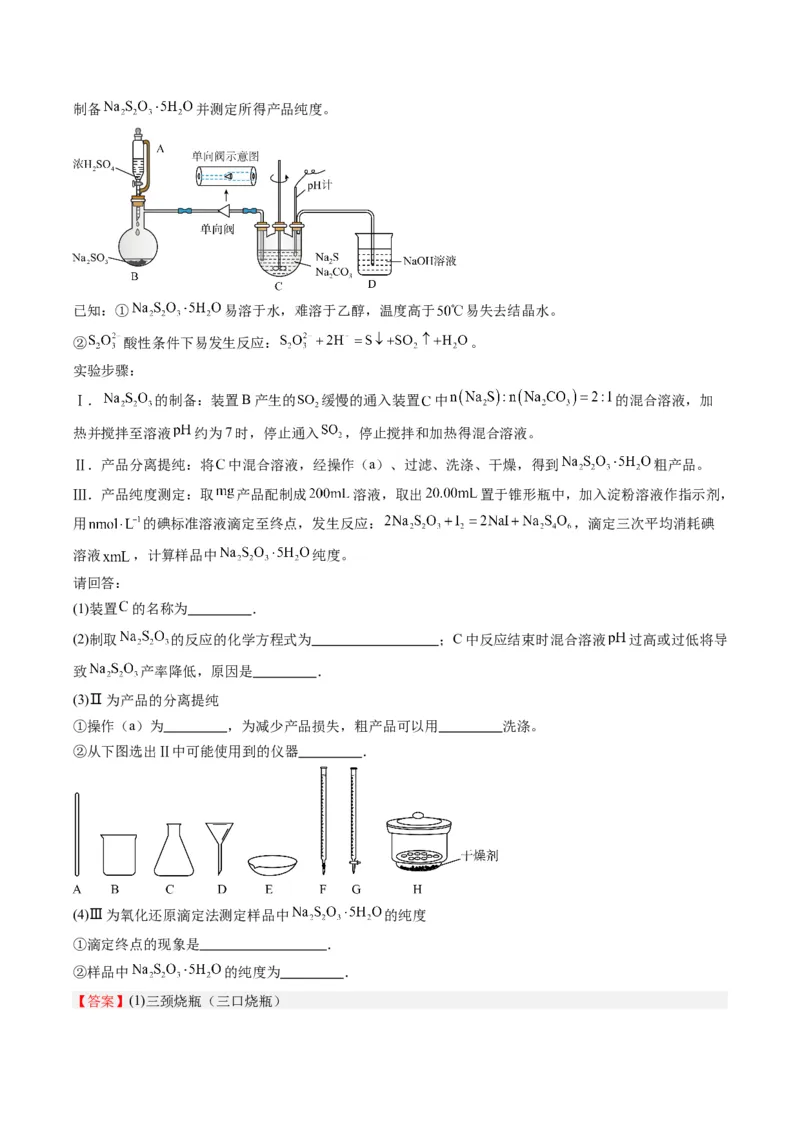
1.(2023·山东德州·德州市第一中学校联考模拟预测)实验室用 通入 和 的混合溶液中来制备 并测定所得产品纯度。
已知:① 易溶于水,难溶于乙醇,温度高于 易失去结晶水。
② 酸性条件下易发生反应: 。
实验步骤:
Ⅰ. 的制备:装置B产生的 缓慢的通入装置 中 的混合溶液,加
热并搅拌至溶液 约为7时,停止通入 ,停止搅拌和加热得混合溶液。
Ⅱ.产品分离提纯:将 中混合溶液,经操作(a)、过滤、洗涤、干燥,得到 粗产品。
Ⅲ.产品纯度测定:取 产品配制成 溶液,取出 置于锥形瓶中,加入淀粉溶液作指示剂,
用 的碘标准溶液滴定至终点,发生反应: ,滴定三次平均消耗碘
溶液 ,计算样品中 纯度。
请回答:
(1)装置 的名称为 .
(2)制取 的反应的化学方程式为 ;C中反应结束时混合溶液 过高或过低将导
致 产率降低,原因是 .
(3)Ⅱ为产品的分离提纯
①操作(a)为 ,为减少产品损失,粗产品可以用 洗涤。
②从下图选出Ⅱ中可能使用到的仪器 .
(4)Ⅲ为氧化还原滴定法测定样品中 的纯度
①滴定终点的现象是 .
②样品中 的纯度为 .
【答案】(1)三颈烧瓶(三口烧瓶)(2) 过高, 反应不充分; 过低,
导致 转化为 和
(3) 蒸发浓缩、冷却结晶 乙醇 ABDEH
(4) 滴入最后半滴碘标准溶液后溶液由无色变蓝色,且半分钟内不恢复原色
【分析】在装置B中浓硫酸与NaSO 反应制备SO ,经过单向阀通入三颈烧瓶内,在合适pH环境下,SO
2 3 2 2
与NaCO、NaS发生反应得到NaSO 混合液,再经分离、提纯得粗产品,用滴定实验测定其纯度。
2 3 2 2 2 3
【解析】(1)由图构造可知,装置C是三颈烧瓶;
(2)SO 具有氧化性,NaS具有还原性,在NaCO 溶液环境下发生氧化还原反应生成NaSO 和CO,其
2 2 2 3 2 2 3 2
化学方程式为:4SO +Na CO+2Na S=3Na SO+CO ,C中反应结束时混合溶液pH过高导致NaCO、NaS
2 2 3 2 2 2 3 2 2 3 2
反应不充分;pH过低,导致NaSO 转化为S和SO ;
2 2 3 2
(3)①从C中反应后混合溶液中提纯 的操作为:蒸发浓缩、冷却结晶、过滤、洗涤、干燥;
由于 难溶于乙醇,所以可以用乙醇洗涤粗产品;
②蒸发浓缩、冷却结晶需要AE,过滤和洗涤需要ABD,干燥需要H,所以Ⅱ中可能使用到的仪器为:
ABDEH;
(4)①淀粉作指示剂,遇碘变蓝色,所以滴定终点的现象是最后一滴碘标准溶液滴入后,溶液由无色变
成蓝色,且半分钟内不恢复原色;
②20.00mL粗产品溶液中含 ,所以样品中
的纯度为: 。
2.(2023上·安徽·高三校联考期中)绿矾( )可作还原剂、着色剂、制药等,在不同温度下分
解得各种铁的氧化物和硫的氧化物。
(1)甲组同学按照上图所示的装置,通过实验检验绿矾的分解产物。装置B中可观察到的现象是 ,甲
组由此得出绿矾的分解产物中含有 。
(2)乙组同学查阅资料发现绿矾受热分解还可能有 放出,为此,丙组同学选用甲组同学的A装置和下图
部分装置设计出了一套检验绿矾分解气态产物的装置(试剂均足量):①乙组同学的实验装置中,依次连接的合理顺序为 。
②E中HCl的作用是 。
③反应结束,观察到A中固体变为红棕色,F由蓝色变粉红色,E、G中均有白色沉淀,将H中的试管从
水槽取出, (填实验操作和现象)证明绿矾分解产物中有 。
(3)将E、G混合物抽滤、洗涤、干燥、称重,发现固体质量之比1∶3.抽滤装置如下图,下列关于抽滤洗涤
的操作正确的是 。
a.抽滤时,先打开水龙头,再将固液混合物转移至布氏漏斗
b.洗涤时,先关闭水龙头,向布氏漏斗中加蒸馏水至淹没沉淀,再打开水龙头
c.洗涤结束后,先将抽滤瓶上的橡胶管取下,再关闭水龙头
(4)取A中少量反应后固体于试管中,先加 (填化学式,下同)溶解,再将溶液分成两份,一份加入
KSCN溶液,另一份加入 ,第一份溶液变红,第二份溶液无明显现象。
(5)综上实验,绿矾分解的化学方程式为 。
【答案】(1)品红褪色
(2) AFEGH 抑制 的溶解 将带火星的木条伸入试管,木条复燃
(3)ac
(4) HCl(或 ) ( 、 也给分)
(5)
【分析】该实验主要目的是检验绿矾分解的产物,使用品红溶液检验 ,含氯化钴的硅胶干燥剂检验水,
盐酸酸化的氯化钡溶液检验 ,将最终得到的铁的氧化物用酸溶解后,用KSCN溶液检验 ,最终得
出绿矾分解的化学方程式。
【解析】(1)甲组由此得出绿矾的分解产物中含有 ,装置B为品红,二氧化硫有漂白性,故装置B
中褪色;
(2)①检验绿矾分解气态产物,由A分解绿矾,D为氢氧化钠溶液,作用应为吸收酸性气体;E为HCl、
的浓溶液,目的为吸收并检验气体中的 ;F为含氯化钴的硅胶干燥剂,遇水变色,目的为检验产
物中的水;G为 、 的浓溶液,目的为吸收并检验气体中的 ,H为收集氧气的装置;整个过程应该先检验水,再检验 ,再检验 ,最终收集并检验 ,由于各装置试剂均为浓溶液,兼具检验
和吸收作用,所以不需要氢氧化钠溶液去吸收酸性气体,故答案为AFEGH;
②E为HCl、 的浓溶液,目的为吸收并检验气体中的 , 也是沉淀,但能溶于盐酸,加HCl
的作用是排除 的干扰,抑制 的溶解;
③氧气收集在H中,利用氧气支持燃烧的特性,检验方法为:将H中的试管从水槽取出,将带火星的木条
伸入试管,木条复燃,证明绿矾分解产物中有 。
(3)a.抽滤时,应先打开水龙头,产生压强差,再将固液混合物转移至布氏漏斗,a正确;
b.洗涤时,应持续打开水龙头,向布氏漏斗中加蒸馏水至淹没沉淀,b错误
c.洗涤结束后,先将抽滤瓶上的橡胶管取下,再关闭水龙头,防止倒吸,c正确;
故选ac。
(4)取A中少量反应后固体于试管中,应先加酸溶解,使铁元素转化为离子,便于检验,一份加入
KSCN溶液检验 ,另一份检验 ,可用 、酸性高锰酸钾溶液等。
(5)综上实验现象,绿矾分解产生二氧化硫、三氧化硫、氧气、三氧化二铁和水,所以绿矾分解的化学
方程式为: 。
3.(2023·河南新乡·统考一模)磷酸亚铁 是生产锂电池的原料,能溶于强酸,不溶于
水。实验室可以绿矾 及 为原料制备磷酸亚铁,主要反应
为 。
I.配制 溶液
(1)实验室常用绿矾配制 溶液,配制过程中需要用到的玻璃仪器除烧杯、量筒、容量瓶外,还有
。若实验需要配制。 的 溶液,则需要称取的绿矾的质量为 g。
Ⅱ.提纯制备晶体
(2)利用工业品十二水合磷酸氢二钠(含 、重金属盐及有色杂质等)提纯得到
晶体。已知: 溶液 在 ,重金属硫化物不溶于水。请将实验步骤补充
完整:
将工业品溶于热水;
① ;
② ;
③ ;
冷却结晶,过滤、洗涤及干燥。
(实验中可选用的试剂: 溶液、 溶液、 溶液、活性炭)
Ⅲ.合成磷酸亚铁及杂质的检验(3)在三颈烧瓶中先加入抗坏血酸(维生素C)稀溶液作底液,然后向烧瓶中滴入 与 的混
合溶液至 时,再滴入 溶液,最终维持 。
①用抗坏血酸稀溶液作底液的作用是 。
②检验产品中是否混有 或 杂质的操作方法是 。
【答案】(1) 玻璃棒、胶头滴管 6.95
(2) 逐滴滴入NaS溶液,至不再生成沉淀为止 用0.1mol⋅L-1HPO 和0.1mol ⋅L-1NaOH溶液调节
2 3 4
溶液pH至8.2~8.4 加入活性炭煮沸,趁热过滤
(3) 防止亚铁离子被氧化 取少量产品溶于适量盐酸中,向其中滴加几滴KSCN溶液,若溶液变为
血红色,说明含有Fe(OH) 或FePO 杂质,反之不含。
3 4
【分析】实验室可以用绿矾(FeSO ⋅7HO)、NaHPO ⋅12HO及CHCOONa⋅3H O为原料制备磷酸亚铁,
4 2 2 4 2 3 2
先配制FeSO 溶液,再提纯NaHPO ⋅12HO晶体,最后合成磷酸亚铁并进行杂质的检验,据此分析解答。
4 2 4 2
【解析】(1)实验室配制FeSO 溶液过程中需要用到的玻璃仪器除烧杯、量筒、容量瓶外,还有玻璃棒、
4
胶头滴管;若实验需要配制250mL 0.1mol⋅L-1的FeSO 溶液,则需要称取的绿矾(FeSO ⋅7HO)的质量为
4 4 2
。
(2)将工业品溶于热水;①逐滴滴入NaS溶液,至不再生成沉淀为止,重金属硫化物不溶于水,用过量
2
NaS溶液除去重金属离子;②NaHPO 溶液pH为8.2~8.4,因此用0.1mol⋅L-1HPO 和0.1mol ⋅L-1NaOH溶
2 2 4 3 4
液调节溶液pH至8.2~8.4;③加入活性炭煮沸,趁热过滤,目的是除去有色杂质;最后冷却结晶,过滤、
洗涤及干燥可得较纯的NaHPO ⋅12HO晶体;故答案为:①逐滴滴入NaS溶液,至不再生成沉淀为止;
2 4 2 2
②用0.1mol⋅L-1HPO 和0.1mol ⋅L-1NaOH溶液调节溶液pH至8.2~8.4;③加入活性炭煮沸,趁热过滤。
3 4
(3)①抗坏血酸(维生素C)具有较强的还原性,可防止亚铁离子被氧化,故答案为:防止亚铁离子被氧化;
②检验产品中是否混有Fe(OH) 或FePO 杂质,只需检验产品中是否含Fe3+即可,其操作方法是:取少量产
3 4
品溶于适量盐酸中,向其中滴加几滴KSCN溶液,若溶液变为血红色,说明含有Fe(OH) 或FePO 杂质,
3 4
反之不含。
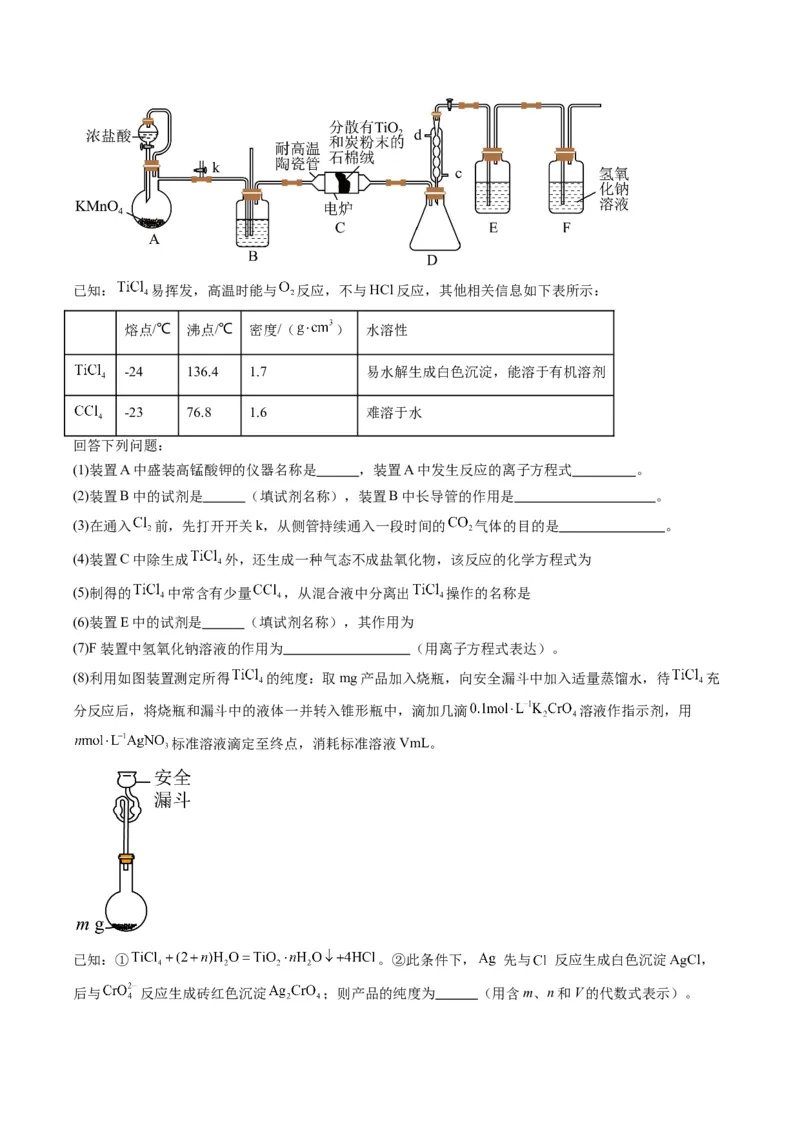
4.(2023上·天津·高三天津市第四十七中学校考) 是制备金属钛的重要中间体。某小组同学利用如
下装置在实验室制备 (夹持装置略去)。已知: 易挥发,高温时能与 反应,不与HCl反应,其他相关信息如下表所示:
熔点/℃ 沸点/℃ 密度/( ) 水溶性
-24 136.4 1.7 易水解生成白色沉淀,能溶于有机溶剂
-23 76.8 1.6 难溶于水
回答下列问题:
(1)装置A中盛装高锰酸钾的仪器名称是 ,装置A中发生反应的离子方程式 。
(2)装置B中的试剂是 (填试剂名称),装置B中长导管的作用是 。
(3)在通入 前,先打开开关k,从侧管持续通入一段时间的 气体的目的是 。
(4)装置C中除生成 外,还生成一种气态不成盐氧化物,该反应的化学方程式为
(5)制得的 中常含有少量 ,从混合液中分离出 操作的名称是
(6)装置E中的试剂是 (填试剂名称),其作用为
(7)F装置中氢氧化钠溶液的作用为 (用离子方程式表达)。
(8)利用如图装置测定所得 的纯度:取mg产品加入烧瓶,向安全漏斗中加入适量蒸馏水,待 充
分反应后,将烧瓶和漏斗中的液体一并转入锥形瓶中,滴加几滴 溶液作指示剂,用
标准溶液滴定至终点,消耗标准溶液VmL。
已知:① 。②此条件下, 先与 反应生成白色沉淀AgCl,
后与 反应生成砖红色沉淀 ;则产品的纯度为 (用含m、n和V的代数式表示)。【答案】(1) 蒸馏烧瓶
(2) 浓硫酸 平衡气压,防止堵塞和倒吸
(3)排除装置中的空气,防止 和 反应
(4)
(5)蒸馏
(6) 浓硫酸 防止F中的水蒸气进入D装置中使 水解
(7)
(8)
【分析】本题利用氯气与Ti反应制备TiCl 。A为制备氯气的装置,C、D分别为制备、收集四氯化钛的装
4
置,因四氯化钛易水解,要求制备和收集过程无水,故在C前、D后都要加干燥装置,所以B、E中盛放
试剂为浓硫酸;F中盛放溶液氢氧化钠溶液,目的是除去未反应的氯气。
【解析】(1)根据装置图可知,A装置中盛装高锰酸钾的仪器是蒸馏烧瓶。制备氯气的离子方程式是:
;
(2)制备的氯气需要干燥再通入C中反应,B中应装浓硫酸,装置B中长导管的作用是平衡气压,防止
堵塞和倒吸;
(3)四氯化钛高温时能与O 反应,在通入Cl 前,从侧管持续通入一段时间的CO 的目的是排除装置中的
2 2 2
空气,防止TiCl 和O 反应;
4 2
(4)这种气态不成盐氧化物是CO,反应的化学方程式为: ;
(5)TiCl 和CCl 互溶,但沸点差异比较大,故从混合液体分离出TiCl 的操作为蒸馏;
4 4 4
(6)四氯化钛易水解,E装置中的试剂是浓硫酸,防止F中的水蒸气进入D装置中,使TiCl 水解;
4
(7)F中盛放溶液氢氧化钠溶液,目的是除去未反应的氯气: ;
(8)由方程式可得关系式TiCl ~HCl~AgNO ,n(TiCl )= mol,TiCl 的纯度为
4 3 4 4
= 。
5.(2023上·河北张家口·高三河北省尚义县第一中学校联考)某化学学习小组经查阅资料发现:
为紫色固体,微溶于 溶液,具有强氧化性,在酸性或中性溶液中快速产生 ,在
碱性溶液中较稳定。现制备高铁酸钾 ,测定其纯度并探究其性质。
(1)制备 (夹持装置略)①A为气体发生装置,写出对应的离子方程式 。
②装置B的作用为 。
③装置C中主要反应的化学方程式为 。
(2)探究 的性质
取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有 。为证明是否是
氧化了 而产生 ,设计以下方案:
方案
取少量a于试管中,…
Ⅰ
用 溶液充分洗涤C中所得固体,再用 溶液将 溶出,得到紫色溶液b;取少量
方案
Ⅱ
b,滴加盐酸,有 产生。
①补全方案Ⅰ中实验步骤:取少量a于试管中, ,但该离子的产生不能判断一定是 被
还原得到,还可能由 产生(用离子反应方程式表示)。
②方案Ⅱ可证明 氧化了 ,用 溶液洗涤的目的是 。
③小组同学对比方案Ⅱ实验和 的制备实验发现: 和 的氧化性强弱关系相反,请你帮助解
释出现矛盾的原因是 。
【答案】(1) 除去氯气中的氯化氢杂质
(2) 滴加KSCN溶液,溶液呈红色 排除 的干扰
或洗去 ,防止 与 在酸性条件下生成氯气 溶液的酸碱性不同
【分析】装置A中KMnO 与浓盐酸反应制备Cl;由于Cl 中混有HCl(g)和HO(g),HCl(g)会消耗Fe(OH)
4 2 2 2 3
和KOH,装置B中盛放饱和食盐水除去Cl 中混有的HCl(g);C装置中Cl 与KOH、Fe(OH) 反应制备
2 2 3
KFeO,在此装置中Cl 还可以直接与KOH反应生成KCl、KClO和HO;D装置中NaOH溶液用于吸收
2 4 2 2
多余Cl,防止污染大气;
2
【解析】(1)①根据题意,KMnO 与浓盐酸反应生成KCl、MnCl 、Cl 和HO,反应中Mn元素的化合价
4 2 2 2由+7价降至+2价,Cl元素的化合价由-1价升至0价,根据电子守恒和原子守恒配平,A中反应的化学方
程式为 ;
②装置B中盛放饱和食盐水,作用为除去氯气中的氯化氢杂质;
③装置C中得到紫色固体和溶液,说明Cl 在碱性环境下将Fe(NO ) 氧化得到KFeO,根据电子守恒和元
2 3 3 2 4
素守恒可得反应方程式为 ;
(2)①方案Ⅰ中实验步骤:取少量a于试管中,滴加KSCN溶液,溶液呈红色;溶液a中含有Fe3+,
Fe3+的产生不能判断 与Cl-一定发生了反应,根据资料“KFeO 在酸性或中性溶液中快速产生O”,
2 4 2
自身被还原成Fe3+,根据得失电子守恒、原子守恒和电荷守恒,可能的反应为
;
②方案Ⅱ可证明 氧化了 ,用 溶液洗涤的目的是排除 的干扰或洗去 ,防止
与 在酸性条件下生成氯气;
③制备KFeO 的原理为 ,在该反应中Cl元
2 4
素的化合价由0价降至-1价,Cl 是氧化剂,Fe元素的化合价由+3价升至+6价,Fe(NO ) 是还原剂,
2 3 3
KFeO 为氧化产物,根据同一反应中,氧化性:氧化剂>氧化产物,得出氧化性Cl> ;方案Ⅱ的反
2 4 2
应为 ,由方案Ⅱ得出氧化性 >Cl,实验表明,Cl 和氧化性强
2 2
弱关系相反;对比两个反应的条件,制备KFeO 在碱性条件下,方案Ⅱ在酸性条件下,说明溶液的酸碱性
2 4
的不同影响物质氧化性的强弱。
6.(2023上·河南·高三校联考)某实验小组以含硒废料(主要成分为Se、S等)提取硒,并测定产品硒的纯
度。回答下列问题:
Ⅰ.提取硒的实验步骤如下:
i.含硒废料用NaNO 和硫酸混合溶液溶解,得到HSeO 和HSeO 混合溶液;
3 2 3 2 4
ii.控制反应温度为80℃,使HSeO 转化为HSeO;
2 4 2 3
iii.调节溶液pH,通入SO ,得到硒单质沉淀。
2
(1)步骤i中使用硫酸的主要目的为 。
(2)用如图所示装置进行实验。
①反应器a的名称为 ,装置A的加热方法为 。
②装置B的主要作用为 。
③步骤iii生成硒单质的化学方程式为 。Ⅱ.测定产品硒的纯度,实验步骤如下:
i.准确称取0.8400g产品并充分研磨,加适量浓硫酸煮沸生成HSeO,再稀释配成500mL的溶液。
2 3
ii.准确量取25.00mL待测液于锥形瓶中,用0.0100mol·L-1酸性KMnO 标准溶液进行滴定,滴定过程中未
4
见浑浊,重复三次实验,实验数据见下表。
实验次
滴定前读数/mL 滴定后读数/mL
数
1 0.10 20.20
2 1.85 21.75
3 0.00 25.06
(3)该产品硒的纯度为 %(结果保留四位有效数字)。
(4)达到滴定终点时,若读数时仰视刻度线,则会导致测定结果 (填“偏大”、“偏小”或“不
变”)。
【答案】(1)提供酸性环境使NO 将含硒废料中的Se元素氧化为HSeO 和HSeO
2 3 2 4
(2) 三颈烧瓶 水浴加热 吸收尾气,防止污染空气 2SO +H SeO+H O=Se +2H SO
2 2 3 2 2 4
(3)94.05
(4)偏大
【分析】某实验小组以含硒废料(主要成分为Se、S等)提取硒,并测定产品硒的纯度,用硫酸和少量硝酸
处理废料,获得亚硒酸和少量硒酸,控制反应温度为80℃,使HSeO 转化为HSeO,将SO 通入亚硒酸
2 4 2 3 2
的溶液中,得到单质硒,以此解答。
【解析】(1)步骤i中使用硫酸的主要目的为:提供酸性环境使NO 将含硒废料中的Se元素氧化为
HSeO 和HSeO。
2 3 2 4
(2)①反应器a的名称为三颈烧瓶,A中需要控制反应温度为80℃,为了均匀加热,装置A的加热方法
为水浴加热;
②装置B的主要作用为吸收尾气,防止污染空气;
③步骤iii中SO 和HSeO 反应生成Se单质和HSO ,根据得失电子守恒和原子守恒配平化学方程式为:
2 2 3 2 4
2SO +H SeO+H O=Se +2H SO 。
2 2 3 2 2 4
(3)实验3中数据误差较大,应该舍去,滴定的反应过程中,Se的化合价有+4升高到+6,Mn的化合价
有+7降低到+2,根据化合价升降守恒和原子守恒,配平的方程式为:
5HSeO+2KMnO =K SeO+2MnSeO+2H SeO+3H O,则0.8400g产品中n(H SeO)=2.5n(KMnO)=2.5×
2 3 4 2 4 4 2 4 2 2 3 4
×0.0100mol·L-1× =0.01mol,该产品硒的纯度为
。(4)达到滴定终点时,若读数时仰视刻度线,会导致标准溶液的体积偏大,硒的纯度测定结果偏大。
7.(2023上·浙江·高三校联考)某化学小组模拟工业生产原理:以废铁屑(含少量 、Mn、C等杂质)
为原料生产配合物乙二胺四乙酸铁钠(EDTA铁钠盐),并测定所制取的样品中铁元素的含量。
已知:①乙二胺四乙酸铁钠,易溶于水和稀酸,微溶于乙醇;该螯合型配合物稳定性好
②氢氧化铁沉淀通常呈胶体状态,有较强的吸附性
Ⅰ.制备乙二胺四乙酸铁钠晶体
实验原理:
实验流程:
方案1:
(1)由 制乙二胺四乙酸铁钠可以选择 (填“酒精灯直接加热”或“水浴加热”)。
(2)氧化剂A可以选择 ,试写出该步反应的离子方程式 。
(3)下列说法正确的是 。
A.为避免 沉淀中裹入过多杂质,可以采用一次性加入氨水
B.该流程中两次用到 溶液,均可用 溶液代替
C.操作④洗涤时宜采用冷水洗涤
D.“一系列的操作”是指“蒸发浓缩,趁热过滤、洗涤、干燥”
E.乙二胺四乙酸铁钠溶液中滴入KSCN溶液不一定会显红色
方案2:用EDTA、 与 反应,制备乙二胺四乙酸铁钠,此法EDTA先被 中和后再和
直接反应。两个方案都有不足之处,方案1的缺点:氢氧化铁沉淀成胶体状态,难以过滤和洗涤。
(4)为使沉淀颗粒增大,实验中往往可以采取 (填实验条件)。
(5)方案2的缺点:产品中含杂质多,纯度不好。方案2后剩余废液可用层柱法(利用筛网孔径与微粒孔径不
同的一种分离方法)可得到反应的副产物 (填名称)。
Ⅱ.测定所制取样品中铁的含量(EDTA标准溶液滴定法)
取 样品溶于水,然后将其中的铁元素用萃取剂从配合物中“反萃取”出来并配成 溶液,取出
加入过量的 标准溶液并加热煮沸,充分反应后,再用 的
标准溶液滴定过量的EDTA至终点,消耗 标准溶液体积为 。
已知: 、 与EDTA反应的化学计量比均为 。
(6)实验室进行萃取操作时,需要打开分液漏斗活塞放气,正确的放气图示___________。A. B. C. D.
(7)计算铁元素的质量分数 。
【答案】(1)水浴加热
(2)
(3)BE
(4)煮沸
(5)氯化钠
(6)C
(7)10.64%
【分析】用废铁屑制备乙二胺四乙酸铁钠晶体,先用NaCO 溶液洗去废铁屑表面的油污,便于后续处理,
2 3
操作①为过滤,滤渣为Fe、Fe O、Mn、C等,用过量的盐酸进行酸浸,将铁屑溶解,然后进行操作②,
2 3
即过滤操作,滤去C等不溶性杂质,滤液B中主要含有Fe2+以及少量的Fe3+、Mn2+,向其中通入氧气,可
以将Fe2+氧化为Fe3+,然后加入过量的氨水将Fe3+转化为Fe(OH) 沉淀,进行操作③,过滤、洗涤操作,可
3
得Fe(OH) 沉淀,然后加入EDTA和NaCO 溶液在70~80℃条件下反应,反应结束后进行蒸发浓缩,冷却
3 2 3
结晶,过滤洗涤,干燥,可得产品。
【解析】(1)由流程图可知制备乙二胺四乙酸铁纳需要的温度为70~80℃,故采取的加热方式为水浴加热。
(2)氧化剂A的作用是将滤液B中的Fe2+氧化为Fe3+,故可以用氧气,反应的离子方程式为
。
(3)A.氢氧化铁沉淀通常呈胶体状态,有较强的吸附性,为避免 沉淀中裹入过多杂质,可以分
几次加入氨水,以便充分反应,减少杂质,A错误。
B.该流程中两次用到 溶液,第一次是溶解废铁屑表面的油脂,第二次是中和掉溶液中的H+,调
节pH,因此均可用 溶液代替,B正确。
C.乙二胺四乙酸铁钠,易溶于水和稀酸,微溶于乙醇,故操作④洗涤时宜采用乙醇洗涤,以便减少洗涤
过程对产品的损耗,C错误。
D.乙二胺四乙酸铁钠,易溶于水,故“一系列的操作”是指“蒸发浓缩,冷却结晶,过滤、洗涤、干
燥”,D错误。
E.乙二胺四乙酸铁钠为螯合型配合物,稳定性好,溶液中不含Fe3+,故滴入KSCN溶液不会显红色,E正
确。
综上所述,故答案为BE。
(4)为使沉淀颗粒增大,实验中往往可以采取煮沸的方法。
(5)方案2中EDTA先被 中和后再和 直接反应,反应后的产物为乙二胺四乙酸铁纳和NaCl,因此反应的副产物为氯化钠。
(6)实验室进行萃取操作时,需要打开分液漏斗的活塞放气,分液漏斗放气时需要用右手掌压紧盖子,
左手拇指、食指和中指握住活塞,把漏斗倒转过来,所以正确的放气图示为C。
(7)EDTA的总物质的量为:0.1600mol/L×0.03L=0.0048mol,已知Fe2+、Zn2+和EDTA为1:1反应,反应
后剩余的EDTA的物质的量等于消耗的Zn2+的物质的量为:0.2000mol/L×0.005L=0.0010mol,25mL中
Fe2+的物质的量为:0.0048mol-0.0010mol=0.0038mol,20.00g样品共计配成250mL溶液,铁元素的质量分
数为
【点睛】本题需要对铁元素的性质,实验的相关知识充分掌握,并能有效的利用题目中所给的已知条件,
综合分析题目中的流程图。
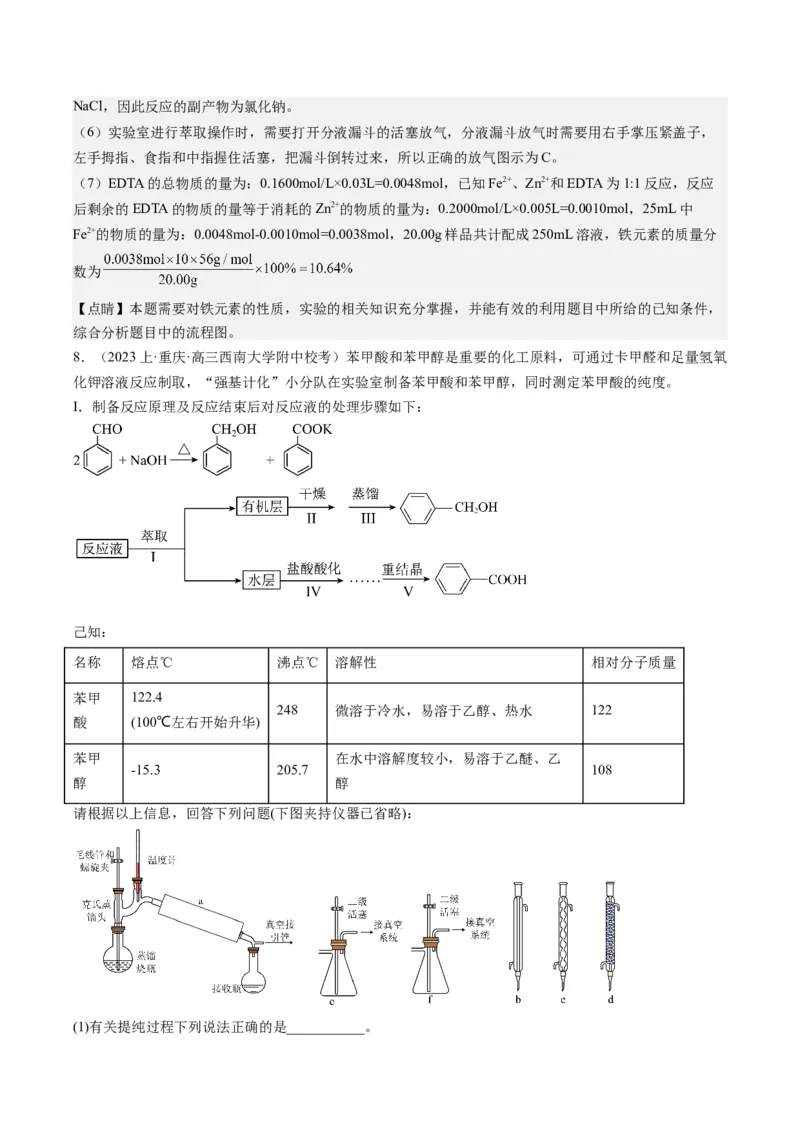
8.(2023上·重庆·高三西南大学附中校考)苯甲酸和苯甲醇是重要的化工原料,可通过卡甲醛和足量氢氧
化钾溶液反应制取,“强基计化”小分队在实验室制备苯甲酸和苯甲醇,同时测定苯甲酸的纯度。
I.制备反应原理及反应结束后对反应液的处理步骤如下:
己知:
名称 熔点℃ 沸点℃ 溶解性 相对分子质量
苯甲 122.4
248 微溶于冷水,易溶于乙醇、热水 122
酸 (100℃左右开始升华)
苯甲 在水中溶解度较小,易溶于乙醚、乙
-15.3 205.7 108
醇 醇
请根据以上信息,回答下列问题(下图夹持仪器已省略):
(1)有关提纯过程下列说法正确的是___________。A.步骤I:可以用乙醇作为萃取剂
B.步骤II:可用无水MgCl 作干燥剂
2
C.若在蒸馏过程中忘记加沸石,应立即停止加热,冷却后再加入沸石
D.步骤V:产品可用酒精灯或沸水浴加热烘干
(2)若用如图装置进行步骤III,则装置a应选用 (从b、c、d中选填,写名称),蒸馏时宜选用减压
蒸馏,优点是 (任写一点),真空接引管应连接装置 (填“e”或“f”)。
(3)步骤III具体操作步骤:安装好减压蒸馏装置→ →先旋紧螺旋夹,打开安全瓶上活塞,使体系
与大气相通,启动油泵抽气、慢慢关闭安全瓶上活塞至完全关闭→ →用一个洁净干燥的接受瓶
接收液体,温度趋于稳定后,待温度计的读数显著升高并稳定后→ →蒸馏完毕,移去热源,慢慢
旋开螺旋夹(避免倒吸),再慢慢打开安全瓶活塞,平稳内外压力,使测压计的水银柱慢慢地恢复原状,然
后关闭油泵和冷却水。
请从下列选项中选择合适的操作填空:
A.开启冷凝水,选用油浴加热蒸馏
B.在蒸馏瓶中加入待蒸液体,并加入1~2粒沸石
C.用一个洁净干燥的接受瓶收集馏分
II.产品的纯度测定
(4)称取mg样品,溶于过量的VmL浓度为0.1mol/L的氢氧化钾溶液中,滴加几滴酚酞溶液,摇匀,用
1
0.1mol/L盐酸滴定,达到滴定终点,记录耗酸体积。做3组平行实验,所消耗盐酸的平均体积为VmL。
2
①滴定终点现象是 。
②产品的纯度是 %
③若用甲基橙作指示剂,则测定结果 (填“偏大”、“偏小”或“无影响”)。
【答案】(1)BC
(2) 直形冷凝管 减压蒸馏沸点低,可防止温度过高时产品被氧化或蒸馏效率高或节约能源 e
(3) B A C
(4) 当滴入最后半滴盐酸时,溶液的颜色由红色变为浅红色,且半分钟内不恢复红色
偏小
【分析】反应液含有苯甲醇和苯甲酸钠,加入乙醚萃取,分液,得到的有机层为苯甲醇和乙醚的混合物,
蒸馏可得到苯甲醇,水层为苯甲酸钠的水溶液,加入盐酸酸化得到苯甲酸,经一系列操作后重结晶得到苯
甲酸。
【解析】(1)A.乙醇与水互溶,不能用作该体系的萃取剂,A错误;
B.无水氯化镁可用作有机体系的干燥剂,B正确;
C.蒸馏过程中忘记加沸石,应将装置冷却至室温后再补加,C正确;
D.苯甲酸在100℃左右升华,不能用酒精灯或用沸水浴加热烘干,D错误;
故选BC。
(2)蒸馏选用直形冷凝管,蒸馏时宜选用减压蒸馏,优点是:减压蒸馏沸点低,可防止温度过高时产品被氧化或蒸馏效率高或节约能源;真空接引管应连接装置:e,抽滤瓶中连接真空系统时导管斜面长的一
端应远离抽滤瓶支管;
(3)步骤III具体操作步骤:安装好减压蒸馏装置→在蒸馏瓶中加入待蒸液体,并加入1~2粒沸石→先旋
紧橡皮管上的螺旋夹,打开安全瓶上活塞,使体系与大气相通→启动油泵抽气,慢慢关闭安全瓶上活塞至
完全关闭→开启冷凝水,选用油浴加热蒸馏→用一个洁净干燥的接受瓶收集馏分→温度趋于稳定后→待温
度计的读数显著升高并稳定→用一个洁净干燥的接受瓶收集馏分→蒸馏完毕,移去热源,慢慢旋开螺旋夹
(避免倒吸),再慢慢打开安全瓶活塞,平稳内外压力,使测压计的水银柱慢慢地恢复原状,然后关闭油泵
和冷却水,故依次填入的顺序为:B、A、C;
(4)①滴定终点现象是:当滴入最后半滴盐酸时,溶液的颜色由红色变为浅红色,且半分钟内不恢复红
色;
②苯甲酸与氢氧化钾先反应(物质的量比为1:1),剩余的氢氧化钾用盐酸进行滴定,故苯甲酸的物质的
量为: ,苯甲酸的纯度为: =
;
③甲基橙的变色范围为3.1-4.4,酸过量,即盐酸消耗的氢氧化钾的量偏大,苯甲酸消耗的氢氧化钾的量偏
少,故苯甲酸的测定结果偏小。