文档内容
专题突破卷 02 元素化合物
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.(2023·上海静安二模)自然界与人类活动对硫的循环均能产生影响。下列说法错误的是( )
A.火山口温度过高,附近的单质硫会被O 直接氧化为SO
2 3
B.大气中的SO 会形成酸雨,最终以HSO 的形式进入地面或海洋
2 2 4
C.工业排放的SO 尾气可与CaO和O 反应生成CaSO
2 2 4
D.常温下,浓HSO 能使铁片钝化是由于其具有强氧化性
2 4
【答案】A
【解析】单质硫与O 反应只能变为SO ,SO 和O 在催化剂、加热条件下发生可逆反应生成SO ,故A错
2 2 2 2 3
误;大气中的SO 会形成酸雨,二氧化硫和水反应生成亚硫酸,亚硫酸被氧气氧化为硫酸,因此最终以
2
HSO 的形式进入地面或海洋,故B正确;工业排放的SO 尾气可与CaO和O 反应生成CaSO ,因此常用
2 4 2 2 4
氧化钙处理工业排放的SO 尾气,故C正确;浓硫酸具有强氧化性,因此常温下,浓HSO 能使铁片钝
2 2 4
化,故D正确。
2.明末科学家宋应星出版的《天工开物》中记载了有关“五金”的内容:“……黄金美者,其值去黑铁
(生铁)一万六千倍,然使釜、鬵(xín,一种炊具)、斤(这里指菜刀、镰刀、锄头等)、斧不呈效于日用之
间……贸迁有无,……”,下列解释正确的是( )
A.明代使用的釜、鬵一类的炊具都属于青铜合金
B.添加了铬、镍的不锈钢菜刀和农具使用后即使不保养,也不会生锈
C.金属的另一个用途就是铸成钱币作为贸易交往中的流通手段
D.黑铁在空气中发生的腐蚀主要是化学腐蚀
【答案】C
【解析】明代使用的釜、鬵一类的炊具都属于铁合金,故A错误;不锈钢制作就是在普通钢中添加铬、镍
等元素改变了钢铁内部结构,不锈钢不容易生锈,家里用的农具是铁合金,如果没及时洗干净后晾干,铁
能与氧气、水同时接触,容易发生电化学腐蚀,容易生锈,故B错误;金属可以用来铸成钱币作为贸易交
往中的流通手段,故C正确;生铁的腐蚀主要是析氢腐蚀和吸氧腐蚀,属于电化学腐蚀,故D错误。
3.下列措施不会直接减少大气中CO 含量的是( )
2
A.以CO 为原料人工合成淀粉
2
B.技术落后企业购买碳排放权
C.企业开展煤改电技术升级
D.捕集CO 并封存于海底
2
【答案】B
【解析】以CO 为原料人工合成淀粉可减少大气中CO 含量,A项不符合题意;技术落后企业购买碳排放
2 2权,其排放的CO 没有减少,B项符合题意;煤改电技术可减少CO 排放,C项不符合题意;捕集CO 并
2 2 2
封存于海底,减少了大气中的CO 含量,D项不符合题意。
2
4.(2024·吉林长春吉大附中实验学校高三考前适应考试)关于下列物质制备方法正确的是
A.工业上以二氧化锰和浓盐酸制备氯气
B.工业上用焦炭和金刚砂反应制备粗硅
C.工业上以饱和食盐水、氨气、二氧化碳为原料制取
D.工业上用氯气与 反应制备漂白粉
【答案】C
【解析】工业上通过电解饱和食盐水制取氯气,以二氧化锰和浓盐酸制备氯气是实验室制法,A项错误;
工业上用焦炭和石英砂(主要成分为二氧化硅)反应制备粗硅,金刚砂的主要成分是碳化硅,B项错误;向
饱和食盐水中依次通入足量氨气、二氧化碳制得碳酸氢钠,C项正确;工业上以氯气与石灰乳反应制备漂
白粉,D项错误。
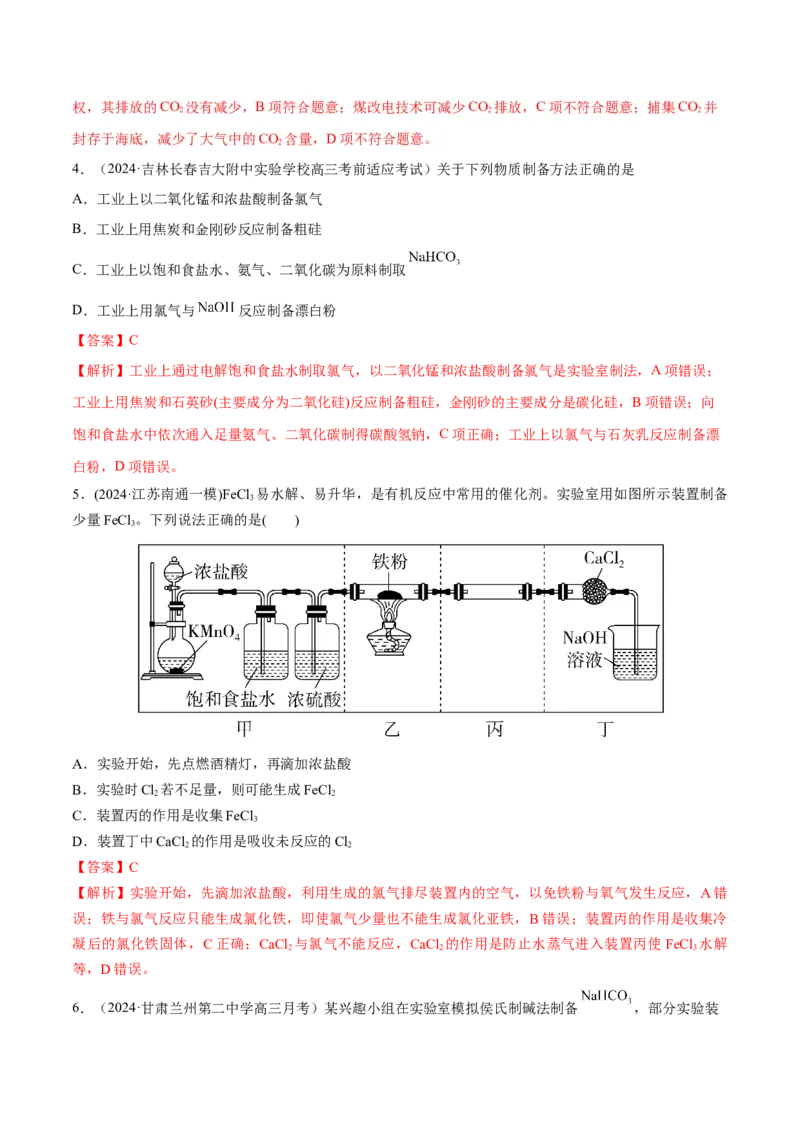
5.(2024·江苏南通一模)FeCl 易水解、易升华,是有机反应中常用的催化剂。实验室用如图所示装置制备
3
少量FeCl 。下列说法正确的是( )
3
A.实验开始,先点燃酒精灯,再滴加浓盐酸
B.实验时Cl 若不足量,则可能生成FeCl
2 2
C.装置丙的作用是收集FeCl
3
D.装置丁中CaCl 的作用是吸收未反应的Cl
2 2
【答案】C
【解析】实验开始,先滴加浓盐酸,利用生成的氯气排尽装置内的空气,以免铁粉与氧气发生反应,A错
误;铁与氯气反应只能生成氯化铁,即使氯气少量也不能生成氯化亚铁,B错误;装置丙的作用是收集冷
凝后的氯化铁固体,C正确;CaCl 与氯气不能反应,CaCl 的作用是防止水蒸气进入装置丙使FeCl 水解
2 2 3
等,D错误。
6.(2024·甘肃兰州第二中学高三月考)某兴趣小组在实验室模拟侯氏制碱法制备 ,部分实验装置如图所示。下列说法正确的是
A.实验过程中向启普发生器中添加液体时,可以取下I处胶塞加入
B.所用试剂有稀硫酸、浓硫酸、CaCO 、饱和食盐水、NH Cl、Ca(OH) 、蒸馏水
3 4 2
C.开始实验时,应先打开活塞II,再打开活塞III
D.反应结束后,试剂 换为冰水,可以促进 晶体的析出
【答案】D
【解析】试剂a为盐酸,试剂b为碳酸钙,用于制取二氧化碳,试剂c为饱和碳酸氢钠溶液用于除去二氧
化碳中的HCl;然后将二氧化碳通入氨化的饱和食盐水中,反应生成碳酸氢钠,过量的氨气用水或硫酸溶
液吸收,且要防止倒吸。实验过程中向启普发生器中添加液体时,应从球形漏斗加入,A项错误;制备
CO 应使用稀盐酸不应使用稀硫酸,生成的CO 无需干燥,NH Cl和Ca(OH) 用于制取NH ,尾气中含有
2 2 4 2 3
NH ,可用稀硫酸吸收,B项错误;CO 在水中溶解度小,开始实验时应先打开活塞Ⅲ,通入NH 营造碱性
3 2 3
环境,增大CO 的溶解度,再打开活塞Ⅱ,通入CO,C项错误;反应结束后将锥形瓶放入冰水浴中可以
2 2
降低的溶解度,促进 晶体的析出,D项正确。
7.(2024·广东肇庆二模)对下列事实的解释正确的是( )
A.二氧化硫气体能用浓硫酸干燥,是因为二氧化硫无还原性
B.医疗上可用硫酸钡作钡餐,是因为硫酸钡可以阻挡X射线通过且不溶于强酸
C.向50 mL 18 mol·L-1的HSO 溶液中加入足量的铜片加热充分反应后,被还原的HSO 的物质的量等于
2 4 2 4
0.45 mol
D.常温下,浓HSO 可以用铝制容器贮存,说明铝与浓HSO 不反应
2 4 2 4
【答案】B
【解析】二氧化硫具有还原性,但不能被浓硫酸氧化,故 A错误;用硫酸钡作X射线透视肠胃的内服药是
因为硫酸钡不溶于盐酸,故B正确;因随着反应的进行,硫酸的浓度降低,稀硫酸不能与铜反应,被还原
的HSO 的物质的量小于0.45 mol,故C错误;因常温下浓硫酸使铝钝化(化学变化),形成致密的氧化膜阻
2 4
碍了反应的继续进行,故D错误。
8.铁及其化合物是中学化学中的一类重要物质,下列关于铁元素的叙述中正确的是 ( )A.2Fe3++Fe===3Fe2+成立,说明氧化性:Fe3+>Fe2+
B.25 ℃,pH=0的溶液中,Al3+、NH、NO、Fe2+可以大量共存
C.5.6 g铁与足量的氯气反应失去电子0.2 mol
D.硫酸亚铁溶液中加入过氧化氢溶液:Fe2++2HO+4H+===Fe3++4HO
2 2 2
【答案】A
【解析】在2Fe3++Fe===3Fe2+中,Fe3+是氧化剂,Fe2+既是氧化产物又是还原产物,氧化性:Fe3+>Fe2
+,A项正确;pH=0的溶液呈强酸性,Fe2+、NO、H+不能大量共存,B项错误;5.6 g铁与足量的氯气反
应失去0.3 mol电子,C项错误;D项电荷和得失电子不守恒,错误。
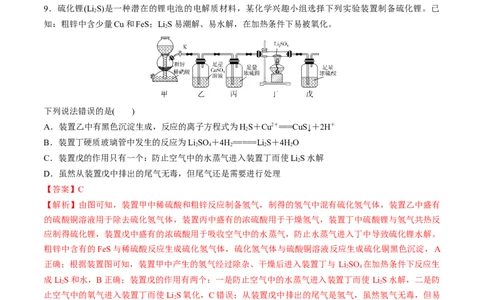
9.硫化锂(Li S)是一种潜在的锂电池的电解质材料,某化学兴趣小组选择下列实验装置制备硫化锂。已
2
知:粗锌中含少量Cu和FeS;LiS易潮解、易水解,在加热条件下易被氧化。
2
下列说法错误的是( )
A.装置乙中有黑色沉淀生成,反应的离子方程式为HS+Cu2+===CuS↓+2H+
2
B.装置丁硬质玻璃管中发生的反应为LiSO +4H=====LiS+4HO
2 4 2 2 2
C.装置戊的作用只有一个:防止空气中的水蒸气进入装置丁而使LiS水解
2
D.虽然从装置戊中排出的尾气无毒,但尾气还是需要进行处理
【答案】C
【解析】由图可知,装置甲中稀硫酸和粗锌反应制备氢气,制得的氢气中混有硫化氢气体,装置乙中盛有
的硫酸铜溶液用于除去硫化氢气体,装置丙中盛有的浓硫酸用于干燥氢气,装置丁中硫酸锂与氢气共热反
应制得硫化锂,装置戊中盛有的浓硫酸用于吸收空气中的水蒸气,防止水蒸气进入丁中导致硫化锂水解。
粗锌中含有的FeS与稀硫酸反应生成硫化氢气体,硫化氢气体与硫酸铜溶液反应生成硫化铜黑色沉淀,A
正确;根据装置图可知,装置甲中产生的氢气经过除杂、干燥后进入装置丁与 LiSO 在加热条件下反应生
2 4
成LiS和水,B正确;装置戊的作用有两个:一是防止空气中的水蒸气进入装置丁而使 LiS水解,二是防
2 2
止空气中的氧气进入装置丁而使LiS氧化,C错误;从装置戊中排出的尾气是氢气,虽然氢气无毒,但易
2
燃,应进行处理,D正确。
10.用铁泥(主要成分为Fe O 、FeO和少量Fe)制备超顺磁性纳米Fe O(平均直径为25 nm)的流程示意图如
2 3 3 4
下:
下列叙述不正确的是 ( )
A.常用热的NaCO 溶液除去铁泥表面的油污
2 3B.步骤②中,主要反应的离子方程式是2Fe3++Fe===3Fe2+
C.步骤④中,反应完成后剩余的HO 无需除去
2 2
D.步骤⑤中,为了验证得到的固体是超顺磁性的Fe O 粒子,可将其均匀分散在水中,做丁达尔效应实验
3 4
【答案】C
【解析】油污在碱性条件下可以发生水解反应,热的纯碱溶液碱性较强,水解效果较好,可用于除去油
污,A正确;滤液A溶质为氯化铁、氯化亚铁、过量的稀盐酸,加入铁粉的主要目的是还原铁离子,主要
反应的离子方程式是2Fe3++Fe===3Fe2+,B正确;步骤④中反应完成后剩余HO,为防止其在步骤⑤中
2 2
继续氧化+2价的铁元素,反应完成后需再加热一段时间除去剩余的HO,C错误;超顺磁性的纳米Fe O
2 2 3 4
粒子平均直径为25 nm,可将其均匀分散在水中,做丁达尔效应实验,D正确。
11.(2023·河北邯郸模拟)水体中的局部氮循环如图所示。下列说法错误的是( )
A.N→NH属于氮的固定
2
B.图示转化过程中N元素表现出7种化合价
C.硝化过程中含N物质被氧化,反硝化过程中含N物质被还原
D.在NH、NH OH、NO和NO中N原子的杂化方式不完全相同
2
【答案】C
【解析】N→NH为空气中游离态的氮转化为氮的化合物,属于氮的固定,A正确;N 、NH、NH OH、
2 2 2
NO、NO、NO、NO中氮元素的化合价分别为0、-3、-1、+3、+5、+2、+1,N元素表现出7种化
2
合价,B正确;硝化过程中N→NH氮元素化合价降低,含N物质被还原,C错误;NH、NH OH中N为
2 2
sp3杂化,NO和NO中N为sp2杂化,N原子的杂化方式不完全相同,D正确。
12.(2023·湖南湘潭开学考)工业上以软锰矿(主要成分为MnO )为原料通过固体碱熔氧化法生产高锰
2
酸钾,主要流程如图所示。下列说法错误的是( )
A. “熔融氧化”应在铁坩埚中进行
B. “锰酸钾歧化”(锰元素的化合价部分升高,部分降低)过程中可以用H SO 代替CO
2 4 2
C. 该流程中可循环使用的物质是MnO
2D. “滤液蒸发结晶”过程中加热蒸发液体至有较多晶体析出时停止加热
【答案】D
【解析】在“熔融氧化”过程中有KOH 参与反应,故不能用瓷坩埚,可以用铁坩埚,A正确;“锰酸钾
歧化”过程中需要加入酸性物质使溶液显酸性,可以用H SO 代替CO ,B正确;锰酸钾发生歧化反
2 4 2
应,生成高锰酸钾和MnO ,MnO 可以循环使用,C正确;“滤液蒸发结晶”过程中温度不能太高,且
2 2
应该在蒸发溶液出现晶膜时停止加热,因为KMnO 受热易分解,D错误。
4
13.(2024·湖北天门中学月考)胶体在生产、生活中有广泛应用(Liepatoff规则:胶核总是选择性地吸附与其
本身组成相似的离子形成胶粒)。硅胶溶液组成如下:
硅胶溶液
下列叙述正确的是( )
A.胶粒中表面离子数目一定大于束缚反离子
B.SiO与硅胶溶液胶核组成相似
C.1 mol Na SiO 和足量盐酸反应得到硅胶粒子数约为6.02×1023
2 3
D.硅胶溶液的胶团中n(SiO)>2n(H+)
【答案】B
【解析】胶粒中SiO带负电荷数大于H+带正电荷数,表面离子数不一定大于束缚反离子数,A错误;由图
示可知,胶核优先吸附SiO,根据Liepatoff规则可得SiO与硅胶溶液胶核组成相似,B正确;许多分子聚
集在一起形成胶粒,故形成胶粒数小于6.02×1023,C错误;胶团不带电荷,胶团中阴离子为硅酸根离子,
阳离子为氢离子,根据电荷守恒,n(SiO)=2n(H+),D错误。
14.(2024·湖北七市联考)通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下
列实验现象的解释正确的是( )
选项 操作及现象 解释
向淀粉碘化钾溶液中加入FeCl 溶液,溶液变
3
A Fe3+能与淀粉发生显色反应
蓝
将生铁放置于潮湿的空气中,铁表面有一层 铁在潮湿的空气中易生成
B
红棕色的斑点 Fe(OH)
3
说明Fe置换出硝酸中的氢,生
C 向稀硝酸中加入少量铁粉,有气泡产生
成了氢气
新制Fe(OH) 露置于空气中一段时间,白色 说明Fe(OH) 易被O 氧化成
2 2 2
D
物质变成了红褐色 Fe(OH)
3
【答案】D【解析】Fe3+将I-氧化生成I ,淀粉遇到I 显蓝色,并非Fe3+能与淀粉发生显色反应,A错误;铁锈的主
2 2
要成分是Fe O·xHO,不是Fe(OH) ,B错误;稀硝酸具有强氧化性,与铁粉反应生成NO,不产生H ,C
2 3 2 3 2
错误;Fe(OH) 易被O 氧化成Fe(OH) ,故新制Fe(OH) 露置于空气中一段时间,白色物质变成了红褐色,
2 2 3 2
D正确。
15.(2024·福建福州二检)工业上采用NaClO氧化法生产高铁酸钾(K FeO),其主要的生产流程如下:
2 4
已知:KFeO 在碱性环境中稳定,在中性和酸性条件下不稳定,难溶于醇等有机溶剂。
2 4
下列说法错误的是( )
A.反应②为3NaClO+2Fe(NO )+10NaOH===2Na FeO↓+3NaCl+6NaNO +5HO
3 3 2 4 3 2
B.由反应③可知,此温度下K (K FeO)>K (Na FeO)
sp 2 4 sp 2 4
C.“提纯”步骤的洗涤剂可以选用CHCOOK溶液、异丙醇
3
D.KFeO 可用于水的消毒
2 4
【答案】B
【解析】反应②中NaClO→Cl-、Fe(NO )→NaFeO 1 mol NaClO反应得2 mol电子,1 mol Fe(NO ) 反应
3 3 2 4, 3 3
失去3 mol电子,根据得失电子守恒、原子守恒可得3NaClO+2Fe(NO ) +10NaOH===2Na FeO↓+3NaCl
3 3 2 4
+6NaNO +5HO,A项正确;反应③中NaFeO 与KOH溶液混合生成KFeO,说明KFeO 的溶解度小于
3 2 2 4 2 4 2 4
NaFeO ,B项错误;因KFeO 在碱性条件下稳定,且在醇中的溶解度小,故可用CHCOOK溶液、异丙
2 4 2 4 3
醇作洗涤剂,C项正确;KFeO 具有强氧化性,可起到杀菌、消毒的作用,D项正确。
2 4
二、非选择题(本题包括4小题,共55分)
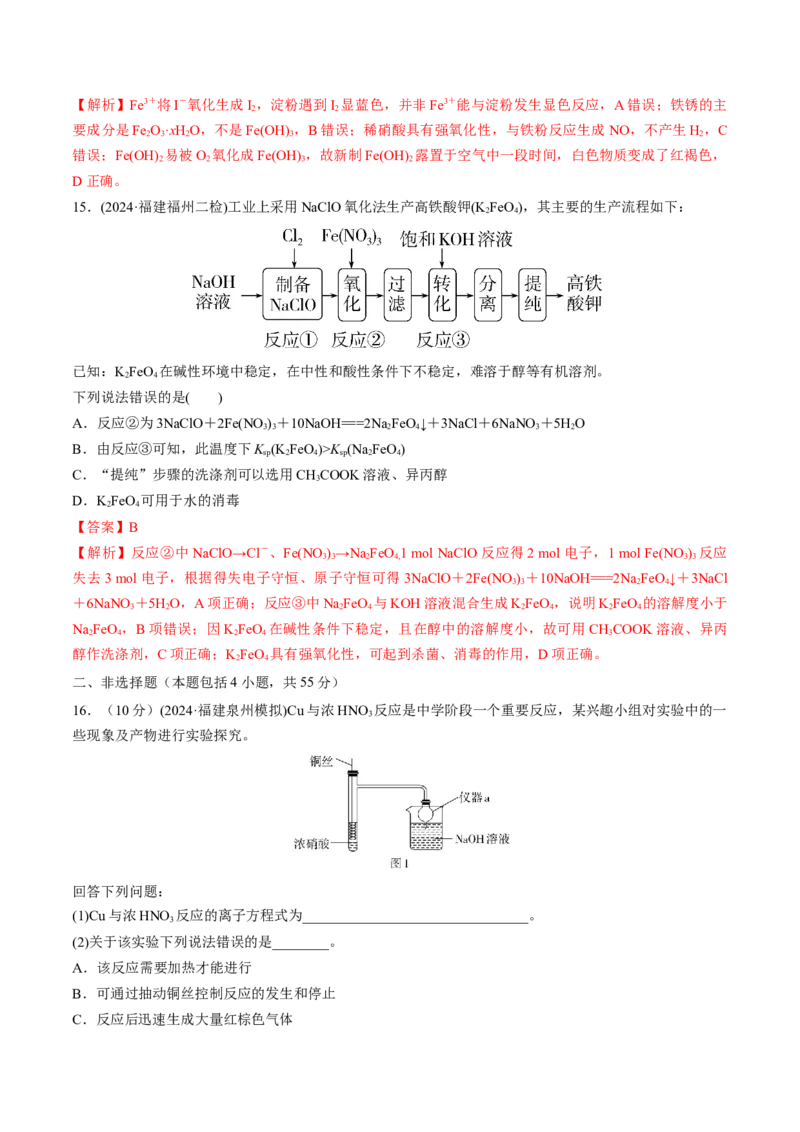
16.(10分)(2024·福建泉州模拟)Cu与浓HNO 反应是中学阶段一个重要反应,某兴趣小组对实验中的一
3
些现象及产物进行实验探究。
回答下列问题:
(1)Cu与浓HNO 反应的离子方程式为________________________________。
3
(2)关于该实验下列说法错误的是________。
A.该反应需要加热才能进行
B.可通过抽动铜丝控制反应的发生和停止
C.反应后迅速生成大量红棕色气体D.烧杯中仅发生中和反应
(3)小组同学发现Cu与浓HNO 反应所得混合溶液为绿色,Cu与稀HNO 反应所得混合溶液为蓝色,针对
3 3
绿色产生的原因展开探究。
【提出猜想】
猜想a:Cu(NO ) 浓度大
3 2
猜想b:NO 溶解在Cu(NO ) 溶液中
2 3 2
猜想c:由于NO 与水反应能够生成HNO ,HNO 与Cu2+能够发生可逆反应:Cu2++xHNO[Cu(NO)]
2 2 2 2 2 x
(x-2)-(绿色)+xH+
【实验探究】
实验ⅰ:配制饱和Cu(NO ) 溶液,溶液呈蓝色。
3 2
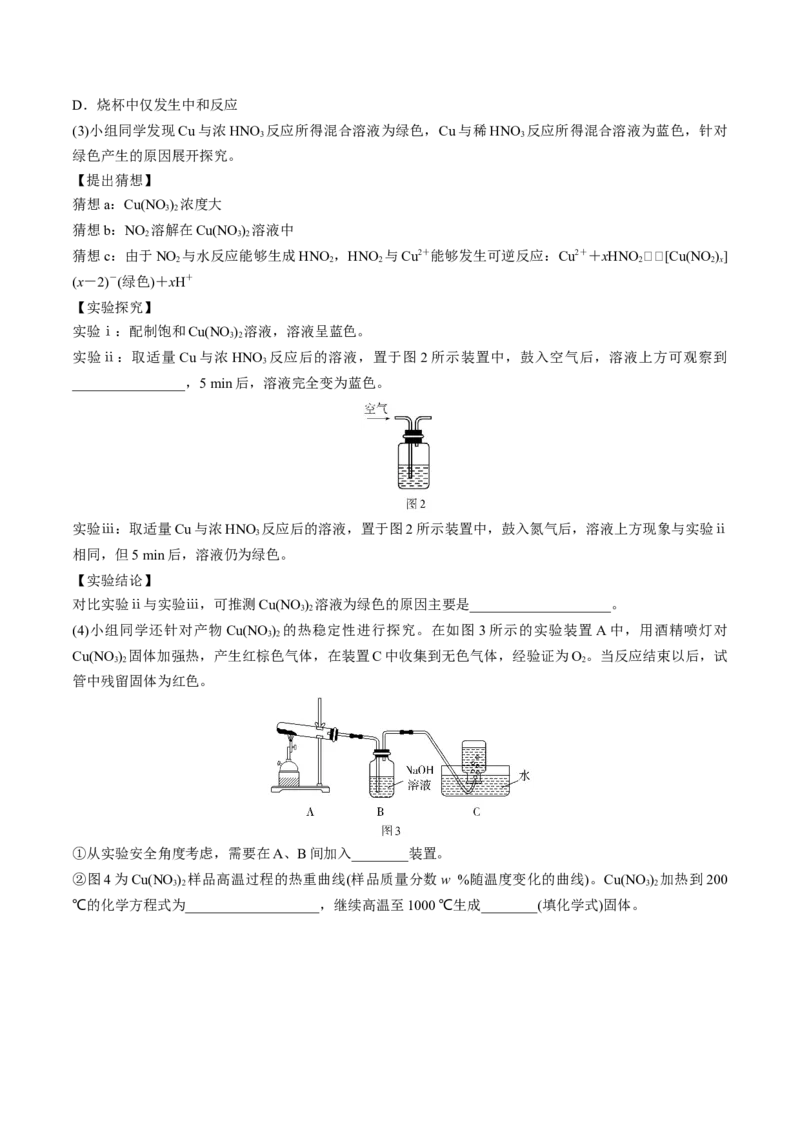
实验ⅱ:取适量Cu与浓HNO 反应后的溶液,置于图2所示装置中,鼓入空气后,溶液上方可观察到
3
________________,5 min后,溶液完全变为蓝色。
实验ⅲ:取适量Cu与浓HNO 反应后的溶液,置于图2所示装置中,鼓入氮气后,溶液上方现象与实验ⅱ
3
相同,但5 min后,溶液仍为绿色。
【实验结论】
对比实验ⅱ与实验ⅲ,可推测Cu(NO ) 溶液为绿色的原因主要是____________________。
3 2
(4)小组同学还针对产物Cu(NO ) 的热稳定性进行探究。在如图3所示的实验装置A中,用酒精喷灯对
3 2
Cu(NO ) 固体加强热,产生红棕色气体,在装置C中收集到无色气体,经验证为O 。当反应结束以后,试
3 2 2
管中残留固体为红色。
①从实验安全角度考虑,需要在A、B间加入________装置。
②图4为Cu(NO ) 样品高温过程的热重曲线(样品质量分数w %随温度变化的曲线)。Cu(NO ) 加热到200
3 2 3 2
℃的化学方程式为___________________,继续高温至1000 ℃生成________(填化学式)固体。【答案】(1)Cu+4H++2NO===Cu2++2NO ↑+2HO(2分)
2 2
(2)AD(2分)
(3)有红棕色气体放出 NO 溶于Cu(NO ) 溶液中(2分)
2 3 2
(4)防倒吸 2Cu(NO )=====2CuO+4NO ↑+O↑(2分) Cu O(2分)
3 2 2 2 2
【解析】(1)铜与浓硝酸反应生成硝酸铜、二氧化氮和 HO,离子方程式为:Cu+4H++2NO===Cu2++
2
2NO ↑+2HO;(2)铜与浓硝酸反应不需要加热,A错误;可以通过抽动铜丝控制反应的发生和停止,B正
2 2
确;铜与浓硝酸反应生成二氧化氮,为红棕色气体,C正确;烧杯中有硝酸和氢氧化钠的中和反应,还有
二氧化氮气体与氢氧化钠发生的氧化还原反应,D错误;(3)实验(ⅰ)证明硝酸铜溶液为蓝色,实验(ⅱ)取
Cu与浓HNO 反应所得绿色溶液通入空气,可以看到溶液上方有红棕色气体放出,是由于空气把溶解在硝
3
酸中的NO 带出,对比实验(ⅲ)通入氮气也有红棕色,但是溶液仍为绿色,原因是空气中的氧气与二氧化
2
氮和HO反应生成硝酸,二氧化氮反应完绿色消失,溶液显蓝色,而通入氮气的没有发生反应,溶液仍然
2
为绿色,证明溶液为绿色的原因主要是NO 溶于Cu(NO ) 溶液中;(4)固体加热产生气体通入溶液中,从实
2 3 2
验安全角度考虑,应该在两种装置之间加防倒吸装置,从热重曲线上得出,加热到 200度时,固体质量剩
余 42.6%,==42.6%,因此加热到 200 度分解为 CuO、NO 、O ,反应的化学方程式为:
2 2
2Cu(NO )=====2CuO+4NO ↑+O↑,加热到1000度时CuO又分解,固体只剩余Cu O了。
3 2 2 2 2
17.(15分)纳米铜是一种性能优异的超导材料,以辉铜矿(主要成分为Cu S)为原料制备纳米铜粉的工艺
2
流程如图1所示。
(1)用黄铜矿(主要成分为CuFeS)、废铜渣和稀硫酸共同作用可获得较纯净的Cu S,其原理如图2所示,该
2 2
反应的离子方程式为__________________________________________。(2)从辉铜矿中浸取铜元素时,可用FeCl 溶液作浸取剂。
3
①反应:Cu S+4FeCl ===2CuCl +4FeCl +S,每生成 1 mol CuCl ,反应中转移电子的物质的量为
2 3 2 2 2
________ ; 浸 取 时 , 在 有 氧 环 境 下 可 维 持 Fe3 + 较 高 浓 度 , 有 关 反 应 的 离 子 方 程 式 为
__________________________________________________________________________。
②浸取过程中加入洗涤剂溶解硫时,铜元素浸取率的变化如图3所示,未洗硫时铜元素浸取率较低,其原
因是__________________________________。
(3)“萃取”时,两种金属离子萃取率与pH的关系如图4所示,当pH>1.7时,pH越大,金属离子萃取率越
低,其中Fe3+萃取率降低的原因是_____________________________
________________________________________________________________________。
(4)用“反萃取”得到的 CuSO 溶液制备纳米铜粉时,该反应中还原产物与氧化产物的质量之比为
4
________。
(5)在萃取后的“水相”中加入适量氨水,静置,再经过滤、________、干燥、________等操作可得到
Fe O 产品。
2 3
【答案】(1)CuFeS +Cu+2H+===Cu S+Fe2++HS↑(2分)
2 2 2
(2)①2 mol(2分) 4Fe2++O +4H+===4Fe3++2HO(2分) ②生成的硫覆盖在Cu S表面,阻碍浸取(2分)
2 2 2
(3)Fe3+水解程度随pH的升高而增大(2分)
(4)32∶7(3分) (5)洗涤(1分) 煅烧(或灼烧) (1分)
【解析】(4)在碱性条件下,Cu2+与NH 反应生成氮气和铜,离子方程式为 2Cu2++NH +4OH-===2Cu↓
2 4 2 4
+N↑+4HO,反应中还原产物为Cu,氧化产物为N,质量之比为(2×64)∶28=32∶7。
2 2 2
18.(15分)(2024·河北部分学校高三选择性考试)中南大学某团队采用浓硫酸、硫酸铵、硫酸氢铵或
氯化铵为改性剂,利用低温焙烧将红土镍矿中的金属转化为相应的硫酸盐;随后采用水为浸出剂,利用水
浸/水解法选择性浸出镍、钴、钪等金属,同时去除铁、铝、铬等金属,实现了红土镍矿(主要成分为镍及
其氧化物)在温和条件下的高效提取。工艺流程(简化版)如图所示。回答下列问题:
(1)基态 核外电子排布式为 。
(2)写出氧化镍与改性剂中硫酸铵反应的离子方程式: 。用 处理尾气,可以将其循环利
用。
(3)磁选分离焙砂,最终得到铁精矿,说明氢还原焙烧时,含铁元素的产物是 。这时,每得到1 mol
该含铁产物,反应转移的电子数为 (用含 的式子表示)。
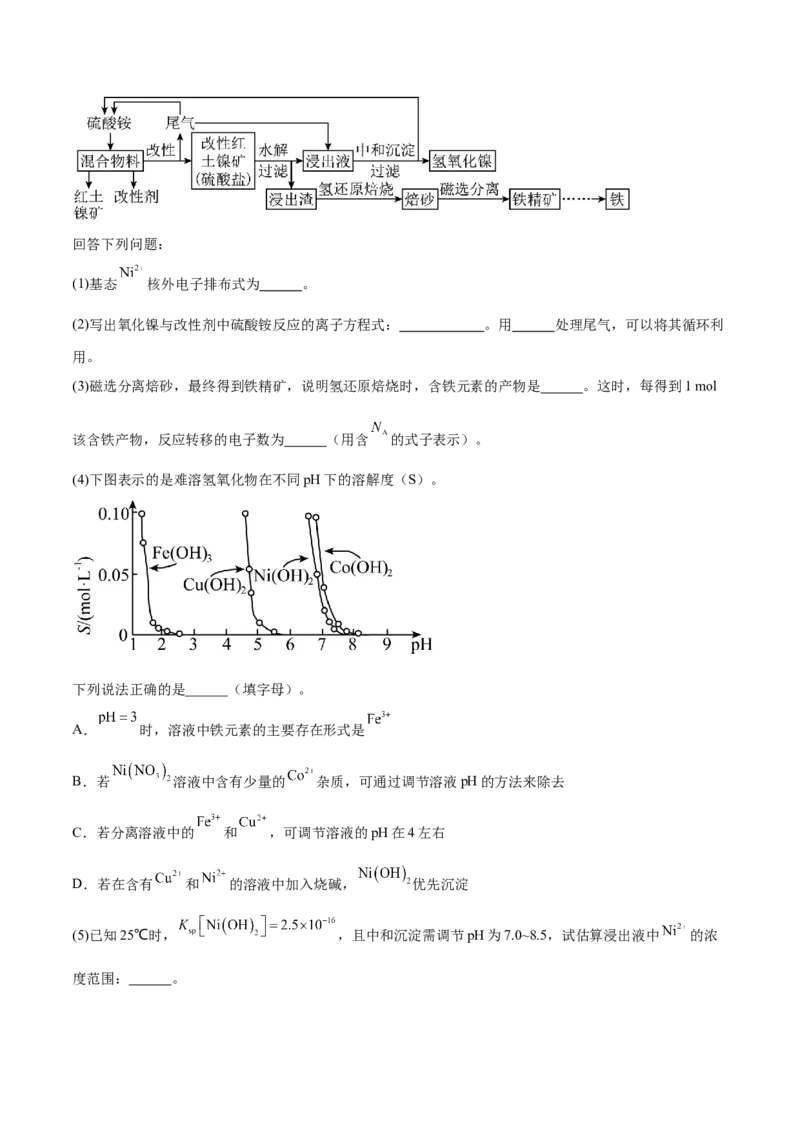
(4)下图表示的是难溶氢氧化物在不同pH下的溶解度(S)。
下列说法正确的是______(填字母)。
A. 时,溶液中铁元素的主要存在形式是
B.若 溶液中含有少量的 杂质,可通过调节溶液pH的方法来除去
C.若分离溶液中的 和 ,可调节溶液的pH在4左右
D.若在含有 和 的溶液中加入烧碱, 优先沉淀
(5)已知25℃时, ,且中和沉淀需调节pH为7.0~8.5,试估算浸出液中 的浓
度范围: 。(6)用含镍2%的100 kg红土镍矿,经上述工艺制得3 kg 固体,镍的回收率为 (保留3位有
效数字)。
【答案】(1)[Ar]3d8(1分)
(2)NiO+2 =Ni2++H O+2NH ↑ (2分) H SO (1分)
2 3 2 4
(3)Fe O (1分) N (1分)
3 4 A
(4)CD(2分)
(5)2.5×10-5mol/L≤c(Ni2+)≤2.5×10-2mol/L(3分)
(6)95.2%(4分)
【解析】用浓硫酸、硫酸铵、硫酸氢铵或氯化铵为改性剂,利用低温焙烧将红土镍矿(主要成分为镍及其
氧化物)中的金属转化为相应的硫酸盐,同时产生尾气NH ;随后采用水为浸出剂,利用水浸/水解法选择
3
性浸出镍、钴、钪等金属,得到相关金属硫酸盐,同时去除铁、铝、铬等金属,将尾气NH 通入浸出液中
3
和沉淀并过滤出Ni(OH) ,浸出渣中有铁、铝、铬的氢氧化物,还原焙烧后转化为氧化物,磁选分离出四
2
氧化三铁,进一步得到铁。(1)Ni元素原子序数为28,基态Ni2+核外电子排布式为[Ar]3d8。(2)氧化镍
与改性剂中硫酸铵反应,硫酸铵是强酸弱碱盐,铵根水解显酸性与NiO反应,NiO+2 =Ni2+
+H O+2NH ↑,尾气是氨气,用硫酸吸收,得硫酸铵,可以循环利用。(3)可以磁选分离说明含铁元素的
2 3
产物是磁性氧化铁,即Fe O,其中有两个Fe为+3价,一个为+2价,氢还原焙烧是还原氢氧化铁,每得到
3 4
1mol Fe O,有1mol Fe3+得1mol电子变为+2价,即转移电子数为N 。(4)由图像知,pH=3时,Fe(OH)
3 4 A 3
溶解度为0,说明铁元素主要存在形式是Fe(OH) ,A错误;根据图像,当Ni2+以氢氧化物形式沉淀时,
3
Co(OH) 溶解度很小,说明Co2+也大量以氢氧化物沉淀,不能除去Co2+,B错误;由图像,pH=4时,
2
Fe3+已经完全以氢氧化物沉淀,而Cu(OH) 溶解度还较大,Cu2+还未沉淀,可以分离Fe3+和Cu2+,C正确;
2
若在含有Cu2+和Ni2+的溶液中加入烧碱,pH增大过程中,Ni(OH) 溶解度先减小为0,说明Ni(OH) 优先沉
2 2
淀,D正确。(5)根据K [Ni(OH) ]=c(Ni2+)c2(OH-)=2.5×10−16,c(Ni2+)= ,pH为7.0~8.5,
sp 2
10-8.5mol/L≤c(H+)≤10-7mol/L,则10-7mol/L≤c(OH-)≤10-5.5mol/L,故2.5×10-5mol/L≤c(Ni2+)≤2.5×10-2mol/L。
(6)3kg Ni(OH) 固体中Ni元素的质量为 =1.903kg,100kg含镍2%的红土镍矿中Ni元素的
2质量为2kg,故Ni的回收率为95.2%。
19.(20分)(2024·山西八校联考)某小组利用数字化实验模拟制备Fe(OH) 并探究其相关性质。
2
Ⅰ.模拟制备Fe(OH)
2
装置如图,打开右瓶上方空气过滤器的气阀(平衡压强,便于FeSO 溶液能够进入右瓶);然后依次打开鲁
4
尔阀、推动注射器,将注射器中的FeSO 溶液加入左瓶的溶液中,促使左瓶中的FeSO 溶液流入右瓶;当
4 4
右瓶中明显有白色沉淀生成时,停止加液,依次关闭鲁尔阀、右瓶上方空气过滤器的气阀,打开左瓶上方
空气过滤器的气阀。
(1)实验证明制备Fe(OH) 的最佳pH是6~8,采用(NH )Fe(SO ) 代替FeSO 、氨水代替NaOH溶液效果更
2 4 2 4 2 4
好的原因是______________________________________
_________________________________________________________________ , NaSO 的 作 用 是
2 3
_____________________________________________________
__________________________________________________________________。
Ⅱ.探究原料FeSO 的相关性质
4
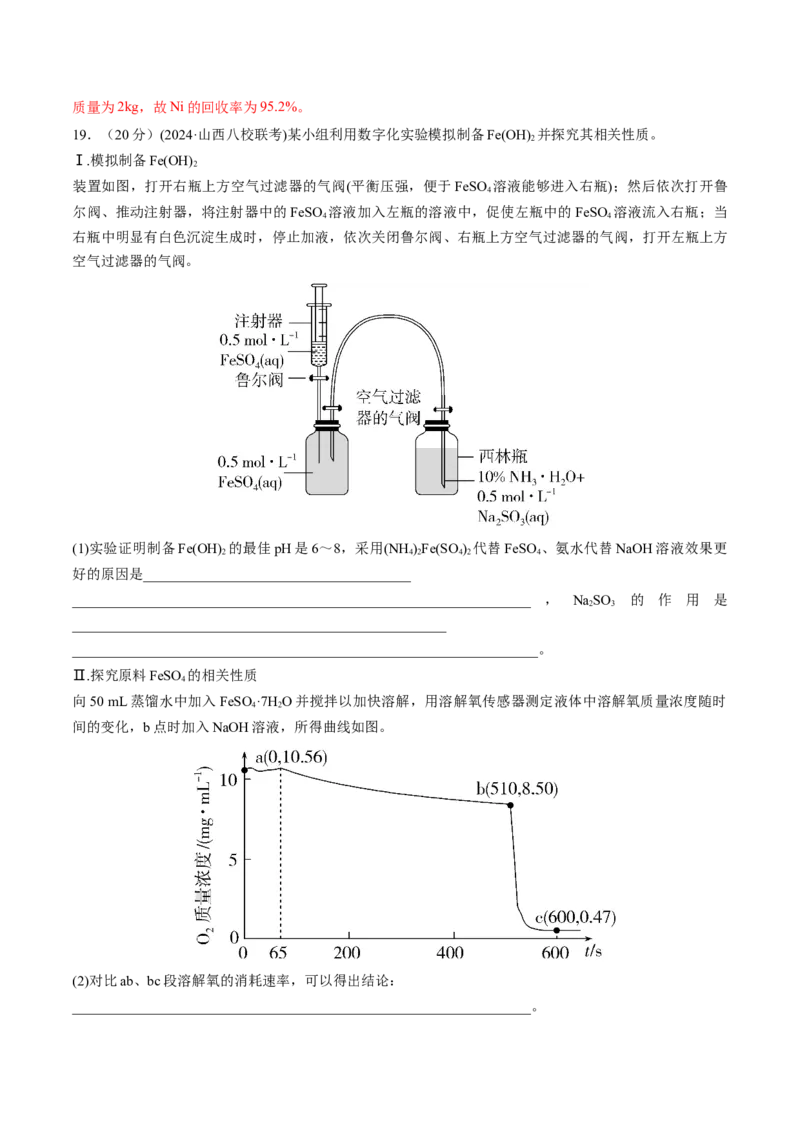
向50 mL蒸馏水中加入FeSO ·7H O并搅拌以加快溶解,用溶解氧传感器测定液体中溶解氧质量浓度随时
4 2
间的变化,b点时加入NaOH溶液,所得曲线如图。
(2)对比ab、bc段溶解氧的消耗速率,可以得出结论:
_________________________________________________________________。(3)已知:在pH≈4时,溶液中Fe2+被氧化成Fe3+的过程中会产生FeOOH,且c(Fe2+)降低量大于c(Fe3+)增
加量,pH几乎不变。用总离子方程式说明原因__________________________________,检验反应后的溶液
中是否存在Fe2+,可以选择的试剂是________。
A.NaOH溶液 B.K[Fe(CN) ]溶液
3 6
C.KSCN溶液
Ⅲ.用铈量法测定市售Fe(OH) 中Fe(Ⅲ)的含量
2
实验步骤如下:
①取一定量产品溶于稀硫酸中,取待测液V mL,以二苯胺磺酸钠作指示剂,用c mol·L-1硫酸铈标准溶液
进行滴定可得出 Fe2+的含量。终点时消耗硫酸铈标准溶液 V mL,反应原理为 2Ce(SO) +
1 4 2
2FeSO ===Ce (SO )+Fe (SO )。
4 2 4 3 2 4 3
②取待测液 V mL,将溶液中的 Fe3+在盐酸介质中用 H(SnCl )还原成 Fe2+,再用 HgCl 氧化过量的
2 4 2
H(SnCl ),反应原理为 2FeCl +H(SnCl )===2FeCl +H(SnCl )、H(SnCl )+2HgCl ===H (SnCl )+
2 4 3 2 4 2 2 6 2 4 2 2 6
Hg Cl↓。重复①的滴定过程,终点时消耗硫酸铈标准溶液V mL。
2 2 2
(4)待测液中c(Fe3+)=________mol·L-1(用含c、V、V 、V 的式子表示);若②中加入的H(SnCl )不足,则
1 2 2 4
测得Fe3+的含量________(填“偏高”“偏低”或“无影响”,下同),若没有加入HgCl ,则测得Fe3+的含
2
量________。
【答案】(1)NH ·H O是弱碱,容易控制pH,氨水中的NH 与溶液中的NH可直接形成缓冲溶液,缓冲能
3 2 3
力更强(3分)
利用NaSO 与溶液和装置中的氧气反应(2Na SO +O===2Na SO ),以减弱反应环境的氧化性(其他合理答
2 3 2 3 2 2 4
案也可) (3分)
(2)碱性条件下,Fe2+更易被O 氧化或Fe(OH) 更易被O 氧化(3分)
2 2 2
(3)12Fe2++3O+2HO===4FeOOH+8Fe3+(2分) B(2分)
2 2
(4) (3分) 偏低(2分) 偏高(2分)
【解析】(1)NaOH 是强碱,NH ·H O 是弱碱,用氨水代替 NaOH 溶液更容易控制 pH,另外用
3 2
(NH )Fe(SO ) 代替FeSO ,氨水中的NH 与溶液中的NH可直接形成缓冲溶液,缓冲能力更强;Fe2+具有
4 2 4 2 4 3
还原性,容易被氧化,NaSO 也具有还原性,可与溶液和装置中的氧气发生反应 2NaSO +
2 3 2 3
O===2Na SO ,可以防止Fe2+被氧化。(2)由图可知,bc段溶解氧的消耗速率远远大于ab段溶解氧的消耗
2 2 4
速率,结合b点时加入NaOH溶液可知,在碱性条件下,Fe2+更易被O 氧化。(3)由题目信息可知,Fe2+被
2
O 氧化为Fe3+和FeOOH,反应的离子方程式为12Fe2++3O +2HO===4FeOOH+8Fe3+;检验亚铁离子通
2 2 2
常选用K[Fe(CN) ](与Fe2+反应生成蓝色沉淀)。(4)由Fe3+~Fe2+~Ce(SO),结合步骤①可知,V mL待测
3 6 4 2
液中n(Fe2+)=c×V×10-3 mol,结合步骤①②可知,V mL待测液中n(Fe2+)+n(Fe3+)=c×V×10-3 mol,则
1 2
V mL待测液中n(Fe3+)=c×(V -V)×10-3 mol,故待测液中c(Fe3+)= mol·L-1;若②中加入的H(SnCl )不
2 1 2 4
足,则待测液中的Fe3+未被完全还原,测得的Fe3+的含量偏低;若没有加入HgCl ,则过量的H(SnCl )会
2 2 4
消耗硫酸铈标准溶液,使测得的V 偏大,造成测得的Fe3+的含量偏高。
2