文档内容
热点题型·选择题攻略
专题 03 阿伏加德罗常数的相关判断
目 录
题型综述
解题攻略
题组01 有关物质结构的阿伏加德罗常数的正误判断
题组02 有关物质变化的阿伏加德罗常数的正误判断
题组03 有关溶液中粒子数目计算的阿伏加德罗常数的正误判断
题组04 有关使用条件的阿伏加德罗常数的正误判断
题组05 有关物质的量等基本概念和公式的规范应用
高考练场
高考试题中对常用化学计量考查的固定题型为“阿伏加德罗常数正误的判断”,四个速项分别从不同的角
度进行设问,主要考查不同量之间的转换,物质结构中以及物质变化过程中微粒数目的判断,根据研究对
象的不同,可将此题型分为五个题组:一是有关物质结构的阿伏加德罗常数的正误判断;二是有关物质变
化的阿伏加德罗常数的正误判断;三是有关溶液中粒子数目计算的阿伏加德罗常数的正误判断;四是有关
使用条件的阿伏加德罗常数的正误判断;五是有关物质的量等基本概念和公式的规范应用。
题组 01 有关物质结构的阿伏加德罗常数的正误判断
【例1-1】阿伏加德罗常数的值为N ,下列说法正确的是
A
A.(2024·江西卷)22.4L15N 含有的中子数为16N
2 A
B.(2024·江西卷)12gC(石墨)中sp2杂化轨道含有的电子数为6N
A
C.(2024·江西卷)1mol[N=C=N]2﹣中含有的π键数为4N
A
D.(2024·广东卷) 中含有 键的数目为
【例1-2】N 为阿伏加德罗常数的值。下列说法正确的是
A
A.(2024·河北卷)1molKO 晶体中离子的数目为3N
2 AB.(2023·福建卷)0.1mol[NH OH]+含有的质子数为1.5N
3 A
C.(2023·西藏四川卷)0.5mol异丁烷分子中共价键的数目为6.5N
A
D.(2022·福建卷)9g水中含有的孤电子对数为2N
A
【提分秘籍】
(1)记特殊物质中所含微粒(分子、原子、电子、质子、中子等)的数目,如Ne、DO、18O、—OH、OH-
2 2
等,理清整体与部分的关系。
(2)记最简式相同的物质,构建解答混合物的模型,如NO 和NO、乙烯(C H)和丙烯(C H)等。
2 2 4 2 4 3 6
(3)记摩尔质量相同的物质,如N、CO、C H 等。
2 2 4
(4)记物质中所含化学键的数目,如一分子HO、C H 中化学键的数目分别为3、3n+1,SiO 中Si—
2 2 n 2n+2 2
O键的数目为4,苯环中不含双键等。
(5)记NaO 中O 为一个阴离子。
2 2 2
(6)记物质的特殊结构,如白磷、SiO、苯等
2
(7)记特殊物质的组成,如He、Ne为单原子分子,O 为三原子分子,P 为四原子分子。
3 4
【变式演练】
【变式1-1】(2024·广东江门·模拟预测)设 为阿伏加德罗常数的值。关于反应
,下列叙述正确的是
A. 中B原子最外层电子数为
B. 固体含 数为
C.标准状况下, 含 键数为
D. 含配位键数为
【变式1-2】(2024·河北·模拟预测)电解饱和食盐水的化学方程式为
, 为阿伏加德罗常数的值,下列说法正确的是
A. 中, 比 少 个电子
B.标准状况下, 的中子数目为
C. 和 中的共价键个数均为
D. 中含有质子总数为
题组 02 有关物质变化的阿伏加德罗常数的正误判断
【例2-1】(2023·海南卷) 代表阿伏加德罗常数的值。下列说法正确的是
A.2.4g镁条在空气中充分燃烧,转移的电子数目为
B.5.6g铁粉与 的HCl的溶液充分反应,产生的气体分子数目为C.标准状况下, 与 充分反应,生成的 分子数目为
D. 完全溶于 所得溶液, 微粒数目为
【例2-2】(2022·河北卷)N 是阿伏加德罗常数的值。下列说法正确的是
A
A.3.9gNa O 与足量水反应,转移电子个数为0.1N
2 2 A
B.1.2gMg在空气中燃烧生成MgO和MgN,转移电子个数为0.1N
3 2 A
C.2.7gAl与足量NaOH溶液反应,生成H 的个数为0.1N
2 A
D.6.0gSiO 与足量NaOH溶液反应,所得溶液中SiO 的个数为0.1N
2 A
【提分秘籍】
1.反应为可逆反应,反应物不能完全转化,如合成氨N+3H 2NH
2 2 3
2.有些物质常温常压下就以聚合分子形式存在。比如2NO NO,2HF (HF) 。
2 2 4 2
3.有些反应浓度不一样,反应就不一样。如铜与硝酸的反应、铜与浓硫酸的反应、二氧化锰与浓盐酸的反
应。
4.有些反应反应物的用量不一样,反应就不一样。如二氧化碳与碱的反应,碳酸钠与盐酸的反应,石灰水
与碳酸氢钠的反应等。
5.电子转移(得失)数目的问题分析,要做到“六注意”:
一要注意是否发生歧化反应,如Cl 与HO或NaOH发生歧化反应时,消耗1 mol Cl 转移1 mol电子;
2 2 2
二要注意变价元素,如1 mol Fe与足量盐酸反应转移2 mol电子,而与足量硝酸反应转移3 mol电子;
三要注意氧化还原的竞争及用量问题,如向FeBr 溶液中通入Cl,Cl 的量不同,转移的电子数不同。
2 2 2
四要注意可逆反应电子转移数目的计算:如某密闭容器盛有0.1 mol N 和0.3 mol H 在一定条件下充分反
2 2
应,转移电子的数目小于0.6 N 。另外,Cl 与HO反应也是可逆反应。
A 2 2
五要注意可涉及与浓酸反应时转移电子数目的计算:如50 mL 18.4 mol/L的浓硫酸与足量铜微热反应,随
着浓硫酸浓度逐渐变稀,稀硫酸不与铜反应,生成SO 分子数小于0.46 N ,转移电子的数目小于0.92
2 A
N 。MnO 与浓盐酸的反应也是类似情况。
A 2
六要注意粗铜精炼时,阳极质量减轻64 g,转移电子物质的量不一定是2 mol。
【变式演练】
【变式2-1】(2025·贵州·一模)设 为阿伏加德罗常数的值。下列叙述正确的是
A.一定条件下, 分解得到气体产物的分子总数为
B. 由 和 组成的混合气体含有的原子总数为
C.标准状况下, 与水完全反应生成 和 时转移的电子数为
D.在核反应 中, 含有的中子数为
【变式2-2】(2024·吉林·一模)N 表示阿伏加德罗常数的值,下列说法中正确的是
A
A.1 L 10 mol·L-1浓盐酸与足量MnO 加热充分反应,生成Cl 的数目为2.5N
2 2 A
B.常温常压下,3.2 g O 和O 混合气体中含有的氧原子数目为0.2N
2 3 A
C.常温下,将5.6 g铁片投入到足量浓硝酸中,生成NO 分子数目为1.5N
2 AD.向FeBr 溶液中通入适量氯气,当有1 mol Br-被氧化时,反应中转移电子的数目一定为2N
2 A
题组 03 有关溶液中粒子数目计算的阿伏加德罗常数的正误判断
【例3-1】N 是阿伏加德罗常数的值。下列说法正确的是
A
A.(2024·河北卷) 溶液中 的数目为
B.(2022·辽宁卷)pH=12的NaCO 溶液中 数目为0.01N
2 3 A
C.(2022·福建卷) 氨水中,含有的 分子数少于
D.(2023·广东卷) 和 的混合物中含 ,则混合物中质子数为
【例3-2】N 是阿伏加德罗常数的值。下列说法正确的是
A
A.(2022·浙江卷)在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B.(2021·广东卷) 的盐酸含有阴离子总数为
C.(2021·浙江卷) 的 水溶液中含有氧原子数为
D.(2021·全国卷) 的 溶液中 离子数为
【提分秘籍】
一看:溶液中是否有弱酸、弱碱离子的水解;
二看:溶液中是否有弱电解质的电离,即是否存在弱电解质或能水解的“弱离子”,如1 L 1 mol·L-1 的乙
酸或1 L 1 mol·L-1 乙酸钠溶液中CHCOO-数目均小于N ;
3 A
三看:是否指明了溶液的体积,如在pH=1的HCl溶液中,因溶液体积未知而无法求算H+的数目;
四看:是否为可逆反应;
五看:所给条件是否与电解质的组成有关,如pH=3的HSO 溶液中c(H+)=10-3 mol·L-1,与电解质组成
2 3
无关;0.05 mol·L-1的Ba(OH) 溶液中c(OH-)=0.1 mol·L-1,与电解质组成有关;
2
特别注意:求溶液中所含H、O原子数时,不要忽略溶剂水中的H、O原子数目。
【变式演练】
【变式3-1】(2024·云南大理·模拟预测) 为阿伏加德罗常数的值。下列说法正确的是
A.含 的溶液中 数目比 多
B.标准状况下, 中电子的数目为
C.含 的浓硫酸与足量铜反应,生成 的分子数为
D. 的乙酸和盐酸混合溶液含有 个
【变式3-2】(2024·安徽池州·三模)设 为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下, 溶于水,溶液中 和 的微粒数目之和为
B. 石墨中含有的碳碳单键数目为C.常温常压下, 与足量 反应,共生成 ,转移电子的数目为
D. 的 溶液显中性, 该溶液中含 的数目为
题组 04 有关使用条件的阿伏加德罗常数的正误判断
【例4-1】N 是阿伏加德罗常数的值。下列说法正确的是
A
A.(2022·全国卷)25℃, 下, 氢气中质子的数目为
B.(2023·西藏四川卷)标准状况下, 中电子的数目为
C.(2022·浙江卷) 乙烷和丙烯的混合气体中所含碳氢键数为
A.(2022·浙江卷)在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
【例4-2】N 是阿伏加德罗常数的值。下列说法正确的是
A
A.(2022·辽宁卷)标准状况下,22.4LHCl气体中H+数目为N
A
B.(2021·湖北卷)标准状况下,11.2LCO和H 的混合气体中分子数为0.5N
2 A
C.(2021·天津卷)22.4L氢气中,H 分子的数目为N
2 A
D.(2021·福建卷) 所含极性共价键的数目为
【提分秘籍】
1.当物质是气体时,应查看所给条件是不是标准状况。
2.当条件是标准状况时,应查看所给物质在标准状况下是不是气体[如CCl 、CHCl 、CHCl(注:CHCl为
4 3 2 2 3
气体)、HO、溴、SO 、己烷、苯、HF、NO 等在标准状况下均不为气体]。
2 3 2
3.已知某种物质的质量、物质的量或微粒个数时,则这些数据不受“温度、压强”外界条件的限制。
4.已知数据是体积时,要关注外界条件是不是标准状况、这种物质是不是气体。
5.已知数据是物质的量浓度或pH时,要关注考题是否给出了溶液的体积。
【变式演练】
【变式4-1】(2024·甘肃平凉·模拟预测)设 为阿伏加德罗常数的值。下列说法正确的是
A. 中含有的离子总数为
B.常温下, 的 溶液中含有的 总数约为
C.含 的 和 的混合物中所含质子数为
D.若反应中生成 ,则转移电子数一定为
【变式4-2】(2024·广东惠州·三模)常温常压下,电化学还原制氨气的总反应方程式:
,设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.9gHO中含有的中子数目为5N
2 A
B.1molN 中含有的π键的数目为2N
2 AC.每生成4molNH 就有6N 电子发生转移
3 A
D.消耗11.2LN 时,产生的O 分子数为0.75N
2 2 A
题组 05 有关物质的量等基本概念和公式的规范应用
【例5-1】设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.(2022·辽宁卷)标准状况下,22.4LHCl气体中H+数目为N
A
B.(2023·广东卷) 和 的混合物中含 ,则混合物中质子数为
C.(2024·广东卷)1molCO和H 的混合气体含有的分子数目为3N
2 A
D.(2022·辽宁卷)pH=12的NaCO 溶液中 数目为0.01N
2 3 A
【例5-2】设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.(2023·浙江卷)4.4gC HO中含有σ键数目最多为0.7N
2 4 A
B.(2023·西藏四川卷)标准状况下, 中电子的数目为
C.(2023·西藏四川卷) 的 溶液中 的数目为
D.(2022·浙江卷)12gNaHSO 中含有 个阳离子
4
【提分秘籍】
1.物质的量只能衡量微观粒子,必须指明具体粒子的种类或化学式。如1 molH和1 molNaCl。
2.物质的量是物理量,摩尔是物质的量的单位,不是物理量。
3.6.02×1023是个纯数值,没有任何物理意义,而阿伏加德罗常数(N )是指1 mol任何微粒所含的粒子数,
A
数值约为6.02×1023;N 6.02×1023/mol。
A
4.摩尔质量、相对原子(或分子)质量的含义不同,不是同一个物理量。二者单位也不同,摩尔质量的单位
是g·mol-1或kg·mol-1,相对原子(或分子)质量的单位为1,当摩尔质量以g·mol-1为单位时,二者在数值
上相等。
5.对具体的物质,其摩尔质量是确定的,不随物质的量的多少而变化,也不随物质的聚集状态而变化。
【变式演练】
【变式5-1】(2024·广东肇庆·二模)化学助力蓝天保卫战。工业上可利用氨水吸收SO 尾气,生成
2
NH HSO ,再将其氧化得到(NH )SO 化肥。设N 为阿伏加德罗常数的值,下列说法正确的是
4 3 4 2 4 A
A.22.4LNH 所含的分子数目为N
3 A
B.64gSO 中所含的σ键数目为2N
2 A
C.2mol 完全氧化生成 ,转移的电子数目为2N
A
D.1L0.1mol/L(NH )SO 溶液中所含的 数目为0.2N
4 2 4 A
【变式5-2】(2024·湖南邵阳·一模) 为阿伏加德罗常数的值。下列叙述正确的是
A.标准状况下, 溶于水,溶液中 、 和 的微粒数之和小于B. 溶液中含有 数目小于
C. 与 完全反应,反应中转移的电子数介于 和 之间
D. 苯乙烯中含有碳碳双键数为
1.(2024·江西卷)我国学者把游离态氮固定在碳上(示踪反应如下),制得的[N=C=N]2﹣离子可用于合成核
酸的结构单元。阿伏加德罗常数的值为N ,下列说法正确的是
A
15N+C(石墨)+2LiH Li[15NC15N]+H
2 2 2
A.22.4L15N 含有的中子数为16N
2 A
B.12gC(石墨)中sp2杂化轨道含有的电子数为6N
A
C.1mol[N=C=N]2﹣中含有的π键数为4N
A
D.生成1mol H 时,总反应转移的电子数为6N
2 A
2.(2024·江西赣州·二模)一种光催化重整聚乳酸生成丙酮酸的过程如图所示。设 为阿伏加德罗常数
的值,下列说法错误的是
A.1mol乳酸分子中含有 键数目为
B.1mol乳酸比1mol丙酮酸多 质子
C.生成1mol丙酮酸,需要消耗
D.1mol丙酮酸与足量 溶液反应,生成 分子数为
3.(2024·贵州卷)二氧化氯 可用于自来水消毒。实验室用草酸 和 制取 的反
应为 。设 为阿伏加德罗常数的值。下列说
法正确的是
A. 中含有的中子数为B.每生成 ,转移电子数为
C. 溶液中含有的 数目为
D.标准状况下, 中含 键数目为
4.(2024·广东卷)设 为阿伏加德罗常数的值。下列说法正确的是
A. 中含有 键的数目为
B. 溶液中含 的数目为
C. 和 的混合气体含有的分子数目为
D. 与 反应生成 ,转移电子数目为
5.(2024·河北卷)超氧化钾 可用作潜水或宇航装置的 吸收剂和供氧剂,反应为
, 为阿伏加德罗常数的值。下列说法正确的是
A. 中 键的数目为
B. 晶体中离子的数目为
C. 溶液中 的数目为
D.该反应中每转移 电子生成 的数目为
6.(2024·浙江金华·二模)工业上用焦炭还原石英砂制得粗硅,下列说法不正确的是( 为阿伏伽德罗常
数)
A. 中含有 键数目为 B.消耗 焦炭转移 电子
C. (氧化产物): 还原产物)=2:1 D.可用氯化氢气体将硅与杂质分离
7.(2024·安徽滁州·二模)已知:
,设N 为阿伏伽德罗常数的数值。下列说法正确的是
A
A.0.1 溶液中含有N 个K+
A
B.1mol 参与反应断裂的π键数目为N
A
C.反应每放出m kJ的热量,生成N 个 分子
A
D.每转移10N 个电子,产生CO 的体积标况下约为44.8L
A 2
8.(2024·吉林卷)硫及其化合物部分转化关系如图。设 为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下, 中原子总数为B. 溶液中, 数目为
C.反应①每消耗 ,生成物中硫原子数目为
D.反应②每生成 还原产物,转移电子数目为
9.(2024·湖南·模拟预测)下列各组指定粒子数目相等的是
A. 和 分别与足量稀硝酸反应转移电子数
B. 乙二醇含 杂化的原子数和常温常压下 氖气含原子数
C. 溶液制得 胶粒数与 溶液中 数
D. 和 的混合气体含分子数和标准状况下 含原子数
10.(2024·重庆·模拟预测) 沸点为-87.5℃,可与 浴液反应:
, 为阿伏加德罗常数的值。下列叙述错误的是
A.生成1mol ,转移的电子数为2
B.生成2mol ,断裂的P-H键与O-H键数目比为3∶4
C.消耗标准状况下11.2L ,生成2molCu
D.消耗含有孤电子对数4 的 ,生成2mol
11.(2023·福建卷)我国新一代载人飞船使用的绿色推进剂硝酸羟胺 在催化剂作用下可
完全分解为 和 。 为阿伏加德罗常数的值,下列说法正确的是
A. 含有的质子数为
B. 固态硝酸羟胺含有的离子数为
C. 硝酸羟胺含有的 键数为
D.硝酸羟胺分解产生 (已折算为标况)的同时,生成 分子数为
12.(2024·安徽合肥·模拟预测)银氨溶液不能储存,因为放置时会析出有强爆炸性的 沉淀。可通过
加入盐酸转化为AgCl沉淀回收,还可利用羟胺回收银,反应如下:
; 。设阿伏加德罗常数值为 。下列说法正确的是
A.向银氨溶液中加入1mol HCl,可以回收AgCl为
B.1mol/L 溶液含有配位键数为2
C.等物质的量的 和羟胺均含有3 个氢原子
D.羟胺有强还原性,当反应中转移电子数为2 时,需消耗2mol
13.(2024·湖南长沙·三模)CuCl 和SO 发生氧化还原反应,离子方程式为
2 2。设 为阿伏加德罗常数的值,下列叙述正确的是
A.1 mol氯化铜固体含有的Cu2+数目小于
B.标准状况下,2.24 L H O中心O原子的价层电子对数为0.4
2
C.1 mol SO 溶于水,电离出的H+数目为2
2
D.生成1 mol CuCl,转移的电子数为
14.(2022·辽宁卷)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.标准状况下,22.4LHCl气体中H+数目为N
A
B.28gC H 分子中含有的 键数目为4N
2 4 A
C.1.8g18O中含有的中子数为N
A
D.pH=12的NaCO 溶液中 数目为0.01N
2 3 A
15.(2023·广东卷)设 为阿伏加德罗常数的值。侯氏制碱法涉及 和 等物质。下
列叙述正确的是
A. 含有的共价键数目为
B. 完全分解,得到的 分子数目为
C.体积为 的 溶液中, 数目为
D. 和 的混合物中含 ,则混合物中质子数为
16.(2024·四川巴中·一模)已知反应: 为阿伏加德罗常数
的值,若消耗 ,下列叙述错误的是
A.转移电子数为 B.还原产物微粒数为
C.含N微粒中N原子均采取 杂化 D.2mol 中 键的数目为
17.(2024·河北邯郸·一模)工业上电解 与 混合溶液制备强氧化剂过二硫酸铵
。设NA为阿伏加德罗常数的值。下列叙述正确的是
A.132 g 固体中阳离子数目小于
B.1 L 的 与 混合溶液中, 数目为
C.1 mol 作氧化剂时,硫原子得电子数目为
D.224 L 气体溶于HO中,溶液中 、 的数目总和为N
2 A
18.(2023·北京卷)离子化合物 和 与水的反应分别为① ;②
。下列说法正确的是A. 中均有非极性共价键
B.①中水发生氧化反应,②中水发生还原反应
C. 中阴、阳离子个数比为 , 中阴、阳离子个数比为
D.当反应①和②中转移的电子数相同时,产生的 和 的物质的量相同
19.(2024·吉林长春·模拟预测)1962年化学家N.Bartlett基于以下两点合成了第一个含有化学键的“惰性
气体”化合物——橙黄色固体配合物 。
①一个现象: 能够氧化 生成 。
②一个事实: 的电离能 与 的电离能 相近。 不溶于 ,遇水则迅
速分解,并放出气体: 。
以 代表阿伏加德罗常数的值。下列说法正确的是
A. 固体中阳离子含有的电子数为
B. 中,含有 键数为
C.反应产生 (标况) ,转移的电子数为
D. 固体中中阴阳离子数共有
20.(2023·浙江卷)N 为阿伏加德罗常数的值,下列说法正确的是
A
A.4.4gC HO中含有σ键数目最多为0.7N
2 4 A
B.1.7gH O 中含有氧原子数为0.2N
2 2 A
C.向1L0.1mol/LCHCOOH溶液通氨气至中性,铵根离子数为0.1N
3 A
D.标准状况下,11.2LCl 通入水中,溶液中氯离子数为0.5N
2 A
21.(2024·河北·模拟预测)在加热条件下,硫单质可以与 溶液反应:
, 为阿伏加德罗常数,下列说法错误的是
A.发生氧化反应与发生还原反应的硫的物质的量之比是
B. 是硫常见的一种单质,结构式为 ,则 中存在 的数目是
C.S的常见单质有 、 、 ,它们之间的转化是化学变化
D.试管内壁上的硫可用热的 溶液或 除去
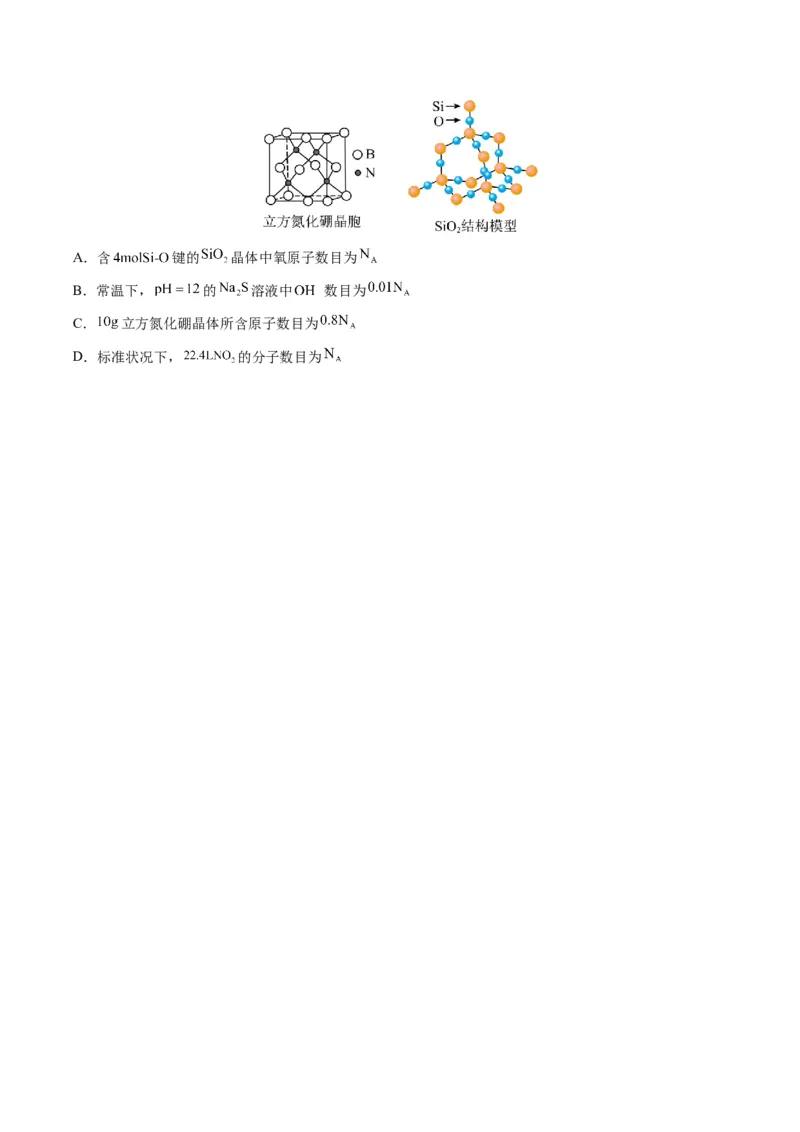
22.(2024·云南·二模)设 为阿伏加德罗常数的值。下列说法正确的是A.含 键的 晶体中氧原子数目为
B.常温下, 的 溶液中 数目为
C. 立方氮化硼晶体所含原子数目为
D.标准状况下, 的分子数目为