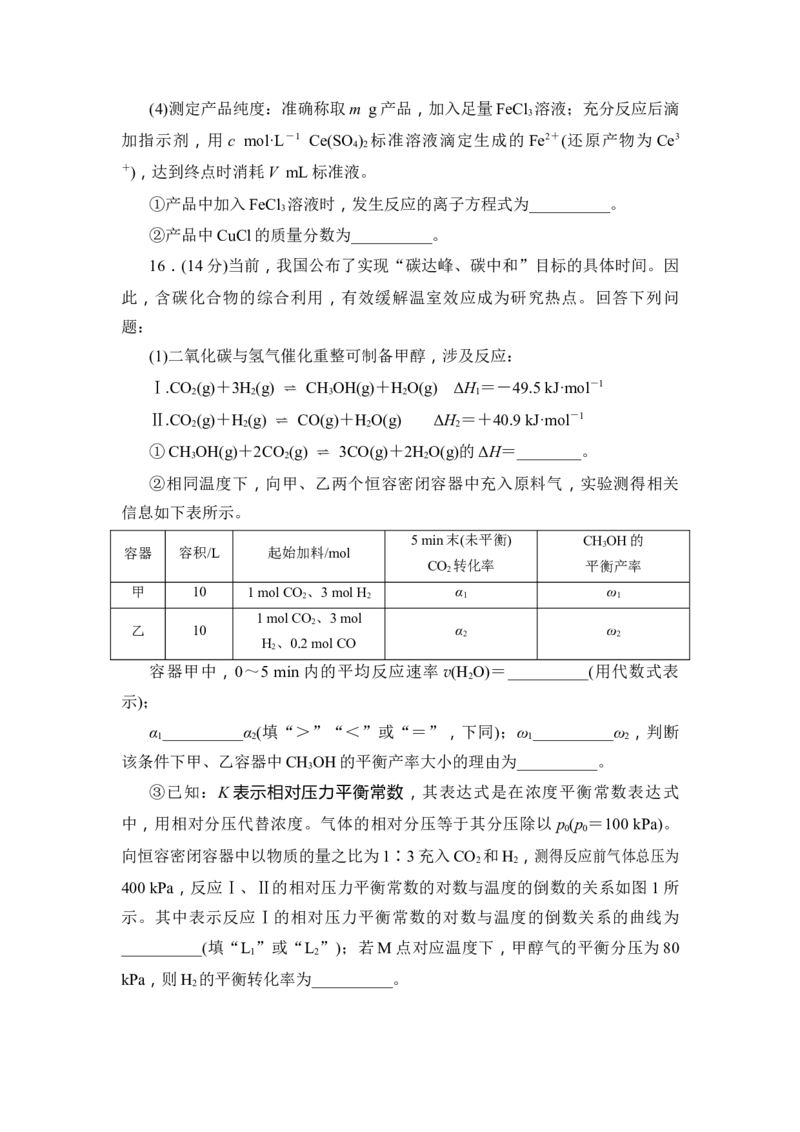文档内容
张家口市 2022-2023 学年度高三年级第一学期期末考试
化 学
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在试卷和答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂
黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答
题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Cl 35.5 Ca 40 Cu 64 Zn 65
一、单项选择题:本题共9小题,每小题3分,共27分。在每小题给出的
四个选项中,只有一项是符合题目要求的。
1.文献中对石油有如下记载:“高奴县有洧水,可燃”;“予知其烟可
用,试扫其烟为墨,黑光如漆,松墨不及也,此物必大行于世”。下列说法正
确的是
A.“洧水”属于一次能源
B.“洧水”属于纯净物
C.“烟”的主要成分为炭黑,属于共价晶体
D.现代石油裂解工艺是为了提供清洁燃料
2.化合物M( )是一种有机合成的中间体。下列关于M的说法错误
的是
A.含有酮羰基、醚键两种官能团
B.可使酸性KMnO 溶液褪色
4
C.能发生取代反应和氧化反应
D.分子中采用sp2杂化的C原子有6个
3.近年,我国在科研领域取得了诸多世界瞩目的成就。下列说法正确的是
A.“天和”核心舱使用的碳化硅属于新型有机材料
B.长征五号火箭使用液氧、液氢作推进剂,可避免环境污染
C.将二氧化碳合成淀粉可有效减少酸雨的形成D.冰墩墩的外壳材料之一亚克力( )由缩聚反应制得
4.卢瑟福发现质子的核反应原理为X+He→Y+1H。其中Y元素的一种同
素异形体可吸收紫外线。下列说法错误的是
A.Y的中子数为9
B.X的最高价含氧酸的浓溶液具有强氧化性
C.相同条件下气体密度:Y >X
2 2
D.X、Y的单质均为非极性分子
5.设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.FeO与O 反应制得1 mol Fe O 时,转移电子的数目为3N
2 3 4 A
B.1 mol HCOONa溶于水形成的溶液中,含有碳原子的数目为N
A
C.密闭容器中H 与I 生成2 mol HI时,充入H 分子的数目为N
2 2 2 A
D.22.4 L(标准状况)乙苯和二甲苯的混合物中,含有分子的数目为N
A
6 . 实 验 室 以 粗 Na SO ( 含 泥 沙 、 MgSO 杂 质 ) 为 原 料 制 备 芒 硝
2 4 4
(Na SO ·10H O)的操作中,下列不需要使用的装置是
2 4 2
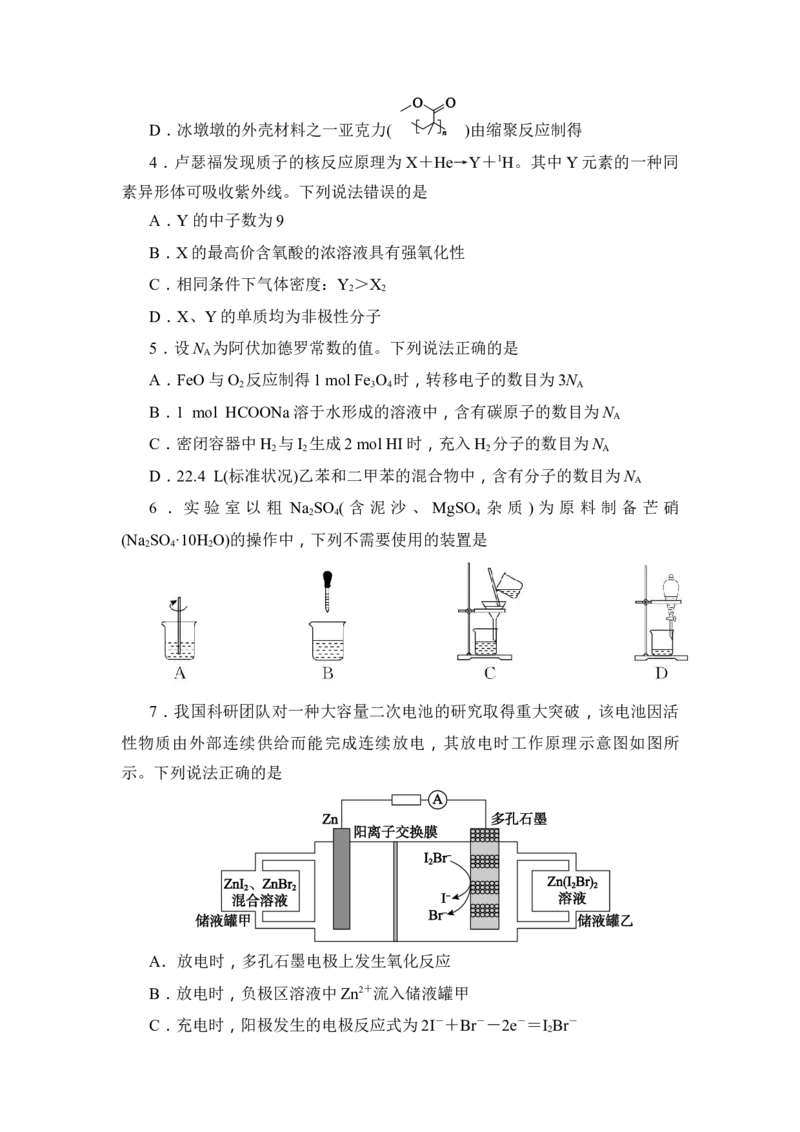
7.我国科研团队对一种大容量二次电池的研究取得重大突破,该电池因活
性物质由外部连续供给而能完成连续放电,其放电时工作原理示意图如图所
示。下列说法正确的是
A.放电时,多孔石墨电极上发生氧化反应
B.放电时,负极区溶液中Zn2+流入储液罐甲
C.充电时,阳极发生的电极反应式为2I-+Br--2e-=I Br-
2D.充电时,导线中通过2 mol e-,理论上阴极质量减少65 g
8.研究表明:质子溶剂参与苯乙烯环氧化反应机理如图所示(R 表示烃
基)。下列说法错误的是
A.电负性:O>C>H B.ROH与H O 能形成分子间氢
2 2
键
C.ROH为反应过程的中间产物 D.步骤③存在着极性键断裂和形
成
9.同一短周期元素M、W、X、Y、Z的原子序数依次增大,M原子的电
子数等于W原子的最外层电子数。五种元素形成的一种化合物在电化学领域有
重要应用,结构如图所示。下列说法正确的是
A.简单离子半径:M>Y>Z
B.最高价氧化物对应水化物酸性:W>X
C.第一电离能:M<W<X<Y<Z
D.Z的简单氢化物的水溶液需保存在细口玻璃瓶中
二、不定项选择题:本题共4小题,每小题4分,共16分。在每小题给出
的四个选项中,有一项或两项符合题目要求。若正确答案只包括一个选项,多
选时,该小题得0分;若正确答案包括两个选项,只选一个且正确的得 2分,
选两个且都正确的得4分,但只要选错一个,该小题得0分。
10.2,5-降冰片二烯(NBD)可有效抑制乙烯的催熟作用,实验室制备
NBD的一种原理如下图所示。下列说法正确的是
A.DCPD与CPD互为同系物
B.CPD的所有原子不可能处于同一平面C.DCPD和NBD中均含有手性碳原子
D.NBD的一氯代物有3种(不含立体异构)
11.砷(As)和镓(Ga)均为生产新型半导体的原料,分别与P、Al同族并相
邻。实验室以废弃 GaAs(含GaAs和少量SiO 、Fe O 和AgCl)为原料制备砷酸
2 2 3
钠晶体(Na AsO )和Ga单质的部分流程如下:
3 4
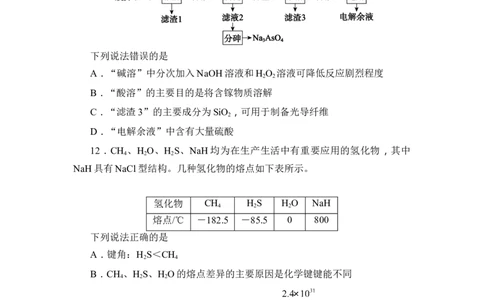
下列说法错误的是
A.“碱溶”中分次加入NaOH溶液和H O 溶液可降低反应剧烈程度
2 2
B.“酸溶”的主要目的是将含镓物质溶解
C.“滤渣3”的主要成分为SiO ,可用于制备光导纤维
2
D.“电解余液”中含有大量硫酸
12.CH 、H O、H S、NaH均为在生产生活中有重要应用的氢化物,其中
4 2 2
NaH具有NaCl型结构。几种氢化物的熔点如下表所示。
氢化物 CH H S H O NaH
4 2 2
熔点/℃ -182.5 -85.5 0 800
下列说法正确的是
A.键角:H S<CH
2 4
B.CH 、H S、H O的熔点差异的主要原因是化学键键能不同
4 2 2
C.若NaH的晶胞参数为a pm,则其密度为 g·cm-3
D.NaH晶体中,Na+填充在H-围成的正八面体中心
13.某科研小组研究表明:臭氧-碱液法脱除废气中的NO是一种高效脱氮
的方法,其中臭氧氧化步骤涉及的反应有:
①NO(g)+O 3 (g) ⇌ NO 2 (g)+O 2 (g) ΔH<0
②2NO(g)+O 2 (g) ⇌ 2NO 2 (g) ΔH<0
③碱液吸收时发生反应2NO +2NaOH=NaNO +NaNO +H O
2 3 2 2在某反应器中以固定速率通入 NO和O ,分别在催化剂Ⅰ、催化剂Ⅱ作用
3
下发生上述反应,相同时间内测得O 的转化率与温度的关系如图所示。
3
下列说法错误的是
A.反应①的平衡常数:K(M)>K(N)
B.在T ℃、催化剂Ⅱ作用下,O 的平衡转化率为a%
1 3
C.催化剂Ⅰ的催化效果比催化剂Ⅱ的好
D.若n(NO )∶n(NaOH)=1∶1充分反应,所得溶液中存在c(Na+)<c(NO)
2
+c(OH-)+c(NO)
三、非选择题:本题共4小题,共57分。
14.(14分)硝酸钾在食品、化工、国防等多领域有广泛应用,受热易分解。
一种新型制备硝酸钾的工艺可通过多个内部循环实现节能减排,具体流程如
下:
回答下列问题:
(1)“转化1”中主要反应的离子方程式为__________;该工序不能控制温
度过高的原因为__________。
(2)“工序X”具体指__________。
(3)滤渣1的主要成分为__________(填化学式);“转化3”中,所加入滤渣
1的量常稍大于转化反应的理论值,其目的为__________。(4)已知:本流程条件下,K (CaCO )=4.9×10-9,则该实验条件下,100 g
sp 3
水中最多溶解CaCO 的质量约为__________g。
3
(5)“转化4”反应生成的气体产物的电子式为__________,写出该物质基
于其物理性质的用途__________(任写1种)。
15.(14分)氯化亚铜广泛用于有机合成、杀菌和化学分析,它是一种白色固
体,难溶于水和乙醇,可溶于氯离子浓度较大的体系,在潮湿空气中易水解和
氧化。学习小组在实验室中制备CuCl并测定产品纯度,进行如下实验探究。回
答下列问题:
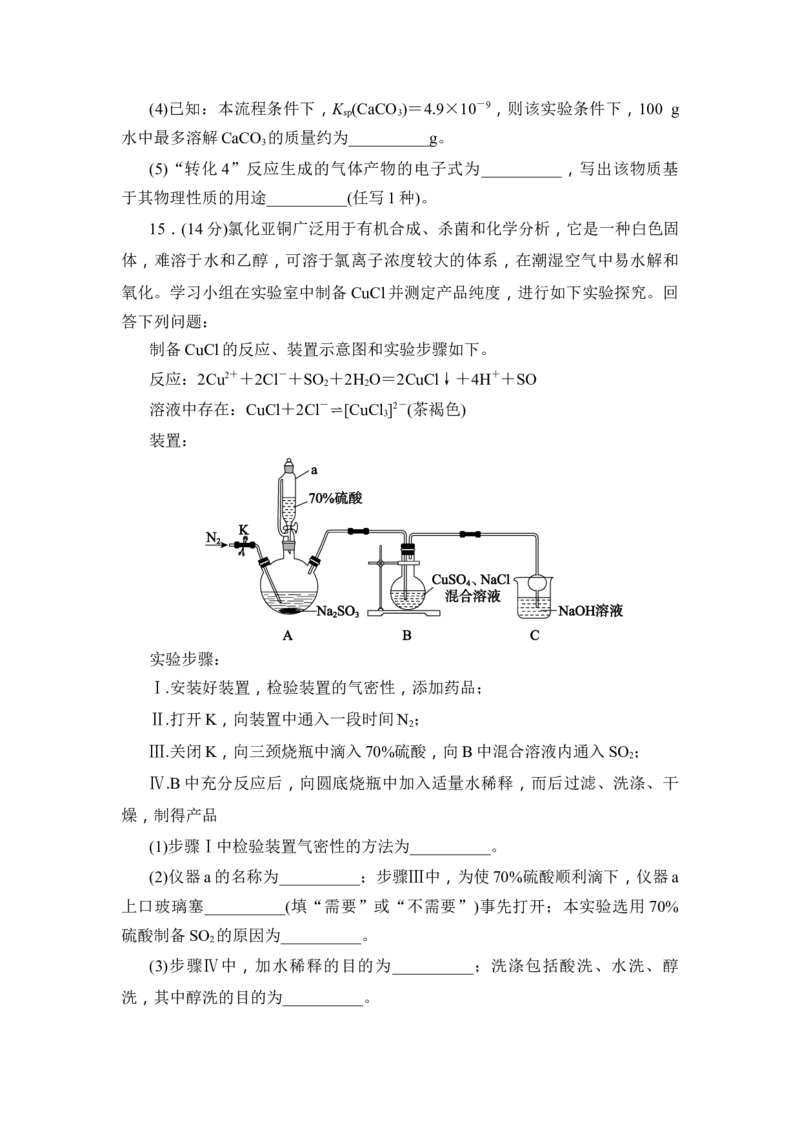
制备CuCl的反应、装置示意图和实验步骤如下。
反应:2Cu2++2Cl-+SO +2H O=2CuCl↓+4H++SO
2 2
溶液中存在:CuCl+2Cl- ⇌[CuCl
3
]2-(茶褐色)
装置:
实验步骤:
Ⅰ.安装好装置,检验装置的气密性,添加药品;
Ⅱ.打开K,向装置中通入一段时间N ;
2
Ⅲ.关闭K,向三颈烧瓶中滴入70%硫酸,向B中混合溶液内通入SO ;
2
Ⅳ.B中充分反应后,向圆底烧瓶中加入适量水稀释,而后过滤、洗涤、干
燥,制得产品
(1)步骤Ⅰ中检验装置气密性的方法为__________。
(2)仪器a的名称为__________;步骤Ⅲ中,为使70%硫酸顺利滴下,仪器a
上口玻璃塞__________(填“需要”或“不需要”)事先打开;本实验选用 70%
硫酸制备SO 的原因为__________。
2
(3)步骤Ⅳ中,加水稀释的目的为__________;洗涤包括酸洗、水洗、醇
洗,其中醇洗的目的为__________。(4)测定产品纯度:准确称取m g产品,加入足量FeCl 溶液;充分反应后滴
3
加指示剂,用 c mol·L-1 Ce(SO ) 标准溶液滴定生成的 Fe2+(还原产物为 Ce3
4 2
+),达到终点时消耗V mL标准液。
①产品中加入FeCl 溶液时,发生反应的离子方程式为__________。
3
②产品中CuCl的质量分数为__________。
16.(14分)当前,我国公布了实现“碳达峰、碳中和”目标的具体时间。因
此,含碳化合物的综合利用,有效缓解温室效应成为研究热点。回答下列问
题:
(1)二氧化碳与氢气催化重整可制备甲醇,涉及反应:
Ⅰ.CO 2 (g)+3H 2 (g) ⇌ CH 3 OH(g)+H 2 O(g) ΔH 1 =-49.5 kJ·mol-1
Ⅱ.CO 2 (g)+H 2 (g) ⇌ CO(g)+H 2 O(g) ΔH 2 =+40.9 kJ·mol-1
①CH 3 OH(g)+2CO 2 (g) ⇌ 3CO(g)+2H 2 O(g)的ΔH=________。
②相同温度下,向甲、乙两个恒容密闭容器中充入原料气,实验测得相关
信息如下表所示。
5 min末(未平衡) CHOH的
3
容器 容积/L 起始加料/mol
CO 转化率 平衡产率
2
甲 10 1 mol CO 、3 mol H α ω
2 2 1 1
1 mol CO 、3 mol
2
乙 10 α ω
2 2
H、0.2 mol CO
2
容器甲中,0~5 min 内的平均反应速率 v(H O)=__________(用代数式表
2
示);
α __________α (填“>”“<”或“=”,下同);ω __________ω ,判断
1 2 1 2
该条件下甲、乙容器中CH OH的平衡产率大小的理由为__________。
3
③已知:K 表示相对压力平衡常数,其表达式是在浓度平衡常数表达式
中,用相对分压代替浓度。气体的相对分压等于其分压除以 p (p =100 kPa)。
0 0
向恒容密闭容器中以物质的量之比为1∶3充入CO 和H ,测得反应前气体总压为
2 2
400 kPa,反应Ⅰ、Ⅱ的相对压力平衡常数的对数与温度的倒数的关系如图 1所
示。其中表示反应Ⅰ的相对压力平衡常数的对数与温度的倒数关系的曲线为
__________(填“L ”或“L ”);若M点对应温度下,甲醇气的平衡分压为80
1 2
kPa,则H 的平衡转化率为__________。
2图1 图2
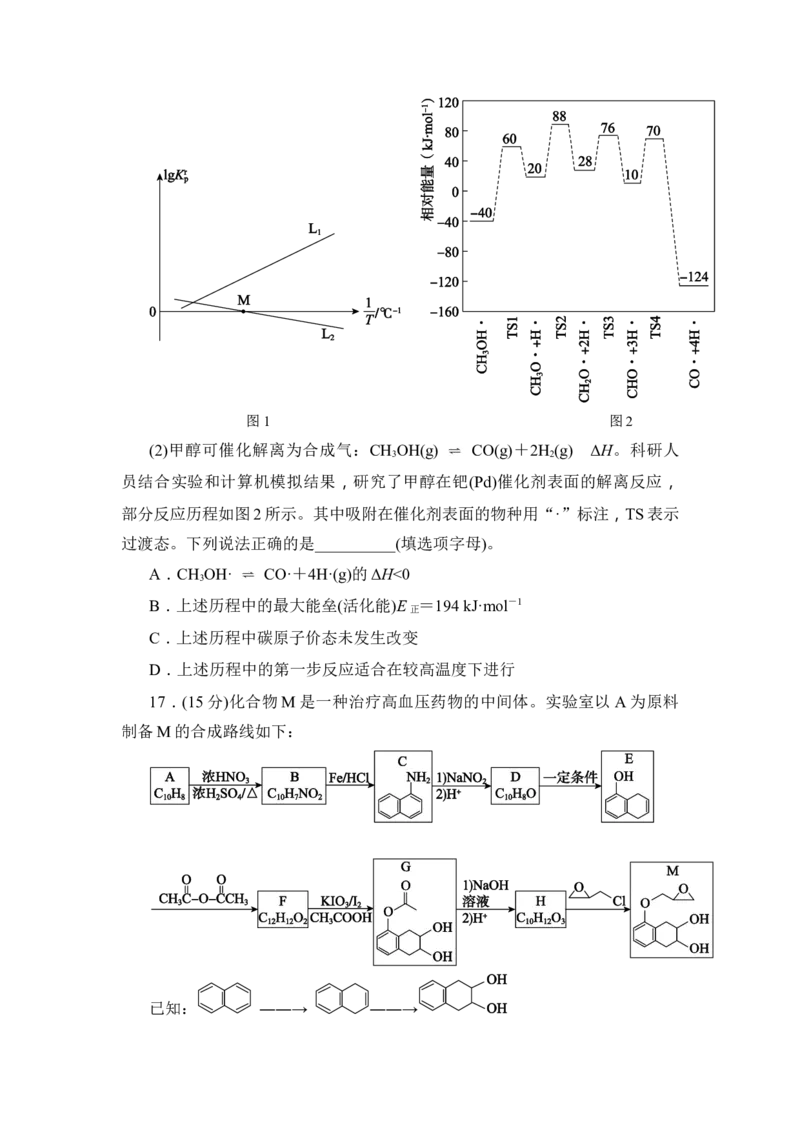
(2)甲醇可催化解离为合成气:CH 3 OH(g) ⇌ CO(g)+2H 2 (g) ΔH。科研人
员结合实验和计算机模拟结果,研究了甲醇在钯(Pd)催化剂表面的解离反应,
部分反应历程如图2所示。其中吸附在催化剂表面的物种用“·”标注,TS表示
过渡态。下列说法正确的是__________(填选项字母)。
A.CH 3 OH· ⇌ CO·+4H·(g)的ΔH<0
B.上述历程中的最大能垒(活化能)E =194 kJ·mol-1
正
C.上述历程中碳原子价态未发生改变
D.上述历程中的第一步反应适合在较高温度下进行
17.(15分)化合物M是一种治疗高血压药物的中间体。实验室以 A为原料
制备M的合成路线如下:
已知: ――→ ――→回答下列问题:
(1)A的结构简式为__________;由B生成C的反应类型为__________。
(2)D中官能团的名称为__________。
(3)由E生成F的反应方程式为__________;设计由E生成F、由G生成H
两步转化的目的为__________。
(4)由H生成M时,常加入适量的碱,所加碱的作用为__________;1个M
分子中含有手性碳的数目为__________。
(5)同时满足下列条件的H的同分异构体有__________种(不含立体异构)。
①苯环上含有两个取代基
②能与NaHCO 溶液反应生成气体
3
③能与FeCl 溶液发生显色反应
3
(6)参照上述合成路线和信息,以A和苯酚为原料(无机试剂任选),设计制
备 的合成路线__________。