文档内容
高频考点 19 化学反应中的能量变化图象
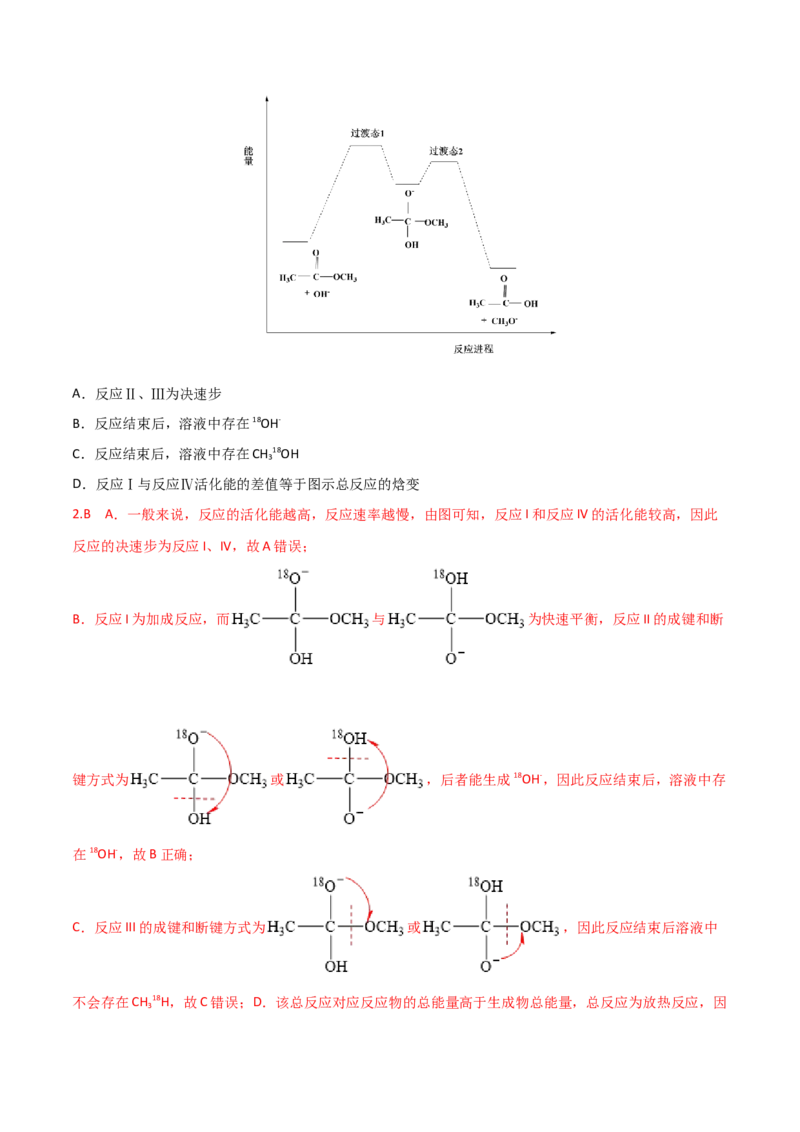
1.(双选)(2022·湖南卷)反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如下图所示:
下列有关四种不同反应进程的说法正确的是( )
A.进程Ⅰ是放热反应 B.平衡时P的产率:Ⅱ>Ⅰ
C.生成P的速率:Ⅲ>Ⅱ D.进程Ⅳ中,Z没有催化作用
1.AD A.由图中信息可知,进程Ⅰ中S的总能量大于产物P的总能量,因此进程I是放热反应,A说法正
确;B.进程Ⅱ中使用了催化剂X,但是催化剂不能改变平衡产率,因此在两个进程中平衡时P的产率相同,
B说法不正确;C.进程Ⅲ中由S•Y转化为P•Y的活化能高于进程Ⅱ中由S•X转化为P•X的活化能,由于这
两步反应分别是两个进程的决速步骤,因此生成P的速率为Ⅲ<Ⅱ,C说法不正确;D.由图中信息可知,
进程Ⅳ中S吸附到Z表面生成S•Z,然后S•Z转化为产物P•Z,由于P•Z没有转化为P+Z,因此,Z没有表
现出催化作用,D说法正确;综上所述,本题选AD。
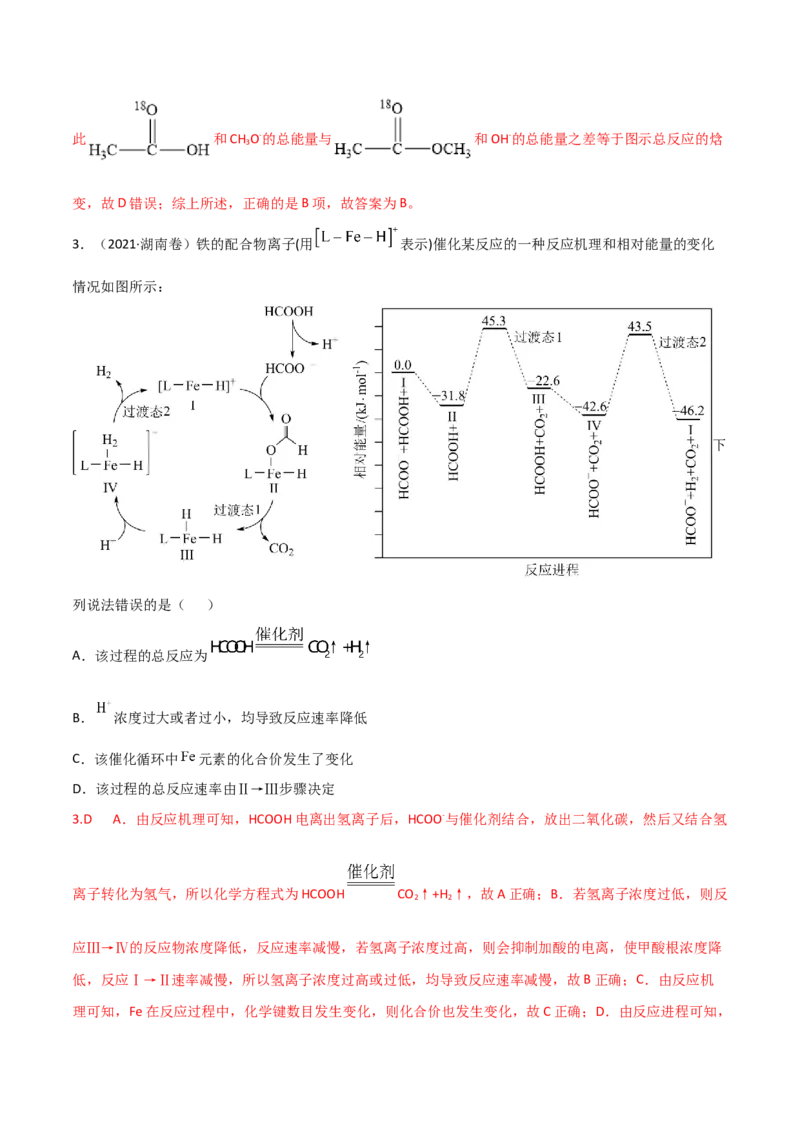
2.(2021·山东卷)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为:
+OH- +CH O-能量变化如图
3
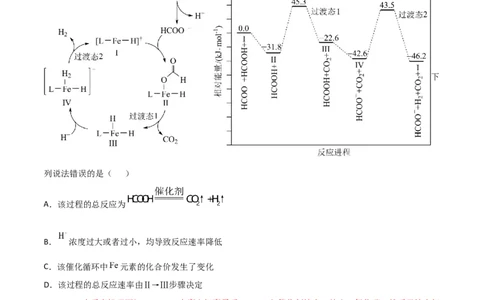
所示。已知 为快速平衡,下列说法正确的是( )A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CH 18OH
3
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
2.B A.一般来说,反应的活化能越高,反应速率越慢,由图可知,反应I和反应IV的活化能较高,因此
反应的决速步为反应I、IV,故A错误;
B.反应I为加成反应,而 与 为快速平衡,反应II的成键和断
键方式为 或 ,后者能生成18OH-,因此反应结束后,溶液中存
在18OH-,故B正确;
C.反应III的成键和断键方式为 或 ,因此反应结束后溶液中
不会存在CH 18H,故C错误;D.该总反应对应反应物的总能量高于生成物总能量,总反应为放热反应,因
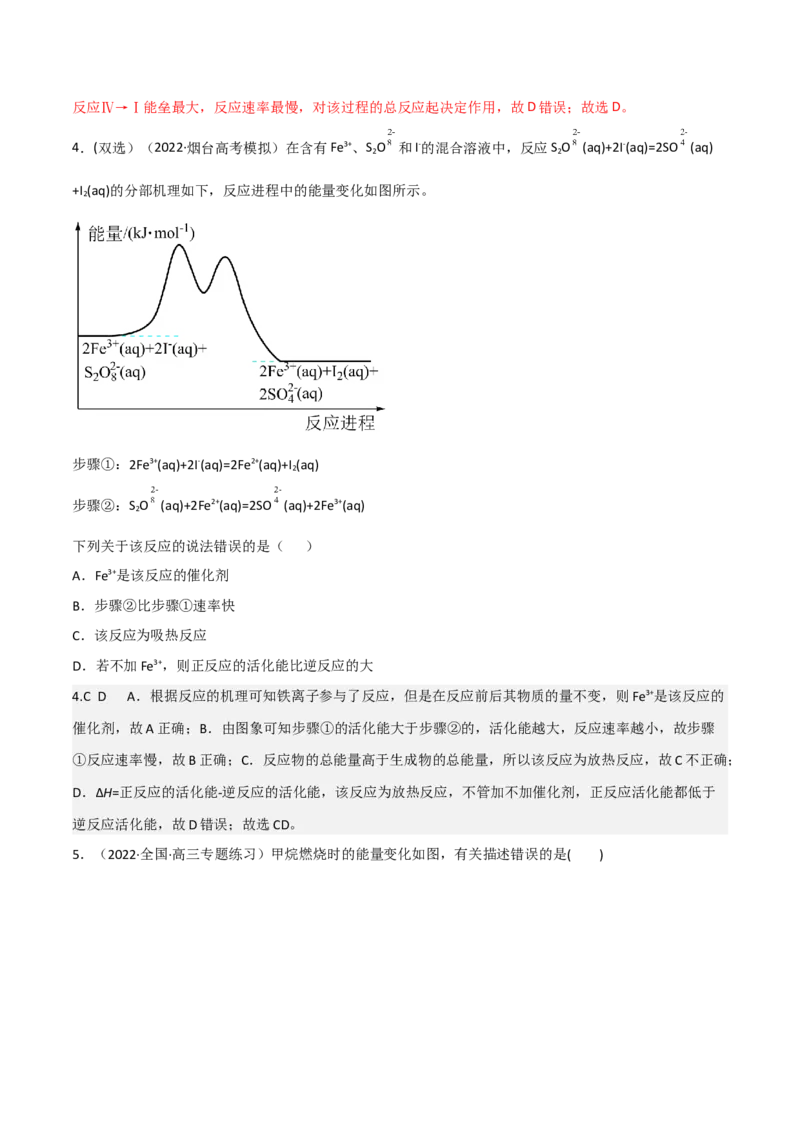
3此 和CH O-的总能量与 和OH-的总能量之差等于图示总反应的焓
3
变,故D错误;综上所述,正确的是B项,故答案为B。
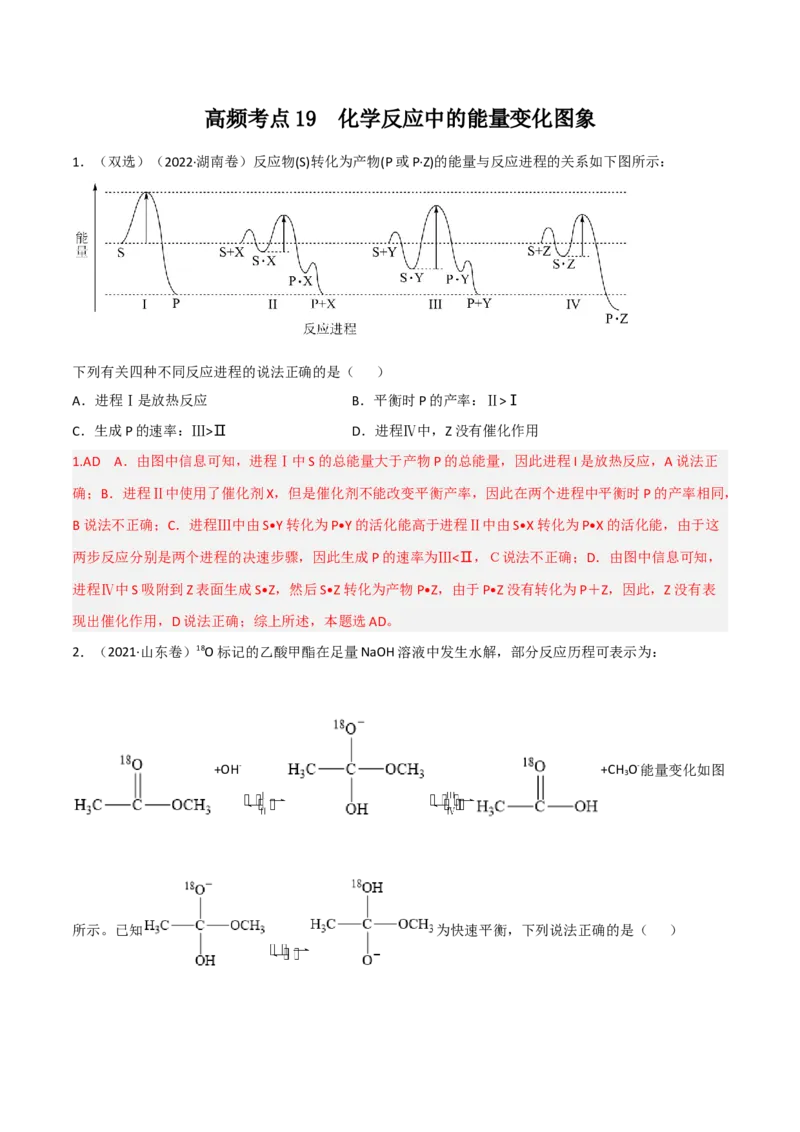
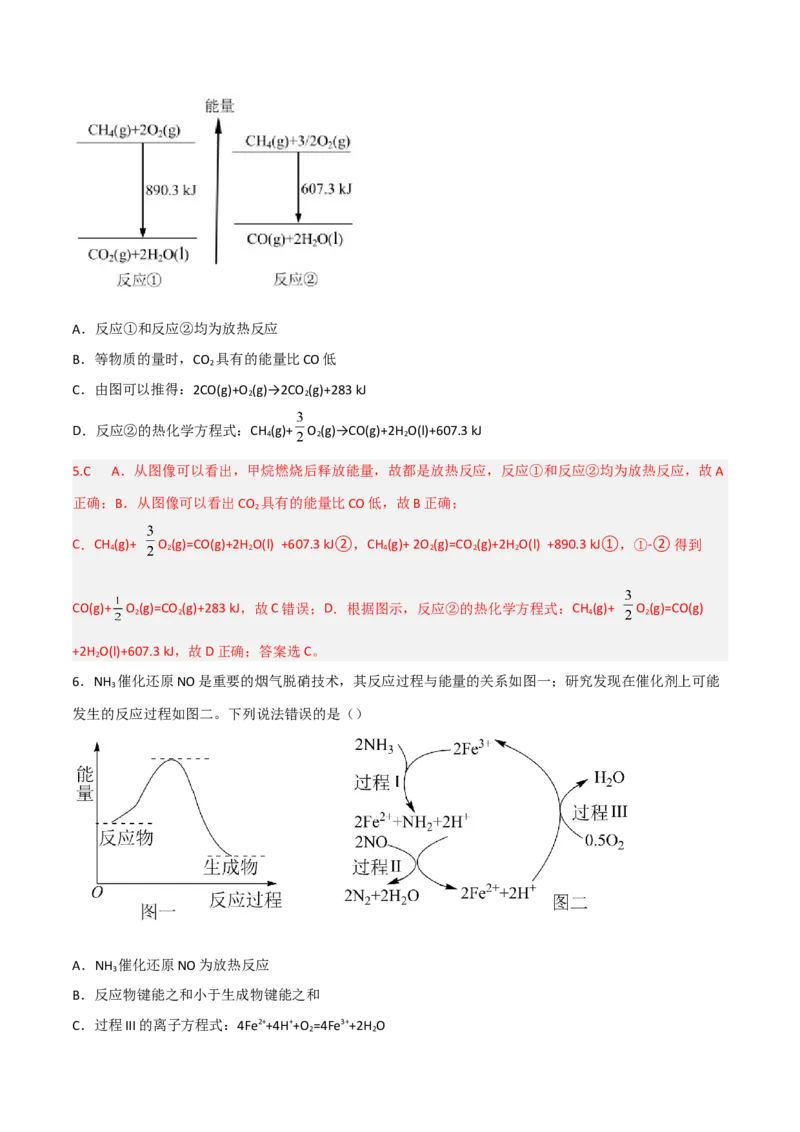
3.(2021·湖南卷)铁的配合物离子(用 表示)催化某反应的一种反应机理和相对能量的变化
情况如图所示:
下
列说法错误的是( )
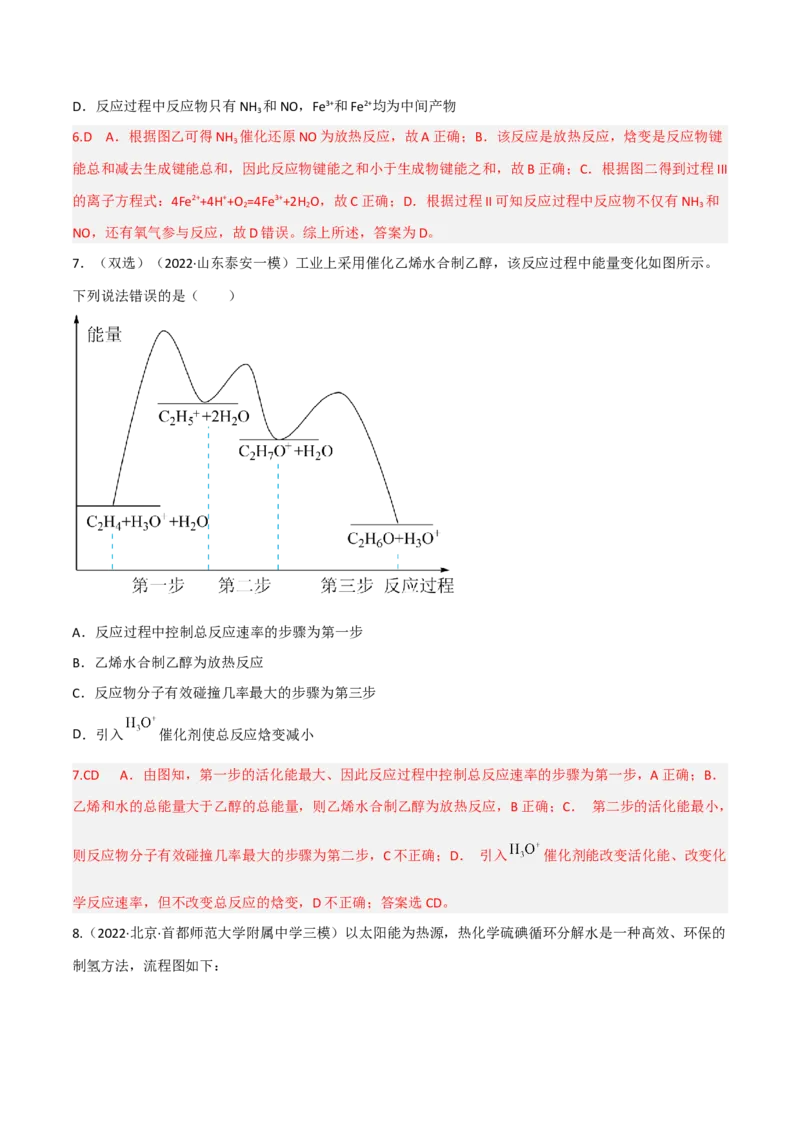
A.该过程的总反应为
B. 浓度过大或者过小,均导致反应速率降低
C.该催化循环中 元素的化合价发生了变化
D.该过程的总反应速率由Ⅱ→Ⅲ步骤决定
3.D A.由反应机理可知,HCOOH电离出氢离子后,HCOO-与催化剂结合,放出二氧化碳,然后又结合氢
离子转化为氢气,所以化学方程式为HCOOH CO ↑+H ↑,故A正确;B.若氢离子浓度过低,则反
2 2
应Ⅲ→Ⅳ的反应物浓度降低,反应速率减慢,若氢离子浓度过高,则会抑制加酸的电离,使甲酸根浓度降
低,反应Ⅰ→Ⅱ速率减慢,所以氢离子浓度过高或过低,均导致反应速率减慢,故B正确;C.由反应机
理可知,Fe在反应过程中,化学键数目发生变化,则化合价也发生变化,故C正确;D.由反应进程可知,反应Ⅳ→Ⅰ能垒最大,反应速率最慢,对该过程的总反应起决定作用,故D错误;故选D。
4.(双选)(2022·烟台高考模拟)在含有Fe3+、S O 和I-的混合溶液中,反应S O (aq)+2I-(aq)=2SO (aq)
2 2
+I (aq)的分部机理如下,反应进程中的能量变化如图所示。
2
步骤①:2Fe3+(aq)+2I-(aq)=2Fe2+(aq)+I (aq)
2
步骤②:S O (aq)+2Fe2+(aq)=2SO (aq)+2Fe3+(aq)
2
下列关于该反应的说法错误的是( )
A.Fe3+是该反应的催化剂
B.步骤②比步骤①速率快
C.该反应为吸热反应
D.若不加Fe3+,则正反应的活化能比逆反应的大
4.C D A.根据反应的机理可知铁离子参与了反应,但是在反应前后其物质的量不变,则Fe3+是该反应的
催化剂,故A正确;B.由图象可知步骤①的活化能大于步骤②的,活化能越大,反应速率越小,故步骤
①反应速率慢,故B正确;C.反应物的总能量高于生成物的总能量,所以该反应为放热反应,故C不正确;
D.ΔH=正反应的活化能-逆反应的活化能,该反应为放热反应,不管加不加催化剂,正反应活化能都低于
逆反应活化能,故D错误;故选CD。
5.(2022·全国·高三专题练习)甲烷燃烧时的能量变化如图,有关描述错误的是( )A.反应①和反应②均为放热反应
B.等物质的量时,CO 具有的能量比CO低
2
C.由图可以推得:2CO(g)+O (g)→2CO (g)+283 kJ
2 2
D.反应②的热化学方程式:CH (g)+ O (g)→CO(g)+2H O(l)+607.3 kJ
4 2 2
5.C A.从图像可以看出,甲烷燃烧后释放能量,故都是放热反应,反应①和反应②均为放热反应,故A
正确;B.从图像可以看出CO 具有的能量比CO低,故B正确;
2
C.CH (g)+ O (g)=CO(g)+2H O(l) +607.3 kJ②,CH (g)+ 2O (g)=CO (g)+2H O(l) +890.3 kJ①,①-②得到
4 2 2 4 2 2 2
CO(g)+ O (g)=CO (g)+283 kJ,故C错误;D.根据图示,反应②的热化学方程式:CH (g)+ O (g)=CO(g)
2 2 4 2
+2H O(l)+607.3 kJ,故D正确;答案选C。
2
6.NH 催化还原NO是重要的烟气脱硝技术,其反应过程与能量的关系如图一;研究发现在催化剂上可能
3
发生的反应过程如图二。下列说法错误的是()
A.NH 催化还原NO为放热反应
3
B.反应物键能之和小于生成物键能之和
C.过程III的离子方程式:4Fe2++4H++O =4Fe3++2H O
2 2D.反应过程中反应物只有NH 和NO,Fe3+和Fe2+均为中间产物
3
6.D A.根据图乙可得NH 催化还原NO为放热反应,故A正确;B.该反应是放热反应,焓变是反应物键
3
能总和减去生成键能总和,因此反应物键能之和小于生成物键能之和,故B正确;C.根据图二得到过程III
的离子方程式:4Fe2++4H++O =4Fe3++2H O,故C正确;D.根据过程II可知反应过程中反应物不仅有NH 和
2 2 3
NO,还有氧气参与反应,故D错误。综上所述,答案为D。
7.(双选)(2022·山东泰安一模)工业上采用催化乙烯水合制乙醇,该反应过程中能量变化如图所示。
下列说法错误的是( )
A.反应过程中控制总反应速率的步骤为第一步
B.乙烯水合制乙醇为放热反应
C.反应物分子有效碰撞几率最大的步骤为第三步
D.引入 催化剂使总反应焓变减小
7.CD A.由图知,第一步的活化能最大、因此反应过程中控制总反应速率的步骤为第一步,A正确;B.
乙烯和水的总能量大于乙醇的总能量,则乙烯水合制乙醇为放热反应,B正确;C. 第二步的活化能最小,
则反应物分子有效碰撞几率最大的步骤为第二步,C不正确;D. 引入 催化剂能改变活化能、改变化
学反应速率,但不改变总反应的焓变,D不正确;答案选CD。
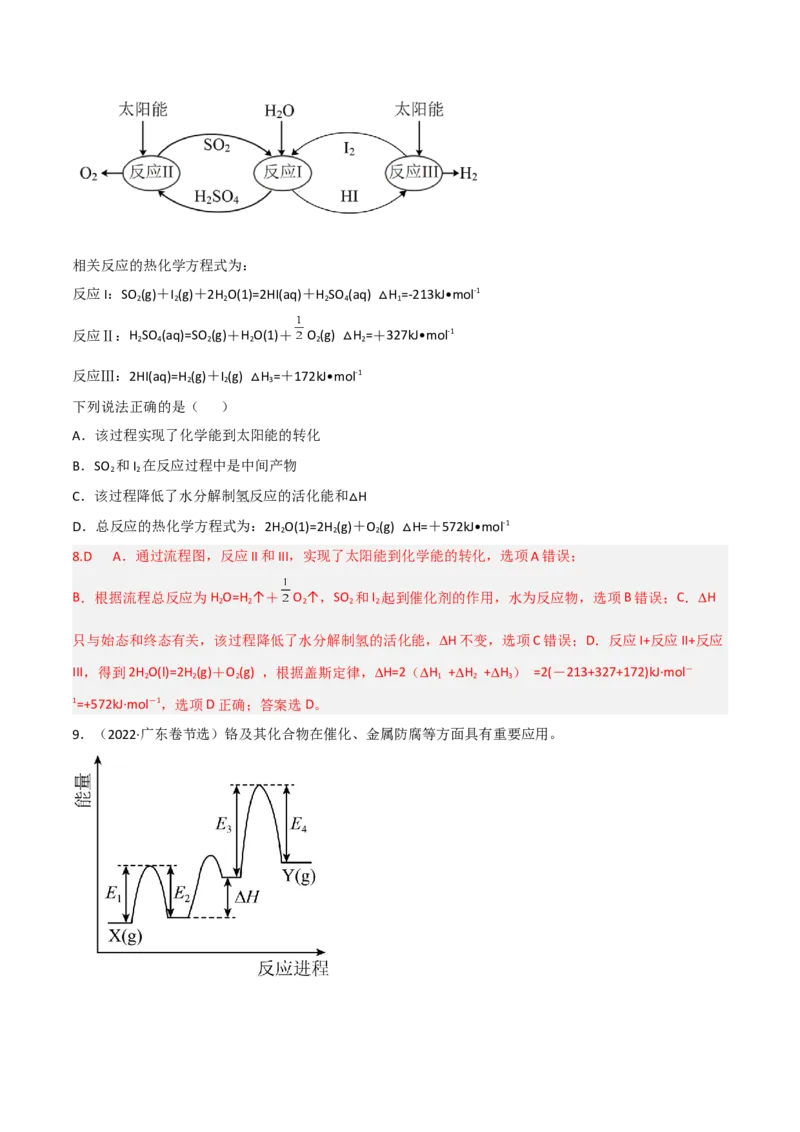
8.(2022·北京·首都师范大学附属中学三模)以太阳能为热源,热化学硫碘循环分解水是一种高效、环保的
制氢方法,流程图如下:相关反应的热化学方程式为:
反应I:SO (g)+I (g)+2H O(1)=2HI(aq)+H SO (aq) H =-213kJ•mol-1
2 2 2 2 4 1
△
反应Ⅱ:H SO (aq)=SO (g)+H O(1)+ O (g) H =+327kJ•mol-1
2 4 2 2 2 2
△
反应Ⅲ:2HI(aq)=H (g)+I (g) H =+172kJ•mol-1
2 2 3
下列说法正确的是( ) △
A.该过程实现了化学能到太阳能的转化
B.SO 和I 在反应过程中是中间产物
2 2
C.该过程降低了水分解制氢反应的活化能和 H
D.总反应的热化学方程式为:2H O(1)=2H (g)△+O (g) H=+572kJ•mol-1
2 2 2
8.D A.通过流程图,反应II和III,实现了太阳能到化△学能的转化,选项A错误;
B.根据流程总反应为H O=H ↑+ O ↑,SO 和I 起到催化剂的作用,水为反应物,选项B错误;C.H
2 2 2 2 2
只与始态和终态有关,该过程降低了水分解制氢的活化能,H不变,选项C错误;D.反应I+反应II+反应
III,得到2H O(l)=2H (g)+O (g) ,根据盖斯定律,H=2(H +H +H ) =2(-213+327+172)kJ·mol-
2 2 2 1 2 3
1=+572kJ·mol-1,选项D正确;答案选D。
9.(2022·广东卷节选)铬及其化合物在催化、金属防腐等方面具有重要应用。(1)催化剂 可由 加热分解制备,反应同时生成无污染气体。
①完成化学方程式: _______ _______。
② 催化丙烷脱氢过程中,部分反应历程如图, 过程的焓变为_______(列式表示)。
③ 可用于 的催化氧化。设计从 出发经过3步反应制备 的路线_______(用“→”表示含
氮物质间的转化);其中一个有颜色变化的反应的化学方程式为_______。
9.(1) N ↑ 4H O (E -E )+ΔH+(E -E ) 2NO+O =2NO
2 2 1 2 3 4 2 2
解析:(1)① 分解过程中,生成Cr O 和无污染气体,根据元素守恒可知,其余生成物为N 、
2 3 2
H O,根据原子守恒可知反应方程式为 ,故答案为:N ↑;4H O。
2 2 2
②设反应过程中第一步的产物为M,第二步的产物为N,则X→M ΔH =(E -E ),M→N ΔH =ΔH,N→Y
1 1 2 2
ΔH =(E -E ) ,根据盖斯定律可知,X(g)→Y(g)的焓变为ΔH +ΔH +ΔH =(E -E )+ΔH+(E -E ),故答案为:(E -
3 3 4 1 1 2 3 1 2 3 4 1
E )+ΔH+(E -E )。
2 3 4
③NH 在Cr O 作催化剂条件下,能与O 反应生成NO,NO与O 反应生成红棕色气体NO ,NO 与H O反
3 2 3 2 2 2 2 2
应生成HNO 和NO,若同时通入O ,可将氮元素全部氧化为HNO ,因此从NH 出发经过3步反应制备
3 2 3 3
HNO 的路线为 ;其中NO反应生成NO 过程中,气体颜色发生变
3 2
化,其反应方程式为2NO+O =2NO ,故答案为: ;
2 2
2NO+O =2NO 。
2 2