文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(河北专用)
黄金卷03
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64 Ce 140
第Ⅰ卷
一、单项选择题:共14题,每题3分,共42分。每题只有一个选项最符合题意。
1.化学与社会发展和人类进步息息相关。下列说法错误的是
A.华为Mate60pro系列“争气机”的芯片材料主要为晶体硅
B.用机械剥离法从石墨中分离出的石墨烯能导电,石墨烯与金刚石互为同素异形体
C.国产飞机C919用到的氮化硅陶瓷是新型无机非金属材料
D.维生素C可用作水果罐头的抗氧化剂是由于其难以被氧化
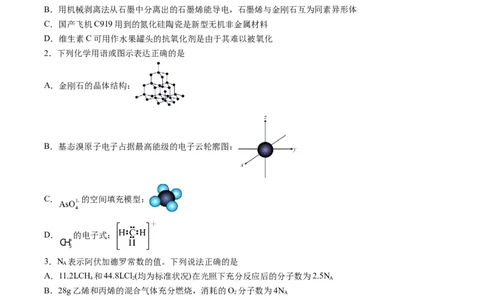
2.下列化学用语或图示表达正确的是
A.金刚石的晶体结构:
B.基态溴原子电子占据最高能级的电子云轮廓图:
C. 的空间填充模型:
D. 的电子式:
3.N 表示阿伏加德罗常数的值。下列说法正确的是
A
A.11.2LCH 和44.8LCl (均为标准状况)在光照下充分反应后的分子数为2.5N
4 2 A
B.28g乙烯和丙烯的混合气体充分燃烧,消耗的O 分子数为4N
2 A
C.1mol14C16O(一氧化碳)中含有15N 个中子
A
D.1molNaHSO 固体中含离子总数为3N
4 A
4.下列反应的离子方程式正确的是
A.向NaHSO 中滴加少量Ba(HCO ) 溶液:
4 3 2
B.向有AgCl沉淀的溶液中滴加氨水,沉淀消失:
C.向FeI 溶液中通入一定量氯气,测得有50%的Fe2+被氧化:
2
D.NaHCO 的水解:
3
5.KMnO 是一种常用的氧化剂,某实验小组利用Cl 氧化KMnO 制备KMnO 的装置如图所示(夹持装置
4 2 2 4 4略)。
已知:KMnO 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
2 4
。
下列说法错误的是
A.试剂X可以是漂白粉或MnO
2
B.装置连接顺序是
C.装置C中每生成1 mol KMnO,消耗Cl 的物质的量大于0.5 mol
4 2
D.若去掉装置A,会导致KMnO 产率降低
4
6.实验探究是化学学习的方法之一、根据下列实验设计的现象所得实验结论正确的是
选项 实验设计 现象 实验结论
在坩埚中加入16.4g ,加热一段时 加热后坩埚内固体为
A 质量为12.8g
和 混合物
间,在干燥器中冷却,称量剩余固体质量
产生白色沉淀,加
B 向鸡蛋清溶液中滴入几滴硫酸铜溶液 蛋白质发生了变性
水后沉淀不溶解
分别用蒸馏水、 溶液喷洒甲、乙 喷洒 溶液的纸
C 能促进纸张的老化
两张白纸,静置、干燥 张老化明显
烧瓶中有红棕色气 木炭具有还原性,能还
D 在烧瓶中加入木炭颗粒与浓硝酸,然后加热
体产生 原
7.X、Y、Z、W为原子序数依次增大的短周期主族元素,X、Y、Z位于同周期且相邻,X与W同族,W
的核外电子总数等于X和Z的核外电子总数之和。下列说法正确的是
A.元素的第一电离能:
B.简单氢化物的稳定性:
C. 中有 键
D. 的空间结构为V形,属于含有极性键的极性分子
8.一种由Cu、In、Te组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,晶体中Te原
子填充在Cu、In围成的四面体空隙中,A点、B点原子的分数坐标分别为 、 ,下列说法
错误的是A.该晶体的化学式为
B.C点原子的分数坐标为
C.晶胞中四面体空隙的占有率为50%
D.晶胞中C、D间距离
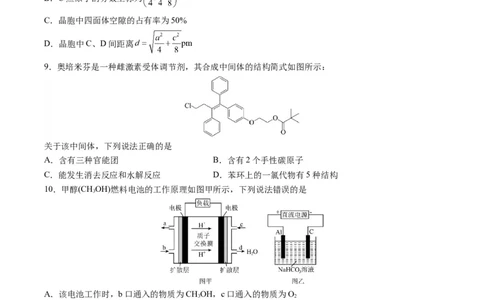
9.奥培米芬是一种雌激素受体调节剂,其合成中间体的结构简式如图所示:
关于该中间体,下列说法正确的是
A.含有三种官能团 B.含有2个手性碳原子
C.能发生消去反应和水解反应 D.苯环上的一氯代物有5种结构
10.甲醇(CHOH)燃料电池的工作原理如图甲所示,下列说法错误的是
3
A.该电池工作时,b口通入的物质为CHOH,c口通入的物质为O
3 2
B.该电池负极的电极反应式为
C.精炼铜时,粗铜应与甲醇燃料电池的正极相连,阴极的电极反应式为 ,电解质溶液为
CuSO 溶液
4
D.用该燃料电池作电源,在实验室中模拟铝制品表面“钝化”处理的过程(如图乙),阳极电极反应为
11.A、B、C、D、E是原子序数依次增大的五种短周期元素且B、C元素相邻,D元素原子的最外层电子
数与核外电子层数相等;A元素可以与B、C、E元素分别形成甲、乙、丙三种物质且甲、乙均为10电子
化合物,丙为18电子化合物。已知:甲+E=丙+B ,甲+丙=丁。下列说法一定正确的是
2 2A.离子半径:E>D>C>B
B.常温下,含D元素的盐溶液pH<7
C.丁物质均由非金属元素组成,只含共价键
D.一元弱酸AEC,其结构式为A-C-E
12.锌是重要的金属材料。以硫化锌精矿(主要含有FeS、CuS等杂质)为原料制备单质锌的工业流程如图所
示,下列说法不正确的是
已知:金属阳离子在阴极的放电顺序和离子浓度有关
A.HO 反应后生成HO
2 2 2
B.烟气主要含 可用钙基固硫法处理
C.电解 溶液时,阴极发生还原反应的是锌离子
D.进一步净化过程可投入铁粉去除Cu
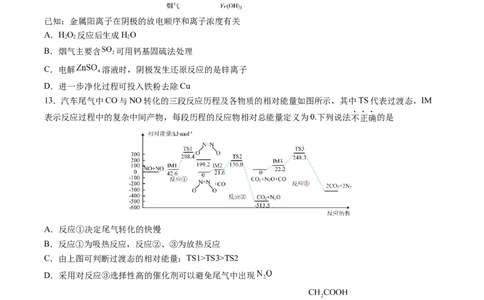
13.汽车尾气中CO与NO转化的三段反应历程及各物质的相对能量如图所示,其中TS代表过渡态,IM
表示反应过程中的复杂中间产物,每段历程的反应物相对总能量定义为0.下列说法不正确的是
A.反应①决定尾气转化的快慢
B.反应①为吸热反应,反应②、③为放热反应
C.由上图可判断过渡态的相对能量:TS1>TS3>TS2
D.采用对反应③选择性高的催化剂可以避免尾气中出现
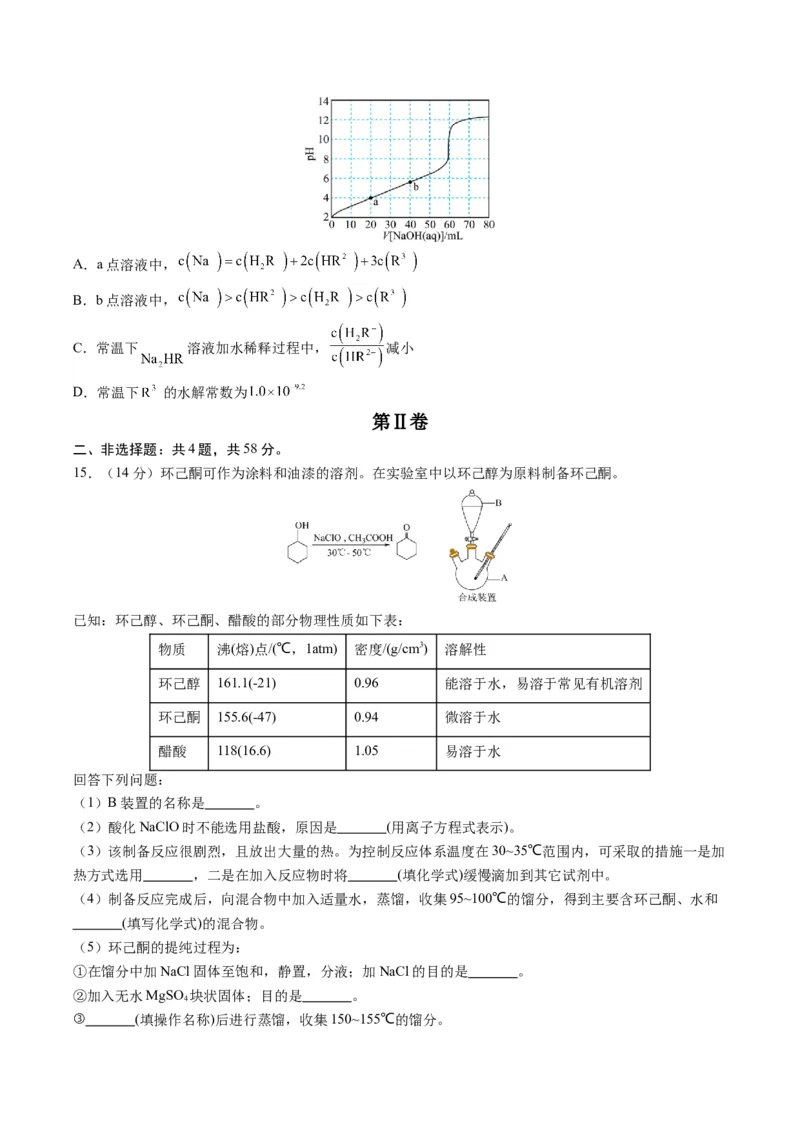
14.柠檬酸是番茄中最常见的天然酸性物质,其分子结构简式为 (用 表示)。常温
下,用 溶液滴定 溶液的滴定曲线如图所示。已知常温下柠
檬酸的电离常数为: 。下列叙述正确的是A.a点溶液中,
B.b点溶液中,
C.常温下 溶液加水稀释过程中, 减小
D.常温下 的水解常数为
第Ⅱ卷
二、非选择题:共4题,共58分。
15.(14分)环己酮可作为涂料和油漆的溶剂。在实验室中以环己醇为原料制备环己酮。
已知:环己醇、环己酮、醋酸的部分物理性质如下表:
物质 沸(熔)点/(℃,1atm) 密度/(g/cm3) 溶解性
环己醇 161.1(-21) 0.96 能溶于水,易溶于常见有机溶剂
环己酮 155.6(-47) 0.94 微溶于水
醋酸 118(16.6) 1.05 易溶于水
回答下列问题:
(1)B装置的名称是 。
(2)酸化NaClO时不能选用盐酸,原因是 (用离子方程式表示)。
(3)该制备反应很剧烈,且放出大量的热。为控制反应体系温度在30~35℃范围内,可采取的措施一是加
热方式选用 ,二是在加入反应物时将 (填化学式)缓慢滴加到其它试剂中。
(4)制备反应完成后,向混合物中加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮、水和
(填写化学式)的混合物。
(5)环己酮的提纯过程为:
①在馏分中加NaCl固体至饱和,静置,分液;加NaCl的目的是 。
②加入无水MgSO 块状固体;目的是 。
4
③ (填操作名称)后进行蒸馏,收集150~155℃的馏分。(6)数据处理。反应开始时加入8.4mL(0.08mol)环己醇,20mL冰醋酸和过量的NaClO溶液。实验结束后
收集到产品0.06mol,则该合成反应的产率为 。合成产品中主要杂质有 。
16.(14分)一种用方铅矿(PbS,含少量FeS)和软锰矿(MnO ,含少量铁、锌的氧化物)联合制备PbSO 和
2 4
MnO 的工艺流程如下:
3 4
已知:(1)PbCl 难溶于冷水,易溶于热水;
2
(2)25℃时,部分难溶物的K
sp
物质 FeS ZnS MnS PbS PbCl PbSO
2 4
K 6.0×10-18 1.2×10-23 2×10-13 8×10-28 1.6×10-5 1.6×10-8
sp
回答下列问题:
(1)“浸取”中,加入饱和NaCl溶液的作用是 。
(2)滤液X中的金属阳离子主要有Mn2+、Zn2+、Pb2+、Fe2+。加入NaS调pH时,杂质离子的沉淀顺序是
2
。
(3)“转化”环节中,当溶液中 时,c(Cl-)= mol/L。流程中,可循环
利用的物质是 (填化学式)。
(4)pH=8.5时,反应温度对MnO 的纯度和产率影响如图所示:
3 4
①写出生成MnO 的离子方程式 。
3 4
②温度高于50℃,MnO 产率下降的主要原因是 。
3 4
(5)已知中心离子或原子上含有未成对电子的物质均有顺磁性。研究表明,MnO 的结构可表
3 4
示为如图所示,则MnO 的简单氧化物形式可写作 ,MnO (填“有”或
3 4 3 4
“无”)顺磁性。
17.(15分)甲酸甲酯(HCOOCH )是一种重要的有机合成中间体,可通过甲醇催化脱氢法制备,其工艺过
3
程包含以下反应:
反应Ⅰ:2CHOH(g)=HCOOCH (g)+2H(g) K, H=+51.2kJ•mol-1
3 3 2 1 1
△反应Ⅱ:CHOH(g)=CO(g)+2H (g) K, H=+90.1kJ•mol-1
3 2 2 2
回答下列问题:
△
(1)反应HCOOCH (g)=2CO(g)+2H(g)的 H= kJ•mol-1,K= (用K、K 表示)。
3 2 3 3 1 2
(2)对于反应Ⅰ:增大压强,平衡 移动(填“向左”“向右”或“不”)。保持压强不变,要缩短
△
反应达到平衡的时间,可采取的措施是 、 。
(3)在400kPa、铜基催化剂存在下,向密闭容器中通入CHOH进行Ⅰ、Ⅱ两个反应。体系中气体平衡组
3
成比例(物质的量分数)随温度变化的理论计算结果如图所示。
①随温度升高,CHOH的平衡组成比例呈现如图所示趋势的原因是 。
3
②550K时,反应2CHOH(g)=HCOOCH (g)+2H(g)的平衡常数K= kPa,CHOH的平衡转化率为
3 3 2 p 3
。
③研究表明,在700K以后升高体系温度,HCOOCH 的产率下降,可能的原因是 。
3
18.(15分)化合物H是一种用于合成γ-分泌调节剂的药物中间体,其合成路线流程图如图:
(1)A中除羟基外还含有官能团的名称为 、 。
(2)B→C的反应类型为 。
(3)写出C→D的化学反应方程式: 。
(4)满足下列条件的C的同分异构体有 种。
①含有苯环,苯环上有三个取代基,其中氨基只与苯环直接相连;
②与氯化铁溶液反应显紫色,与NaHCO 溶液反应有气体产生。
3
(5)写出同时满足下列条件的C的一种同分异构体的结构简式: 。
①含有苯环,且分子中有一个手性碳原子;
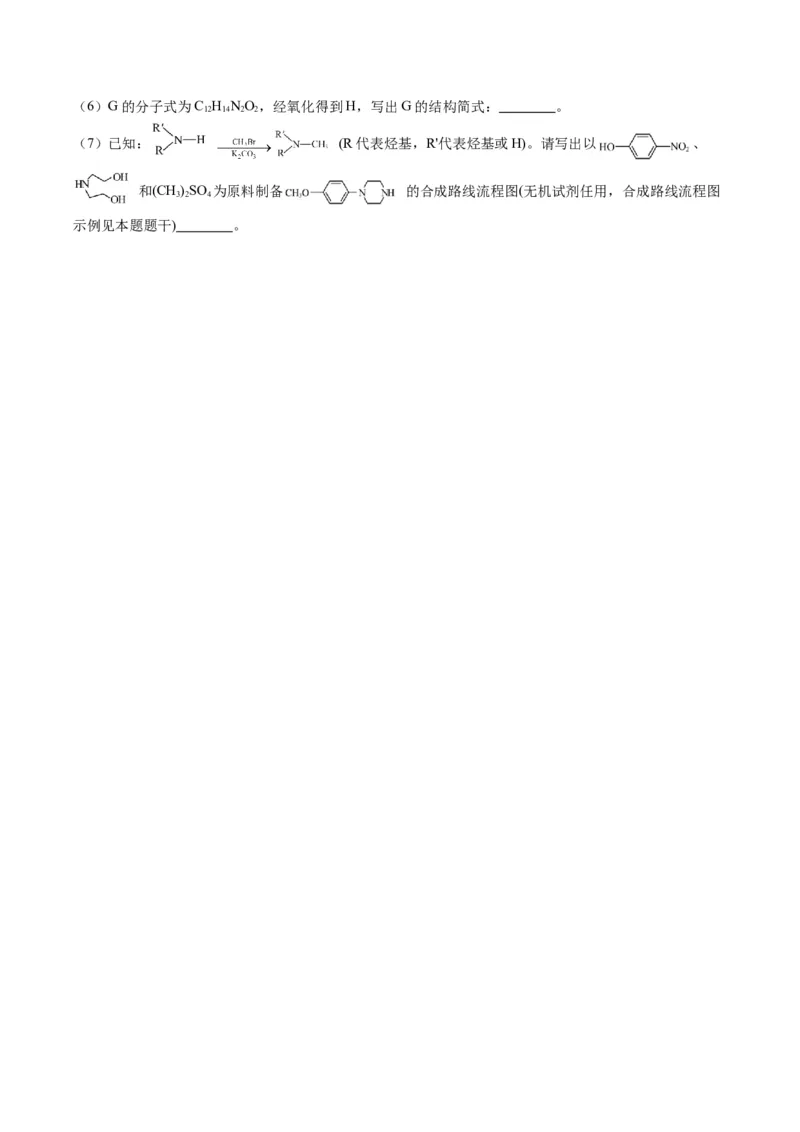
②能发生水解反应,水解产物之一是α-氨基酸,另一水解产物分子中只有2种不同化学环境的氢。(6)G的分子式为C H NO,经氧化得到H,写出G的结构简式: 。
12 14 2 2
(7)已知: (R代表烃基,R'代表烃基或H)。请写出以 、
和(CH)SO 为原料制备 的合成路线流程图(无机试剂任用,合成路线流程图
3 2 4
示例见本题题干) 。