文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(上海专
用)
黄金卷05
(考试时间:60分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64
一、海洋中的氮循环(本题共21分)
氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。
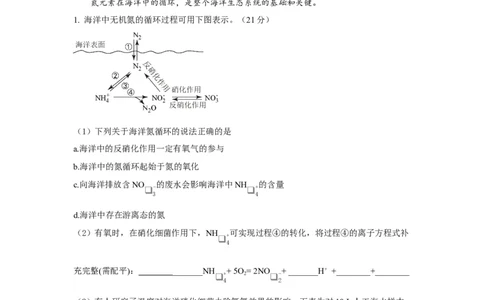
1. 海洋中无机氮的循环过程可用下图表示。(21分)
(1)下列关于海洋氮循环的说法正确的是
a.海洋中的反硝化作用一定有氧气的参与
b.海洋中的氮循环起始于氮的氧化
c.向海洋排放含NO 的废水会影响海洋中NH 的含量
- +
❑ ❑
3 4
d.海洋中存在游离态的氮
(2)有氧时,在硝化细菌作用下,NH 可实现过程④的转化,将过程④的离子方程式补
+
❑
4
充完整(需配平): _______NH + 5O = 2NO + _______H+ +________+________
+ 2 -
❑ ❑
4 2
(3)有人研究了温度对海洋硝化细菌去除氨氮效果的影响,下表为对10 L人工海水样本
的监测数据:
处理24 h 处理48 h
温度/℃ 样本氨氮含量/mg
氨氮含量/mg 氨氮含量/mg
20 1008 838 788
25 1008 757 46830 1008 798 600
40 1008 977 910
硝化细菌去除氨氮的最佳反应温度是 ,在最佳反应温度时,48 h内去除氨氮反
应的平均速率是 mg/(L·h)。
(4)海洋中的氮循环起始于氮的固定,氮的固定是几百年来科学家一直研究的课题。下表
列举了不同温度下大气固氮和工业固氮的部分K值。
大气固氮 工业固氮
反应 N 2 (g)+O 2 (g) ⇌ N 2 (g)+3H 2 (g) ⇌
2NO(g) 2NH (g)
3
温度/℃ 27 2000 25 400 450
K 3.84×10-31 0.1 5×108 0.507 0.152
分析数据可知:大气固氮反应属于 (填“吸热”或“放热”)反应。从平衡视角
考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原
因 。
(5)25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减
小,主要原因是(填序号) 。
a.氨水与氯化铵发生化学反应
b.氯化铵溶液水解显酸性,增加了c(H+)
c.铵根离子浓度增大,抑制了氨水的电离,使c(OH―)减小
(6)室温下,如果将0.1mol NH Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损
4
失), 、 和 三种粒子的物质的量之和等于0.1mol。
二、甲烷与碳中和(本题共18分)
甲烷(CH)是仅次于二氧化碳(CO)的全球第二大温室气体,比二氧化碳在大气中
4 2
更加活跃。全球大气中的甲烷属于痕量气体,其排放量的微小增加将会导致大气中甲烷浓
度的明显升高。
2.新能源是未来能源发展的方向,积极发展氢能是实现“碳达峰、碳中和”的重要举措。
(1)近年来CH-HO催化重整制氢是氢能源获取的重要途径,主要反应如下:(18分)
4 2
反应I:CH(g)+HO(g)❑3H(g)+CO(g) ΔH
4 2 2 1
⇌
反应II:CO(g)+HO(g)❑H(g)+CO (g) ΔH
2 2 2 2
⇌反应III:CH(g)+2HO(g)❑4H(g)+CO (g) ΔH
4 2 2 2 3
⇌
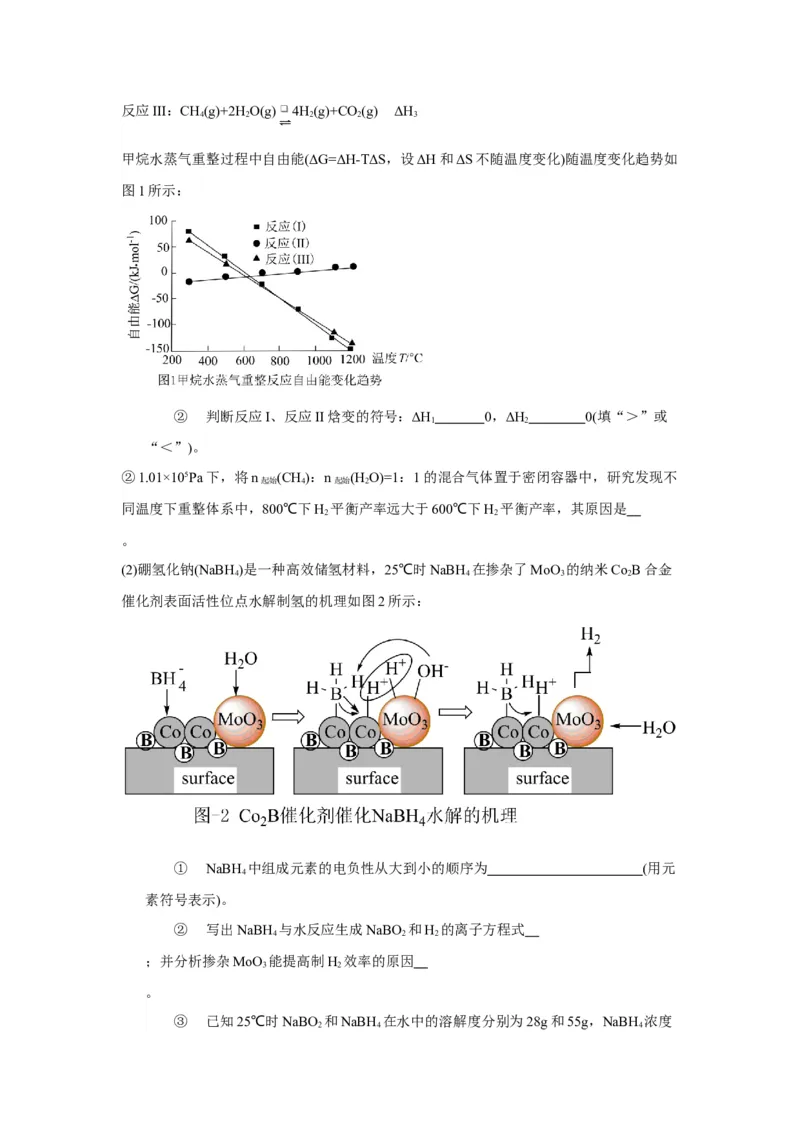
甲烷水蒸气重整过程中自由能(ΔG=ΔH-TΔS,设ΔH和ΔS不随温度变化)随温度变化趋势如
图1所示:
② 判断反应I、反应II焓变的符号:ΔH 0,ΔH 0(填“>”或
1 2
“<”)。
②1.01×105Pa下,将n (CH):n (H O)=1:1的混合气体置于密闭容器中,研究发现不
起始 4 起始 2
同温度下重整体系中,800℃下H 平衡产率远大于600℃下H 平衡产率,其原因是
2 2
。
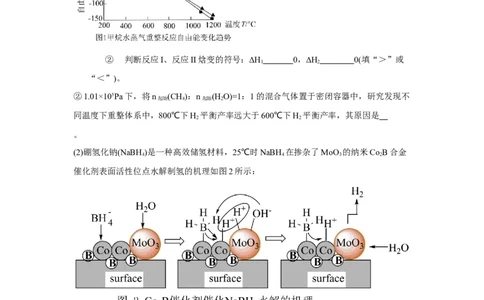
(2)硼氢化钠(NaBH )是一种高效储氢材料,25℃时NaBH 在掺杂了MoO 的纳米Co B合金
4 4 3 2
催化剂表面活性位点水解制氢的机理如图2所示:
① NaBH 中组成元素的电负性从大到小的顺序为 (用元
4
素符号表示)。
② 写出NaBH 与水反应生成NaBO 和H 的离子方程式
4 2 2
;并分析掺杂MoO 能提高制H 效率的原因
3 2
。
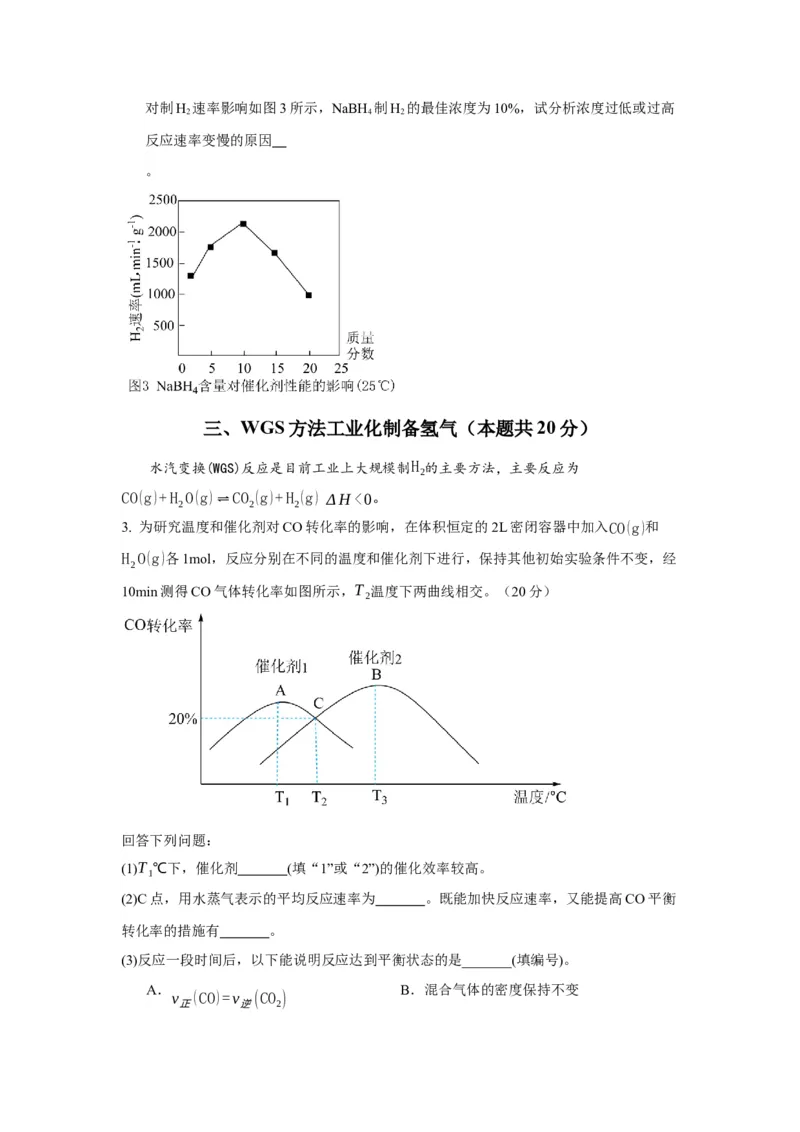
③ 已知25℃时NaBO 和NaBH 在水中的溶解度分别为28g和55g,NaBH 浓度
2 4 4对制H 速率影响如图3所示,NaBH 制H 的最佳浓度为10%,试分析浓度过低或过高
2 4 2
反应速率变慢的原因
。
三、WGS方法工业化制备氢气(本题共20分)
水汽变换(WGS)反应是目前工业上大规模制H 的主要方法,主要反应为
2
CO(g)+H O(g)⇌ CO (g)+H (g) ΔH<0。
2 2 2
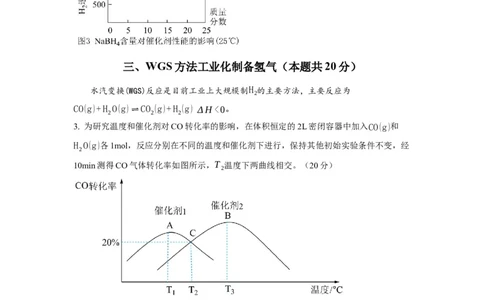
3. 为研究温度和催化剂对CO转化率的影响,在体积恒定的2L密闭容器中加入CO(g)和
H O(g)各1mol,反应分别在不同的温度和催化剂下进行,保持其他初始实验条件不变,经
2
10min测得CO气体转化率如图所示,T 温度下两曲线相交。(20分)
2
回答下列问题:
(1)T ℃下,催化剂 (填“1”或“2”)的催化效率较高。
1
(2)C点,用水蒸气表示的平均反应速率为 。既能加快反应速率,又能提高CO平衡
转化率的措施有 。
(3)反应一段时间后,以下能说明反应达到平衡状态的是_______(填编号)。
A. B.混合气体的密度保持不变
v (CO)=v (CO )
正 逆 2C.H 的体积分数不变 D.容器的压强不变
2
(4)A点时,反应 (填“是”或“不是”)处于平衡状态,原因是
。
(5)水汽变换过程通常需要在高温高压的条件下进行,且制得的H 不纯。中国科学院大连化
2
学物理研究所提出并实现了一种低能耗制备高纯氢气的新策略——室温电化学水汽变换。
实验装置示意图如图:
分析图示电化学过程,写出对应的电极反应方程式:
① 阴极产生H : 。
2
② 阳极CO放电: 。
四、钇矿石制取金属钇(本题共18分)
钇是稀土元素之一。我国蕴藏着丰富的钇矿石(YFeBeSiO ),用NaOH初步处理钇矿
2 2 2 10
石可以得到Y(OH)、FeO、NaSiO 和NaBeO 的共熔物。
3 2 3 2 3 2 2
4. 工业上利用该共熔物制取氧化钇,并获得副产物铍,流程如图:(18分)
已知i.铍和铝处于元素周期表的对角线位置,化学性质相似;
ii.Fe3+、Y3+形成氢氧化物沉淀时的pH如表:
离
开始沉淀时的pH 完全沉淀时的pH子
Fe3+ 2.1 3.1
Y3+ 6.0 8.3
(1)滤渣1的主要成分是 。
(2)过滤2所得滤液中含有NaCl、BeCl 和少量HCl。为提纯BeCl 。选择合理步骤并排序完
2 2
成系列操作1 。
a.加入适量的盐酸 b.通入过量的CO c.过滤
2
d.加入过量的NaOH溶液 e.加入过量的氨水 f.洗涤
(3)由BeCl 溶液制得BeCl 固体的操作为 。
2 2
(4)用氨水调节pH=a时,a的取值范围是 。
(5)计算常温下Y3++3H O❑Y(OH) +3H+的平衡常数K= 。(常温下
2 3
⇌
K [Y(OH) ]=8.0×10-23)
sp 3
(6)“除杂”中NaBeO 与过量盐酸反应的离子方程式为
2 2
。
(7)常见的由BeCl 固体生产Be的工业方法有两种:①电解法:电解NaCl-BeCl 混合熔融
2 2
盐制备Be;②热还原法:熔融条件下,钾还原BeCl 制备Be。以上两种方法你认为哪种更
2
好并说明理由 。
五、高血压治疗中间体药物双咪唑的合成(本题共23分)
替米沙坦是唯一经过FDA批准的具有心脑血管保护作用的沙坦类药物,可逆转左心室
肥厚,对于高血压合并左心室肥厚、心功能不全、冠心病等患者,可以作为首选用药。
5. 双咪唑是合成治疗高血压药物替米沙坦的一种中间体,其合成路线如下:(23分)已知: 。请回答:
(1)化合物A中所含官能团的名称为 。
(2)下列有关说法正确的是_____________________________________________。
A.②的反应类型为还原反应
B.双咪唑的分子式为C H N
18 22 4
C.化合物D在酸性、碱性条件下水解,均可生成盐
D.常温下,化合物F在水中有较大的溶解度
(3)③的化学方程式为______________________ 。
(4)E的结构简式为______________________ 。
(5)写出3种同时符合下列条件的化合物H的同分异构体的结构简式 。
①分子中只含有1个环,且为连有−NO 的苯环;
2
②分子中共有3种不同化学环境的氢原子。
(6)参照上述合成路线,设计由 和 合成 的路线
(其它无机试剂任选)。