文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(湖南专用)
黄金卷08
(考试时间:75分钟;试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 O-16 K-39 I-127
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.今年世界环境日的主题为“建设人与自然和谐共生的现代化”。下列关于环境保护的说法正确的是
A.绿色化学的核心思想是治理经济发展所带来的环境污染
B.废纸、玻璃、塑料瓶属于可回收垃圾
C.研发新型催化剂将CO 分解成C和O,同时放出热量,体现了“碳中和”理念
2 2
D.NO 、SO 、CO 都会导致酸雨的形成
2 2 2
【答案】B
【详解】A.绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染,直接从源头上
杜绝污染,故A错误;
B.废纸、玻璃、塑料瓶属于可回收垃圾,故B正确;
C.二氧化碳分解生成碳和氧气为吸热反应,故C错误;
D.酸雨的形成是由于SO 、NO 而引起的,CO 不会导致酸雨的形成,故D错误;
2 2 2
故选B。
2.“高山流水觅知音”。下列中国古乐器中,主要由硅酸盐材料制成的是
A.九霄环佩木古琴 B.裴李岗文化骨笛 C.商朝后期陶埙 D.曾侯乙青铜编钟
A.A B.B C.C D.D
【答案】C
【详解】A.九霄环佩木古琴主要构成是木材,动物筋制得,A错误;
B.裴李岗文化骨笛由动物骨骼构成,B错误;
C.商朝后期陶埙属于陶瓷,由硅酸盐制成,C正确;D.曾侯乙青铜编钟主要由合金材料制成,D错误;
故选C。
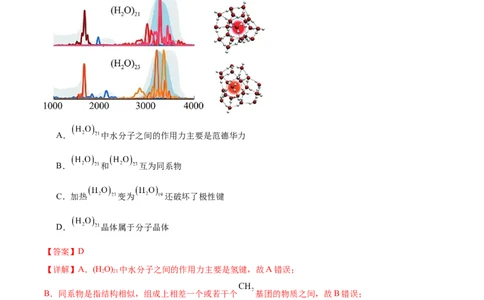
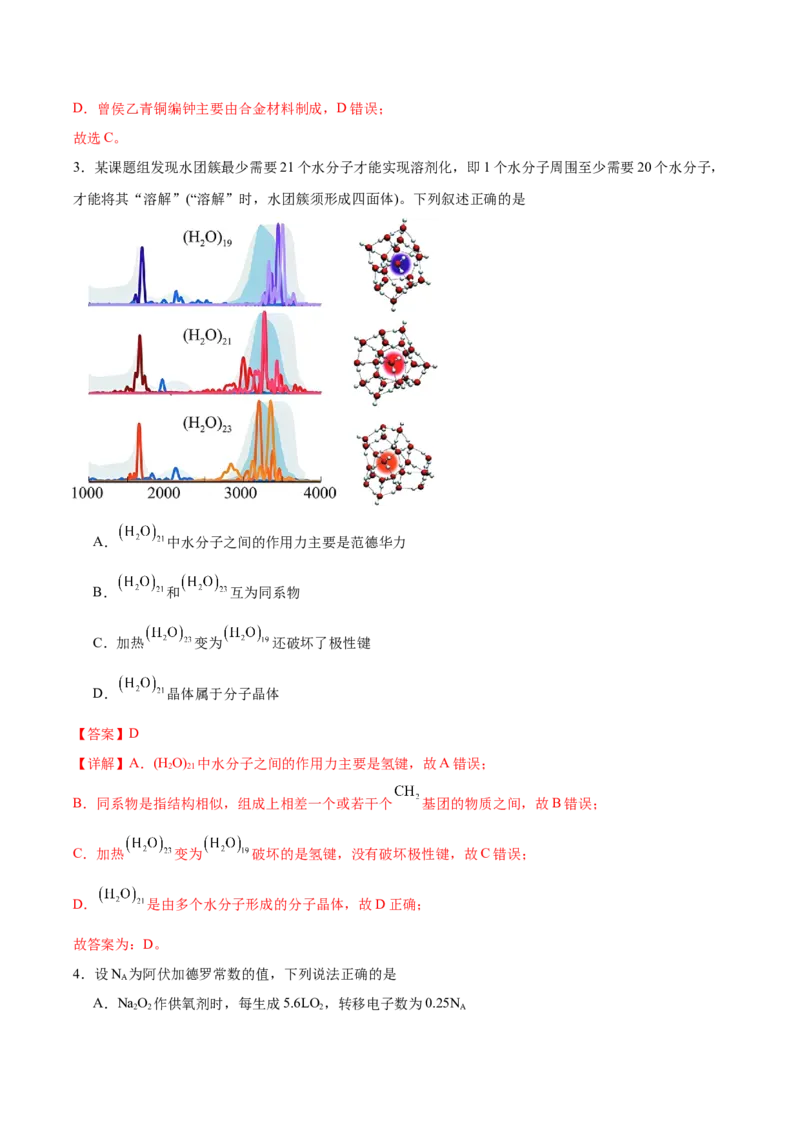
3.某课题组发现水团簇最少需要21个水分子才能实现溶剂化,即1个水分子周围至少需要20个水分子,
才能将其“溶解”(“溶解”时,水团簇须形成四面体)。下列叙述正确的是
A. 中水分子之间的作用力主要是范德华力
B. 和 互为同系物
C.加热 变为 还破坏了极性键
D. 晶体属于分子晶体
【答案】D
【详解】A.(H O) 中水分子之间的作用力主要是氢键,故A错误;
2 21
B.同系物是指结构相似,组成上相差一个或若干个 基团的物质之间,故B错误;
C.加热 变为 破坏的是氢键,没有破坏极性键,故C错误;
D. 是由多个水分子形成的分子晶体,故D正确;
故答案为:D。
4.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.NaO 作供氧剂时,每生成5.6LO ,转移电子数为0.25N
2 2 2 AB.工业合成氨时,每反应1molN ,生成的极性共价键数目为6N
2 A
C.电解精炼铜时,阳极质量每减少64g,电路中转移2mol电子
D.明矾净水时,0.1mol/LAl3+形成的Al(OH) 胶粒的数目为0.1N
3 A
【答案】B
【详解】A.NaO 作供氧剂时,O元素化合价从-1升高至0价,生成1mol O 转移2mol电子,未指明标准
2 2 2
状况,5.6LO 的物质的量无法计算,不确定转移电子数目,A错误;
2
B.工业上合成NH 反应为:N+3H 2NH ,每反应1 mol N ,反应产生2 mol NH ,产生
3 2 2 3 2 3
N-H极性键物质的量是6 mol,则生成的极性共价键数目为6N ,B正确;
A
C.电解精炼铜时,阳极反应消耗的金属有Cu及活动性比Cu强的金属,而活动性比Cu弱的金属则形成阳
极泥沉淀在阳极底部,故阳极质量每减少64 g,反应过程中转移电子的物质的量不一定是2 mol,则通过
电路的电子数不一定就是2N ,C错误;
A
D.只有溶液浓度,缺少溶液体积,不能计算Al3+的数目,且Al(OH) 胶粒是许多Al(OH) 的集合体,也不
3 3
能确定Al(OH) 胶粒的数目,D错误;
3
故合理选项是B。
5.下列化学反应对应的离子方程式表示正确的是
A.向NH Al(SO ) 中滴加Ba(OH) 使 恰好完全沉淀:Al3++2 +2Ba2++4OH-=
4 4 2 2
+2H O+2BaSO↓
2 4
B.向新制氯水中加入少量CaCO :2Cl+H O+CaCO =Ca2++2Cl-+CO ↑+2HClO
3 2 2 3 2
C.向NaHS溶液中滴加少量的CuSO 溶液:Cu2++HS-=CuS↓+H+
4
D.Fe O 溶于HI溶液:Fe O+8H+=Fe2++2Fe3++4H O
3 4 3 4 2
【答案】B
【详解】A.由于 恰好完全沉淀,说明NH Al(SO ) 与Ba(OH) 物质的量之比为1:2,而与OH-反应
4 4 2 2
的先后顺序为 ,故反应离子方程式为:
,A错误;
B.氯气溶于水生成盐酸和次氯酸,加入少量CaCO 后生成氯化钙、二氧化碳、水,故反应离子方程式为
3
,B正确;C.HS-与Cu2+反应生成CuS和HS,故反应离子方程式为: ,C错误;
2
D.Fe O 溶于HI溶液生成Fe2+、I 和HO,反应离子方程式为: ,D错误。
3 4 2 2
故选B。
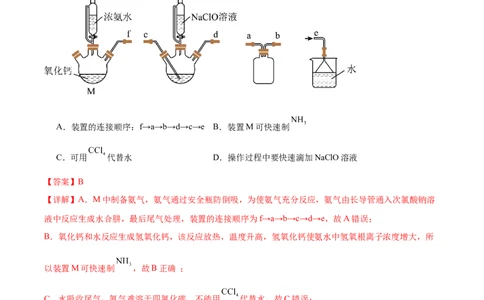
6.水合肼( )可用作还原剂。其制备原理为: 。用下图装置
制取水合肼的相关说法正确的是
A.装置的连接顺序:f→a→b→d→c→e B.装置M可快速制
C.可用 代替水 D.操作过程中要快速滴加NaClO溶液
【答案】B
【详解】A.M中制备氨气,氨气通过安全瓶防倒吸,为使氨气充分反应,氨气由长导管通入次氯酸钠溶
液中反应生成水合肼,最后尾气处理,装置的连接顺序为f→a→b→c→d→e,故A错误;
B.氧化钙和水反应生成氢氧化钙,该反应放热,温度升高,氢氧化钙使氨水中氢氧根离子浓度增大,所
以装置M可快速制 ,故B正确 ;
C.水吸收尾气,氨气难溶于四氯化碳,不能用 代替水,故C错误;
D.次氯酸钠具有氧化性,若操作过程中快速滴加NaClO溶液,可能 被NaClO氧化,故D错误;
选B。
7.我国科研人员发现氟磺酰基叠氮(FSO N)是一种安全、高效的“点击化学”试剂,其结构式如图,其中
2 3
S为+6价。下列说法正确的是A.该分子中元素的简单氢化物的稳定性:HF>H O>NH >H S
2 3 2
B.该分子中N原子均为sp2杂化
C.电负性:F>O>S>N
D.第一电离能:F>O>N>S
【答案】A
【详解】A.元素非金属性越强,简单氢化物越稳定。该分子中元素的简单氢化物的稳定性:
HF>H O>NH >H S,故A正确;
2 3 2
B.该分子中带正电荷的N原子为sp杂化,故B错误;
C.元素非金属性越强电负性越大,电负性:F>O >N>S,故C错误;
D.第一电离能:F>N >O >S,故D错误;
选A。
8.中科院天津工业生物技术研究所科研团队在实验室首次实现了以CO 为原料人工合成淀粉,其合成路
2
线如图所示。下列说法正确的是
A.上述流程中①②③涉及到的反应类型分别是还原反应、氧化反应、加成反应
B.1mol甲醛与足量新制Cu(OH) 悬浊液反应,最多产生1mol Cu O沉淀
2 2
C.DHA分子中σ键和π键的数目之比为7∶1
D.淀粉和纤维素的分子式相同,二者互为同分异构体
【答案】A
【详解】A.由题干转化流程图可知,上述流程中①为CO 和H 反应生成CHOH,该反应类型为还原反应,
2 2 3
②为CHOH催化氧化为HCHO,该反应类型为氧化反应,③3分子HCHO发生加成反生成DHA,该反应
3
类型为加成反应,A正确;
B.已知HCHO+4Cu(OH) +2NaOH 2Cu O↓+Na CO+6H O,故1mol甲醛与足量新制Cu(OH) 悬浊液
2 2 2 3 2 2
反应,最多产生2mol Cu O沉淀,B错误;
2
C.已知分子中单键均为σ键,双键为1个σ键和1个π键,由题干DHA分子结构简式可知,DHA中含有2个O-H、2个C-O,4个C-H、2个C-C和1个C=O,故DHA分子中σ键和π键的数目之比为11∶1,C错
误;
D.淀粉和纤维素的分子组成均能表示为:(C H O)n,但由于n值不同,即分子式不相同,则二者不是互
6 10 5
为同分异构体,D错误;
故答案为:A。
9.“空气吹出法”海水提溴的工艺流程如图。下列说法正确的是
A.B可选用SO 进入吸收塔,反应中体现SO 氧化性
2 2
B.通入吹出塔的气体A和通入蒸馏塔的气体C可能是同一物质
C.精馏装置需要蒸馏烧瓶、分液漏斗、冷凝管
D.该流程中为了达到富集溴元素的目的进行了两次氧化还原反应
【答案】B
【分析】浓缩酸化后的海水中含有Br-,用氧化剂(氯气等)氧化为Br ,然后用热空气吹出,Br 进入吸收
2 2
塔,用吸收剂吸收,再加入C将溴元素转化为Br ,最后精馏。
2
【详解】A.B可选用SO 进入吸收塔, ,SO 体现还原性,A错误;
2 2
B.通入吹出塔气体A和通入蒸馏塔气体C可能是氯气,把Br-氧化为Br ,B正确;
2
C. 精馏装置不需要分液漏斗,C错误;
D. 该流程中为了达到富集溴元素的目的进行了三次氧化还原反应,D错误;
故答案选B。
10.低钠氧化铝具有较高的催化活性,一种电渗析法生产低钠氧化铝的装置如图所示,将偏铝酸钠溶液加
入阴极室,不含钠离子的碱性缓冲液加入阳极室,最终在阳极室得到产品。下列说法正确的是A.中间的离子交换膜为阳离子交换膜
B.该装置将化学能转化为电能
C.随着反应的进行,阴极室溶液的 不断增大
D.相同条件下,阴、阳极产生的气体的体积比为1:2
【答案】C
【详解】A.偏铝酸钠溶液加入阴极室,不含钠离子的碱性缓冲液加入阳极室,最终在阳极室得到产品,
可知 通过离子交换膜进入阳极室,中间的离子交换膜为阴离子交换膜,故A错误;
B.该装置是电渗析法生产低钠氧化铝,将电能转化为化学能,故B错误;
C.根据图示,阴极室发生反应 ,阴极生成氢氧根离子,随着反应的进行,阴极室
溶液的 不断增大,故C正确;
D.阴极室发生反应 ,阳极室总反应为 ,根据电子守恒,相
同条件下,阴、阳极产生的气体的体积比为2:1,故D错误;
选C。
11.为探究类卤离子 与 的还原性强弱,某同学进行了如下实验:
①分别配制0.1mol·L-1的KSCN溶液、FeSO 溶液;
4
②向0.1mol·L-1的KSCN溶液中滴加酸性KMnO 溶液,酸性KMnO 溶液褪色;
4 4
③向0.1mol·L-1的FeSO 溶液中滴加酸性KMnO 溶液,酸性KMnO 溶液褪色;
4 4 4④向等体积浓度均为0.1mol·L-1的KSCN和FeSO 混合溶液中滴加酸性KMnO 溶液,溶液先变红后褪色。
4 4
下列说法正确的是
A.实验①中必须用到分液漏斗、锥形瓶等玻璃仪器
B.实验②中 将 还原为
C.实验③中反应的离子方程式为
D.实验④说明还原性:
【答案】C
【详解】A.该实验中不需要用到分液漏斗,A错误;
B. 酸性条件下可将SCN-氧化成(SCN) ,而不是还原,B错误;
2
C.酸性高锰酸钾与亚铁离子反应的离子方程式为 ,C正确;
D.在等体积浓度均为0.1mol/L的KSCN和FeSO 混合溶液中滴加酸性高锰酸钾,溶液先变红,说明亚铁
4
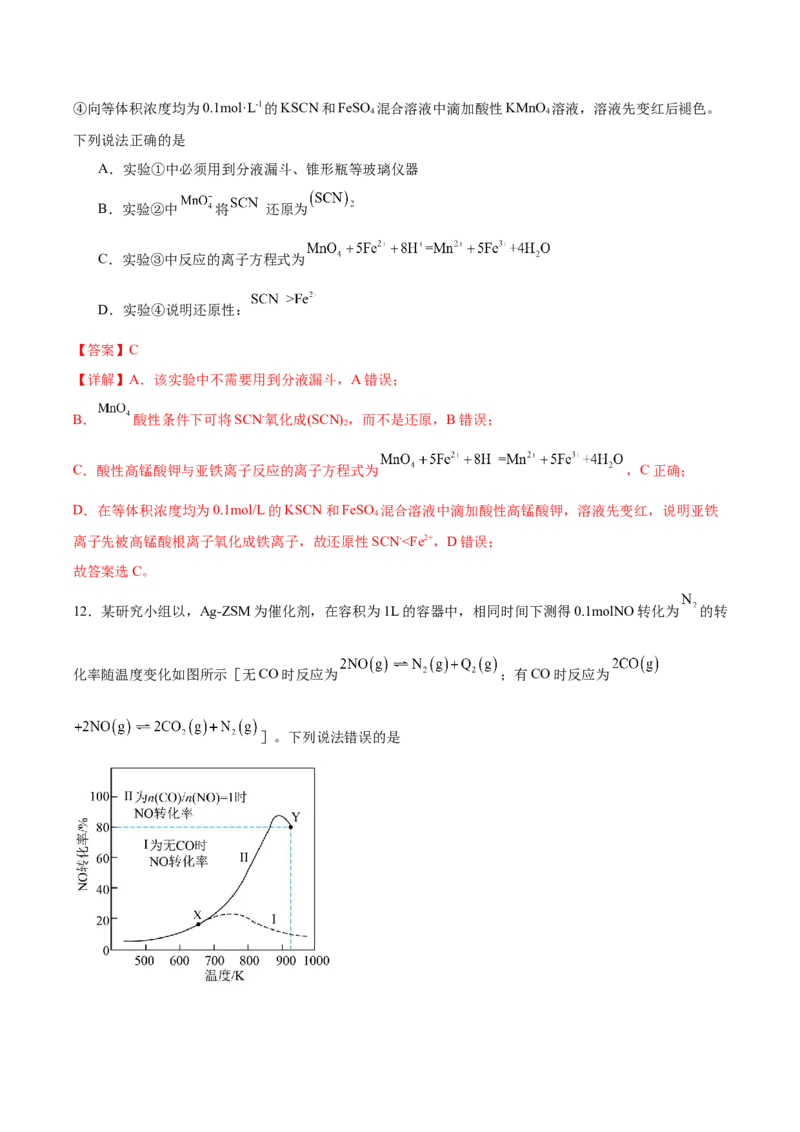
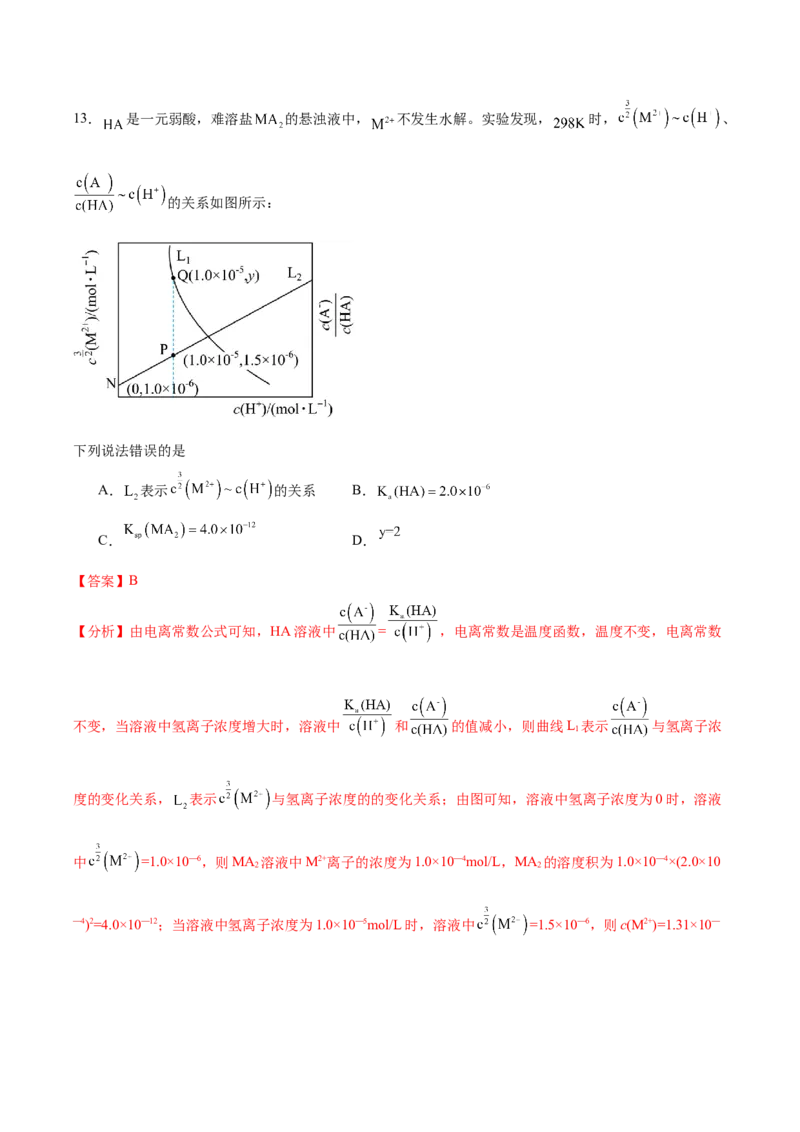
离子先被高锰酸根离子氧化成铁离子,故还原性SCN-、=或<);
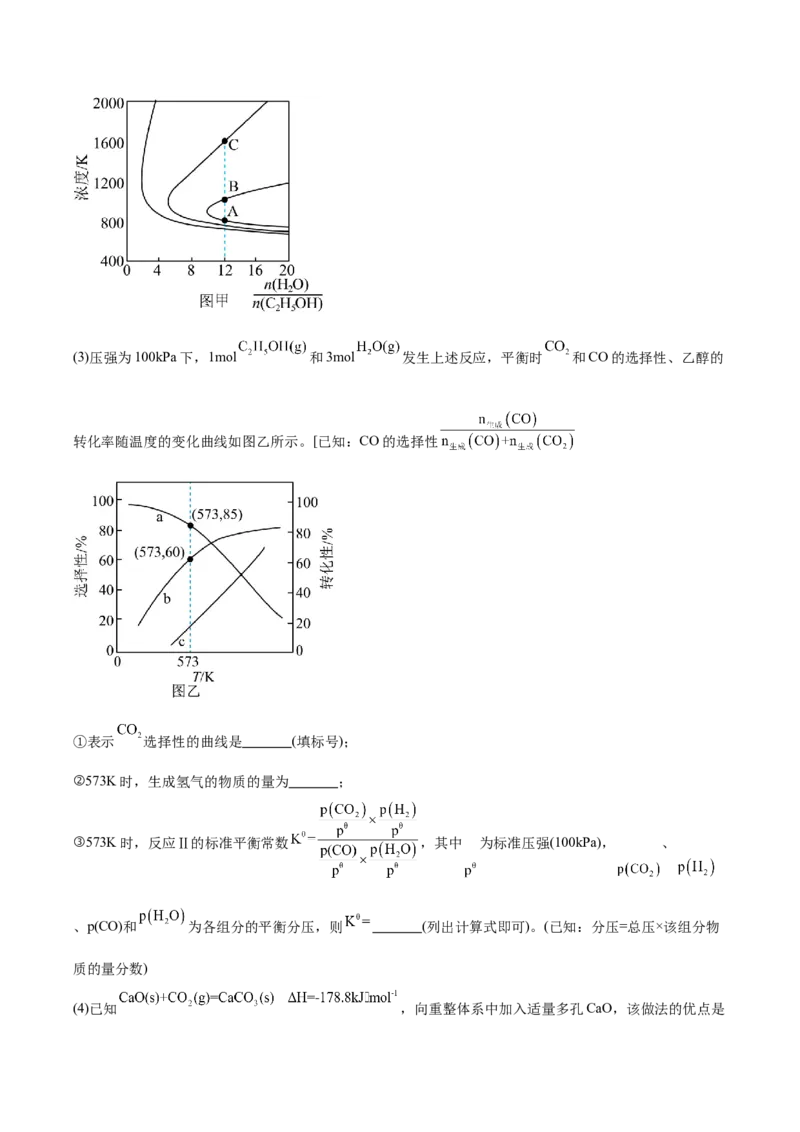
②A、B两点 产率相等的原因是 。(3)压强为100kPa下,1mol 和3mol 发生上述反应,平衡时 和CO的选择性、乙醇的
转化率随温度的变化曲线如图乙所示。[已知:CO的选择性
①表示 选择性的曲线是 (填标号);
②573K时,生成氢气的物质的量为 ;
③573K时,反应Ⅱ的标准平衡常数 ,其中 为标准压强(100kPa), 、
、p(CO)和 为各组分的平衡分压,则 (列出计算式即可)。(已知:分压=总压×该组分物
质的量分数)
(4)已知 ,向重整体系中加入适量多孔CaO,该做法的优点是(答出一点即可)。
【答案】(14分)(1)+173.3(2分)
(2) > (2分) B点温度高于A点,升高温度,反应Ⅱ逆向移动消耗氢气的量与反应Ⅰ正向移动产生
的量相等(2分)
(3) a (2分) 3.42 (2分) (2分)
(4)多孔CaO与 接触面积大,吸收 速率快、使得反应Ⅱ正向进行,提高氢气的产率,反应放热,同
时为反应提供热能(2分)
【详解】(1)根据盖斯定律,反应Ⅰ+2×反应Ⅱ得到反应Ⅲ,ΔH=ΔH +2×ΔH =(+255.7-41.2×2)kJ/
3 1 2
mol=+173.3kJ/mol。
(2)①每条曲线表示氢气相同的平衡产率,则在C点曲线上取一个点与B点温度相同标为点D,D点与B
点相比温度相同,但是 小于B点,增大 反应Ⅰ、Ⅱ、Ⅲ均正向移动,氢气的产率
增大,因此产率B点>C点。
②A、B两点 相同,B点温度高于A点,升高温度,反应Ⅱ逆向移动消耗氢气的量与反应Ⅰ、
Ⅲ正向移动产生H 的量相等,因此A、B两点氢气产率相等。
2
(3)①反应Ⅰ、Ⅲ为吸热反应,反应Ⅱ为放热反应,随着温度的升高,反应Ⅰ、Ⅲ平衡正向移动,反应
Ⅱ平衡逆向移动,反应Ⅱ逆向移动CO 转化为CO,故温度升高CO的选择性增大,CO 的选择性减小。表
2 2
示CO 选择性的曲线为a。
2
②CO 的选择性= ×100%=85%,故0.15n(CO )=0.85n(CO),300℃平衡C HOH的转化
2 2 2 5
率为60%,即n(CO)+n(CO)=0.6×2mol=1.2mol,得出n(CO)=0.18mol,n(CO )=1.02mol,则
2 2
n(H )=3.06+0.36=3.42mol,故答案为:3.42;
2
③CO的选择性为15%,CO 的选择性为85%,则n(CO):n(CO)=0.85:0.15,乙醇的转化率为0.6,
2 2
n(CO)+n(CO)=1×0.6×2=1.2,解得n(CO)=0.18mol,n(CO)=1.02mol,设反应Ⅰ转化乙醇xmol,
2 2,设反应Ⅱ转化COymol,
, 由2x-y=0.18、y=1.02,解得x=1.1,y=1.02,
则平衡时n(H O)=1.38mol,n(H )=3.42mol,n(C HOH)=0.4mol,n(CO)=0.18mol,n(CO)=1.02mol,反应Ⅱ
2 2 2 5 2
前后气体分子数不变,则 。
(4)已知CaO与CO 反应生成CaCO ,多孔CaO与CO 接触面积大,吸收CO 速率快,使得反应Ⅱ和Ⅲ
2 3 2 2
正向进行,提高氢气的产率同时为反应提供热能。
17.(14分)单质钨的化学性质比较稳定,主要用来制造灯丝和高速切削合金钢、超硬模具。工业上利用
黑钨矿(主要成分为FeWO 和MnWO ,还含少量Si、As的化合物)生产钨的工艺流程如图所示。已知:常
4 4
温下钨酸难溶于水。WO 难溶于水,能与水蒸气反应生成一种挥发性极强的水钨化合物WO(OH) 回答下
3 2 2.
列问题:
(1)焙烧过程中生成MnO 的化学方程式为 ,为加快此过程的反应速率,可采取的措施有
2
(答出两条)。
(2)沉钨时pH过低,可形成多钨酸根离子,其中最重要的是 和 ,写出生成 的离子方
程式: 。
(3)滤渣的成分为 (填化学式),常温时HAsO 、HAsO 水溶液中含砷的各物种的分布分数如图
3 3 3 4
所示,写出净化时加入HO 发生的主要反应的离子方程式: 。
2 2(4)还原制备W单质时要适当加快氢气的流速,目的是 。
(5)操作Ⅰ的名称为 ,若黑钨矿中钨的质量分数为ω,提炼过程中利用率为m,欲用nkg黑钨矿
制得纯度≥99%的金属钨,则产品中杂质含量最大为 kg。
【答案】(14分)(1) (2分) 碎黑钨矿、适
当提高温度、加快通入空气的速度等(2分)
(2) (2分)
(3) (2分) (2分)
(4)用氢气带出反应生成的水蒸气,避免三氧化钨与水蒸气反应生成 (1分)
(5) 过滤 (1分) (2分)
【分析】向黑钨矿(主要成分为 ,含有少量 的化合物)中通入空气和 ,主要
反应为 、
, 生成相应的盐,水浸时,氧化铁和二氧化
锰不溶于水,钨酸钠溶于水,故过滤后得到的滤液主要含钨酸钠和硅酸钠,滤渣的主要成分是,调 ,加入过氧化氢, 被氧化为 ,加入氯化镁,生成难溶于水的
。继续加盐酸,钨酸钠和盐酸反应生成钨酸和氯化钠,常温下钨酸难溶于水,过滤得
到钨酸,加热钨酸分解产生三氧化钨和水,由于 能与分解产生的水蒸气反应生成挥发性极强的水钨化
合物 ,故要适当加快氢气的流速带走水蒸气;
【详解】(1)焙烧过程中生成MnO 的化学方程式为
2
,为加快此过程的反应速率,可采取的措施有碎黑
钨矿、适当提高温度、加快通入空气的速度等;
(2)沉钨时pH过低,可形成多钨酸根离子,其中最重要的是 和 ,生成 的离子方
程式为: ;
(3)根据分析可知,滤渣的成分为 ,常温时HAsO 、HAsO 水溶液中含砷的各物种
3 3 3 4
的分布分数如图所示,净化时加入HO 生成 和水,发生的主要反应的离子方程式为:
2 2
;
(4)还原制备W单质时要适当加快氢气的流速,目的是用氢气带出反应生成的水蒸气,避免三氧化钨与
水蒸气反应生成 ;
(5)继续加盐酸,钨酸钠和盐酸反应生成钨酸和氯化钠,常温下钨酸难溶于水,过滤得到钨酸,加热钨
酸分解产生三氧化钨和水,由于 能与分解产生的水蒸气反应生成挥发性极强的水钨化合物 ,
故要适当加快氢气的流速带走水蒸气;用 还原三氧化钨生成钨,制备的产品金属钨中纯钨为 ,最少占产品的 ,假设杂质最多为
,最多占产品的 ,故有 。
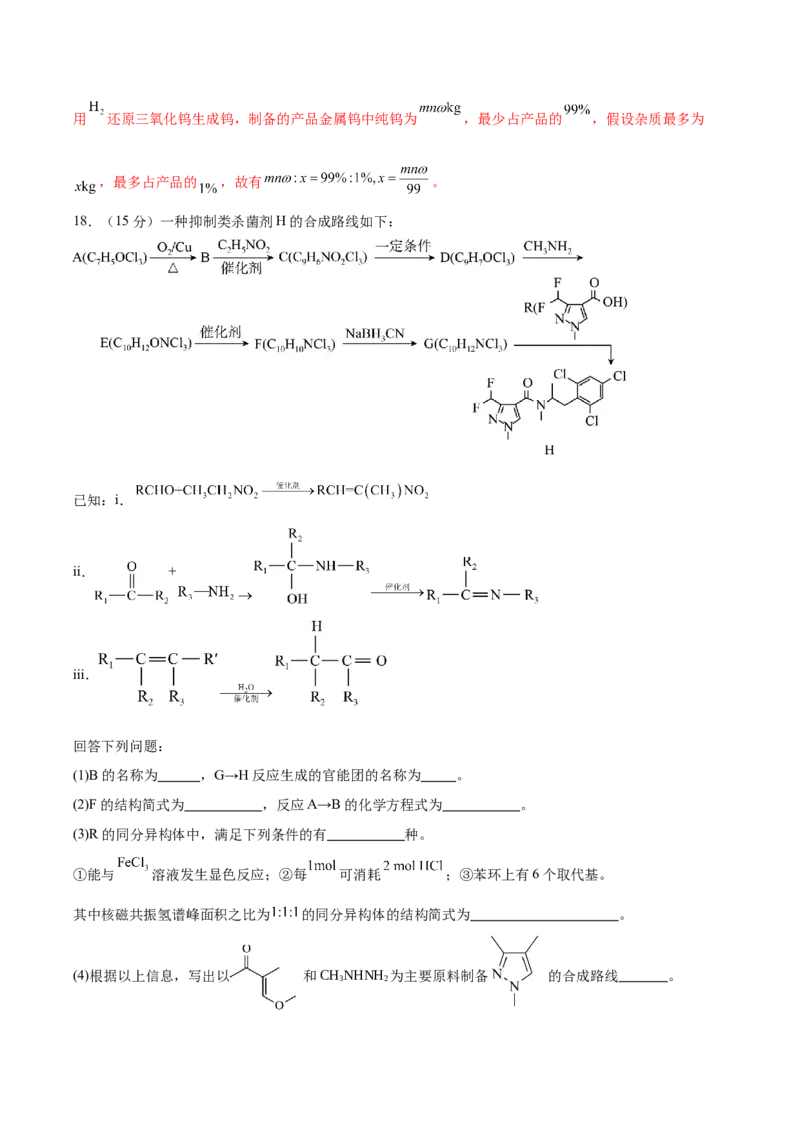
18.(15分)一种抑制类杀菌剂H的合成路线如下:
已知:i.
ii. +
iii.
回答下列问题:
(1)B的名称为 ,G→H反应生成的官能团的名称为 。
(2)F的结构简式为 ,反应A→B的化学方程式为 。
(3)R的同分异构体中,满足下列条件的有 种。
①能与 溶液发生显色反应;②每 可消耗 ;③苯环上有6个取代基。
其中核磁共振氢谱峰面积之比为 的同分异构体的结构简式为 。
(4)根据以上信息,写出以 和CHNHNH 为主要原料制备 的合成路线 。
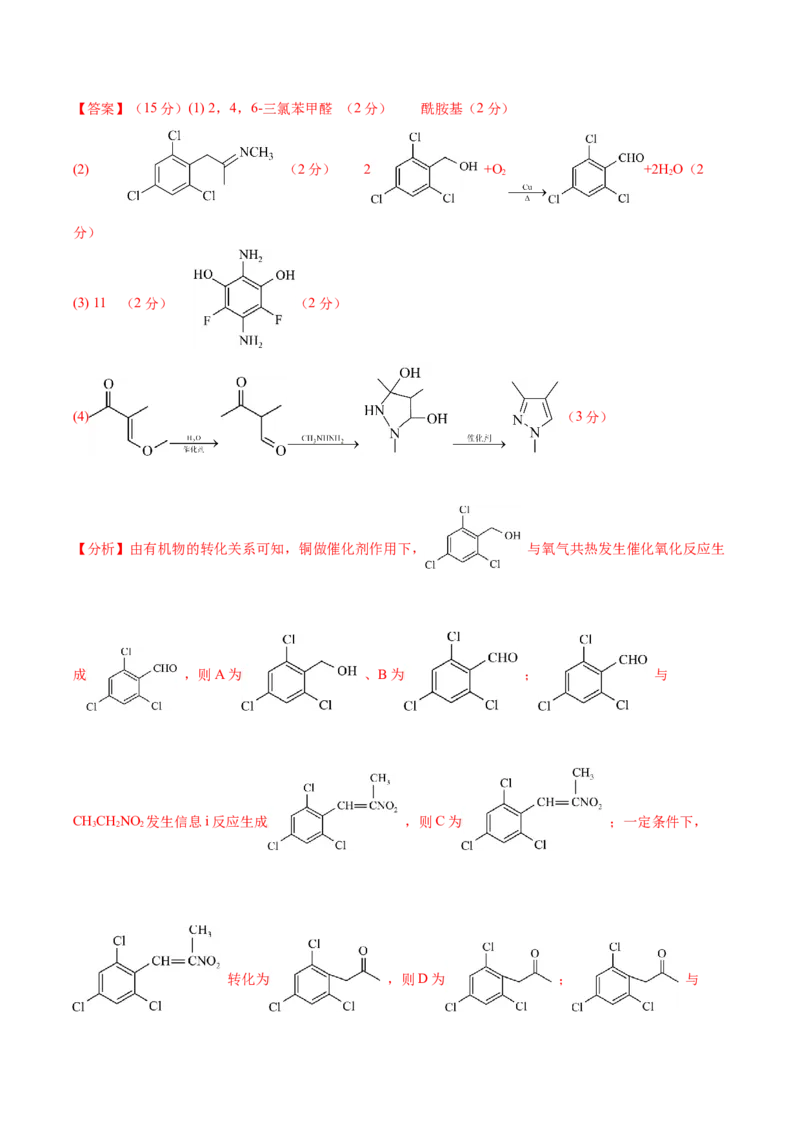
3 2【答案】(15分)(1) 2,4,6-三氯苯甲醛 (2分) 酰胺基(2分)
(2) (2分) 2 +O +2H O(2
2 2
分)
(3) 11 (2分) (2分)
(4) (3分)
【分析】由有机物的转化关系可知,铜做催化剂作用下, 与氧气共热发生催化氧化反应生
成 ,则A为 、B为 ; 与
CHCHNO 发生信息i反应生成 ,则C为 ;一定条件下,
3 2 2
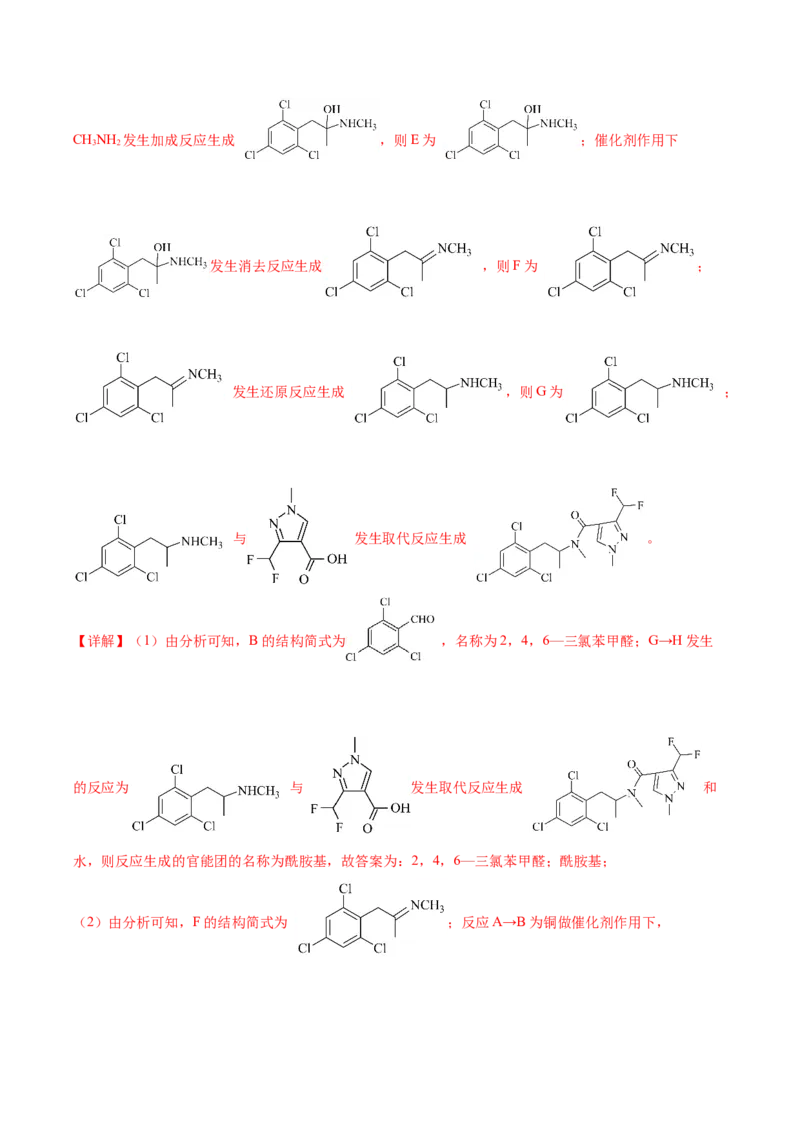
转化为 ,则D为 ; 与CHNH 发生加成反应生成 ,则E为 ;催化剂作用下
3 2
发生消去反应生成 ,则F为 ;
发生还原反应生成 ,则G为 ;
与 发生取代反应生成 。
【详解】(1)由分析可知,B的结构简式为 ,名称为2,4,6—三氯苯甲醛;G→H发生
的反应为 与 发生取代反应生成 和
水,则反应生成的官能团的名称为酰胺基,故答案为:2,4,6—三氯苯甲醛;酰胺基;
(2)由分析可知,F的结构简式为 ;反应A→B为铜做催化剂作用下,与氧气共热发生催化氧化反应生成 和水,反应的化学方程式为2
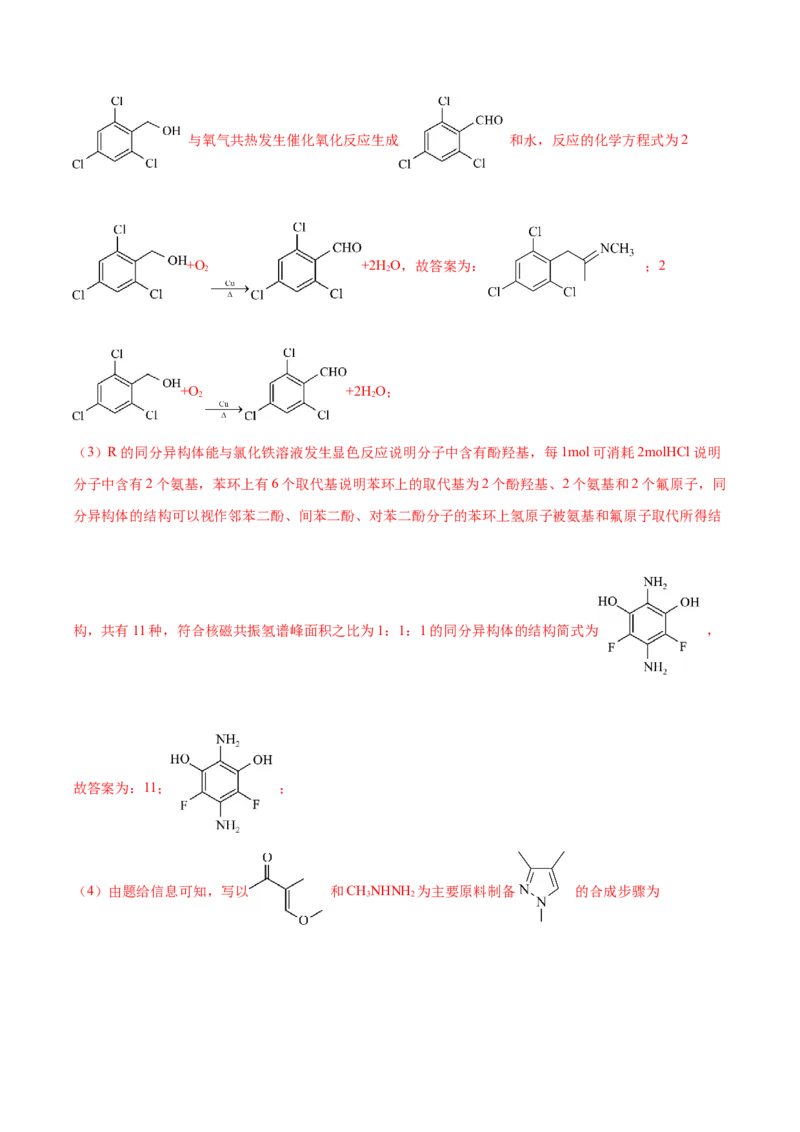
+O +2H O,故答案为: ;2
2 2
+O +2H O;
2 2
(3)R的同分异构体能与氯化铁溶液发生显色反应说明分子中含有酚羟基,每1mol可消耗2molHCl说明
分子中含有2个氨基,苯环上有6个取代基说明苯环上的取代基为2个酚羟基、2个氨基和2个氟原子,同
分异构体的结构可以视作邻苯二酚、间苯二酚、对苯二酚分子的苯环上氢原子被氨基和氟原子取代所得结
构,共有11种,符合核磁共振氢谱峰面积之比为1:1:1的同分异构体的结构简式为 ,
故答案为:11; ;
(4)由题给信息可知,写以 和CHNHNH 为主要原料制备 的合成步骤为
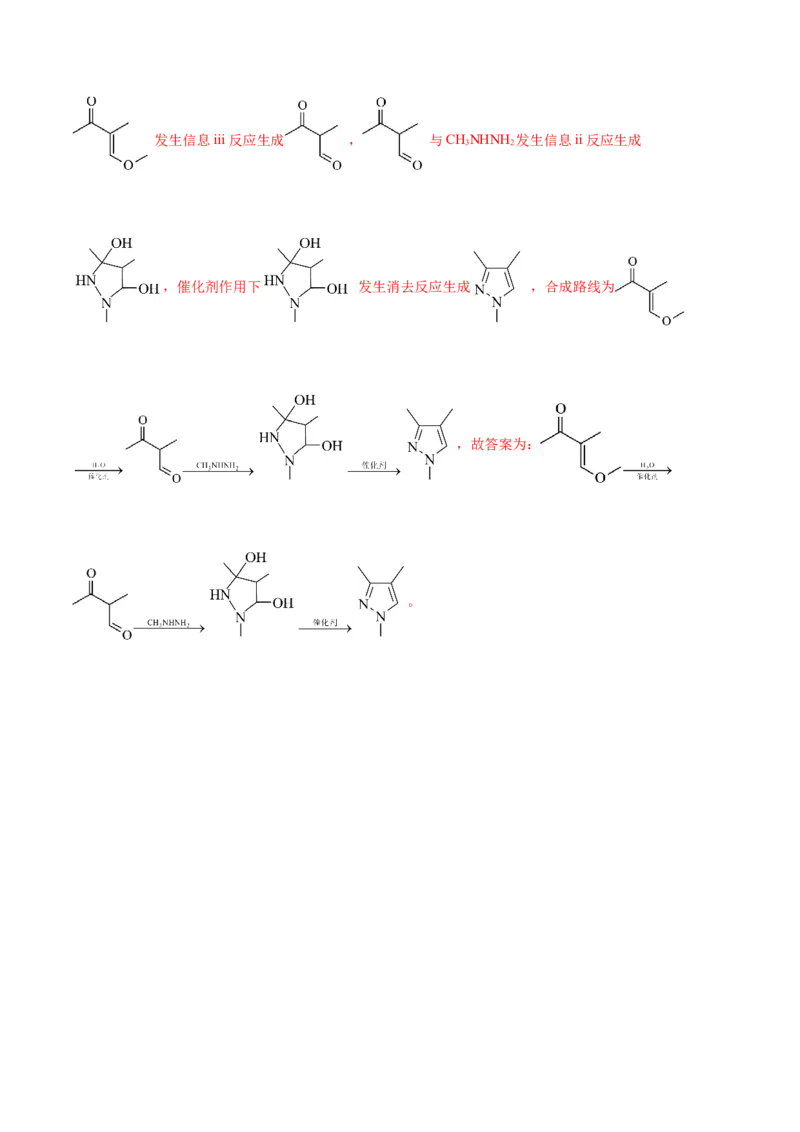
3 2发生信息iii反应生成 , 与CHNHNH 发生信息ii反应生成
3 2
,催化剂作用下 发生消去反应生成 ,合成路线为
,故答案为:
。