文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(湖南专用)
黄金卷08
(考试时间:75分钟;试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 O-16 K-39 I-127
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.今年世界环境日的主题为“建设人与自然和谐共生的现代化”。下列关于环境保护的说法正确的是
A.绿色化学的核心思想是治理经济发展所带来的环境污染
B.废纸、玻璃、塑料瓶属于可回收垃圾
C.研发新型催化剂将CO 分解成C和O,同时放出热量,体现了“碳中和”理念
2 2
D.NO 、SO 、CO 都会导致酸雨的形成
2 2 2
2.“高山流水觅知音”。下列中国古乐器中,主要由硅酸盐材料制成的是
A.九霄环佩木古琴 B.裴李岗文化骨笛 C.商朝后期陶埙 D.曾侯乙青铜编钟
A.A B.B C.C D.D
3.某课题组发现水团簇最少需要21个水分子才能实现溶剂化,即1个水分子周围至少需要20个水分子,
才能将其“溶解”(“溶解”时,水团簇须形成四面体)。下列叙述正确的是A. 中水分子之间的作用力主要是范德华力
B. 和 互为同系物
C.加热 变为 还破坏了极性键
D. 晶体属于分子晶体
4.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.NaO 作供氧剂时,每生成5.6LO ,转移电子数为0.25N
2 2 2 A
B.工业合成氨时,每反应1molN ,生成的极性共价键数目为6N
2 A
C.电解精炼铜时,阳极质量每减少64g,电路中转移2mol电子
D.明矾净水时,0.1mol/LAl3+形成的Al(OH) 胶粒的数目为0.1N
3 A
5.下列化学反应对应的离子方程式表示正确的是
A.向NH Al(SO ) 中滴加Ba(OH) 使 恰好完全沉淀:Al3++2 +2Ba2++4OH-=
4 4 2 2
+2H O+2BaSO↓
2 4
B.向新制氯水中加入少量CaCO :2Cl+H O+CaCO =Ca2++2Cl-+CO ↑+2HClO
3 2 2 3 2
C.向NaHS溶液中滴加少量的CuSO 溶液:Cu2++HS-=CuS↓+H+
4
D.Fe O 溶于HI溶液:Fe O+8H+=Fe2++2Fe3++4H O
3 4 3 4 2
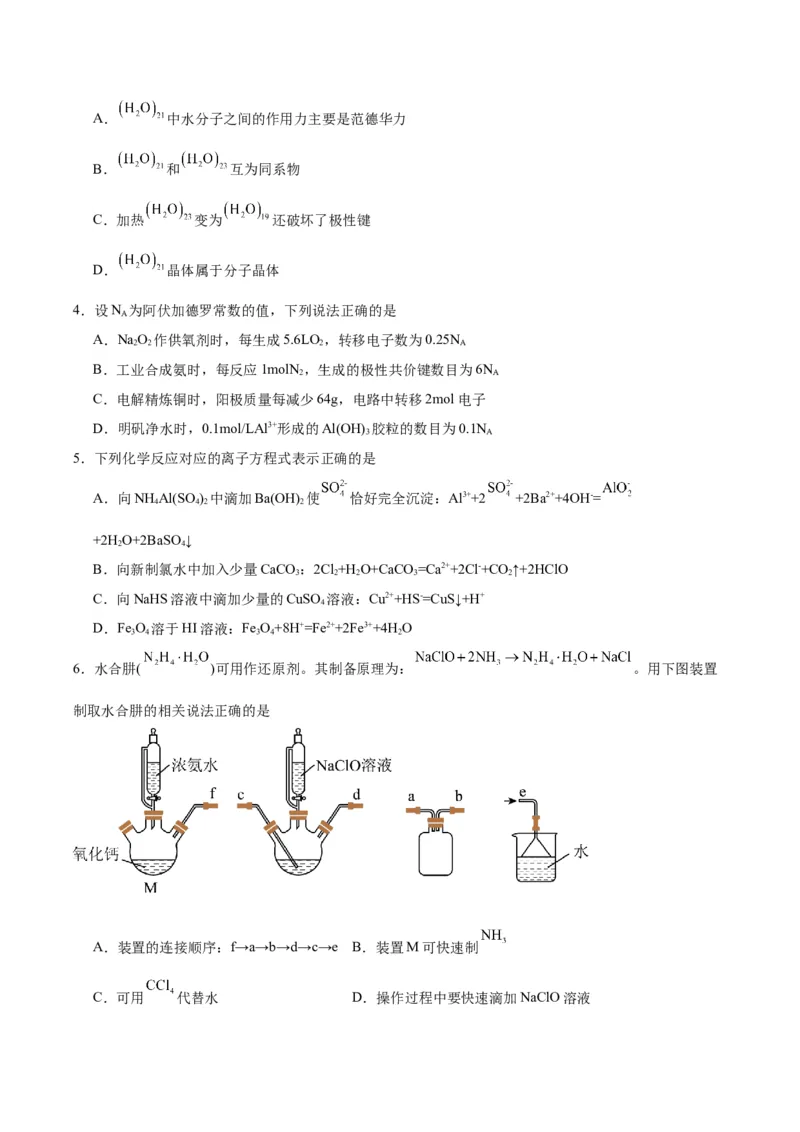
6.水合肼( )可用作还原剂。其制备原理为: 。用下图装置
制取水合肼的相关说法正确的是
A.装置的连接顺序:f→a→b→d→c→e B.装置M可快速制
C.可用 代替水 D.操作过程中要快速滴加NaClO溶液7.我国科研人员发现氟磺酰基叠氮(FSO N)是一种安全、高效的“点击化学”试剂,其结构式如图,其中
2 3
S为+6价。下列说法正确的是
A.该分子中元素的简单氢化物的稳定性:HF>H O>NH >H S
2 3 2
B.该分子中N原子均为sp2杂化
C.电负性:F>O>S>N
D.第一电离能:F>O>N>S
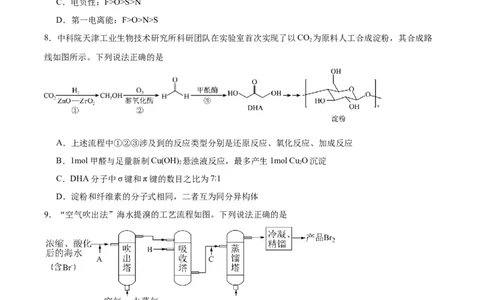
8.中科院天津工业生物技术研究所科研团队在实验室首次实现了以CO 为原料人工合成淀粉,其合成路
2
线如图所示。下列说法正确的是
A.上述流程中①②③涉及到的反应类型分别是还原反应、氧化反应、加成反应
B.1mol甲醛与足量新制Cu(OH) 悬浊液反应,最多产生1mol Cu O沉淀
2 2
C.DHA分子中σ键和π键的数目之比为7∶1
D.淀粉和纤维素的分子式相同,二者互为同分异构体
9.“空气吹出法”海水提溴的工艺流程如图。下列说法正确的是
A.B可选用SO 进入吸收塔,反应中体现SO 氧化性
2 2
B.通入吹出塔的气体A和通入蒸馏塔的气体C可能是同一物质
C.精馏装置需要蒸馏烧瓶、分液漏斗、冷凝管
D.该流程中为了达到富集溴元素的目的进行了两次氧化还原反应
10.低钠氧化铝具有较高的催化活性,一种电渗析法生产低钠氧化铝的装置如图所示,将偏铝酸钠溶液加
入阴极室,不含钠离子的碱性缓冲液加入阳极室,最终在阳极室得到产品。下列说法正确的是A.中间的离子交换膜为阳离子交换膜
B.该装置将化学能转化为电能
C.随着反应的进行,阴极室溶液的 不断增大
D.相同条件下,阴、阳极产生的气体的体积比为1:2
11.为探究类卤离子 与 的还原性强弱,某同学进行了如下实验:
①分别配制0.1mol·L-1的KSCN溶液、FeSO 溶液;
4
②向0.1mol·L-1的KSCN溶液中滴加酸性KMnO 溶液,酸性KMnO 溶液褪色;
4 4
③向0.1mol·L-1的FeSO 溶液中滴加酸性KMnO 溶液,酸性KMnO 溶液褪色;
4 4 4
④向等体积浓度均为0.1mol·L-1的KSCN和FeSO 混合溶液中滴加酸性KMnO 溶液,溶液先变红后褪色。
4 4
下列说法正确的是
A.实验①中必须用到分液漏斗、锥形瓶等玻璃仪器
B.实验②中 将 还原为
C.实验③中反应的离子方程式为
D.实验④说明还原性:
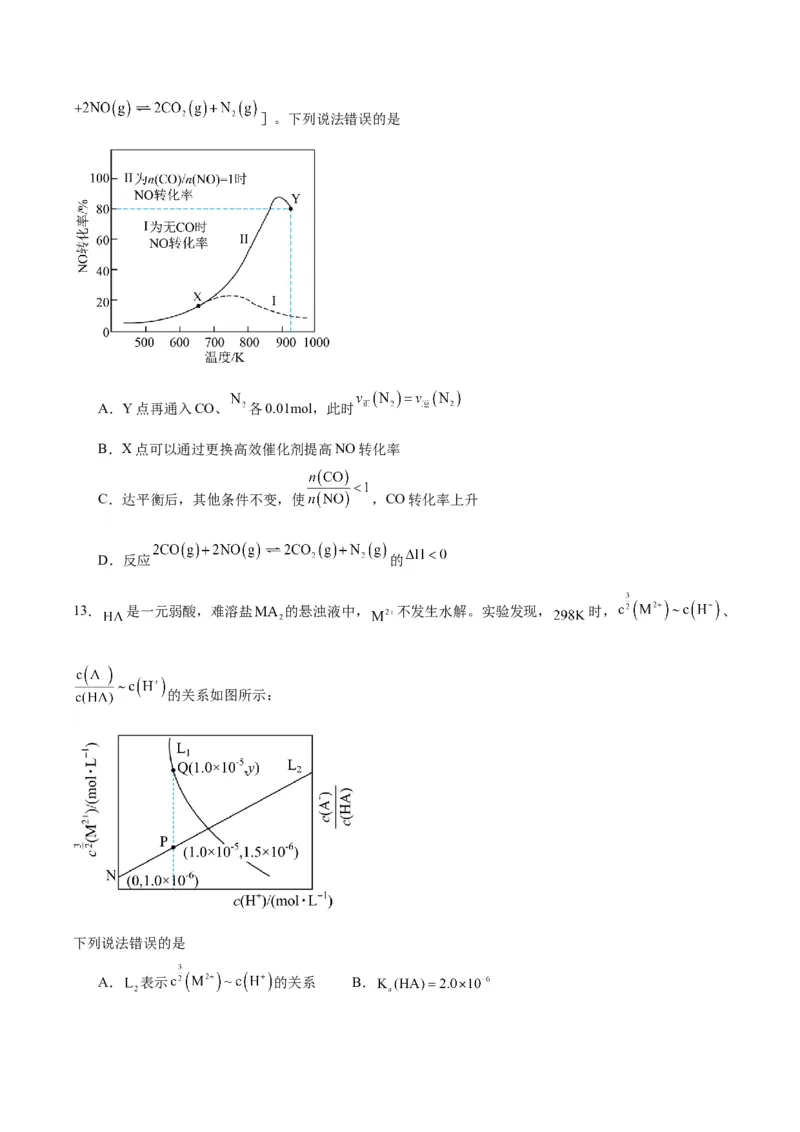
12.某研究小组以,Ag-ZSM为催化剂,在容积为1L的容器中,相同时间下测得0.1molNO转化为 的转
化率随温度变化如图所示[无CO时反应为 ;有CO时反应为]。下列说法错误的是
A.Y点再通入CO、 各0.01mol,此时
B.X点可以通过更换高效催化剂提高NO转化率
C.达平衡后,其他条件不变,使 ,CO转化率上升
D.反应 的
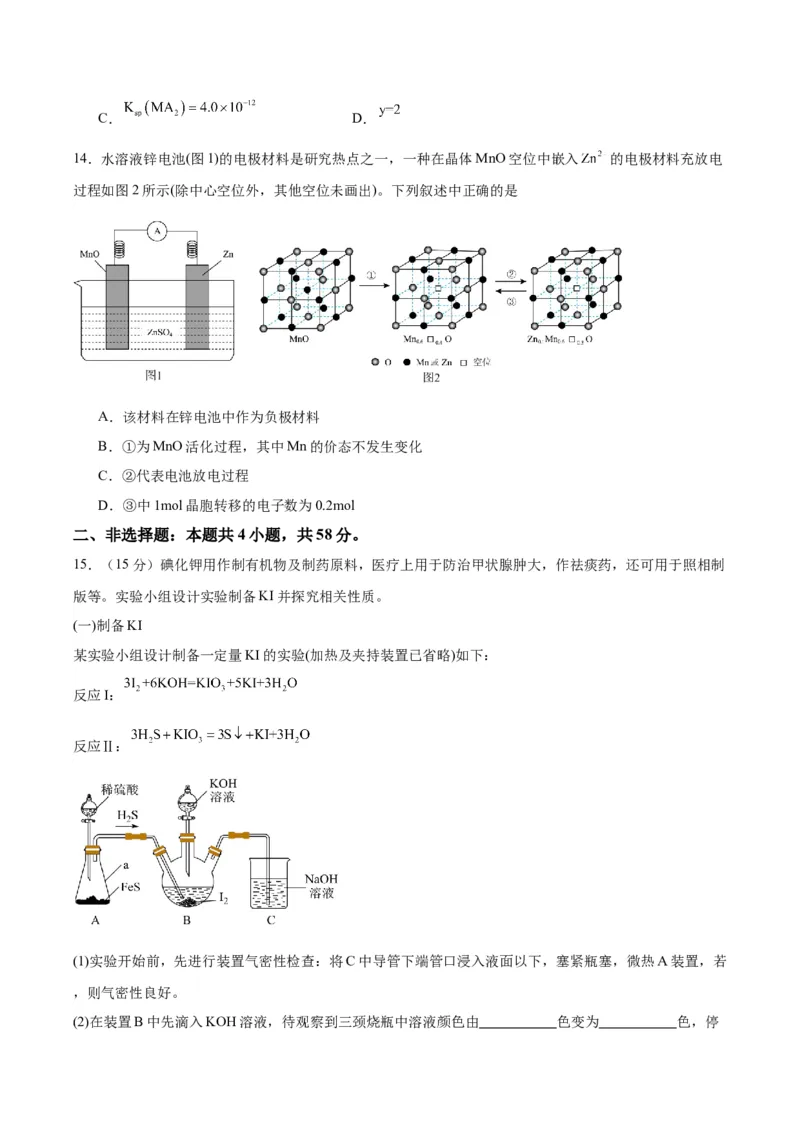
13. 是一元弱酸,难溶盐 的悬浊液中, 不发生水解。实验发现, 时, 、
的关系如图所示:
下列说法错误的是
A. 表示 的关系 B.C. D.
14.水溶液锌电池(图1)的电极材料是研究热点之一,一种在晶体MnO空位中嵌入 的电极材料充放电
过程如图2所示(除中心空位外,其他空位未画出)。下列叙述中正确的是
A.该材料在锌电池中作为负极材料
B.①为MnO活化过程,其中Mn的价态不发生变化
C.②代表电池放电过程
D.③中1mol晶胞转移的电子数为0.2mol
二、非选择题:本题共4小题,共58分。
15.(15分)碘化钾用作制有机物及制药原料,医疗上用于防治甲状腺肿大,作祛痰药,还可用于照相制
版等。实验小组设计实验制备KI并探究相关性质。
(一)制备KI
某实验小组设计制备一定量KI的实验(加热及夹持装置已省略)如下:
反应I:
反应Ⅱ:
(1)实验开始前,先进行装置气密性检查:将C中导管下端管口浸入液面以下,塞紧瓶塞,微热A装置,若
,则气密性良好。
(2)在装置B中先滴入KOH溶液,待观察到三颈烧瓶中溶液颜色由 色变为 色,停止滴入KOH溶液;然后打开装置A中分液漏斗活塞,待三颈烧瓶和烧杯中产生气泡的速率接近相等时停
止通气,反应完成。
(3)实验中不能用稀硝酸代替稀硫酸的根本原因是 。
(4)装置B中所得KI溶液经分离提纯后得到KI粗产品,为测定KI的纯度,称取1.0g样品溶于水,然后用
0.0500mol·L-1酸性KMnO 标准溶液滴定( ),杂质不与酸性KMnO
4 4
溶液反应。平行滴定三次,滴定到终点平均消耗酸性KMnO 标准溶液20.00mL,则样品的纯度为
4
(保留两位有效数字)。
(二)实验探究:FeCl 与KI的反应
3
序号 操作 现象
取5mL0.1mol·L-1KI溶液,滴加0.1mol·L-1 FeCl 溶液5~6滴(混 溶液变为棕黄色,20min后棕
实验I 3
合溶液的pH=5) 黄色变深
实验
取少量实验I中棕黄色溶液于试管中,滴加2滴KSCN溶液 溶液变红,20min后红色变浅
Ⅱ
(5)证明实验I中有I 生成,加入的试剂为(有机溶剂除外) 。
2
(6)已知在酸性较强的条件下,I-可被空气氧化为I,为探究实验I中20min后棕黄色变深的原因,甲同学
2
提出假设:该反应条件下空气将I-氧化为I,使实验I中溶液棕黄色变深。甲同学设计的实验为:
2
,若20min后溶液不变蓝,证明该假设不成立。(可选试剂:0.1mol·L-1KI溶液、0.1mol·L-1FeCl 溶液、淀
3
粉溶液、稀硫酸)
(7)乙同学查阅资料可知:① ;②FeCl 与KI反应的平衡体系中还存在反应
3
, 呈棕褐色。依据资料从平衡移动原理解释实验Ⅱ中20min后溶液红色变浅的原因:
。
16.(14分)氢能将在实现“双碳”目标中起到重要作用,乙醇与水催化重整制氢发生以下反应。
反应Ⅰ:
反应Ⅱ:
回答下列问题:
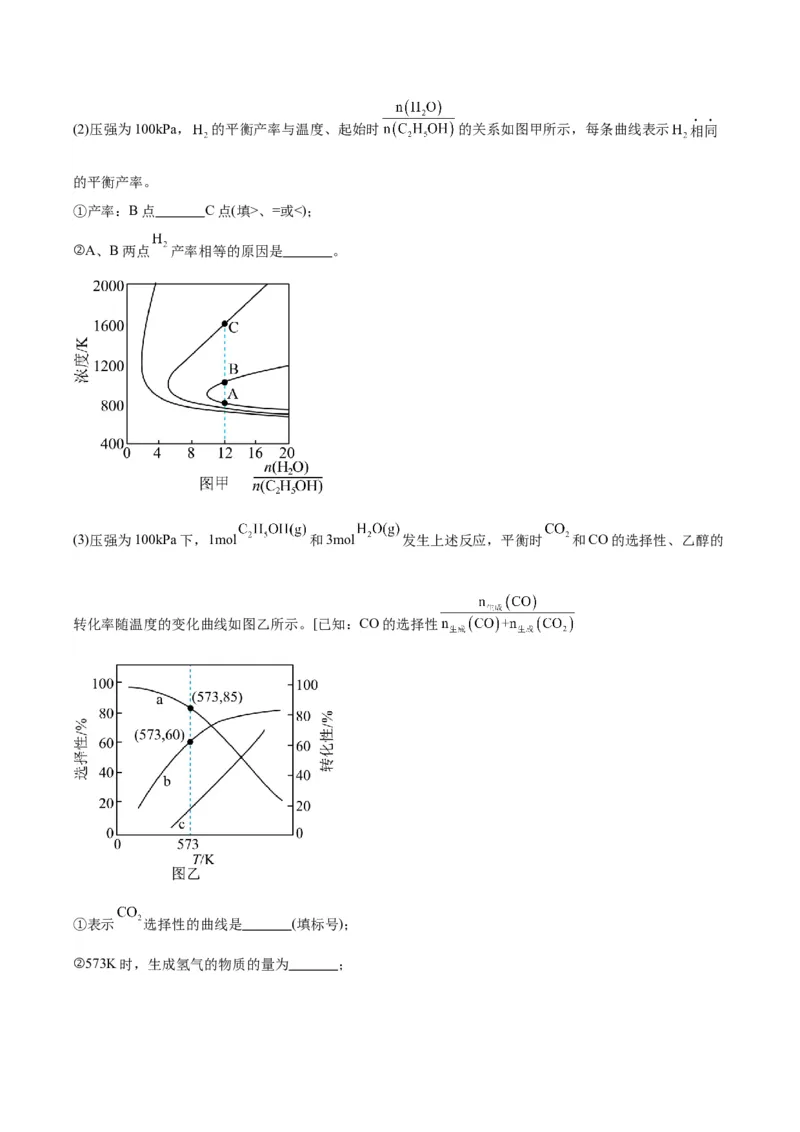
(1)已知反应 ,(2)压强为100kPa, 的平衡产率与温度、起始时 的关系如图甲所示,每条曲线表示 相同
的平衡产率。
①产率:B点 C点(填>、=或<);
②A、B两点 产率相等的原因是 。
(3)压强为100kPa下,1mol 和3mol 发生上述反应,平衡时 和CO的选择性、乙醇的
转化率随温度的变化曲线如图乙所示。[已知:CO的选择性
①表示 选择性的曲线是 (填标号);
②573K时,生成氢气的物质的量为 ;③573K时,反应Ⅱ的标准平衡常数 ,其中 为标准压强(100kPa), 、
、p(CO)和 为各组分的平衡分压,则 (列出计算式即可)。(已知:分压=总压×该组分物
质的量分数)
(4)已知 ,向重整体系中加入适量多孔CaO,该做法的优点是
(答出一点即可)。
17.(14分)单质钨的化学性质比较稳定,主要用来制造灯丝和高速切削合金钢、超硬模具。工业上利用
黑钨矿(主要成分为FeWO 和MnWO ,还含少量Si、As的化合物)生产钨的工艺流程如图所示。已知:常
4 4
温下钨酸难溶于水。WO 难溶于水,能与水蒸气反应生成一种挥发性极强的水钨化合物WO(OH) 回答下
3 2 2.
列问题:
(1)焙烧过程中生成MnO 的化学方程式为 ,为加快此过程的反应速率,可采取的措施有
2
(答出两条)。
(2)沉钨时pH过低,可形成多钨酸根离子,其中最重要的是 和 ,写出生成 的离子方
程式: 。
(3)滤渣的成分为 (填化学式),常温时HAsO 、HAsO 水溶液中含砷的各物种的分布分数如图
3 3 3 4
所示,写出净化时加入HO 发生的主要反应的离子方程式: 。
2 2(4)还原制备W单质时要适当加快氢气的流速,目的是 。
(5)操作Ⅰ的名称为 ,若黑钨矿中钨的质量分数为ω,提炼过程中利用率为m,欲用nkg黑钨矿
制得纯度≥99%的金属钨,则产品中杂质含量最大为 kg。
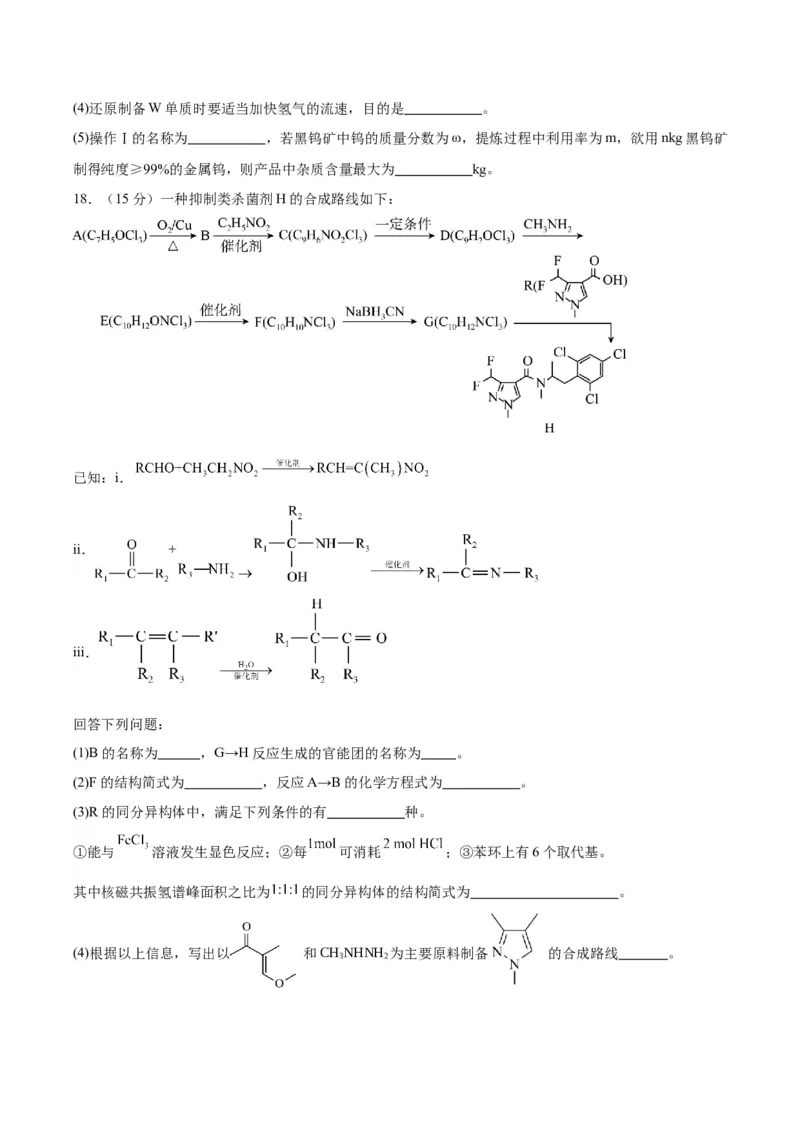
18.(15分)一种抑制类杀菌剂H的合成路线如下:
已知:i.
ii. +
iii.
回答下列问题:
(1)B的名称为 ,G→H反应生成的官能团的名称为 。
(2)F的结构简式为 ,反应A→B的化学方程式为 。
(3)R的同分异构体中,满足下列条件的有 种。
①能与 溶液发生显色反应;②每 可消耗 ;③苯环上有6个取代基。
其中核磁共振氢谱峰面积之比为 的同分异构体的结构简式为 。
(4)根据以上信息,写出以 和CHNHNH 为主要原料制备 的合成路线 。
3 2