文档内容
铁及其化合物(2)同步练习
(答题时间:25分钟)
一、选择题:本题包括12小题,每小题4分,共48分。
1. 将下列四种化合物溶于稀盐酸,滴加硫氰化钾溶液,没有颜色变化,再加氯水即呈现
红色的是( )
A. FeO B. Fe O C. Fe O D. Fe (SO )
2 3 3 4 2 4 3
2. 向某溶液中加入含Fe2+的溶液后,无明显变化。当再滴入几滴新制氯水后,混合溶液
变成红色,则下列结论错误的是( )
A. 该溶液中一定含有SCN-
B. 氧化性:Cl>Fe3+
2
C. Fe2+与SCN-能形成红色物质
D. Fe2+被氧化为Fe3+
3. 把铁粉、铜粉置于FeCl 溶液中,充分反应后加入KSCN不显红色,下列情况不能成
3
立的是( )
A. 铁不剩余,Cu剩余
B. 铁、铜均剩余
C. 铁剩余,含Cu2+
D. 铜剩余,含Fe2+
4. 有NaCl、FeCl 、FeCl 、CuCl 、AlCl 五种溶液,用一种试剂就可把它们鉴别开来,
2 3 2 3
这种试剂是( )
A. 盐酸 B. 烧碱溶液 C. 氯水 D. KSCN溶液
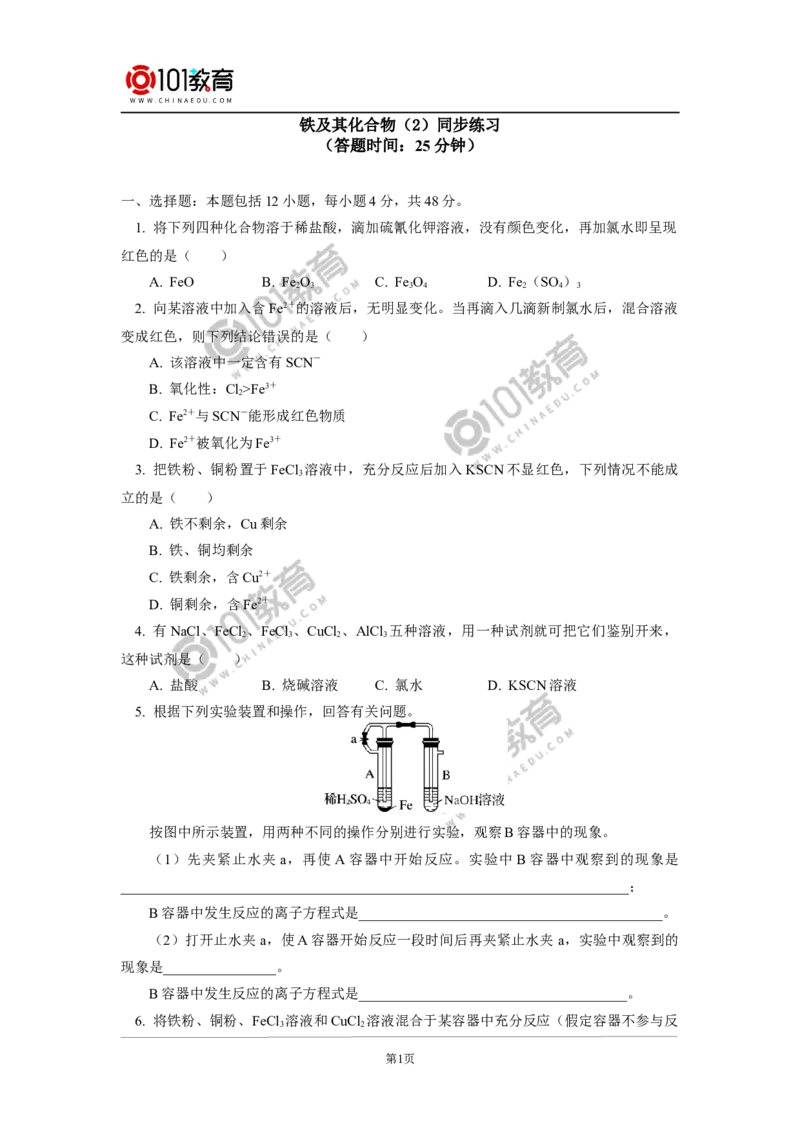
5. 根据下列实验装置和操作,回答有关问题。
按图中所示装置,用两种不同的操作分别进行实验,观察B容器中的现象。
(1)先夹紧止水夹a,再使A容器中开始反应。实验中 B容器中观察到的现象是
________________________________________________________________________;
B容器中发生反应的离子方程式是___________________________________________。
(2)打开止水夹a,使A容器开始反应一段时间后再夹紧止水夹 a,实验中观察到的
现象是________________。
B容器中发生反应的离子方程式是______________________________________。
6. 将铁粉、铜粉、FeCl 溶液和CuCl 溶液混合于某容器中充分反应(假定容器不参与反
3 2
第1页应)。试判断下列情况下,溶液中存在的金属离子和金属单质。
(1)若铁粉有剩余,则容器中不可能有____________________________________;
(2)若氯化铜有剩余,则容器中可能有_____________________________________;
(3)若氯化铁和氯化铜都有剩余,则容器中不可能有____________,可能有
__________。
第2页铁及其化合物(2)同步练习参考答案
1. 【答案】A
【解析】Fe O 与HCl反应,既有FeCl 生成,又有FeCl 生成。
3 4 3 2
2. 【答案】C
【解析】溶液中的Fe2+与加入的新制氯水发生反应:2Fe2++Cl =2Fe3++2Cl-,故氧
2
化性:Fe3+