文档内容
钠及其化合物(2)同步练习
(答题时间:25分钟)
一、选择题:本题包括12小题,每小题4分,共48分。
1. 一定量的NaO 与CO 反应,得到固体物质41.8 g,恰好与1 L 1 mol·L-1的稀盐酸完
2 2 2
全反应。下列说法正确的是( )
A. 41.8 g固体物质为NaCO
2 3
B. 41.8 g固体物质为0.1 mol Na CO 和0.4 mol Na O 的混合物
2 3 2 2
C. 一定量的NaO 为78 g
2 2
D. 41.8 g固体物质为31.2 g NaHCO 和10.6 g Na CO 的混合物
3 2 3
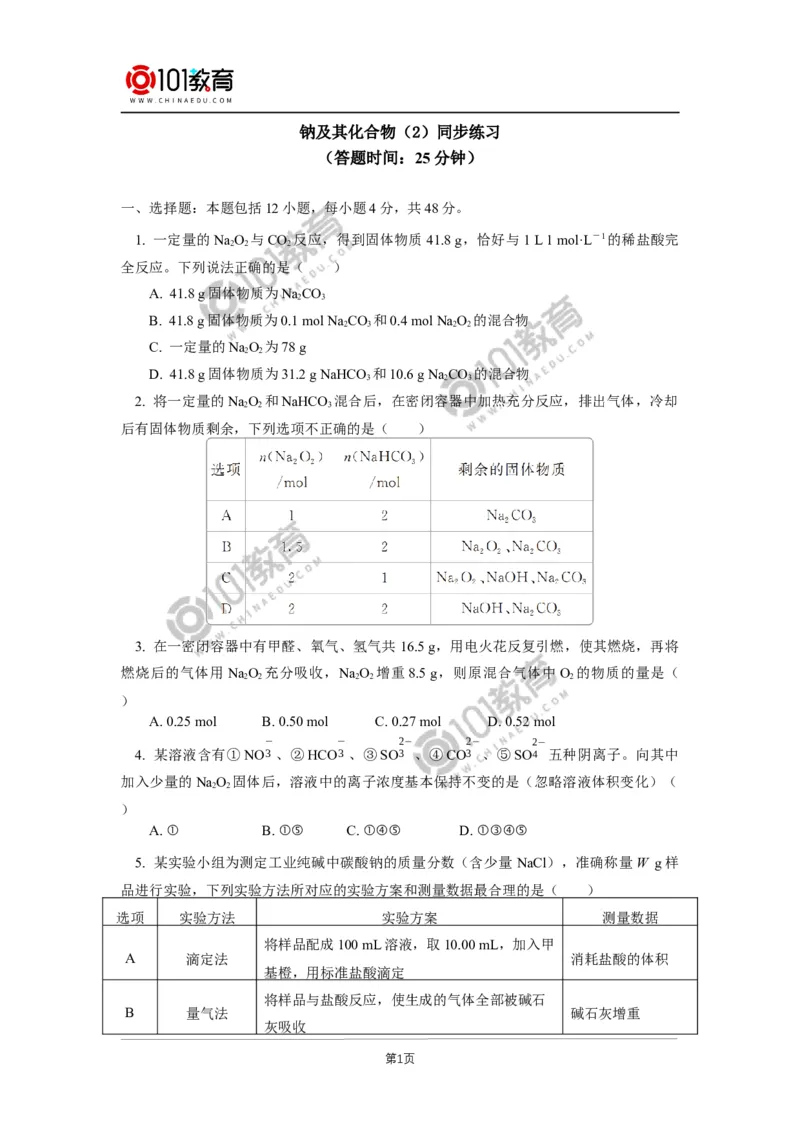
2. 将一定量的NaO 和NaHCO 混合后,在密闭容器中加热充分反应,排出气体,冷却
2 2 3
后有固体物质剩余,下列选项不正确的是( )
3. 在一密闭容器中有甲醛、氧气、氢气共 16.5 g,用电火花反复引燃,使其燃烧,再将
燃烧后的气体用NaO 充分吸收,NaO 增重8.5 g,则原混合气体中O 的物质的量是(
2 2 2 2 2
)
A. 0.25 mol B. 0.50 mol C. 0.27 mol D. 0.52 mol
− − 2− 2− 2−
4. 某溶液含有①NO3 、②HCO3 、③SO3 、④CO3 、⑤SO4 五种阴离子。向其中
加入少量的NaO 固体后,溶液中的离子浓度基本保持不变的是(忽略溶液体积变化)(
2 2
)
A. ① B. ①⑤ C. ①④⑤ D. ①③④⑤
5. 某实验小组为测定工业纯碱中碳酸钠的质量分数(含少量 NaCl),准确称量W g样
品进行实验,下列实验方法所对应的实验方案和测量数据最合理的是( )
选项 实验方法 实验方案 测量数据
将样品配成100 mL溶液,取10.00 mL,加入甲
A 滴定法 消耗盐酸的体积
基橙,用标准盐酸滴定
将样品与盐酸反应,使生成的气体全部被碱石
B 量气法 碱石灰增重
灰吸收
第1页将样品放入烧杯中,置于天平上,加入足量盐
C 重量法 减轻的质量
酸
将样品与盐酸反应,气体通过排水量气装置量
D 量气法 排出水的体积
气
二、非选择题
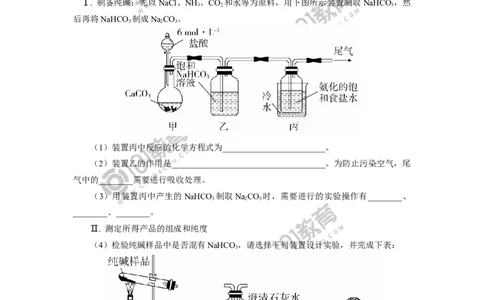
6. 某化学兴趣小组模拟“侯氏制碱法”制纯碱并进行后续实验。
Ⅰ. 制备纯碱:先以NaCl、NH 、CO 和水等为原料,用下图所示装置制取NaHCO ,然
3 2 3
后再将NaHCO 制成NaCO。
3 2 3
(1)装置丙中反应的化学方程式为________________________。
(2)装置乙的作用是____________________________________。为防止污染空气,尾
气中的________需要进行吸收处理。
(3)用装置丙中产生的NaHCO 制取NaCO 时,需要进行的实验操作有________、
3 2 3
________、________。
Ⅱ. 测定所得产品的组成和纯度
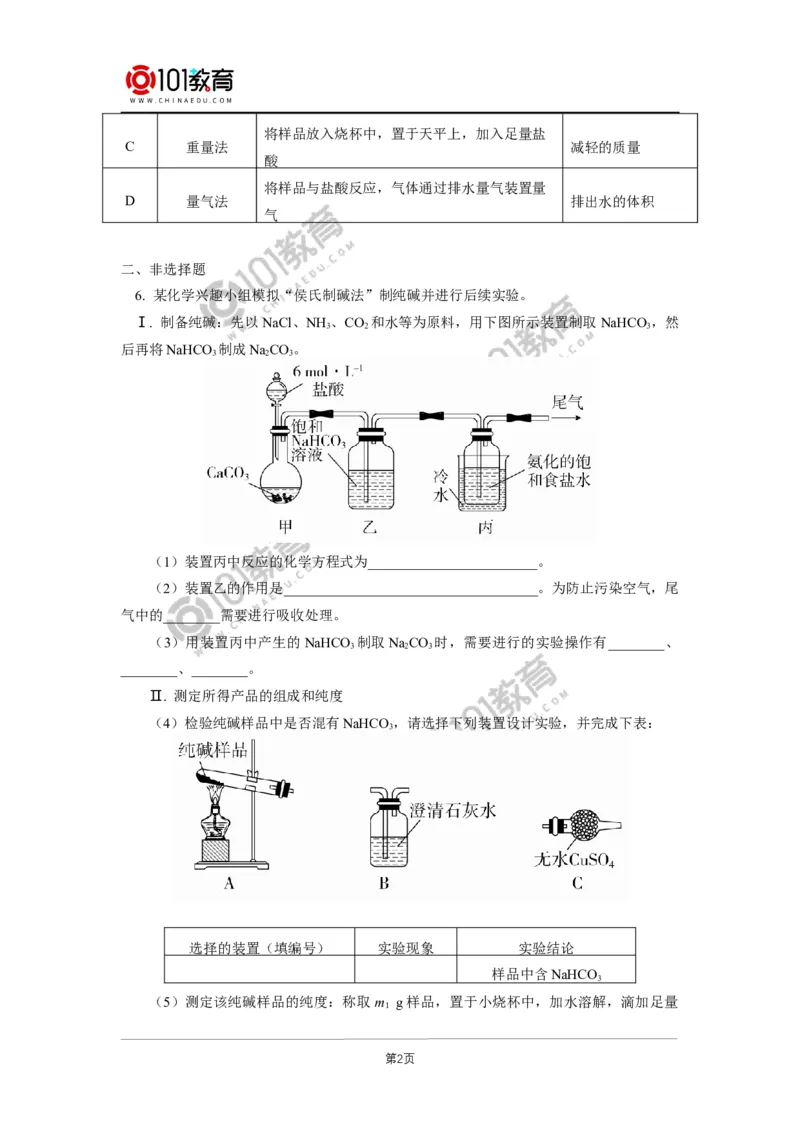
(4)检验纯碱样品中是否混有NaHCO ,请选择下列装置设计实验,并完成下表:
3
选择的装置(填编号) 实验现象 实验结论
样品中含NaHCO
3
(5)测定该纯碱样品的纯度:称取 m g样品,置于小烧杯中,加水溶解,滴加足量
1
第2页CaCl 溶液。将反应混合物过滤、洗涤、干燥、称量,得到固体的质量为 m g。则该纯碱
2 2
样品的纯度为 ____________。
7. 有一含NaCl、NaCO·10H O和NaHCO 的混合物,某同学设计如图所示的实验装置,
2 3 2 3
通过测量反应产生的CO 和HO的质量,来确定该混合物中各组分的质量分数。
2 2
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是________。
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰
的U形管D的质量。
③打开活塞K、K,关闭K,缓缓鼓入空气数分钟,其目的是________。
1 2 3
④关闭活塞K、K,打开K,点燃酒精灯加热至不再产生气体。装置B中发生反应的
1 2 3
化学方程式为___________________________________________________________。
⑤打开活塞K ,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U
1
形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是
____________________________________________________________________。
②E处干燥管中盛放的药品是________,其作用是____________________________,
如果实验中没有该装置,则会导致测量结果NaHCO 的质量分数________(填“偏大”、
3
“偏小”或“无影响”)。
③若样品质量为w g,反应后C、D装置增加的质量分别为m g、m g,则混合物中
1 2
NaCO·10H O的质量分数为______(用含w、m、m 的代数式表示)。
2 3 2 1 2
第3页钠及其化合物(2)同步练习参考答案
1. 答案:B
【解析】如果41.8 g固体全为NaCO,其物质的量为0.39 mol,则其不可能恰好与1 L
2 3
1 mol·L-1的稀盐酸完全反应,A错误;设41.8 g固体物质中,含NaCO 的物质的量为x
2 3
mol,NaO 的物质的量为y mol,则有106 g·mol-1×x mol+78 g·mol-1×y mol=41.8 g,2(x
2 2
+y)mol=1 mol·L-1×1 L=1 mol,解得x=0.1,y=0.4,B正确;根据Na元素守恒,可知
1 1
2 2
n(NaO )= n(NaCl)= n(HCl)=0.5 mol,即原NaO 的质量为39 g,C错误;
2 2 2 2
NaO 与CO 反应不可能生成NaHCO ,D错误。
2 2 2 3
2. 答案:B
【解析】将 NaO 与 NaHCO 混合加热,有关的反应方程式依次为 2NaHCO
2 2 3 3
NaCO +CO↑+HO、2CO +2NaO===2Na CO +O 、2NaO +2HO===4NaOH+O↑。
2 3 2 2 2 2 2 2 3 2 2 2 2 2
当NaO 与NaHCO 的物质的量之比为1∶2时,二者反应的总方程式为2NaO +4NaHCO
2 2 3 2 2 3
4NaCO +O↑+2HO;当NaO 与NaHCO 的物质的量之比为1∶1时,二者反应的总
2 3 2 2 2 2 3
方程式为 2NaO +2NaHCO 2NaCO +O↑+2NaOH,即当 n(NaO )∶n
2 2 3 2 3 2 2 2
(NaHCO )≤1∶2时,反应后剩余固体为 NaCO ,当1∶2<n(NaO )∶n(NaHCO )
3 2 3 2 2 3
≤1∶1,反应后剩余固体的成分为NaCO 和NaOH,当n(NaO )∶n(NaHCO )>1∶1时,
2 3 2 2 3
反应后剩余固体为NaO、NaOH、NaCO,由此可以判断A、C、D正确,B错误。
2 2 2 3
3. 答案:A
【解析】HCHO、O 、H 混合物燃烧生成CO 、HO,CO 、HO与NaO 反应的化学
2 2 2 2 2 2 2 2
方程式为:
2CO+2NaO===2Na CO+O①
2 2 2 2 3 2
2HO+2NaO===4NaOH+O↑②
2 2 2 2
甲醛可以表示为CO·H ,反应①相当于CO与NaO 反应生成NaCO ,因此相当于甲
2 2 2 2 3
醛中的碳、氧按CO比例进入NaCO;反应②相当于H 进入NaOH中,即混合物中甲醛的
2 3 2
H和H 进入NaOH中,故只考虑净反应,则HCHO、O 、H 中的O 的质量即为剩余气体
2 2 2 2
的质量,即16.5 g-8.5 g=8 g,共0.25 mol,A正确。
4. 答案:A
2− 2− 2−
【解析】过氧化钠具有强氧化性,可将SO3 氧化为SO4 ,故加入过氧化钠后SO3
2− − 2−
、SO4 浓度均发生变化;过氧化钠溶于水生成 NaOH,OH-与HCO3 反应生成CO3 ,导
− 2− −
致溶液中HCO3 和CO3 浓度发生变化,故只有NO3 浓度基本保持不变。
5. 答案:A
【解析】用甲基橙作指示剂,盐酸滴定样品溶液发生的反应为 NaCO +
2 3
第4页2HCl===2NaCl+CO↑+HO,根据消耗标准盐酸的体积确定n(HCl),再结合反应计算n
2 2
(NaCO )及m(NaCO ),从而确定纯碱中碳酸钠的质量分数,A正确;样品与盐酸反
2 3 2 3
应产生的CO 中含有水蒸气,均被碱石灰吸收,导致测定结果偏高,且测量碱石灰增重不
2
属于量气法,B错误;CO 逸出带出水蒸气,质量差变大,导致测定结果偏高,C错误;
2
CO 能溶于水,不能用排水法收集,可用排饱和NaHCO 溶液的方法收集CO,D错误。
2 3 2
6. 答案:(1)NH +CO+HO+NaCl===NaHCO↓+NH Cl
3 2 2 3 4
(2)除去CO 中的HCl气体 氨气(NH )
2 3
(3)过滤 洗涤 灼烧
(4)A、B B中溶液变浑浊(或A、C C中物质变蓝或A、C、B C中物质变蓝,
B中溶液变浑浊)
106m
2
m
(5) 1 %
【解析】(1)NaHCO 的溶解度不大,在氨化的饱和食盐水中通入过量CO 可析出
3 2
NaHCO 沉淀。
3
(2)用装置甲和相应药品制得的CO 中混有HCl,用装置乙可以除去HCl。氨化的饱
2
和食盐水可挥发出污染环境的NH ,尾气应进行处理。
3
(3)装置丙中产生了NaHCO 沉淀,将过滤后得到的NaHCO 进行洗涤,然后灼烧即
3 3
可得到纯碱。
(4)用酒精灯加热时,NaCO 受热不分解,NaHCO 受热分解可生成CO 、HO和
2 3 3 2 2
NaCO ,加热纯碱样品,只要能检验出有 CO 或 HO 生成即可说明纯碱样品中含有
2 3 2 2
NaHCO 。
3
m
2
100
(5)实验所得沉淀为CaCO ,n(NaCO )=n(CaCO )= mol,m(NaCO )
3 2 3 3 2 3
106m 106m 106m
2 2
2
100 100m m
= g,纯碱样品的纯度为 1 ×100%= 1 %。
7. 答案:(除标注外,每空2分)(1)①检查装置气密性(1分) ③除去装置中的水
蒸气和二氧化碳
④2NaHCO NaCO+HO↑+CO↑
3 2 3 2 2
NaCO·10H O NaCO+10HO↑
2 3 2 2 3 2
(2)①NaCO·10H O和NaHCO 的质量分数测定结果偏小,NaCl的质量分数测定结
2 3 2 3
果偏大
②碱石灰 防止空气中的CO 和水蒸气进入D中影响测定结果 偏大(1分)
2
18m
286(m − 2 )
1 44
180w
③ ×100%(3分)
第5页【解析】本题考查考生对元素化合物的认识和理解以及对实验数据的分析处理能力。
(1)①组装好实验装置后首先应检查装置气密性。③由于装置中存在CO 和水蒸气,应先
2
鼓入空气除去装置中的CO 和水蒸气。④由物质的性质可知该装置在加热时发生的反应为
2
2NaHCO NaCO+HO↑+CO↑、NaCO·10H O NaCO+10HO↑。
3 2 3 2 2 2 3 2 2 3 2
(2)①加热后有部分CO 和水蒸气会残留在装置中,必须鼓入空气使其排出完全被吸
2
收,若不鼓入空气,则测得的NaHCO 和NaCO·10H O的质量分数偏小,NaCl的质量分
3 2 3 2
数偏大。②装置E是防止空气中的CO 和水蒸气进入装置D,故干燥管中盛放的药品是碱
2
石灰,如果没有该装置,会使测得的NaHCO 的质量分数偏大。③由题目信息知反应放出
3
的CO 的质量为m g,根据反应的化学方程式2NaHCO NaCO+HO↑+CO↑,可计
2 2 3 2 3 2 2
18m
2
44
算出该反应中产生的水的质量为 g,从而计算出NaCO·10H O分解产生水的质量为
2 3 2
18m
2
44
(m- )g,再根据NaCO·10H O NaCO+10HO↑,计算出NaCO·10H O的
1 2 3 2 2 3 2 2 3 2
18m
286(m − 2 )
1 44
180
质量为 ,最后计算出混合物中NaCO·10H O的质量分数为
2 3 2
18m
286(m − 2 )
1 44
180w
×100%。
第6页