文档内容
化学反应与能量变化(2)同步练习
(答题时间:25分钟)
一、选择题:
1. 下列有关电池叙述正确的是( )
A. 水果电池是高效环保的家用电池
B. 锌锰干电池是一种常用的二次电池
C. 锌锰干电池碳棒是负极,锌片是正极
D. 锌锰干电池工作一段时间后锌外壳逐渐变薄
2. 下列说法正确的是( )
A. 镍氢电池、锂电池和碱性锌锰干电池都是二次电池
B. 燃料电池是一种高效但是会污染环境的新型电池
C. 化学电池的反应基础是氧化还原反应
D. 铅蓄电池放电的时候正极材料是Pb,负极材料是PbO
2
3. 有关原电池的下列说法中正确的是( )
A. 在外电路中电子由正极流向负极
B. 在原电池中负极发生还原反应
C. 原电池工作时,阳离子向正极方向移动
D. 原电池中正极一定是不活泼金属
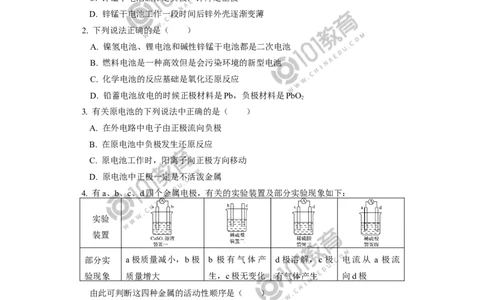
4. 有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
实验
装置
部分实 a极质量减小,b极 b 极有气体产 d极溶解,c极 电流从 a 极流
验现象 质量增大 生,c极无变化 有气体产生 向d极
由此可判断这四种金属的活动性顺序是( )
A. a>b>c>d B. b>c>d>a
C. d>a>b>c D. a>b>d>c
5. 已知四种金属A、B、C、D,根据下列事实:①A+B2+=A2++B;②D+2HO=D
2
(OH)+H↑;③以B、E为电极与E的盐溶液组成原电池,电极反应为E2++2e-=E,B
2 2
-2e-=B2+,由此可知,A2+、B2+、D2+、E2+的氧化性强弱关系是( )
A. D2+>A2+>B2+>E2+
B. A2+>B2+>D2+>E2+
C. D2+>E2+>A2+>B2+
第1页D. E2+>B2+>A2+>D2+
6. 锌、稀硫酸和铜组成的原电池装置中,当导线中有 1 mol电子通过时,理论上两极的
变化是( )
①锌片溶解32. 5 g;②锌片增重32. 5 g;③铜片上析出1 g H;④铜片上析出1 mol H
2 2
A. ①③ B. ①④
C. ②③ D. ②④
二、填空题
7. 理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=
2Ag +Cu2+”设计一个化学电池(正极材料用石墨棒)回答下列问题:
(1)该电池的负极材料是________,发生________(填“氧化”或“还原”)反应,
电解质溶液是______________________;
(2)正极上出现的现象是 _________________________________________;
(3)若导线上转移电子1 mol,则生成银____g。
8. 微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是 Ag O和
2
Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-=ZnO+HO,Ag O+HO+2e
2 2 2
-=2Ag+2OH-,总反应为Ag O+Zn=ZnO+2Ag。根据反应式回答问题:
2
(1)Zn是________极,Ag O发生________反应。
2
(2)电子由________极流向________极(填“Zn”或“Ag O”),当通过电路1 mol电
2
子时,负极消耗物质的质量是________g。
(3)在使用过程中,电解质溶液中 KOH的物质的量________(填“增大”“减小”
或“不变”)。
第2页化学反应与能量变化(2)同步练习参考答案
1.【答案】D
【解析】水果电池产生的电流非常微弱,不能作为家用电池,A错误;锌锰干电池是
一种常用的一次电池,其中锌作负极,碳棒作正极,锌锰干电池工作时,Zn放电消耗,故
工作一段时间后锌外壳会逐渐变薄,故B、C错误,D正确。
2.【答案】C
【解析】碱性锌锰干电池是一次电池;燃料电池是一种高效且不会污染环境的新型电
池;铅蓄电池放电的时候正极材料是PbO2,负极材料是Pb。
3.【答案】C
【解析】在原电池中,电子从负极流向正极;原电池中负极发生氧化反应;随着反应
的进行,阳离子在正极被还原,所以电解质溶液中的阳离子向正极移动;原电池中一般正
极金属比负极金属活泼性差,但不一定是不活泼金属,故选C。
4. 【答案】C
【解析】装置一是原电池,a极质量减小,说明a极金属易失去电子形成离子,故a极
金属比b极金属活泼;装置二没有形成原电池,可知b比c活泼,且c位于金属活动性顺序
表中氢的后面;装置三和四均形成原电池,易知d比c活泼,d比a活泼。因此四种金属的
活动性顺序为d>a>b>c,故选C。
5.【答案】D
【解析】由①知,A比B活泼;由②知,D的活泼性较强,能置换出HO中的氢,故
2
D 的活泼性大于 A;由③知,B 作负极,活泼性大于 E,则金属的活动性顺序是
D>A>B>E,而金属单质的还原性越弱,其阳离子的氧化性越强,故D正确。
6.【答案】A
【解析】由电池总反应Zn+2H+=Zn2++H↑、正极反应2H++2e-=H↑、负极反应
2 2
Zn-2e-=Zn2+可知,每当1 mol电子通过铜片时,会有0. 5 mol(即32. 5 g)锌溶解,铜
片上析出0. 5 mol(即1 g)H2。
7.【答案】(1)Cu 氧化 AgNO 溶液
3
(2)石墨棒上出现银白色物质
(3)108
【解析】在Cu+2Ag+=2Ag +Cu2+中,Cu作还原剂,应作原电池的负极,失去电子,
发生氧化反应;Ag+作氧化剂,在原电池的正极得电子,故石墨棒上有银白色物质析出,且
每转移1 mol电子,则生成银108 g;电解质是含Ag+的可溶性盐,通常是AgNO 溶液。
3
8.【答案】(1)负 还原 (2)Zn Ag O 32. 5 (3)不变
2
【解析】(1)根据电极反应可知Zn失电子被氧化而溶解,Ag O得电子被还原发生还
2
第3页原反应。(2)发生原电池反应时,电子由负极经外电路到正极,即电子从Zn极经外电路
到Ag O极,当通过电路1 mol电子时,负极消耗Zn的质量是32. 5 g。(3)电池中KOH
2
只起到增强导电的作用,不参与反应,故电池使用过程中KOH的量不变。
第4页