文档内容
甲烷和烷烃的性质同步练习
(答题时间:40分钟)
一、选择题
1. 关于烷烃的说法不正确的是( )
A. 所有链状烷烃均符合通式C H
n 2n+2
B. 烷烃分子中一定存在C—C σ键
C. 烷烃分子中的碳原子均采取sp3杂化
D. 烷烃分子中碳原子不一定在一条直线
2. 下列有关烷烃的叙述中,正确的是( )
A. 常温常压下,所有烷烃都为气体
B. 除甲烷外,大多数烷烃都能使酸性KMnO 溶液褪色
4
C. 在一定条件下,烷烃能与氯气、溴水等发生取代反应
D. 烷烃在空气中都能燃烧,但不一定产生淡蓝色火焰
3. 下列物质的命名中肯定正确的是( )
A. 2,2二甲基丁烷
B. 3,3二甲基丁烷
C. 2甲基3乙基丁烷
D. 4甲基3乙基己烷
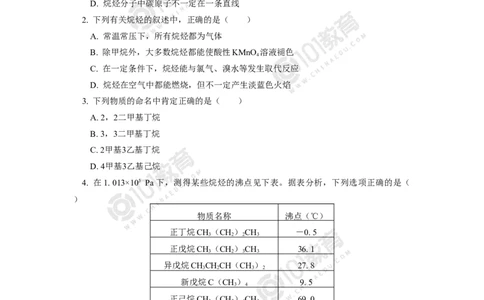
4. 在1. 013×105 Pa下,测得某些烷烃的沸点见下表。据表分析,下列选项正确的是(
)
物质名称 沸点(℃)
正丁烷CH(CH)CH -0. 5
3 2 2 3
正戊烷CH(CH)CH 36. 1
3 2 3 3
异戊烷CHCHCH(CH) 27. 8
3 2 3 2
新戊烷C(CH) 9. 5
3 4
正己烷CH(CH)CH 69. 0
3 2 4 3
A. 在标准状况下,新戊烷是气体
B. 在1. 013×105 Pa、20 ℃时,C H 都是液体
5 12
C. 烷烃随碳原子数的增加,沸点降低
D. C H 随着支链数的增加,沸点降低
5 12
5. 下列有机物:①正丁烷,②丙烷,③2甲基丁烷,④异丁烷,⑤己烷。沸点由高到低
的顺序为( )
A. ②①④③⑤ B. ⑤③④①②
第1页C. ⑤③①④② D. ②①③④⑤
二、填空题
6. (1) 的名称为_________________。
(2)写出下列各种有机物的结构简式。
①2,3二甲基4乙基己烷:___________________________。
②支链只有一个乙基且相对分子质量最小的烷烃:
_______________________________________________________
_____________________________________________________。
第2页甲烷和烷烃的性质同步练习参考答案
1.【答案】B
【解析】甲烷中不存在C—C键,B错误。
2.【答案】D
【解析】常温常压下,碳原子数小于或等于4的烷烃为气体,碳原子数大于4的烷烃
为液体或固体;烷烃的化学性质一般比较稳定,通常不与强酸、强碱、强氧化剂(如酸性
KMnO 溶液)和强还原剂反应;烷烃在光照条件下可与卤素单质发生取代反应,但不与溴
4
水反应;烷烃在空气中都能燃烧,甲烷、乙烷等燃烧时产生淡蓝色火焰,但随着烷烃中碳
原子数的增加,其含碳量升高,在空气中燃烧往往不充分,火焰明亮,甚至伴有黑烟。
3.【答案】A
【解析】先根据选项名称写结构简式,再重新命名。
4.【答案】D
【解析】新戊烷的沸点是9. 5 ℃,标准状况下是液体,在1. 013×105 Pa、20 ℃时是气
体,则A、B均错误;随碳原子数的增加,烷烃的沸点逐渐升高,C错误;C H 的3种同
5 12
分异构体中,随着支链数的增加,沸点逐渐降低,D正确。
5.【答案】C
【解析】五种有机物均为烷烃,烷烃分子中碳原子数目越多,其沸点越高;碳原子数
目相同的烷烃,其支链越多,沸点越低,故五种烷烃的沸点由高到低的顺序为⑤③①④②。
6.【答案】(1)2,3,4,5四甲基己烷
第3页乙烯和烯烃的性质同步练习
(答题时间:40分钟)
一、选择题
1. 下列关于乙烯和乙烷相比较的说法中,不正确的是( )
A. 乙烯属于不饱和链烃,乙烷属于饱和链烃
B. 乙烯分子中所有原子位于同一平面上,乙烷分子则为立体结构,所有原子不在同一
平面上
C. 乙烯和乙烷中的共价键均有σ键和π键
D. 乙烯能使酸性KMnO 溶液褪色,乙烷不能
4
2. 丙烯是一种重要的化工原料、燃料,下列有关丙烯及聚丙烯的说法正确的是( )
A. 丙烯与等物质的量的氯化氢加成,只生成一种产物
B. 1 mol丙烯完全燃烧的耗氧量为4. 5 mol
C. 聚丙烯的链节是—CH—CH—CH—
2 2 2
D. 1 mol丙烯和1 mol聚丙烯完全燃烧放出CO 的量相同
2
3. 下列说法正确的是( )
A. C H 与C H 一定互为同系物
2 4 4 8
B. 乙烯和乙烷都能使酸性KMnO 溶液褪色
4
C. 1丁烯与2丁烯互为同分异构体
D. 新戊烷和2,2二甲基丙烷互为同分异构体
4. 下列有机物分子中,可存在顺反异构体的是( )
A. CH =CHCH B. CH=CHCH CH
2 3 2 2 3
C. CHCH=C(CH) D. CH CH=CHCl
3 3 2 3
5. 分子式为C HCl且可以因发生加成反应使溴的四氯化碳溶液褪色的有机物的可能结构
3 5
(考虑顺反异构)共有( )
A. 3种 B. 4种 C. 5种 D. 6种
6. 某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双
键,核磁共振氢谱表明分子中只有一种类型的氢原子。
(1)A的结构简式为___________________________________。
(2)A中的碳原子是否都处于同一平面?________(填“是”或“不是”)。是否存
在顺反异构?________(填“存在”或“不存在”)。
(3)A与HO发生反应的方程式为_________________________
2
_____________________________________________________。
(4)A发生加聚反应生成的产物结构简式为
_____________________________________________________。
第4页第5页乙烯和烯烃的性质同步练习参考答案
1.【答案】C
【解析】乙烷中只有σ键无π键,C不正确。
2.【答案】B
【解析】丙烯结构不对称,与 HCl 加成可得到两种产物 CHCHClCH 、
3 3
6
(3+ )
4
CHClCH CH ,A错误;1 mol丙烯(C H )与O 完全反应,耗氧量为 mol=4. 5
2 2 3 3 6 2
mol,B正确;聚丙烯的链节是—CH—CH(CH )—,C错误;丙烯和聚丙烯的分子式不
2 3
同,相对分子质量不同,等物质的量的丙烯和聚丙烯完全燃烧放出 CO 的量不相同,D错
2
误。
3.【答案】C
【解析】C H 可以是烯烃也可以是环烷烃,A项错误;乙烯能使酸性KMnO 溶液褪色,
4 8 4
而乙烷不能,B项错误;新戊烷和2,2二甲基丙烷是同一种物质,D项错误。
4.【答案】 D
5.【答案】B
【解析】根据氯原子的位置不同,可写出3种结构简式:
CH =CHCH Cl、CH =CClCH 、CHCl=CHCH ,其中CHCl=CHCH 还存在顺反异
2 2 2 3 3 3
构体,故共有4种可能的结构。
6.【答案】
【解析】(1)红外光谱表明分子中含有碳碳双键,说明可能是烯烃,由该烃的相对分
子质量及烯烃的通式C H 14n=84,n=6,从而得出该烃的分子式是C H ;又该烃分子
n 2n, 6 12
结构中只有一种化学环境的氢原子,说明它的结构对称,推断出它的结构是
。
第6页(2)根据双键碳原子及与其相连的原子一定在同一平面上的结构特点,该烯烃中的碳
原子均处于同一平面;由于双键碳原子连接的基团都是甲基,故该烯烃不存在顺反异构。
(3)含 可以与HO加成反应。
2
(4)含 可以发生加聚反应。
第7页乙炔和炔烃的性质同步练习
(答题时间:40分钟)
一、选择题
1. 下列说法正确的是( )
A. 丙炔分子中的三个碳原子不可能在同一直线上
B. 乙炔分子中碳碳三键中的三个共价键性质完全相同
C. 分子组成符合C H 的链烃一定是炔烃
n 2n-2
D. 在所有符合通式C H 的炔烃中,乙炔所含氢元素的质量分数最小
n 2n-2
2. 鉴别甲烷、乙烯、乙炔三种气体可采用的方法是( )
A. 通入溴水中,观察溴水是否褪色
B. 通入酸性高锰酸钾溶液中,观察溶液颜色是否变化
C. 点燃,检验燃烧产物
D. 点燃,观察火焰明亮程度及产生黑烟量的多少
3. 块状固体电石遇水会剧烈反应生成乙炔气体。实验室若用此法制取乙炔,选择的装置
最好是( )
4. 某烃与溴的四氯化碳溶液反应生成CHBr CBr CHCH,则与该烃属于不同类别的该烃
2 2 2 3
的同分异构体是( )
A. B.
C. CHCHCH CH D. CH CH—CH CH
3 2 2 2 2
5. 下面有关丙烷、丙烯和丙炔的说法正确的是( )
A. 如图所示,丙烷、丙烯、丙炔的球棍模型分别为:
B. 相同物质的量的3种物质完全燃烧,生成的气体在标准状况下的体积比为3∶2∶1
C. 相同质量的3种物质完全燃烧,丙烷消耗的氧气量最多
D. 丙烷的一氯代物只有1种
6. 某烃的结构简式如下,下列说法不正确的是( )
第8页A. 1 mol该烃完全燃烧消耗O 11 mol
2
B. 与氢气完全加成后的每个产物分子中含2个甲基
C. 1 mol该烃完全加成消耗3 mol Br
2
D. 每个分子中一定共平面的碳原子有6个
二、非选择题
7. 下图所示的实验装置可用于制取乙炔。
请回答下列问题:
(1)图中A管的作用是 ,制取乙炔的化学方程式是 。
( 2 ) 将 乙 炔 通 入 酸 性 KMnO 溶 液 中 , 可 以 观 察 到 的 现 象 是
4
,乙炔发生了 反应。
(3)将乙炔通入溴的四氯化碳溶液中,可以观察到的现象是 ,乙
炔发生了 反应。
(4)为了安全,点燃乙炔前应 ,乙炔燃烧时的实验现象是 。
*8. 实验室制得的乙炔中常混有HS、PH 等杂质气体。如图是两学生设计的实验装置,
2 3
用来测定电石样品中CaC 的纯度,右边的反应装置相同而左边的气体发生装置不同。
2
(1)A瓶中的液体可以从酸性KMnO 溶液和CuSO 溶液中选择,应该选择 ,
4 4
它的作用是 。
(2)写出实验室制取乙炔的化学方程式: 。
(3)装置Ⅰ的主要缺点是 ;
装置Ⅱ的主要缺点是 ;
若选用Ⅱ装置来完成实验,则应采取的措施是 。
(4)若称取m g电石,反应完全后,测得 B处溴水增重 n g,则CaC 的纯度为
2
。
第9页第10页乙炔和炔烃的性质同步练习参考答案
1.【答案】D
【解析】丙炔分子中存在类似乙炔分子的碳碳三键直线形结构,丙炔分子中的三个碳
原子在同一直线上,故A错误;每个碳碳三键是由1个σ键和2个π键构成的,其中σ键
稳定、π键不稳定,分子中碳碳间的三个共价键性质不完全相同,故B错误;分子组成符
合C H 的链烃,可能含有2个碳碳双键,为二烯烃,也可能含有1个碳碳三键,为炔烃,
n 2n-2
2
n
故C错误;符合通式C H 的炔烃中,1个碳原子结合的氢原子的平均数目为2- ,n越
n 2n-2
2
n
大,2- 的值越大,氢元素的质量分数越大,则乙炔所含氢元素的质量分数最小,故 D正
确。
2.【答案】D
【解析】乙烯和乙炔均可以使溴水和酸性高锰酸钾溶液褪色,故A、B项错误;甲烷、
乙烯、乙炔均属于烃类,完全燃烧的产物均为 CO 和HO,故无法根据燃烧产物鉴别,C
2 2
项错误;由于甲烷、乙烯、乙炔中碳元素的百分含量有差别,故燃烧时产生的现象是不同
的,分别点燃甲烷、乙烯、乙炔,火焰越来越明亮,黑烟越来越浓,D项正确。
3.【答案】B
【解析】实验室用块状电石与饱和食盐水在常温下反应,发生装置应选择固液常温型
装置;由于反应比较剧烈而需严格控制加饱和食盐水的速率,故应选择B装置。
4.【答案】D
【解析】由生成的卤代烃的结构简式可知该烃为 ,与该烃属于不同
类别的该烃的同分异构体不是炔烃,可以是二烯烃。
5.【答案】C
【解析】由乙炔的结构知,丙炔分子中的3个碳原子应该在同一条直线上,A项错误;
相同物质的量的3种物质完全燃烧,生成CO 的物质的量相等,标准状况下水不为气体,
2
体积忽略不计,则标准状况下生成的气体体积相等,故体积比应为 1∶1∶1,B项错误;
三种物质中丙烷的含氢量最高,故等质量的3种物质充分燃烧,丙烷耗氧量最多,C项正
确;丙烷分子中存在2种不同类型的氢原子,则它的一氯代物有2种,D项错误。
6.【答案】B
12
4
【解析】该有机物分子式为C H ,1 mol该烃完全燃烧消耗O 的物质的量为(8+
8 12 2
)mol=11 mol,A项正确;该烃的每个分子中有一个支链,与氢气完全加成后的产物为
CHCHCHCH(CHCH )CHCH ,它的每个分子中含有3个甲基,B项错误;该烃的每
3 2 2 2 3 2 3
个分子中含有一个碳碳双键和一个碳碳三键,1 mol该烃完全加成消耗3 mol Br ,C项正确;
2
第11页结合乙烯和乙炔的结构判断,该烃的每个分子中一定共平面的碳原子有6个,D项正确。
7.【答案】(1)调节液面高度,控制反应的发生和停止
CaC +2H O Ca(OH)+C H↑
2 2 2 2 2
(2)酸性KMnO 溶液褪色 氧化
4
(3)溴的四氯化碳溶液褪色 加成
(4)检验乙炔的纯度 火焰明亮并伴有浓烈的黑烟
【解析】(1)本题中给出的制取乙炔的实验装置应用的是连通器原理,通过上下移动
A管调节右管液面的高度,控制电石与饱和食盐水中的水反应的发生和停止。制取乙炔的
化学方程式为CaC +2H O Ca(OH) +C H↑。(2)将乙炔通入酸性KMnO 溶液中,乙
2 2 2 2 2 4
炔发生氧化反应而使酸性KMnO 溶液褪色。(3)将乙炔通入溴的四氯化碳溶液中,乙炔
4
发生加成反应而使溴的四氯化碳溶液褪色。(4)点燃乙炔前应先检验乙炔的纯度,乙炔燃
烧时产生明亮的火焰并伴有浓烈的黑烟。
8.【答案】(1)CuSO 溶液 除去乙炔中混有的HS和PH 等杂质气体
4 2 3
(2)CaC +2H O Ca(OH)+C H↑
2 2 2 2 2
(3)少量乙炔会从长颈漏斗中逸出,引起实验误差,且不易控制液体的添加量
反应产生的泡沫会堵塞导管
在导管口处塞上一团棉花
32n
13m
(4) ×100%
【解析】(1)酸性高锰酸钾溶液具有强氧化性,能氧化乙炔,因此选择硫酸铜溶液除
去乙炔中混有的HS和PH 等杂质气体。
2 3
(2)实验室制取乙炔的化学方程式为CaC +2H O Ca(OH)+C H↑。
2 2 2 2 2
(3)根据装置Ⅰ的结构可知其主要缺点是少量乙炔会从长颈漏斗中逸出,引起实验误
差,且不易控制液体的添加量。装置Ⅱ的主要缺点是反应产生的泡沫会堵塞导管;根据以
上分析可知若选用装置Ⅱ来完成实验,则应采取的措施是在导管口处塞上一团棉花。
(4)若称取m g电石,反应完全后,测得B处溴水增重n g,则根据方程式C H+2Br
2 2 2
n
×64
n 26
26 m
CHBr CHBr 可知生成的乙炔的物质的量是 mol,所以CaC 的纯度为 ×100%=
2 2 2
32n
13m
×100%。
第12页