文档内容
第一章 物质及其变化
第一节 物质的分类及转化 课时作业
第二课时 分散系和胶体
基础达标
1.分散系是混合分散体系的简称,下列关于分散系的说法正确的是( )
A.根据体系的稳定性,可将分散系分为溶液、胶体和浊液
B.一种分散系的分散质可以是固态、液态或气态,但只能是纯净物
C.利用丁达尔效应可以区分溶液和胶体,它利用了光的折射原理
D.用光束照射碳素墨水会出现丁达尔效应
2.下列有关叙述不正确的是( )
A.稀豆浆、硅酸、氯化铁溶液都为胶体
B.用可见光束照射以区别溶液和胶体
C.用石膏或盐卤点制豆腐与胶体的性质有关
D.明矾能生成氢氧化铝胶体,可用作净水剂
3.下列关于胶体和溶液的说法中正确的是( )
A.胶体不均一、不稳定,静置后易产生沉淀,溶液均一、稳定、静置不产生沉淀
B.溶液和胶体都是纯净物,浊液是混合物
C.光线通过时,胶体产生丁达尔效应,溶液则无丁达尔效应
D.只有胶状物如胶水、果冻类的物质才能称为胶体
4.下列关于胶体的认识错误的是( )
A.鸡蛋清溶液中加入饱和(NH )SO 溶液生成白色沉淀,属于物理变化
4 2 4
B.纳米材料微粒直径一般从几纳米到几十纳米(1 nm=10-9 m),因此纳米材料属于胶
体
C.往Fe(OH) 胶体中逐滴加入稀硫酸会产生沉淀而后沉淀逐渐溶解
3
D.水泥厂、冶金厂常用高压电除去烟尘,是因为烟尘微粒带电荷
5.下列实验装置或操作与粒子直径的大小无直接关系的是( )6.某种胶体在电泳时,它的粒子向阴极移动。在该胶体中分别加入下列物质不会发生
聚沉的是( )
①蔗糖溶液 ②硫酸镁溶液 ③硅酸胶体(胶粒带负电荷) ④氢氧化铁胶体
A.①③ B.①④
C.②③ D.③④
7.我们常用“往伤口上撒盐”来比喻某些人乘人之危的行为,其实从化学的角度来
说,“往伤口上撒盐”的做法并无不妥。那么,这种做法的化学原理是( )
A.胶体的电泳 B.血液的氧化还原反应
C.血液中发生复分解反应 D.胶体的聚沉
8.分别将6滴饱和FeCl 溶液滴入下列试剂中:
3
①5mL20℃蒸馏水中
②5mL沸水中并加热至红褐色
③5mL20℃蒸馏水中,然后再加入少量0.1mol·L-1的NaOH溶液
下列有关相应分散系的说法中不正确的是( )
A.分散质粒子直径:①<②<③
B.分散系稳定性:①>②>③
C.仅凭观察法就可将①②③三种分散系区别开来
D.向三种分散系中均加入HNO 酸化的AgNO 溶液后,只有①中会产生白色沉淀
3 3
9.下列现象或新技术应用中,不涉及胶体性质的是( )
A.在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀
B.使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血
C.清晨,在茂密的森林中, 常常可以看到从枝叶间透过的一道道光柱
D.肾衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
10.下列说法正确的是( )
①泥浆中泥沙是溶质、水是溶剂 ②常用医用酒精中,水是溶剂,酒精是溶质 ③凡
是分散质能通过半透膜的分散系即属于胶体 ④胶体的聚沉属于物理过程 ⑤豆腐属于胶
体
⑥胶体带电是电泳的前提条件
A.①②③④⑤ B.②④⑤
C.除③都正确 D.全不正确
能力提升
11.将饱和FeCl 溶液滴加到沸水中能制得Fe(OH) 胶体,下列有关说法正确的是(
3 3)
A.溶液和胶体的本质区别是能否发生布朗运动
B.含0.1 mol FeCl 的溶液形成胶体后,胶体粒子为0.1 mol
3
C.分散系中分散质粒子的直径:Fe(OH) 悬浊液>Fe(OH) 胶体>FeCl 溶液
3 3 3
D.可通过观察液体是否澄清透明来区别溶液和胶体
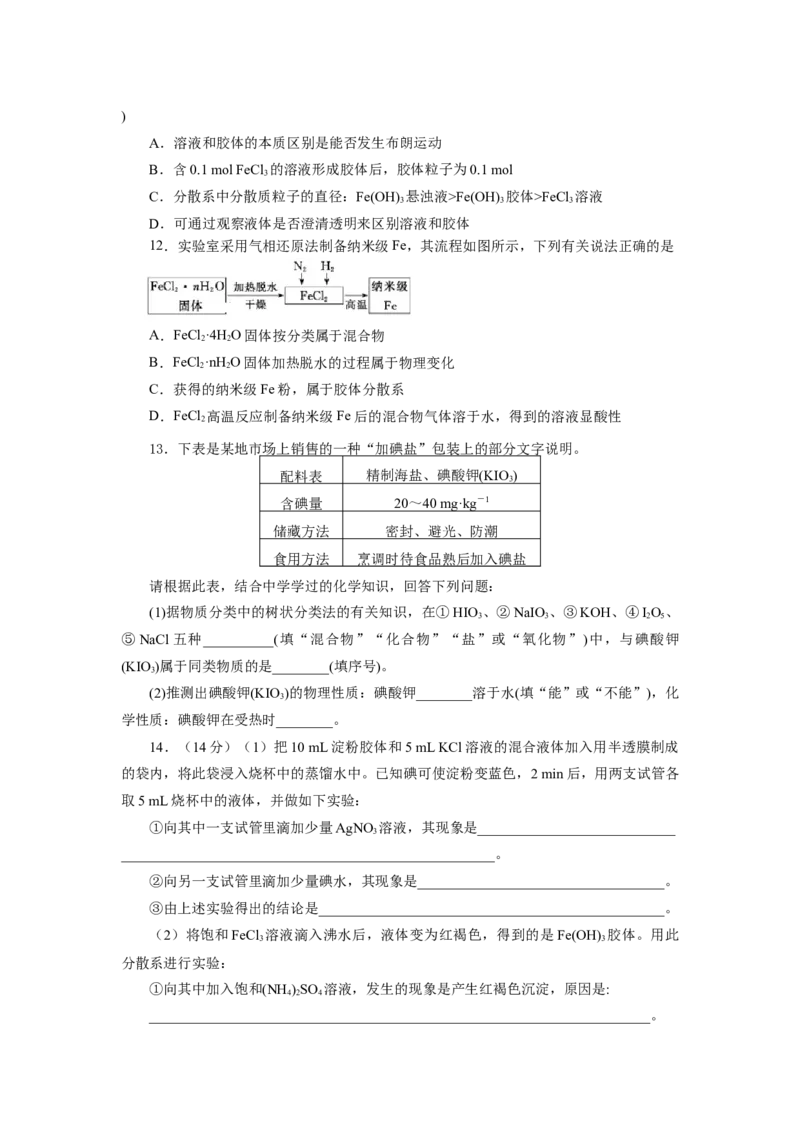
12.实验室采用气相还原法制备纳米级Fe,其流程如图所示,下列有关说法正确的是
A.FeCl ·4H O固体按分类属于混合物
2 2
B.FeCl ·nH O固体加热脱水的过程属于物理变化
2 2
C.获得的纳米级Fe粉,属于胶体分散系
D.FeCl 高温反应制备纳米级Fe后的混合物气体溶于水,得到的溶液显酸性
2
13.下表是某地市场上销售的一种“加碘盐”包装上的部分文字说明。
配料表 精制海盐、碘酸钾(KIO )
3
含碘量 20~40 mg·kg-1
储藏方法 密封、避光、防潮
食用方法 烹调时待食品熟后加入碘盐
请根据此表,结合中学学过的化学知识,回答下列问题:
(1)据物质分类中的树状分类法的有关知识,在①HIO 、②NaIO 、③KOH、④IO 、
3 3 2 5
⑤NaCl五种__________(填“混合物”“化合物”“盐”或“氧化物”)中,与碘酸钾
(KIO )属于同类物质的是________(填序号)。
3
(2)推测出碘酸钾(KIO )的物理性质:碘酸钾________溶于水(填“能”或“不能”),化
3
学性质:碘酸钾在受热时________。
14.(14分)(1)把10 mL淀粉胶体和5 mL KCl溶液的混合液体加入用半透膜制成
的袋内,将此袋浸入烧杯中的蒸馏水中。已知碘可使淀粉变蓝色,2 min后,用两支试管各
取5 mL烧杯中的液体,并做如下实验:
①向其中一支试管里滴加少量AgNO 溶液,其现象是____________________________
3
_____________________________________________________。
②向另一支试管里滴加少量碘水,其现象是___________________________________。
③由上述实验得出的结论是_________________________________________________。
(2)将饱和FeCl 溶液滴入沸水后,液体变为红褐色,得到的是Fe(OH) 胶体。用此
3 3
分散系进行实验:
①向其中加入饱和(NH )SO 溶液,发生的现象是产生红褐色沉淀,原因是:
4 2 4
_______________________________________________________________________。②向其中逐滴加入过量稀硫酸,现象是先产生红褐色沉淀后沉淀又逐渐溶解形成黄色
溶液,原因是________________________________________________________________。
③提纯此分散系的方法叫______________________________。
直击高考
15.下列有关胶体等分散系制备、性质的相关说法不正确的是( )
A.向沸水中逐滴加入FeCl 饱和溶液,继续煮沸至液体呈红褐色,停止加热即制得
3
Fe(OH) 胶体
3
B.向Fe(OH) 胶体中逐滴加入稀硫酸至过量,现象为先生成红褐色沉淀,之后沉淀溶
3
解
C.依据丁达尔效应可将分散系分为溶液、胶体与浊液
D.将Fe(OH) 胶体与硅酸溶胶相互混合,混合液变浑浊
3
16.将少量饱和FeCl 溶液分别滴加到下列物质中,得到三种分散系,完成相关问题:
3
甲:饱和FeCl 溶液滴加到冷水中;
3
乙:饱和FeCl 溶液滴加到NaOH溶液中;
3
丙:饱和FeCl 溶液滴加到沸水中。
3
(1)将丙继续加热煮沸得到红褐色透明液体,反应的化学方程式为
_________________。
(2)用最简单的方法判断丙中是否成功制备胶体,请写出相关的操作、现象和结论:
______________________________________________________。
(3)向经过检验后的丙中逐滴加入稀盐酸,会出现一系列变化:
①先出现和乙中相同的现象,原因为_______________________________________。
②随后发生变化得到和甲相同的溶液,此反应的离子反应方程式为
__________________。
(4)向丙中加入电极通电后,Fe(OH) 胶体粒子移向_______极;(填“阴极”或“阳
3
极”)
(5)可用如图所示的装置除去Fe(OH) 胶体中的杂质离子来提纯Fe(OH) 胶体,实验
3 3
过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中
加入AgNO 溶液,若__________________(填实验现象),则说明该Fe(OH) 胶体中的杂质
3 3
离子已经完全除去。