文档内容
年初中学业水平考试
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Mg-24 S-32 Cl-35.5 Ca-40
Fe-56 Cu-64 Zn-65
一、选择题(本题包括6个小题,每小题2分,共12分。每小题只有一个选项符合题意)
1.中国政府承诺“努力争取2060年前实现碳中和”,“碳中和”是使碳排放与碳吸收达平衡,
实现二氧化碳相对“零排放”。为了实现碳中和,从实际出发,以下措施不可行的是( )
A.鼓励拼车或乘坐公共交通出行
B.推广垃圾分类处理,加强资源回收利用
C.禁止使用煤、石油等化石能源
D.采用物理或化学方法,捕集或吸收废气中的二氧化碳
2.手机使用的锂(Li)电池是新型的高能电池,以质量轻、电容量大而受到重视。某种锂电池的
总反应可表示为Li+MnO LiMnO ,下列说法正确的是( )
2 2
A.该反应属于化合反应
B.反应前后锂元素的化合价不变
C.MnO 中含有氧分子
2
D.LiMnO 属于氧化物
2
3.推理是化学学习中常用的思维方法,下列推理正确的是( )
A.离子是带电的粒子,所以带电的粒子一定是离子
B.置换反应有单质和化合物生成,所以有单质和化合物生成的反应一定是置换反应
C.化学变化伴随有能量变化,所以有能量变化的一定是化学变化
D.化合物含有不同种元素,所以由不同种元素组成的纯净物一定是化合物
4.下列实验操作能达到实验目的的是( )
实验操作
加过量的Ca(OH) 溶液,过滤
2
点燃,在火焰上方罩一干冷烧杯
加足量的水溶解、过滤
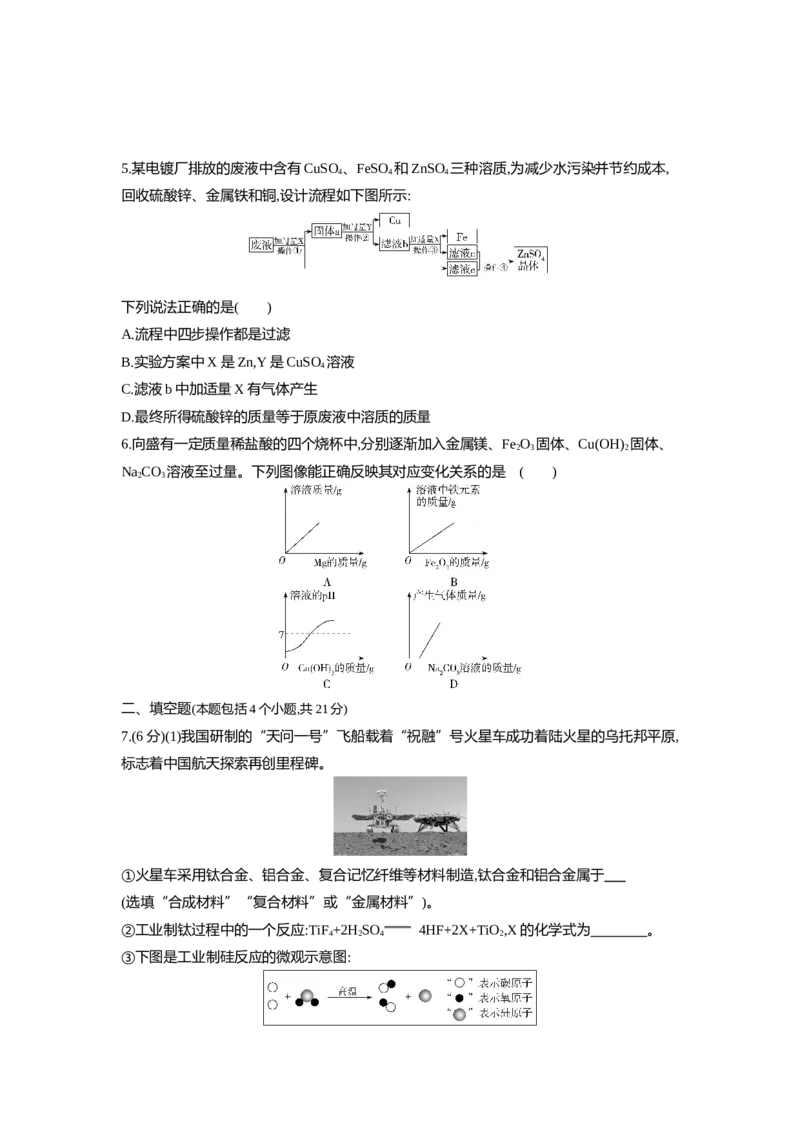
黄铜片和铜片相互刻画5.某电镀厂排放的废液中含有CuSO 、FeSO 和ZnSO 三种溶质,为减少水污染并节约成本,
4 4 4
回收硫酸锌、金属铁和铜,设计流程如下图所示:
下列说法正确的是( )
A.流程中四步操作都是过滤
B.实验方案中X是Zn,Y是CuSO 溶液
4
C.滤液b中加适量X有气体产生
D.最终所得硫酸锌的质量等于原废液中溶质的质量
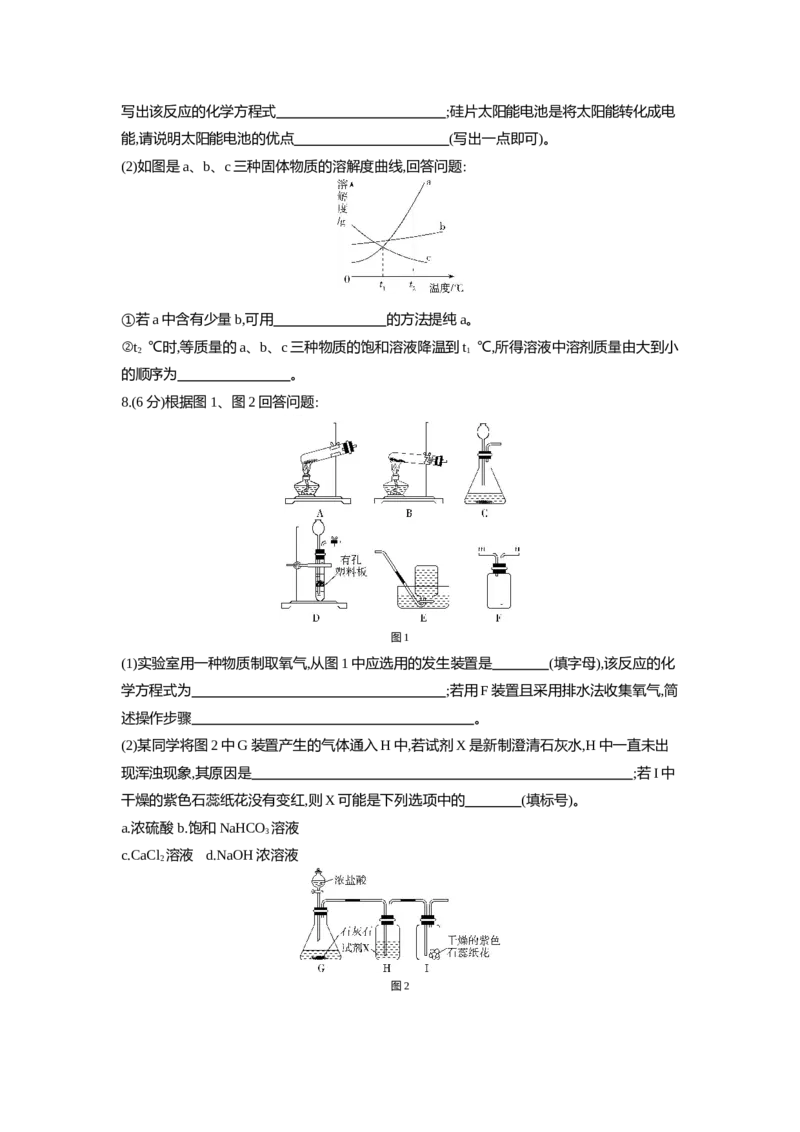
6.向盛有一定质量稀盐酸的四个烧杯中,分别逐渐加入金属镁、Fe O 固体、Cu(OH) 固体、
2 3 2
NaCO 溶液至过量。下列图像能正确反映其对应变化关系的是 ( )
2 3
二、填空题(本题包括4个小题,共21分)
7.(6分)(1)我国研制的“天问一号”飞船载着“祝融”号火星车成功着陆火星的乌托邦平原,
标志着中国航天探索再创里程碑。
①火星车采用钛合金、铝合金、复合记忆纤维等材料制造,钛合金和铝合金属于
(选填“合成材料”“复合材料”或“金属材料”)。
②工业制钛过程中的一个反应:TiF +2H SO 4HF+2X+TiO ,X的化学式为 。
4 2 4 2
③下图是工业制硅反应的微观示意图:写出该反应的化学方程式 ;硅片太阳能电池是将太阳能转化成电
能,请说明太阳能电池的优点 (写出一点即可)。
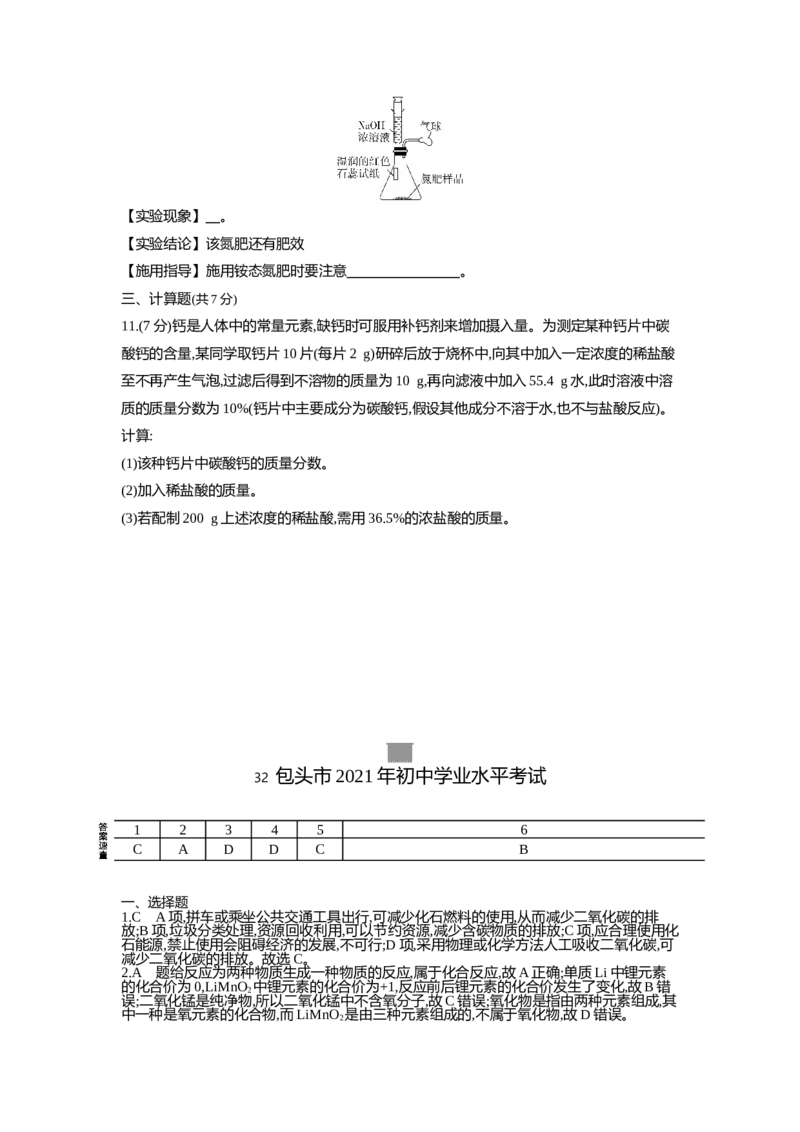
(2)如图是a、b、c三种固体物质的溶解度曲线,回答问题:
①若a中含有少量b,可用 的方法提纯a。
②t ℃时,等质量的a、b、c三种物质的饱和溶液降温到t ℃,所得溶液中溶剂质量由大到小
2 1
的顺序为 。
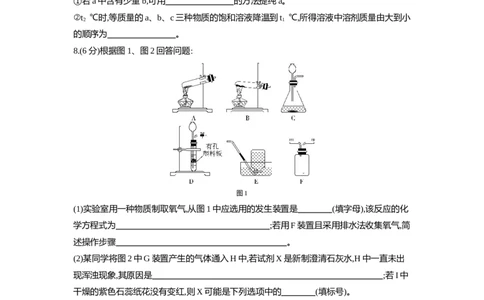
8.(6分)根据图1、图2回答问题:
图1
(1)实验室用一种物质制取氧气,从图1中应选用的发生装置是 (填字母),该反应的化
学方程式为 ;若用F装置且采用排水法收集氧气,简
述操作步骤 。
(2)某同学将图2中G装置产生的气体通入H中,若试剂X是新制澄清石灰水,H中一直未出
现浑浊现象,其原因是 ;若I中
干燥的紫色石蕊纸花没有变红,则X可能是下列选项中的 (填标号)。
a.浓硫酸 b.饱和NaHCO 溶液
3
c.CaCl 溶液 d.NaOH浓溶液
2
图29.(4分)有一包固体物质,可能含有BaCl 、NaCO、BaCO 、NaSO 和NaOH中的一种或几
2 2 3 3 2 4
种,某小组同学为了探究其组成,取少量该固体进行如图实验:(微溶物视为可溶物)
回答问题:
(1)白色沉淀A是 (填化学式)。
(2)溶液b中一定大量存在的离子是
(填离子符号)。
(3)原固体中一定含有的物质是 ,可能含有的物质是 。
10.(5分)某农场有一袋标签已破损的铵态氮肥,破损标签内容如图所示,同学们对这袋氮肥的
成分进行探究并验证其还有肥效,设计了如下实验活动。
活动一:探究氮肥的成分。
【猜想与假设】
猜想1:NHNO
4 3
猜想2:(NH )SO
4 2 4
猜想3:NHHCO
4 3
猜想4:NHCl
4
经分析,同学们一致认为猜想2不合理,理由是
。
【实验探究】
(1)取少量样品于试管中,滴加稀盐酸,观察到无气泡产生,则该氮肥的成分一定不是
(填化学式)。
(2)为了确定该氮肥究竟是剩余两种中的哪一种,写出实验操作、现象及结论
。
活动二:验证氮肥还有肥效。
【实验操作】如图向盛有氮肥样品的锥形瓶中注入NaOH浓溶液。【实验现象】 。
【实验结论】该氮肥还有肥效
【施用指导】施用铵态氮肥时要注意 。
三、计算题(共7分)
11.(7分)钙是人体中的常量元素,缺钙时可服用补钙剂来增加摄入量。为测定某种钙片中碳
酸钙的含量,某同学取钙片10片(每片2 g)研碎后放于烧杯中,向其中加入一定浓度的稀盐酸
至不再产生气泡,过滤后得到不溶物的质量为10 g,再向滤液中加入55.4 g水,此时溶液中溶
质的质量分数为10%(钙片中主要成分为碳酸钙,假设其他成分不溶于水,也不与盐酸反应)。
计算:
(1)该种钙片中碳酸钙的质量分数。
(2)加入稀盐酸的质量。
(3)若配制200 g上述浓度的稀盐酸,需用36.5%的浓盐酸的质量。
32
包头市2021年初中学业水平考试
1 2 3 4 5 6
C A D D C B
一、选择题
1.C A项,拼车或乘坐公共交通工具出行,可减少化石燃料的使用,从而减少二氧化碳的排
放;B项,垃圾分类处理,资源回收利用,可以节约资源,减少含碳物质的排放;C项,应合理使用化
石能源,禁止使用会阻碍经济的发展,不可行;D项,采用物理或化学方法人工吸收二氧化碳,可
减少二氧化碳的排放。故选C。
2.A 题给反应为两种物质生成一种物质的反应,属于化合反应,故A正确;单质Li中锂元素
的化合价为0,LiMnO 中锂元素的化合价为+1,反应前后锂元素的化合价发生了变化,故B错
2
误;二氧化锰是纯净物,所以二氧化锰中不含氧分子,故C错误;氧化物是指由两种元素组成,其
中一种是氧元素的化合物,而LiMnO 是由三种元素组成的,不属于氧化物,故D错误。
23.D 离子是带电的粒子,但带电的粒子不一定是离子,如电子是带负电荷的粒子,故A错误;
一种单质和一种化合物反应生成另一种单质和另一种化合物的反应是置换反应,有单质和化
合物生成的反应,如果反应物不是单质和化合物,就不属于置换反应,故B错误;有能量变化的
不一定是化学变化,如干冰升华过程中有能量变化,是物理变化,故C错误;化合物一定是由不
同种元素组成的,由不同种元素组成的纯净物一定是化合物,故D正确。
易错警示 化学反应过程中一定有能量变化,但有能量变化的过程不一定发生化学变化,如物质溶解过程中的吸热、放热
现象,制冷剂在使用过程中伴随着能量变化,这些变化均不属于化学变化。
4.D A项,加入过量的Ca(OH) 溶液会引入新的杂质,不能达到实验目的;B项,甲烷燃烧有水
2
生成,也会使干冷烧杯的内部出现水雾,无法检验甲烷中是否混有氢气;C项,加足量的水会使
CaCl 溶解形成CaCl 溶液,没有得到CaCl 固体;D项,黄铜合金比铜的硬度大,用黄铜片在铜
2 2 2
片上刻画会留下刻痕,铜片在黄铜片上刻画不会出现刻痕,能达到实验目的;故选D。
5.C 操作④是从滤液中得到晶体的操作,为蒸发结晶,不是过滤,故A错误;根据流程图可知,
滤液c为ZnSO 溶液,所以加入的X为Zn,发生的反应有Zn+CuSO ZnSO+Cu、
4 4 4
Zn+FeSO ZnSO+Fe,固体a为生成的Cu、Fe和过量的Zn的混合物,过量的Y应为稀硫
4 4
酸,若加入过量的CuSO 溶液,会使滤液b中引入杂质CuSO ,故B错误;在Cu、Fe和过量的
4 4
Zn的混合物中加入过量的稀硫酸,发生的反应有Zn+H SO ZnSO+H ↑、Fe+H SO
2 4 4 2 2 4
FeSO +H ↑,所以滤液b中含有的溶质有生成的FeSO 、ZnSO 和剩余的HSO ,加入适量Zn,
4 2 4 4 2 4
发生的反应有Zn+H SO ZnSO+H ↑、Zn+FeSO ZnSO+Fe,有氢气生成,故C正确;
2 4 4 2 4 4
由于回收过程中加入了稀硫酸和锌,所以最后得到的硫酸锌的质量比原废液中的多,故D错
误。
6.B A项,向一定质量的稀盐酸中逐渐加入金属镁,溶液的质量增加,但开始时溶液的质量不
为零,图像不正确;B项,向一定质量的稀盐酸中逐渐加入氧化铁固体,稀盐酸与氧化铁反应,溶
液中铁元素的质量由0开始逐渐增大,当二者恰好完全反应时铁元素的质量最大,再加入氧化
铁时不再发生反应,溶液中铁元素的质量不再变化,图像正确;C项,稀盐酸呈酸性,溶液的pH
小于7,向一定质量的稀盐酸中逐渐加入Cu(OH) ,发生酸碱中和反应,溶液的酸性减弱,溶液的
2
pH增大,当完全反应后,继续加入Cu(OH) ,由于Cu(OH) 难溶于水,溶液呈弱碱性,pH略大于
2 2
7,图像不正确;D项,向一定质量的稀盐酸中逐渐加入NaCO 溶液,开始就有气体产生,图像中
2 3
的起点应从0开始,图像不正确。
易错警示 向一定质量的稀盐酸中逐渐加入金属镁,溶液的质量增加;由于原烧杯中有稀盐酸,所以开始时溶液的质量不
为零。
二、填空题
7.答案 (6分)(1)①金属材料 ②SO ③2C+SiO 2CO↑+Si 无污染或绿色环保或节
3 2
能(答案合理即可)
(2)①降温结晶(或冷却热饱和溶液) ②c>b>a
解析 (1)①钛合金和铝合金属于金属材料。②根据质量守恒定律可知,化学反应前后原子的
种类和数目不变,该反应中反应前有1个钛原子、4个氟原子、4个氢原子、2个硫原子和8
个氧原子,反应后已知物质中含有1个钛原子、4个氟原子、4个氢原子和2个氧原子,所以
“2X”中含有2个硫原子和6个氧原子,故X的化学式为SO 。③根据微观示意图可知反应
3
物为C和SiO,生成物为CO和Si,反应的化学方程式为2C+SiO 2CO↑+Si;太阳能电池绿
2 2
色环保、节能、没有污染。
(2)①根据溶解度曲线可知,a物质的溶解度随温度升高变化很大,b物质的溶解度随温度升高
变化不大,所以a物质中含有少量b物质,可用降温结晶(或冷却热饱和溶液)的方法提纯。②
在t℃时,a、b、c三种物质的溶解度由大到小的顺序为a>b>c,所以等质量的三种物质的饱
2
和溶液中溶剂的质量由大到小的顺序为c>b>a,降温到t℃时,a、b物质的溶液会析出固体、
1
c物质的溶液变为不饱和溶液,但三种溶液中溶剂的质量不变,即所得溶液中溶剂质量由大到
小的顺序为c>b>a。
易错警示 对于溶解度随温度升高而增大的物质来说,降低饱和溶液的温度会析出固体,溶液中的溶质质量减少,但溶剂
的质量不变。
8.答案 (6分)(1)B 2KMnO KMnO +MnO+O ↑(2分) 先将集气瓶装满水,再将氧气
4 2 4 2 2
从m端管口通入
(2)浓盐酸挥发,使生成的二氧化碳中混有较多的氯化氢而不能生成碳酸钙沉淀 ad解析 (1)根据图1可知,A装置试管口没有略向下倾斜,C装置长颈漏斗下端没有浸没至液面
以下,装置均错误;D装置也不能用于实验室制取氧气,只有B装置能用于实验室制取氧气。
根据B装置的试管口放了一团棉花可知,是用加热高锰酸钾的方法制取氧气,反应的化学方
程式为2KMnO KMnO +MnO+O ↑。用F装置采用排水法收集氧气的操作步骤为先将
4 2 4 2 2
集气瓶装满水,再将氧气从m端管口通入,以便将水排出,收集到纯净的氧气。(2)G装置用浓
盐酸和石灰石反应制取二氧化碳,由于浓盐酸具有挥发性,会使生成的二氧化碳气体中含有氯
化氢气体,将气体通入新制澄清石灰水中,氯化氢会与氢氧化钙反应而不能生成碳酸钙沉淀。
若I中干燥的紫色石蕊纸花没有变红,说明得到的气体是干燥的,或者气体被试剂X吸收了;
浓硫酸具有吸水性,氢氧化钠浓溶液能吸收二氧化碳和氯化氢,气体在通过这两种试剂后,都
不能使I中干燥的紫色石蕊纸花变红,故选ad。
9.答案 (4分)(1)BaCO
3
(2)Na+、H+、S O2-、Cl-
4
(3)Na CO、BaCl BaCO 、NaOH
2 3 2 3
解析 在固体加水溶解后得到的白色沉淀A中加入过量的稀硝酸,沉淀全部溶解,说明白色
沉淀A是BaCO ,不含BaSO,因为BaSO 不溶于稀硝酸,BaCO 能溶于稀硝酸,推知原固体中
3 4 4 3
不含NaSO ,所以溶液a中含有HNO、Ba(NO );在滤液1中加入过量的稀硫酸有气体产生,
2 4 3 3 2
根据题意可知气体为二氧化碳,推知原固体中含有NaCO;将溶液a、b混合产生白色沉淀B,
2 3
溶液a中含有的Ba(NO ) 与稀硫酸反应生成硫酸钡白色沉淀,即白色沉淀B为BaSO;向滤液
3 2 4
2中加入硝酸银溶液得到白色沉淀C,说明滤液2中含有的Cl-来自溶液b,推知原固体中含有
BaCl ;所以原固体中一定含有BaCl 、NaCO,可能含有BaCO 、NaOH,一定不含NaSO 。
2 2 2 3 3 2 4
(1)白色沉淀A为BaCO 。(2)BaCl 与NaCO 反应生成BaCO 和NaCl,在滤液1中加过量的
3 2 2 3 3
稀硫酸产生二氧化碳气体,说明滤液1中含NaCO,发生的反应为HSO +Na CO
2 3 2 4 2 3
NaSO +H O+CO↑,所以溶液b中含有NaSO 、NaCl和剩余的HSO ,一定大量存在的离子
2 4 2 2 2 4 2 4
为Na+、S O2-、Cl-、H+。(3)原固体中一定含有BaCl
2
、Na
2
CO
3
,可能含有BaCO
3
、NaOH。
4
10.答案 (5分)【猜想与假设】从标签中的化学式可知,铵根离子数为1,所以不是硫酸铵
【实验探究】(1)NH HCO (2)取少量样品于试管中加水溶解,滴加硝酸银溶液,若有白色沉
4 3
淀产生,则该氮肥是NH Cl;若无白色沉淀产生,则该氮肥是NH NO
4 4 3
【实验现象】湿润的红色石蕊试纸变蓝,气球变大
【施用指导】避免与碱性物质混合使用
解析
【猜想与假设】根据标签的化学式可知,铵根离子数为1,硫酸铵的化学式为(NH )SO ,所以
4 2 4
不是硫酸铵。
【实验探究】(1)碳酸氢铵能与稀盐酸反应生成二氧化碳气体,该氮肥中滴加稀盐酸没有气泡
产生,说明不是NH HCO 。(2)检验该氮肥是NH NO 还是NH Cl,只需要检验它的水溶液中
4 3 4 3 4
是否含有Cl-。具体方法是取少量该氮肥于试管中,加入适量水使其溶解,然后滴加硝酸银溶
液,若产生白色沉淀,则该氮肥是NH Cl;若无白色沉淀产生,则该氮肥是NH NO 。
4 4 3
【实验现象】铵盐都能与NaOH浓溶液反应放出氨气,氨气能使湿润的红色石蕊试纸变蓝;由
于该氮肥还有肥效,所以向盛有氮肥样品的锥形瓶中注入NaOH浓溶液时会放出氨气,会观察
到湿润的红色石蕊试纸变蓝,气球变大。
【施用指导】由于铵态氮肥能与碱性物质反应放出氨气而使肥效降低,所以施用时应避免与
碱性物质混合使用。
三、计算题
11.答案 (7分)解:(1)该种钙片中碳酸钙的质量分数
20 g-10 g
×100%=50%(1分)
10×2 g
(2)设反应所消耗的氯化氢的质量为x,生成氯化钙的质量为y,二氧化碳的质量为z。
CaCO +2HCl CaCl +CO ↑+H O(1分)
3 2 2 2
100 73 111 4410 g x y z
100 10 g
= x=7.3 g }
73 x
100 10 g (2分)
= y=11.1 g
111 y
100 10 g
= z=4.4 g
44 z
设加入稀盐酸质量为M。
11.1 g
×100%=10%
10 g+M-4.4 g+55.4 g
M=50 g(2分)
(3)设需用36.5%的浓盐酸的质量为N。
7.3 g
200 g× ×100%=N×36.5%
50 g
N=80 g(1分)
7.3 g
(或:200 g× ×100%÷36.5%=80 g)
50 g
答:(略)
(其他解法合理均给分)
解析 (1)根据10片钙片的质量和剩余不溶物的质量计算出钙片中碳酸钙的质量,进而计算
出钙片中碳酸钙的质量分数。(2)根据钙片中碳酸钙的质量,利用化学方程式分别计算出消耗
HCl的质量、生成CaCl 和CO 的质量;再根据题给CaCl 溶液中溶质的质量分数求出加入稀
2 2 2
盐酸的质量。(3)根据计算出的HCl的质量和稀盐酸的质量,利用质量分数的计算公式求出反
应所用稀盐酸中HCl的质量分数;最后根据稀释前后溶质的质量不变求出需要的浓盐酸的质
量。