文档内容
第一章 原子结构与性质
第一节 原子结构
1.1.2 构造原理与电子排布式 电子云与原子轨道
一.选择题
1.下列有关原子核外电子的能量与运动状态的说法正确的是( )
A. 在同一原子中,2p、3p、4p……能级的电子轨道数依次增多
B. 在同一能级上运动的电子,其能量一定相同
C. 在同一能级上运动的电子,其运动状态有可能相同
D. 在同一原子中,1s、2s、3s、4s……能级的原子轨道的平均半径相同
2.下列说法中正确的是( )
A. [Ne]3s2表示的是Mg原子
B. 3p2表示第三能层有2个电子
C. 同一原子中,1s、2s、3s电子的能量逐渐减小
D. 2p、3p、4p能级容纳的最多电子数依次增多
3.X2+的核外电子排布式为1s22s22p6,下列说法正确的是( )
A. X可能为稀有元素
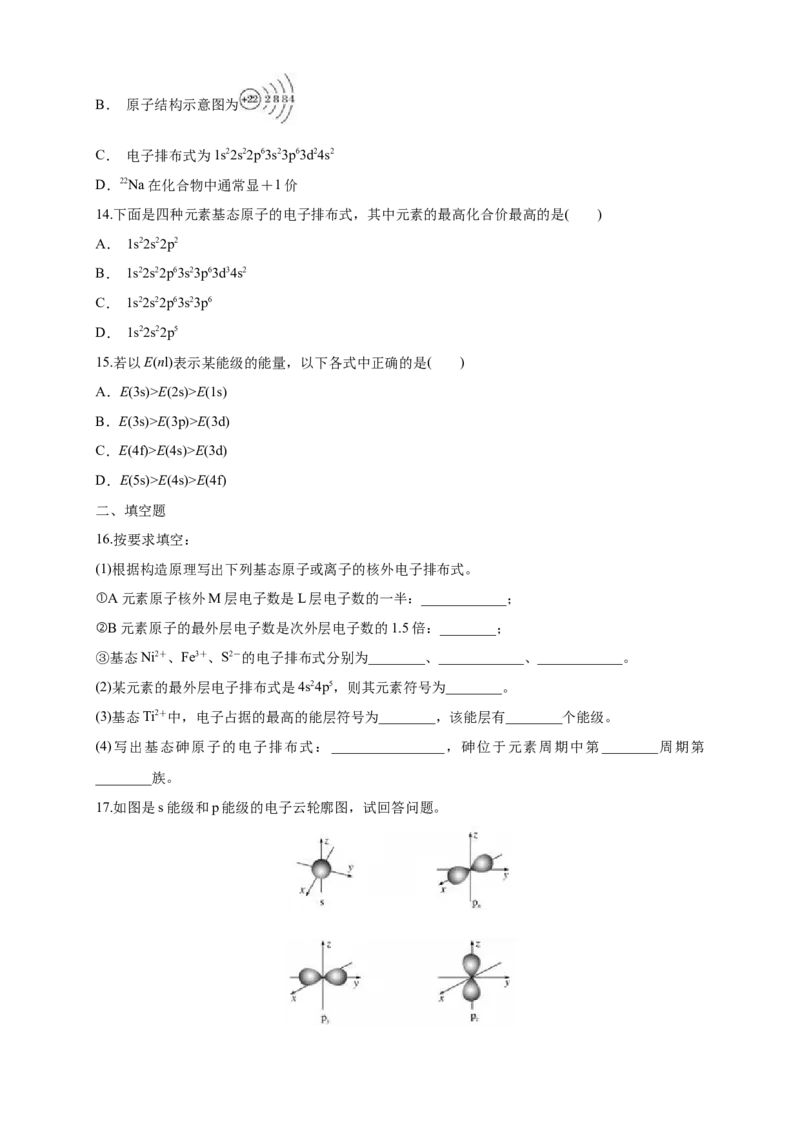
B. X原子的核外电子排布为1s22s22p63s2
C. X原子的核外电子排布为1s22s22p62d2
D. X2+的最外电子层上有6个电子
4.4p轨道填充一半的元素,其原子序数是( )
A. 15 B. 33 C. 35 D. 51
5.X、Y两元素可形成XY 型化合物,则X、Y原子最外层的电子排布可能是( )
2 3
A. X:3s23p1 Y:3s23p5
B. X:2s22p2 Y:2s22p4
C. X:3s23p1 Y:3s23p4
D. X:3s2 Y:2s22p3
6.下列说法中正确的是( )
A. 1s电子云呈球形,表示电子绕原子核做圆周运动
B. 电子云图中的小黑点密度大,说明该原子核外空间电子数目多C.ns能级的原子轨道图可表示为
D. 3d3表示3d能级有3个轨道
7.观察1s轨道电子云示意图,判断下列说法正确的是( )
A. 一个小黑点表示1个自由运动的电子
B. 1s轨道的电子云形状为圆形的面
C. 电子在1s轨道上运动像地球围绕太阳旋转
D. 1s轨道电子云的点的疏密表示电子在某一位置出现机会的多少
8.A原子的结构示意图为 。则x、y及该原子3p能级上的电子数分别为( )
A. 18、6、4
B. 20、8、6
C. 18、8、6
D. 15~20、3~8、1~6
9.某种原子的电子排布式为1s22s22p63s23p1,有关该原子的下列说法中正确的是( )
A. 该原子核内有13个中子
B. 该原子的简化电子排布式为[He]3s23p1
C. 该原子最外层有1个电子
D. 该原子第二能层上有8 个电子
10.电子在一个原子的下列能级中排布时,最后一个排布的是( )
A.ns B.np C. (n-1)d D. (n-2)f
11.表示一个原子在第三个能层上有10个电子可以写成( )
A. 3s10 B. 3d10 C. 3s23p63d2 D. 3s23p53d3
12.氧离子中电子的运动状态有( )
A. 3种 B. 8种 C. 10种 D. 12种
13.22Na是制造核弹的主要原料之一,下列关于基态22Na的说法正确的是( )
A. 电子排布式为B. 原子结构示意图为
C. 电子排布式为1s22s22p63s23p63d24s2
D.22Na在化合物中通常显+1价
14.下面是四种元素基态原子的电子排布式,其中元素的最高化合价最高的是( )
A. 1s22s22p2
B. 1s22s22p63s23p63d34s2
C. 1s22s22p63s23p6
D. 1s22s22p5
15.若以E(nl)表示某能级的能量,以下各式中正确的是( )
A.E(3s)>E(2s)>E(1s)
B.E(3s)>E(3p)>E(3d)
C.E(4f)>E(4s)>E(3d)
D.E(5s)>E(4s)>E(4f)
二、填空题
16.按要求填空:
(1)根据构造原理写出下列基态原子或离子的核外电子排布式。
①A元素原子核外M层电子数是L层电子数的一半:____________;
②B元素原子的最外层电子数是次外层电子数的1.5倍:________;
③基态Ni2+、Fe3+、S2-的电子排布式分别为________、____________、____________。
(2)某元素的最外层电子排布式是4s24p5,则其元素符号为________。
(3)基态Ti2+中,电子占据的最高的能层符号为________,该能层有________个能级。
(4)写出基态砷原子的电子排布式:________________,砷位于元素周期中第________周期第
________族。
17.如图是s能级和p能级的电子云轮廓图,试回答问题。(1)s电子云轮廓图呈________形,每个s能级有________个原子轨道;p电子云轮廓图呈________
状,每个p能级有________个原子轨道,其能量关系为____________(填“相同”或“不相同”)。
(2)元素X的原子最外层的电子排布式为nsnnpn+1,原子中能量最高的是________电子;元素X的名
称是____,它的氢化物的电子式是________。
(3)若元素Y的原子最外层的电子排布式为nsn-1npn+1,那么Y的元素符号应为________,原子的电
子排布图为______________________________。
18.有A、B、C、D四种元素,其中A元素是1826年一位法国青年科学家发现的,他在研究海水制
盐时向剩余的副产物(苦卤)中通入氯气后发现溶液的颜色变深,经过一步提取可得红棕色液体,有
刺激性气味;B、C、D的核外电子层数不超过3个,D原子核内的质子数正好等于C原子核内质子
数的2倍,而它们的最外层电子数相等;D原子的最内层电子数是B原子核外电子数的2倍。回答
下列问题:
(1)四种元素分别为A.________、B.________、C.________、D.________。
(2)A原子的电子排布式为______________,D原子的原子结构示意图为________。
(3) 写 出 由 上 述 元 素 组 成 的 单 质 和 化 合 物 相 互 作 用 生 成 沉 淀 的 两 个 化 学 方 程 式
__________________________、____________________。
19.有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20。其中A为非金属元素,
A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级
电子数是s能级电子数的两倍,C原子最外层上的电子数等于D原子最外层上电子数的一半。请回
答下列问题:
(1)A是________,B是________,C是________,D是________,E是________。
(2)由这五种元素组成的一种化合物是(写化学式)__________。写出该物质的一种主要用途:
______________。
(3)写出C元素基态原子的电子排布式:______________。
(4)写出D元素原子的价电子排布式________________。