文档内容
第一节 物质的分类及转化
第1课时 物质的分类
基础巩固
1.有些古文或谚语包含了丰富的化学知识,下列解释正确的是
A.“日照香炉生紫烟”是因为发生了碘的升华现象
B.“熬胆矾铁釜,久之亦化为铜”该过程发生了置换反应
C.“绳锯木断,水滴石穿”发生的均为物理变化
D.“玉不琢不成器”,“百炼方能成钢”发生的均为化学变化
【答案】B
【解析】
A.日照香炉生紫烟”描述的现象中,“烟”此处实为雾,雾在太阳光的照射下产生的丁达尔效应象是紫烟,
与碘的升华无关,故A错误;
B.“熬胆矾铁釜,久之亦化为铜”该过程发生了硫酸铜和铁的置换反应,生成硫酸亚铁和单质铜,故B正
确;
C.绳锯木断是属于形状变化是物理变化,水滴石穿过程中,水中的碳酸与碳酸钙发生化学变化,所以涉
及化学变化,故C错误;
D.“玉不琢不成器”只描述了玉石的形状发生改变,属于物理变化,故D错误;
故选B。
2. 在一定条件下,跟酸、碱、盐都能反应的物质是( )
A.CaO B.Na CO C.CaCO D.CO
2 3 3 2
【答案】B
【解析】CaO是碱性氧化物,与碱不发生反应;CO 是酸性氧化物,与酸不发生反应;Na CO 和CaCO 都是盐,
2 2 3 3
但后者难溶于水,不与碱、盐发生反应,前者可以,如可分别与盐酸、氢氧化钙、氯化钙等发生反应。
3.实现下列物质的转化时,只有加入酸才能通过一步反应实现的是
A.Fe O →Fe (SO ) B.Zn→ZnCl
2 3 2 4 3 2
C.NaOH→NaCl D.BaCl →BaSO
2 4
【答案】A
【解析】
A.Fe O 是难溶性碱性氧化物,只有与酸反应才能转化为盐,A符合题意;
2 3
B.活泼金属Zn可以与盐酸或CuCl 等比Zn活动性弱的金属的盐溶液通过置换反应得到ZnCl ,B与题意不
2 2
符;
C.NaOH与盐酸或CuCl 等盐溶液反应都可得到NaCl,C与题意不符;
2
D.BaCl 与H SO 或可溶性硫酸盐反应都可得到BaSO ,D与题意不符。
2 2 4 4
答案为A。
学科网(北京)股份有限公司4.通过对酸、碱、盐知识的学习,我们已经知道固体氢氧化钠可以作为某些气体的干燥剂,下列潮湿的气体
不能用固体氢氧化钠干燥的是( )。
A.H B.CO C.CO D.O
2 2 2
【答案】B
【解析】H、CO、O 均不与氢氧化钠反应,均可以用氢氧化钠来干燥,A、C、D三项不符合题意;二氧化
2 2
碳能与氢氧化钠反应生成碳酸钠,不可以用氢氧化钠来干燥,B符合题意。
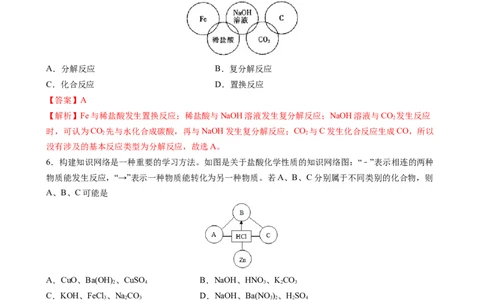
5.北京冬奥会或第24届冬季奥林匹克运动会在2022年2月4日至2022年2月20日在中华人民共和国北
京市和河北省张家口市联合举行。某同学在奥运五连环中填入了5种物质,相连环物质间能发生反应,
不相连环物质间不能发生反应。你认为“五连环”中物质间发生的反应,没有涉及的基本反应类型
A.分解反应 B.复分解反应
C.化合反应 D.置换反应
【答案】A
【解析】Fe与稀盐酸发生置换反应;稀盐酸与NaOH溶液发生复分解反应;NaOH溶液与CO 发生反应
2
时,可认为CO 先与水化合成碳酸,再与NaOH发生复分解反应;CO 与C发生化合反应生成CO,所以
2 2
没有涉及的基本反应类型为分解反应,故选A。
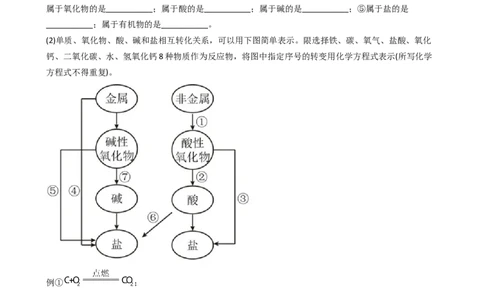
6.构建知识网络是一种重要的学习方法。如图是关于盐酸化学性质的知识网络图:“﹣”表示相连的两种
物质能发生反应,“→”表示一种物质能转化为另一种物质。若A、B、C分别属于不同类别的化合物,则
A、B、C可能是
A.CuO、Ba(OH) 、CuSO B.NaOH、HNO、KCO
2 4 3 2 3
C.KOH、FeCl 、NaCO D.NaOH、Ba(NO )、HSO
3 2 3 3 2 2 4
【答案】B
【解析】A.盐酸不与硫酸铜反应,盐酸不能转化为氢氧化钡,氢氧化钡不与氧化铜反应,故A不符合题
意;
B.盐酸和氢氧化钠、碳酸钾都能反应,和硝酸银反应生成硝酸,硝酸和氢氧化钠、碳酸钾都能反应,故
B符合题意;
C.氯化铁和碳酸钠均为盐,属于相同类别的化合物,故C不符合题意;
D.盐酸不能转化为硝酸钡,盐酸不与硫酸反应,氢氧化钠与硝酸钡不反应,故D不符合题意;
答案选B。
7.氯化锌在工业上作为生产活性炭的活化剂,使活性炭成为多孔性物,增大其表面积。在Zn、ZnO、
学科网(北京)股份有限公司ZnCO 、盐酸和CaCl 溶液五种物质中,每两种物质反应能生成ZnCl 的组合有
3 2 2
A.2 种 B.3 种 C.4 种 D.5 种
【答案】B
【解析】Zn、ZnO、ZnCO 均可与盐酸反应生成ZnCl,而与CaCl 不反应,共计有3种组合,答案为B。
3 2 2
8.单质到盐的转化关系可表示为:
下述转化关系不正确是
A.Mg MgO MgCl MgSO
2 4
B.Na NaO NaOH CHCOONa
2 3
C.C CO HCO NaCO
2 2 3 2 3
D.S SO HSO CaSO
2 2 3 3
【答案】A
【解析】A.镁能够在氧气中燃烧生成氧化镁,氧化镁溶于盐酸生成氯化镁,但氯化镁与硫酸钠不能发生
复分解反应生成MgSO ,故A错误;
4
B.常温下,钠能够与氧气反应生成氧化钠,氧化钠与水反应生成氢氧化钠,氢氧化钠与乙酸反应生成乙
酸钠,故B正确;
C.碳在氧气中燃烧生成二氧化碳,二氧化碳与水反应生成碳酸,碳酸与氧化钠反应生成碳酸钠, 故C
正确;
D.硫在氧气中燃烧生成二氧化硫,二氧化硫与水反应生成亚硫酸,亚硫酸与氢氧化钙反应生成亚硫酸钙
沉淀,故D正确;
故选A。
9.(1)将碳酸钙、稀盐酸、铁、氧气四种物质填写到下面的适当位置。
化合物:①
{ {
物质
纯净物 单质{金属单质:②
非金属单质:③
混合物:④
(2)从(1)中的四种物质中选出一种或几种为反应物,按下述反应类型,各写一个化学方程式。
①分解反应: ___________________________________。
②化合反应: ___________________________________。
③置换反应: ___________________________________。
④复分解反应: ___________________________________。
[答案](1)①碳酸钙 ②铁 ③氧气 ④稀盐酸
(2)①CaCO CaO+CO ↑
3 2
学科网(北京)股份有限公司②3Fe+2O Fe O
2 3 4
③Fe+2HCl FeCl +H ↑
2 2
④CaCO +2HCl CaCl +H O+CO↑
3 2 2 2
【解析】(1)碳酸钙属于化合物,稀盐酸属于混合物,铁属于金属单质,氧气属于非金属单质。
(2)CaCO 可以受热分解,Fe和O 可以化合生成Fe O,盐酸和铁可以发生置换反应,CaCO 与盐酸可以发生复
3 2 3 4 3
分解反应。
10.分类法是学习化学的重要方法之一。
(1)现有下列10种物质:①H O、②空气、③Mg、④CaO、⑤H SO 、⑥Ca(OH) 、⑦液氯、⑧碘酒、
2 2 4 2
⑨C H OH、⑩NaHCO 。其中,属于混合物的是___________(填序号,下同);属于单质的是___________;
2 5 3
属于氧化物的是___________;属于酸的是___________;属于碱的是___________;⑤属于盐的是
___________;属于有机物的是___________。
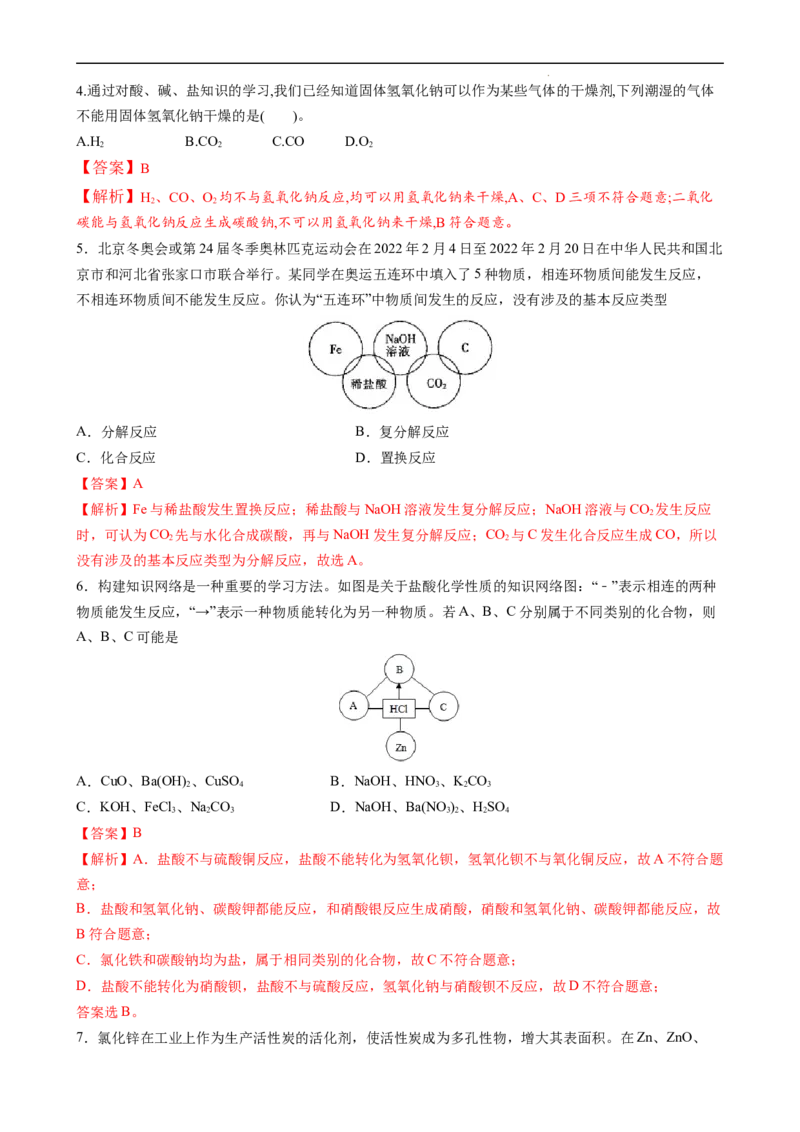
(2)单质、氧化物、酸、碱和盐相互转化关系,可以用下图简单表示。限选择铁、碳、氧气、盐酸、氧化
钙、二氧化碳、水、氢氧化钙8种物质作为反应物,将图中指定序号的转变用化学方程式表示(所写化学
方程式不得重复)。
例① ;
③___________;④___________;⑤___________;⑥___________。
【答案】(1) ②⑧ ③⑦ ①④ ⑤ ⑥ ⑩ ⑨
(2)
【解析】
(1)①H O是由氢氧两种元素组成的纯净物,H O属于氧化物;②空气中含有氮气、氧气、二氧化碳等多
2 2
种物质,空气是混合物;③Mg是由镁元素组成的纯净物,属于金属单质;④CaO由钙、氧两种元素组成,
属于氧化物;⑤H SO 电离出的阳离子全是氢离子,H SO 属于酸;⑥Ca(OH) 电离出的阴离子全是氢氧根
2 4 2 4 2
学科网(北京)股份有限公司离子,Ca(OH) 属于碱;⑦液氯是液态氯气,属于非金属单质;⑧碘酒是碘的酒精溶液,属于混合物;
2
⑨C H OH是乙醇,含有C元素,属于有机物;⑩NaHCO 能电离出钠离子和碳酸根离子,NaHCO 属于盐;
2 5 3 3
属于混合物的是②空气、⑧碘酒;属于单质的是③Mg、⑦液氯;属于氧化物的是①H O、④CaO;属于
2
酸的是⑤H SO ;属于碱的是⑥Ca(OH) ;⑤属于盐的是⑩NaHCO ;属于有机物的是⑨C H OH。
2 4 2 3 2 5
(2)
③表示酸性氧化物和碱反应生成盐和水,反应方程式为 ;④表示金属与
酸反应生成盐和氢气,反应方程式为 ;⑤表示碱性氧化物和酸反应生成氧和水,
反应方程式是 ;⑥表示酸和碱反应生成盐和水,反应方程式是
。
能力提升
11.下列物质有给定条件下的转化均能一步实现的是
A.Fe O Fe FeCl
2 3 3
B.HO H HO
2 2 2 2
C.CaCl 溶液 CaCO CO
2 3 2
D.CuSO 溶液 Cu CuO
4
【答案】D
【解析】
A. 铁与稀盐酸反应生成的是氯化亚铁,不是氯化铁,不能一步实现,A错误;
B. 过氧化氢分解生成的是氧气和水,不能生成氢气,B错误;
C. 由于盐酸的酸性大于碳酸,所以氯化钙溶液中通入二氧化碳,不能生成碳酸钙沉淀,C错误;
D. 铁比铜活泼,故铁可以与硫酸铜反应生成硫酸亚铁和铜,铜可以与氧气反应生成氧化铜,D正确;
答案选D。
12.有关物质之间的部分转化关系如图所示,其中“—”表示物质之间能发生化学反应,“→”表示物
质之间的转化关系。下列说法中正确的是( )
A.物质X是一种常见的酸性氧化物
B.反应②一定有盐参加反应
C.向Ca(OH) 溶液中加入CaO,所得溶液的溶质质量分数一定增大
2
D.图中的部分反应可能是置换反应
【答案】A
【解析】各反应如下:①CaO+H O=Ca(OH) ;②可以是Ca(OH) 与碳酸盐反应,也可以是Ca(OH) 与
2 2 2 2
学科网(北京)股份有限公司CO 反应;③CaCO CaO+CO ↑;X可以与CaCO 相互转化,故X可能是CO 也可能是CaCl ,同时X
2 3 2 3 2 2
可以与Ca(OH) 反应,故X应为CO,则反应④Ca(OH) +CO =CaCO ↓+H O;⑤CaCO CaO+CO ↑或
2 2 2 2 3 2 3 2
CaCO +2HCl=CaCl +CO ↑+H O⑥Ca(OH) +CO =CaCO ↓+H O。
3 2 2 2 2 2 3 2
A.物质X是CO 是一种常见的酸性氧化物,A项正确;
2
B.②可以是Ca(OH) 与CO 反应,B项错误;
2 2
C.若Ca(OH) 溶液饱和,加入CaO后所得溶液的溶质质量分数不变,C项错误;
2
D.图中的所有反应均为酸、碱、盐、酸性氧化物之间的反应,不可能存在置换反应,D项错误;
答案选A。
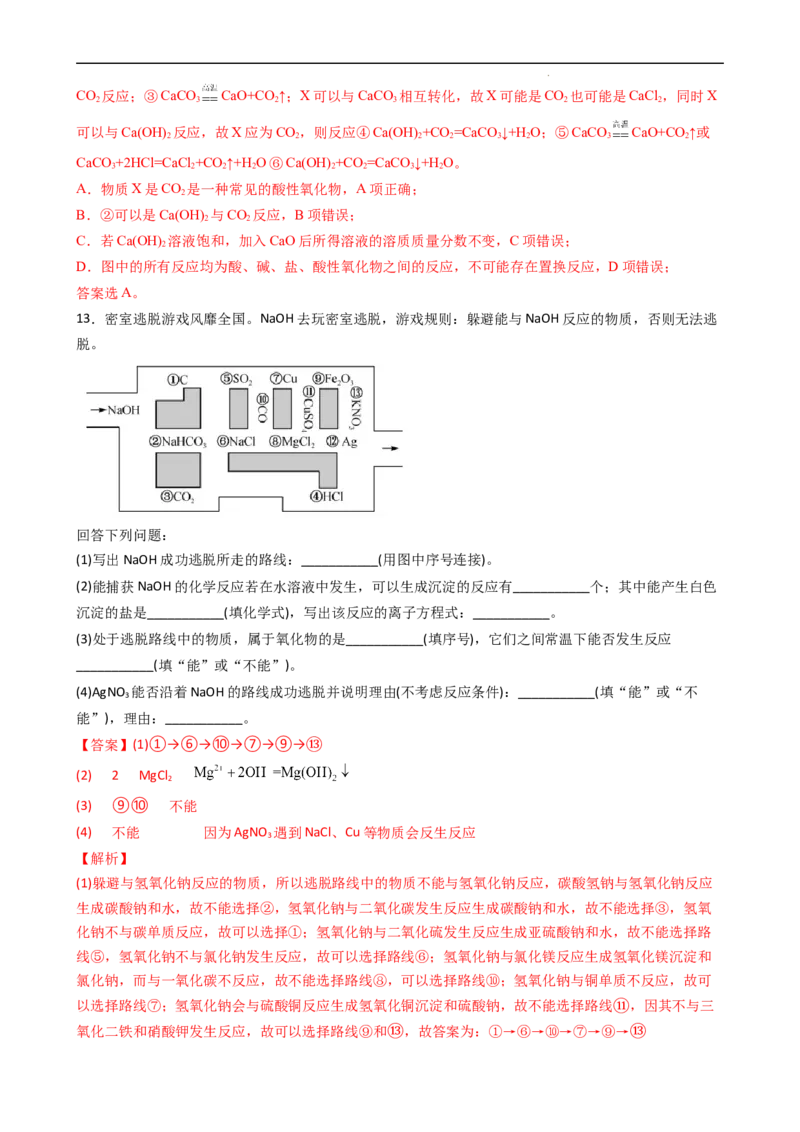
13.密室逃脱游戏风靡全国。NaOH去玩密室逃脱,游戏规则:躲避能与NaOH反应的物质,否则无法逃
脱。
回答下列问题:
(1)写出NaOH成功逃脱所走的路线:___________(用图中序号连接)。
(2)能捕获NaOH的化学反应若在水溶液中发生,可以生成沉淀的反应有___________个;其中能产生白色
沉淀的盐是___________(填化学式),写出该反应的离子方程式:___________。
(3)处于逃脱路线中的物质,属于氧化物的是___________(填序号),它们之间常温下能否发生反应
___________(填“能”或“不能”)。
(4)AgNO 能否沿着NaOH的路线成功逃脱并说明理由(不考虑反应条件):___________(填“能”或“不
3
能”),理由:___________。
【答案】(1)①→⑥→⑩→⑦→⑨→
(2) 2 MgCl ⑬
2
(3) ⑨⑩ 不能
(4) 不能 因为AgNO 遇到NaCl、Cu等物质会反生反应
3
【解析】
(1)躲避与氢氧化钠反应的物质,所以逃脱路线中的物质不能与氢氧化钠反应,碳酸氢钠与氢氧化钠反应
生成碳酸钠和水,故不能选择②,氢氧化钠与二氧化碳发生反应生成碳酸钠和水,故不能选择③,氢氧
化钠不与碳单质反应,故可以选择①;氢氧化钠与二氧化硫发生反应生成亚硫酸钠和水,故不能选择路
线⑤,氢氧化钠不与氯化钠发生反应,故可以选择路线⑥;氢氧化钠与氯化镁反应生成氢氧化镁沉淀和
氯化钠,而与一氧化碳不反应,故不能选择路线⑧,可以选择路线⑩;氢氧化钠与铜单质不反应,故可
以选择路线⑦;氢氧化钠会与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,故不能选择路线 ,因其不与三
氧化二铁和硝酸钾发生反应,故可以选择路线⑨和 ,故答案为:①→⑥→⑩→⑦→⑨→
⑪
⑬ ⑬
学科网(北京)股份有限公司(2)氢氧化钠溶液与氯化镁溶液、硫酸铜溶液发生反应会生成沉淀,反应的化学方程式分别为:
、 ,其中氢氧化镁为白色沉淀,
氢氧化铜为蓝色沉淀,所以能捕获NaOH的化学反应若在水溶液中发生,可以生成沉淀的反应有2个,其
中能产生白色沉淀的盐是氯化镁,故答案为:2;MgCl ;
2
(3)由两种元素组成,其中一种元素是氧元素的化合物叫做氧化物,处于逃脱路线中的物质,属于氧化物
的是一氧化碳和三氧化二铁,一氧化碳和三氧化二铁在高温下能发生反应,常温下不能,故答案为:
⑨⑩;不能
(4)AgNO 会与路线中的NaCl、Cu等物质发生反应,所以其不能沿着NaOH的路线成功逃脱,故答案为:
3
不能;因为AgNO 遇到NaCl、Cu等物质会反生反应
3
14.(素养题)铜器久置于空气中会和空气中的水蒸气、CO 、O 作用产生“绿锈”,“绿锈”俗称“铜
2 2
绿”[化学式为Cu (OH) CO],“铜绿”能跟酸反应生成铜盐和CO 、HO。某同学利用下述系列反应实
2 2 3 2 2
现了“铜→铜绿→……→铜”的转化:
铜――→铜绿――→A――→Cu(OH) ――→B――→Cu
2
(1)从三种不同分类标准回答,“铜绿”属于哪类物质:
________________________________________________________________。
(2)请写出“铜绿”与盐酸反应的化学方程式:
________________________________________________________________
________________________________________________________________。
(3)写出④、⑤的化学方程式:
④____________________________________________________、
⑤____________________________________________________。
(4)上述转化过程中属于化合反应的是________,属于复分解反应的是________,属于分解反应的是
________。
(5)以 Cu 为原料,其他试剂自选,设计制备 CuSO 的实验方案,并用流程图表示出来
4
_______________________________________________________。
【答案】 (1)盐、铜盐、碱式盐(或碳酸盐)
(2)Cu (OH) CO+4HCl===2CuCl +CO↑+3HO
2 2 3 2 2 2
(3)Cu(OH) =====CuO+HO CuO+H=====Cu+HO
2 2 2 2
(4)① ②③ ④
(5)Cu――→CuO―――――→CuSO
4
【解析】 (1)铜绿的成分是Cu (OH) CO,属于盐类,也属于碱式盐或碳酸盐等。
2 2 3
(2)铜绿不溶于水,若将铜绿转化成Cu(OH) ,必首先将铜绿转化成易溶于水的铜盐,而易溶的铜盐与
2
NaOH溶液反应生成Cu(OH) 沉淀,故反应②的方程式为Cu (OH) CO+4HCl===2CuCl +CO↑+3HO。
2 2 2 3 2 2 2
(3)Cu(OH) 不溶于水,受热能分解,故④的反应方程式为Cu(OH) =====CuO+HO,反应⑤是H 还原
2 2 2 2
CuO,反应方程式为CuO+H=====Cu+HO。
2 2
(4)反应①是指Cu与O 、CO 和HO的化合生成碱式碳酸铜;反应②是铜绿与盐酸反应生成A(成分是
2 2 2
CuCl ),是复分解反应;反应③是A与NaOH反应生成Cu(OH) ,是复分解反应;反应④是Cu(OH) 受热
2 2 2
分解生成B(成分是CuO),是分解反应;反应⑤是B与H 反应生成Cu,是置换反应。
2
学科网(北京)股份有限公司(5)注意Cu与HSO (稀)不能直接反应。先将Cu转化为CuO,再用CuO与HSO 反应制CuSO 。
2 4 2 4 4
学科网(北京)股份有限公司学科网(北京)股份有限公司