文档内容
第三章 铁 金属材料
第一节 铁及其化合物
第三课时 铁的重要化合物—铁盐和亚铁盐
【学习目标】1.通过学习铁盐和亚铁盐,学会从物质类别和元素价态的视角认识具有变价元素物质间
的转化关系,并建立认识模型,丰富研究物质的思路和方法。
2.通过实验探究铁盐和亚铁盐的化学性质,并能用化学方程式或离子方程式正确表示。体会实验对认
识和研究物质性质的重要作用,形成证据意识。
3.结合应用实例,将铁盐和亚铁盐的性质的知识运用于解决生产、生活中简单的化学问题,强化性质
决定用途的观念。
【学习重点】铁盐与亚铁盐的转化,Fe2+、Fe3+ 的检验
【学习难点】Fe、Fe2+、 Fe3+ 转化关系模型的建构
【课前预习】
旧知回顾:1.Fe O 与盐酸反应生成 种好过盐,离子方程式为:
3 4
;与稀硝酸只能生成 盐。
2.将氢氧化钠溶液滴加到硫酸亚铁溶液中,观察到的现象为
。反应发化学方程式为:
。
新知预习:1.从化合价改变角度预测Fe2+和Fe3+的性质:Fe2+具有 性和 性,如硫酸
亚铁与氯水反应的离子方程式为 。Fe3+具有 性,如硫酸铁与铁粉反
应的离子方程式为 ,也具有一定的还原性。如在碱性条件下用NaClO氧化
硫酸铁制备NaFeO。
2 4
2.在FeCl 溶液中,滴加KSCN溶液,现象为 ,反应的离子方程
3
式为 。
【课中探究】
情景导入:铁是人体必需的微量元素中含量最多的一种(约4~5克),缺铁性贫血已成为仅次于结核
病的全球患病率最高、耗资最大的公共卫生问题。那么铁元素在人体中又是以什么形式存在呢?本节课我
们先来学习铁盐和亚铁盐的检验方法。(见PPT图片)
一、Fe2+、Fe3+ 的检验
活动一、探究Fe3+、Fe2+的性质
任务一、观察FeCl 溶液和FeCl 溶液样品,从物质类别的角度认识它们具有什么样的性质?
2 3
任务二、阅读教材P68-69页内容,结合所学知识,从元素价态的角度思考铁盐和亚铁盐检验哪些化学性质?填写下表内容。
铁盐具有(氧化性) 亚铁盐具有(氧化还原性)
颜色
溶解性
与碱反应
化学 与氧化剂 ——
性质
与还原剂
任务二、应用探究:根据已有的知识和经验,结合上述信息,设计简单方法来证明补铁剂中的铁元素
是二价铁还是三价铁呢?
【对应训练】1.将过氧化钠投入FeCl 溶液中,可观察到的实验现象是( )
2
A.无气体产生 B.没有沉淀生成
C.有红褐色沉淀生成 D.有白色沉淀生成
2.下列说法正确的是( )
A.FeCl 不能通过化合反应制得
2
B.Fe(OH) 只能由可溶性铁盐和碱通过复分解反应制得
3
C.溶液中加入NaOH溶液,生成红褐色沉淀,则溶液中一定含有Fe2+
D.除去FeCl 溶液中少量的CuCl 杂质,可向溶液中加入过量铁粉,然后过滤
2 2
活动二、探究Fe3+、Fe2+的检验方法
任务一、实验探究:完成教材P68页【实验3-2】,根据表格内容思考如何检验溶液中的Fe3+、Fe2+?
并填写表格其它内容。
①观察法:
②化学法:
盐溶液
Fe3+ Fe2+
添加试剂
NaOHKSCN
KMnO (H+)
4
淀粉- KI
Cu
注意:
任务二、问题探究:如何检验混合溶液中同时含有Fe2+和Fe3+?上述检验检验的方法中,加入KSCN
溶液,无明显现象,一定能证明溶液中含有Fe2+吗?
任务三、归纳小结:Fe3+、Fe2+的检验方法及要注意问题是什么?
①Fe3+、Fe2+的检验常用方法:
Fe3+ Fe2+
颜色法
加碱法 现象: 现象:
原理: 原理:
加KSCN法 现象: 现象:
原理: 原理:
②Fe3+、Fe2+的检验注意事项:
【对应训练】1.要证明某溶液中不含Fe3+而可能含有Fe2+进行如下实验操作时,最佳顺序为( )
①加入足量氯水 ②加入足量酸性KMnO 溶液 ③加入少量NH SCN溶液
4 4
A.①③ B.③② C.③① D.①②③2.证明某溶液只含有Fe2+而不含Fe3+最佳的实验方法是( )
A.先滴加氯水,再滴加KSCN溶液后显红色
B.先滴加KSCN溶液,不显红色,再滴加氯水后显红色
C.滴加NaOH溶液,先产生白色沉淀,后变灰绿,最后显红褐色
D.加入几滴酸性高锰酸钾溶液,高锰酸钾溶液褪色
二、Fe、Fe2+、Fe3+的转化(铁三角)
活动一、探究Fe、Fe2+、Fe3+的氧化(还原)性
任务一、实验探究:完成教材P68页【实验3-3】,思考基于元素价态的角度Fe2+和Fe3+具有哪些性
质?填写表格内容。
①Fe2+:
②Fe3+:
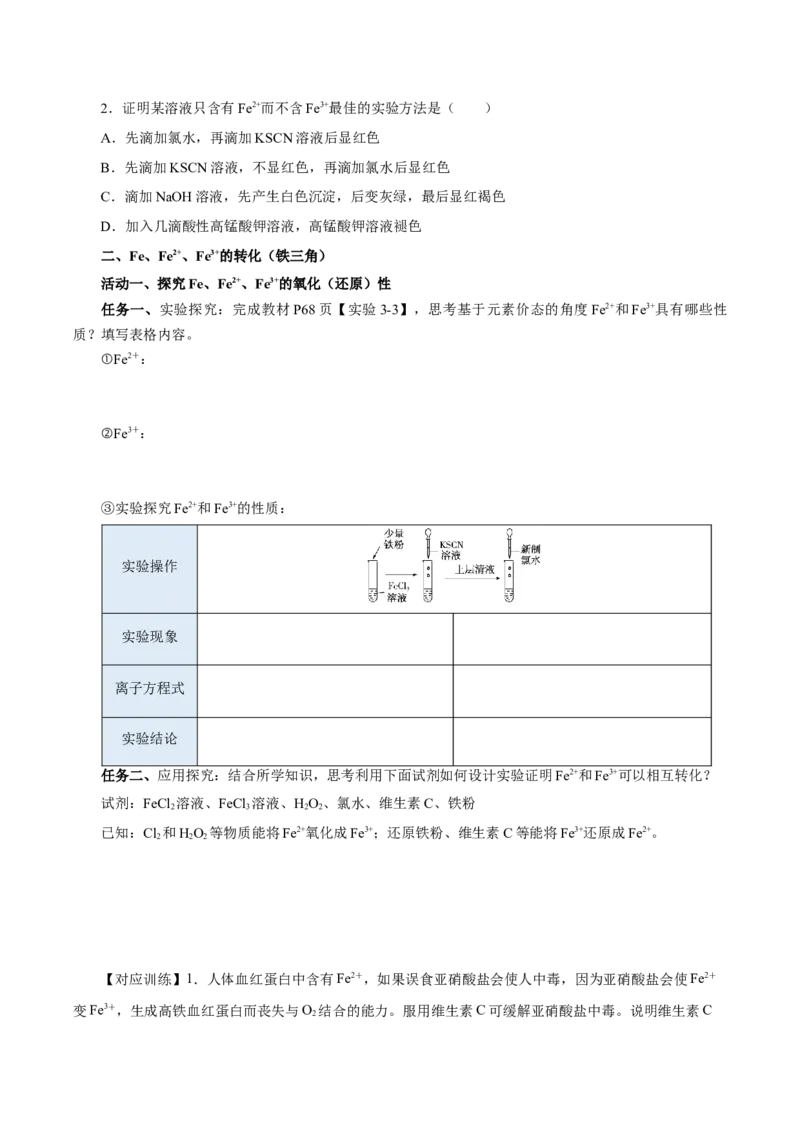
③实验探究Fe2+和Fe3+的性质:
实验操作
实验现象
离子方程式
实验结论
任务二、应用探究:结合所学知识,思考利用下面试剂如何设计实验证明Fe2+和Fe3+可以相互转化?
试剂:FeCl 溶液、FeCl 溶液、HO、氯水、维生素C、铁粉
2 3 2 2
已知:Cl 和HO 等物质能将Fe2+氧化成Fe3+;还原铁粉、维生素C等能将Fe3+还原成Fe2+。
2 2 2
【对应训练】1.人体血红蛋白中含有Fe2+,如果误食亚硝酸盐会使人中毒,因为亚硝酸盐会使Fe2+
变Fe3+,生成高铁血红蛋白而丧失与O 结合的能力。服用维生素C可缓解亚硝酸盐中毒。说明维生素C
2具有( )
A.氧化性 B.还原性 C.酸性 D.碱性
2.已知 Cu+2Fe3+=2Fe2++Cu2+。向FeCl 、CuCl 的混合溶液中加入一定量的铁粉,充分反应后仍有固
3 2
体存在,则下列判断不正确的是( )
A.溶液中一定不含Fe3+ B.溶液中一定含Fe2+
C.剩余固体中一定含Cu D.溶液中一定含Cu2+
活动二、探究Fe、Fe2+、Fe3+的转化
任务一、讨论交流:基于元素价态,结合所学知识,构建Fe、Fe2+、Fe3+的三角转化关系。
①转化关系:
②需要注意的问题:
任务二、根据Fe2+与Fe3+在一定条件下可以相互转化的性质,你认为有哪些应用?
①判断离子共存:
②除杂:
溶液 杂质 除杂方法
:
FeCl FeCl
2 3
FeCl FeCl
3 2
FeCl CuCl
2 2
任务 三、应用
探究:取一小块覆铜板,用油性笔在覆铜板上画上设计好的图案,然后浸入盛有FeCl3溶液的小烧杯中。
过一段时间后,取出覆铜板并用水清洗干净。观察实验现象,并展示制作的图案。
【答案要点】①现象:
②原理(方程式):
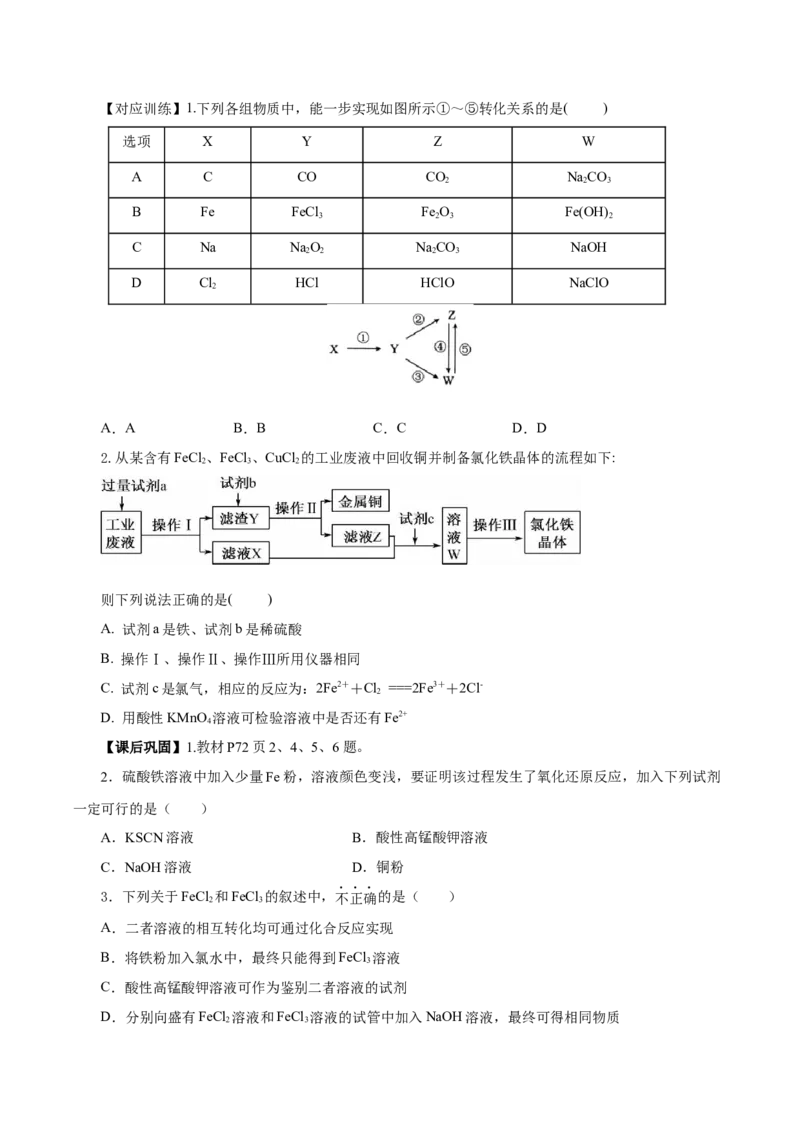
③应用:【对应训练】1.下列各组物质中,能一步实现如图所示①~⑤转化关系的是( )
选项 X Y Z W
A C CO CO NaCO
2 2 3
B Fe FeCl Fe O Fe(OH)
3 2 3 2
C Na NaO NaCO NaOH
2 2 2 3
D Cl HCl HClO NaClO
2
A.A B.B C.C D.D
2.从某含有FeCl 、FeCl 、CuCl 的工业废液中回收铜并制备氯化铁晶体的流程如下:
2 3 2
则下列说法正确的是( )
A. 试剂a是铁、试剂b是稀硫酸
B. 操作Ⅰ、操作Ⅱ、操作Ⅲ所用仪器相同
C. 试剂c是氯气,相应的反应为:2Fe2++Cl ===2Fe3++2Cl-
2
D. 用酸性KMnO 溶液可检验溶液中是否还有Fe2+
4
【课后巩固】1.教材P72页2、4、5、6题。
2.硫酸铁溶液中加入少量Fe粉,溶液颜色变浅,要证明该过程发生了氧化还原反应,加入下列试剂
一定可行的是( )
A.KSCN溶液 B.酸性高锰酸钾溶液
C.NaOH溶液 D.铜粉
3.下列关于FeCl 和FeCl 的叙述中,不正确的是( )
2 3
A.二者溶液的相互转化均可通过化合反应实现
B.将铁粉加入氯水中,最终只能得到FeCl 溶液
3
C.酸性高锰酸钾溶液可作为鉴别二者溶液的试剂
D.分别向盛有FeCl 溶液和FeCl 溶液的试管中加入NaOH溶液,最终可得相同物质
2 34.下列离子的检验方法合理的是( )
A.向某溶液中通入氯气,然后再加入KSCN溶液变红色,不能说明原溶液中含Fe2+
B.向某溶液中加入NaOH溶液,最终得到红褐色沉淀,说明溶液中含Fe3+
C.向某溶液中滴加 KSCN溶液呈红色,说明不含Fe2+
D.向某溶液中加入NaOH溶液得白色沉淀,又观察到逐渐变成红褐色,说明只含Fe2+不含Mg2+
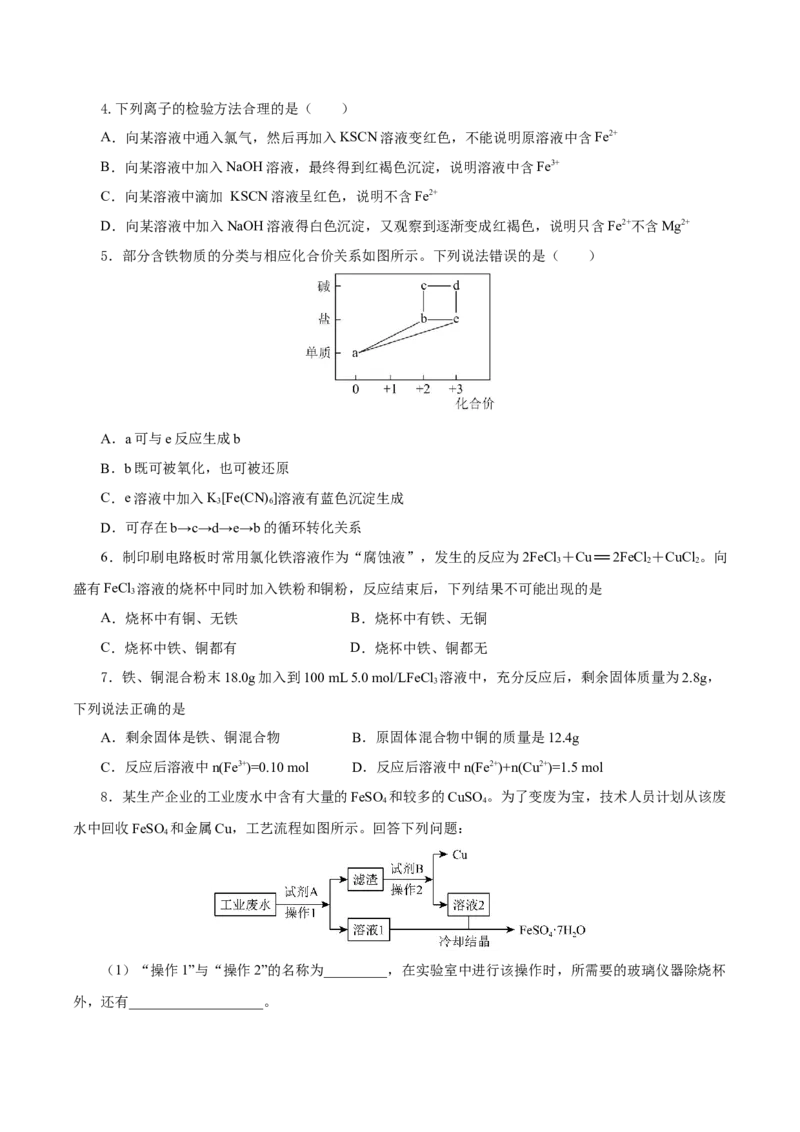
5.部分含铁物质的分类与相应化合价关系如图所示。下列说法错误的是( )
A.a可与e反应生成b
B.b既可被氧化,也可被还原
C.e溶液中加入K[Fe(CN) ]溶液有蓝色沉淀生成
3 6
D.可存在b→c→d→e→b的循环转化关系
6.制印刷电路板时常用氯化铁溶液作为“腐蚀液”,发生的反应为2FeCl +Cu=2FeCl +CuCl 。向
3 2 2
盛有FeCl 溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
3
A.烧杯中有铜、无铁 B.烧杯中有铁、无铜
C.烧杯中铁、铜都有 D.烧杯中铁、铜都无
7.铁、铜混合粉末18.0g加入到100 mL 5.0 mol/LFeCl 溶液中,充分反应后,剩余固体质量为2.8g,
3
下列说法正确的是
A.剩余固体是铁、铜混合物 B.原固体混合物中铜的质量是12.4g
C.反应后溶液中n(Fe3+)=0.10 mol D.反应后溶液中n(Fe2+)+n(Cu2+)=1.5 mol
8.某生产企业的工业废水中含有大量的FeSO 和较多的CuSO 。为了变废为宝,技术人员计划从该废
4 4
水中回收FeSO 和金属Cu,工艺流程如图所示。回答下列问题:
4
(1)“操作1”与“操作2”的名称为_________,在实验室中进行该操作时,所需要的玻璃仪器除烧杯
外,还有___________________。(2)加入试剂A的目的是将Cu2+全部转化为Cu,以便回收铜单质,发生反应的离子方程式为
______________________________。
(3)“滤渣”的成分为________________,加入的试剂B为__________(填化学式)。
(4)要鉴别“溶液2”中的金属阳离子,所需实验操作及实验现象是:
__________________________________________________________________________。