文档内容
第三章 铁 金属材料
第一节 铁及其化合物 课时作业
第三课时 铁的重要化合物—铁盐和亚铁盐
1.为检验FeCl 溶液中是否含有Fe3+,可选择的试剂是( )
2
A.稀盐酸 B.AgNO 溶液
3
C.KSCN溶液 D.HO
2 2
【答案】C
【解析】铁离子能够与硫氰化钾溶液发生络合反应,生成血红色溶液,而亚铁离子与
硫氰化钾混合没有此现象,因此检验FeCl 溶液中是否含有Fe3+,可选择的试剂KSCN溶
2
液;故选C。
2.证明某溶液只含有Fe2+而不含有Fe3+的实验方法是( )
A.只需滴加硫氰化钾溶液
B.先滴加硫氰化钾溶液,不显红色,再滴 加氯水后显红色
C.先滴加氯水,再滴加硫氰化钾溶液后显红色
D.滴加氢氧化钠溶液,立即产生红褐色沉淀
【答案】B
【解析】A.只滴加KSCN溶液,根据溶液是否显红色,能检验出溶液中是否含有
Fe3+,无法验证Fe2+存在,故A错误;B.KSCN与Fe3+作用使溶液显红色,与Fe2+作用无
此现象,先滴加KSCN溶液,不显红色,说明原溶液不含有Fe3+,再滴加氯水后显红色,
说明滴加氯水后溶液中有Fe3+,证明原溶液含有Fe2+,故B正确;C.先滴加氯水,氯气将
Fe2+氧化成Fe3+,即使原溶液不含Fe3+,滴加KSCN溶液后也显红色,无法证明原溶液是否
含有Fe3+,故C错误;D.滴加NaOH溶液,立即产生红褐色沉淀,说明含有Fe3+,无法验
证Fe2+存在,故D错误;故选B。
3.下列反应对应的离子方程式正确的是( )
A.Fe (SO ) 溶液中加入足量Ba(OH) 溶液:Fe3++3OH-=Fe(OH) ↓
2 4 3 2 3
B.漂白粉使用时加醋酸:ClO-+H+=HClO
C.将FeSO 溶液与酸性KMnO 溶液混合:5Fe2++MnO
4 4
4
-
基础达标
+8H+=5Fe3++Mn2++4H O
2D.四氧化三铁溶于稀硝酸中:Fe O+8H+=2Fe3++Fe2++4H O
3 4 2
【答案】C
【解析】A.硫酸根和钡离子要生成沉淀,离子方程式为2Fe3++3SO
4
-2
+3Ba2++6OH-
=2Fe(OH) ↓+3BaSO ↓,故A错误;B.醋酸是弱电解质不能拆,ClO-
3 4
+CH3COOH=HClO+CH3COO-,故B错误;C.FeSO 被酸性KMnO 氧化生成Fe3+,5Fe2+
4 4
+MnO 4
-
+8H+=5Fe3++Mn2++4H O,故C正确;D.四氧化三铁溶于稀硝酸中生成Fe3+和
2
NO:3Fe O+NO
3 4
3
-
+28H+=9Fe3++NO↑+14HO,故D错误; 故答案为C
2
4.室温下,下列各组离子在指定溶液中能大量共存的是( )
A.NaOH溶液中:Na+、K+、CO2-、SO 2-
3 4
B.FeCl 溶液中:K+、Mg2+、SO 2-、OH-
2 4
C.KCO 溶液中:Na+、Ba2+、Cl-、OH-
2 3
D.HSO 溶液中:K+、NH +、NO -、HCO -
2 4 4 3 3
【答案】A
【解析】A.NaOH溶液中,Na+、K+、CO2-、SO 2-都能稳定存在,则离子可以大量共
3 4
存,A符合题意;B.FeCl 、Mg2+都能与OH-反应,生成Fe(OH) 、Mg(OH) 沉淀,B不符
2 2 2
合题意;C.KCO 溶液中,Ba2+会生成BaCO 沉淀,离子不能大量共存,C不符合题意;
2 3 3
D.HSO 溶液中,HCO -会转化为CO 和水,离子不能大量共存,D不符合题意;故选
2 4 3 2
A。
5.下列检验或鉴别的说法中,不正确的是( )
A.用相互滴加的方法可以鉴别盐酸和NaCO 溶液
2 3
B.向某溶液中滴加几滴BaCl 溶液,产生白色沉淀,则原溶液中一定含SO 2-
2 4
C.某溶液的焰色试验呈黄色,该溶液中可能含有钾元素
D.某溶液滴入KSCN溶液不变红,再滴入氯水后溶液变红,则原溶液中一定含有
【答案】B
【解析】A.盐酸少量,与碳酸钠反应不生成气体;盐酸过量,与碳酸钠反应生成气
体,改变滴定顺序可鉴别,故A正确; B.白色沉淀可能为氯化银或硫酸钡,由实验操作
和现象可知,原溶液中也可能含有银离子,不一定含硫酸根离子,故B错误; C.钠元素
的焰色为黄色,观察钾元素的焰色需透过蓝色的钴玻璃,由实验操作和现象可知,该溶液
中可能含有钾元素,故C正确; D.滴入KSCN溶液不变红,可知不含铁离子,再滴入氯水后溶液变红,可知亚铁离子被氧化为铁离子,则原溶液中一定含有Fe2+,故D正确; 答
案B。
6.铁盐与亚铁盐在工业生产和生活中具有重要应用。三氯化铁在水溶液中易形成氢氧
化铁胶体,具有吸附作用,可用作净水剂。三氯化铁溶液可用作印刷电路板刻剂,反应化
学方程式为2FeCl +Cu=2FeCl +CuCl 。硫酸亚铁溶液可用于脱除烟气中的二氧化硫等
3 2 2
有害气体。下列离子能在印刷电路板的蚀刻废液中大量存在的是( )
A.H+ B.MnO - C.OH- D.Ag+
4
【答案】A
【解析】根据题意,用 FeCl 作刻蚀液水,会发生反应:2FeCl +Cu=2FeCl +
3 3 2
CuCl ,反应完全后,得到的蚀刻废液中成分应为FeCl 、FeCl 和CuCl 等,根据物质性质
2 2 3 2
分析解答。A项,H+与FeCl 、FeCl 和CuCl 等的微粒不能反应,可以共存,符合题意;B
2 3 2
项,MnO -具有强氧化性,能够与FeCl 的Fe2+发生反应产生FeCl ,不能大量共存,不符
4 2 3
合题意;C项,FeCl 、FeCl 和CuCl 等金属阳离子都会与OH-发生反应形成Fe(OH) 、
2 3 2 2
Fe(OH) 、Cu(OH) 沉淀,不能大量共存,不符合题意;D项,Ag+与盐溶液中的Cl-反应产
3 2
生AgCl白色沉淀,不能大量共存,不符合题意。
7.维生素C又称“抗坏血酸”,能帮助人体将食物中摄取的、不易吸收的Fe3+转化
为易吸收的Fe2+,下列有关分析错误的是( )
A.维生素C具有还原性
B.Fe3+转化为Fe2+发生了氧化反应
C.维生素C药片应隔绝空气保存
D.向Fe3+的溶液中加入Cu,也能将Fe3+转化为Fe2+
【答案】B
【解析】A项,维生素C能够将Fe3+转化为易吸收的Fe2+,Fe元素化合价降低,得到
电子被还原,说明维生素C具有还原性,正确;B项,Fe3+转化为Fe2+时,Fe元素化合价
降低,得到电子被还原,发生了还原反应,错误;C项,维生素C药片具有强的还原性,
容易被空气中的氧气氧化,因此应隔绝空气保存,正确;D项,向Fe3+的溶液中加入Cu,
会发生反应:2Fe3++Cu=2Fe2++Cu2+,因此Cu单质也能将Fe3+转化为Fe2+,正确。
8.将1.12g铁粉加入到25mL2mol·L-1的氯化铁溶液中,充分反应后,其结果是(
)
A.铁粉剩余,溶液呈浅绿色,Cl-基本不变
B.向溶液中滴入无色KSCN溶液,不显血红色C.氧化产物与还原产物的物质的量之比为2:5
D.溶液中Fe2+与Fe3+物质的量之比为6:1
【答案】D
1.12g
【解析】n(Fe)= mol=0.02mol,25mL2mol·L-1的氯化铁溶液中
56g/mol
n(Fe3+)=0.025L×2mol/L=0.05mol
A.由反应:Fe+2Fe3+=3Fe2+可知Fe3+过量,呈黄色,Cl-浓度基本不变,选项A错误;B.
往溶液中滴入无色KSCN溶液,溶液显红色,选项B错误;C.由反应:Fe+2Fe3+=3Fe2+可
知氧化产物与还原产物的物质的量之比为1:2,选项C错误;D.反应后溶液中n(Fe2+)=
3n(Fe)=0.06mol,n(Fe3+)=0.01mol,Fe2+和Fe3+的物质的量之比为6∶1,选项D正确;故答
案选D。
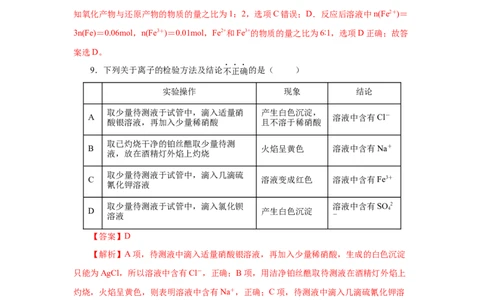
9.下列关于离子的检验方法及结论不正确的是( )
实验操作 现象 结论
取少量待测液于试管中,滴入适量硝 产生白色沉淀,
A 溶液中含有Cl-
酸银溶液,再加入少量稀硝酸 且不溶于稀硝酸
取已灼烧干净的铂丝醮取少量待测
B 火焰呈黄色 溶液中含有Na+
液,放在酒精灯外焰上灼烧
取少量待测液于试管中,滴入几滴硫
C 溶液变成红色 溶液中含有Fe3+
氰化钾溶液
取少量待测液于试管中,滴入氯化钡 溶液中含有SO 2
D 产生白色沉淀 4
溶液 -
【答案】D
【解析】A项,待测液中滴入适量硝酸银溶液,再加入少量稀硝酸,生成的白色沉淀
只能为AgCl,所以溶液中含有Cl-,正确;B项,用洁净铂丝醮取待测液在酒精灯外焰上
灼烧,火焰呈黄色,则表明溶液中含有Na+,正确;C项,待测液中滴入几滴硫氰化钾溶
液,溶液变为红色,则溶液中一定含有Fe3+,正确;D项,待测液中滴入氯化钡溶液,产
生的白色沉淀可能为AgCl、BaSO、BaCO 等,则溶液中不一定含有SO 2-,不正确。
4 3 4
10.下列关于“摩尔盐”[(NH )Fe(SO )·6H O]的说法不正确的是( )
4 2 4 2 2
A.具有较强的还原性,可使高锰酸钾酸性溶液褪色
B.可用于治疗缺铁性贫血,还可用于制造红色颜料铁红(Fe O)、磁性氧化铁(Fe O)
2 3 3 4
等
C.加水溶解,再滴加KSCN溶液,若溶 液变红色,说明摩尔盐已氧化变质D.加水溶解,与过量NaOH溶液反应的离子方程式:Fe2++2OH-=Fe(OH) ↓
2
【答案】D
【解析】A.摩尔盐的化学式为(NH )Fe(SO )·6H O可知,Fe为+2价,具有较强的还
4 2 4 2 2
原性,可使高锰酸钾酸性溶液褪色,故A正确;B.摩尔盐的化学式为(NH )Fe(SO )·6H O
4 2 4 2 2
可知,Fe为+2价,可用于治疗缺铁性贫血,还可用于制造红色颜料铁红(Fe O)、磁性氧化
2 3
铁(Fe O),故B正确;C.Fe为+2价,不能使KSCN溶液变红色。加水溶解,再滴加
3 4
KSCN溶液,若溶液变红色,说明摩尔盐已氧化变质,故C正确;D.摩尔盐的化学式为
(NH )Fe(SO )·6H O可知, Fe2+ NH 都能与碱反应,且Fe(OH) 不稳定,在空气中容易被
4 2 4 2 2 2
氧化,故D错误;故答案:D。
能力提升
11.室温下,下列实验探究方案能达到探究目的的是( )
选项 探究方案 实验目的
向某溶液中滴加少量氯水,然后滴入几滴
A 探究溶液中是否含有Fe2+
KCSN溶液,观察现象
淀粉溶液加入稀硫酸,加热,冷却后滴入
B 探究淀粉是否发生水解
碘水,观察溶液颜色变化
向Fe(NO ) 溶液中滴入硫酸酸化的HO 溶
C 3 2 2 2 验证氧化性:HO>Fe3+
液,观察溶液颜色变化 2 2
将NaAlO 溶液与NaHCO 溶液混合,观
D 2 3 验证结合质子能力:AlO->CO 2-
察现象 2 3
A.A B.B C.C D.D
【答案】D
【解析】A.先加入氯水,氯水中的Cl 能将Fe2+氧化为Fe3+,再加入KSCN溶液,溶
2
液一定会变红,不能检验原溶液中是否含有Fe2+,故A错误;B.淀粉溶液加入稀硫酸,
加热,冷却后滴入碘水,溶液变蓝色,淀粉可能部分水解,故B错误;C.酸性溶液中硝
酸根离子、HO 均可氧化亚铁离子为铁离子,由操作和现象不能比较HO、Fe3+的氧化
2 2 2 2
性,故C错误;D.将NaAlO 溶液与NaHCO 溶液混合,发生反应AlO-+H O+HCO -
2 3 2 2 3
=Al(OH) ↓+CO 2-,出现白色沉淀,说明AlO-得到质子的能力强于CO2-,故D正确;故选
3 3 2 3
D。12.已知:①PbO 固体与浓盐酸反应,产生黄绿色气体;②向KSCN和FeBr 的混合
2 2
溶液中通入少量实验①产生的气体(仅与一种离子反应),溶液变红色;③取少量FeCl 溶液
3
滴在淀粉-KI试纸上,试纸变蓝。下列判断错误的是( )
A.上述实验中有三个氧化还原反应
B.通过上述实验可得到结论,氧化性:PbO >Cl>Br >Fe3+>I
2 2 2 2
C.实验②能证明Fe2+有还原性,不能证明Fe3+有氧化性
D.实验①生成的气体能使湿润的淀粉-KI试纸变蓝
【答案】B
【解析】A. 反应①浓盐酸生成了氯气、反应②为氯气和溴化亚铁的反应,反应③碘
离子转变为碘单质,均有元素化合价变化、为氧化还原反应,A正确;B.反应②为少量
氯气和溴化亚铁的反应、但仅与一种离子反应,变红是生成铁离子和硫氰根离子反应所
致、则能证明氯气氧化性大于铁离子、但不能证明氯气的氧化性大于溴单质,B错误;C.
实验②能证明Fe2+有还原性,不能证明Fe3+有氧化性,实验③能证明Fe3+有氧化性,C正
确;D. 实验①生成的气体为氯气,氯气能置换出碘单质、能使湿润的淀粉-KI试纸变
蓝,D正确;答案选B。
13.某学生在学习了检验食品中的铁 元素后,设想在课外研究测定某补血剂中铁元素
(+2价)含量,其设计实验流程如下:
下列说法不正确的是
A.步骤②时以用新制氯水替代HO
2 2
B.步骤①需要在研钵中研磨,研磨时研杵应保持垂直
C.取步骤②操作后的溶液,滴加几滴KSCN溶液可检验补血剂是否己因氧化变质
D.每片补血剂中铁元素的质量为0.07wg
【答案】C
【解析】将补血剂研细,向药片中加入稀硫酸,然后过滤分离滤液和不溶性物质,向
滤液中加入双氧水,将Fe2+氧化为Fe3+,向溶液中加入过量氨水溶液得到氢氧化铁沉淀,
将红褐色沉淀灼烧得到红棕色固体Fe O,以此来解答。A.双氧水的作用为将Fe2+氧化为
2 3
Fe3+,氯水也可以Fe2+氧化为Fe3+,故可以用新制氯水替代HO,A正确;B.步骤①将补
2 2血剂研细,需要在研钵中研磨,进行研磨操作时,研钵应放在不易滑动的物体上,研杵应
保持垂直,B正确;C.步骤②操作后的溶液中一定含铁离子,滴加几滴KSCN溶液不能
检验补血剂是否已因氧化变质,应检验②之前的滤液是否含铁离子证明,C错误;D.wg
为Fe O,由Fe元素守恒可知,每片补血剂中铁元素的质量为 =0.07wg,D正确;
2 3
综上所述答案为C。
14.某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl 溶液,
3
继续煮沸至液体是透明的__________色,停止加热,即制得Fe(OH) 胶体。用激光笔照射
3
烧杯中的液体,可以看到________________________________________________。
(2)甲组同学通过研究pH对FeSO 稳定性的影响,得到如图1所示结果,增强Fe2+稳定
4
性的措施为__________________________________________________________。
(3)乙组同学为探究Fe (SO ) 与Cu的反应,进行如图2所示实验:
2 4 3
①Fe3+与Cu反应的离子方程式为
_____________________________________________。
②为了探究白色沉淀产生的原因,向学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.SCN-的化学性质与I-相似;
iii.2Cu2+4I-=2CuI↓+I
2填写实验方案:
实验方案 实验现象
少骤1:取4mL0.2mol/L的FeSO 溶液,向其中滴加3滴
4 无明显现象
0.1mo/LKSCN溶液
步骤2:取4mL_________mol/L的CuSO 溶液,向其中滴
4 产生白色沉淀
加3滴0.1moI/LKSCN溶液
Cu 与SCN-反应的离子方程式为_____________________________________。
(4)市售某种补铁口服液的主要成分是葡萄糖酸亚铁。根据名称认为该糖浆中含有
Fe2+,设计方案进行验证。
方案 试剂X
方案i 1mL1mol/L酸性KMnO 溶液
4
方案ii 依次加入5滴KSCN溶液。1mL氨水
①方案冲预期现象与实验现象相同,并不能证明补铁口服液中一定含有Fe2+,猜想理
由是
____________________________________________________________________________。
②方案ii中现象是
___________________________________________________________,则证明口服液中含
Fe2+。
【答案】(1) 红褐 一条光亮的通路
(2)增强溶液的酸性或降低溶液的pH
(3) 2Fe3++Cu=2Fe2++Cu2+ 0.1 2Cu2++4SCN =2CuSCN↓+(SCN)
2
(4) 高锰酸钾褪色说明被还原,补铁口服液中除了有Fe2+以外还有其他还原剂,因此褪
色不一定证明是高锰酸钾与Fe2+反应 加入KSCN后无明显现象,加入氯水后溶液变血
红色
【解析】(1)配制Fe(OH) 胶体:在小烧杯中加入20mL蒸馏水,加热至沸腾后,向
3
沸水中滴入几滴饱和FeCl 溶液,继续煮沸至液体是透明的红褐色,停止加热;胶体可以发
3
生丁达尔效应,即用激光笔照射烧杯中的液体,可以看到一条光亮的通路;
(2)如图1可知随着pH的增大Fe2+被氧化的量增大,所以增强Fe2+稳定性的措施为
增强溶液的酸性或降低溶液的pH;(3)Cu有还原性,Fe2+有氧化性,可以发生氧化还原反应,即2Fe3++Cu=2Fe2++Cu2+;
由化学反应可知生成两份的Fe2+同时生成了一份的Cu2+,为了探究白色沉淀产生的原因,
需控制量的比值相等,步骤一取4mL0.2mol/L的FeSO 溶液,向其中滴加3滴0.1mo/
4
LKSCN溶液,则步骤二取4mL 0.1mol/L的CuSO 溶液,向其中滴加3滴0.1moI/LKSCN溶
4
液,已知SCN-的化学性质与I-相似,2Cu2+4I-=2CuI↓+I ,CuSCN是难溶于水的白色固体,
2
所以Cu2+与SCN-反应的离子方程式为2Cu2++4SCN =2CuSCN↓+(SCN) ;
(4)补铁口服液为混合物,其主要成分是葡萄糖酸亚铁,里面还可能含有其他的还原
剂,能使有氧化性的高锰酸钾褪色;Fe2+的检验:加入KSCN后无明显现象,加入氯水后
溶液变血红色,即为Fe2+;则证明口服液中含Fe2+。
直击高考
15.一定条件下,将一定量Fe O 溶于过量盐酸生成FeCl 和FeCl ,分别取少量反应
3 4 2 3
后的溶液进行以下实验,有关实验描述正确的是
A.滴加KSCN溶液,若溶液变红色证明溶液中含有Fe3+
B.加入5.6 g铁粉恰好完全反应,则Fe O 的质量为23.2 g
3 4
C.用溶液在铜片上写字,一段时间后洗去溶液,观察到铜片表面无明显现象
D.先向溶液中通入氯气,再滴加KSCN溶液,若变红色证明溶液中含有Fe2+
【答案】A
【解析】A项,三价铁遇到硫氰化钾后溶液会变成红色,故滴加KSCN溶液,若溶液
变红色证明溶液中含有Fe3+,正确;B项,原溶液中盐酸有剩余,加入铁粉后会和盐酸反
应,故无法通过铁的量计算四氧化三铁的量,错误;C项,溶液中有三价铁离子,可以和
铜单质反应,故用溶液在铜片上写字,一段时间后洗去溶液,会发现有铜被溶解,错误;
D项,溶液变红也可能是原来溶液中就有三价铁而使溶液变红,错误。
16.某研究小组欲探究Fe2+能否与HO 溶液反应。
2 2
(查阅资料)i.Fe2+具有较强的还原性, 具有较强的氧化性。
ii.Fe3+遇SCN-可生成Fe(SCN) ,Fe(SCN) 溶液呈血红色,可用于Fe3+的检验。
2 3
(提出猜想)
(1)小组同学经过讨论后,认为HO 溶液可以与FeSO 溶液反应,请从化合价的角
2 2 4
度加以解释:_________________________________________________。(设计实验)
(2)实验I:在试管中加入FeSO 溶液和HO 溶液,再加入 溶液,发现溶液
4 2 2
______,小组同学认为Fe2+和HO 溶液反应生成了Fe3+。
2 2
(3)甲同学注意到盛放FeSO 溶液的试剂瓶中有空气,因此不同意该结论,他的理由
4
是_______________________________________________________。
重新设计实验:
实验II:在试管中加入FeSO 溶液,然后加入 溶液,发现溶液无明显变化,再
4
加入HO 溶液,发现溶液变红。
2 2
(获得结论)
(4)过氧化氢___________(填“能”或者“不能”)氧化 。
(发现异常)
乙同学继续向实验II所得溶液中滴加溶液,发现溶液褪色。
小组同学经过重新查阅资料后,发现可以将SCN-氧化为SO 2-。乙同学设计实验III并
4
证实了该资料中的说法。
(5)补全实验III的方案:在试管中加入HO 溶液,加入KSCN溶液,再加入
2 2
___________,产生________________。
(总结反思)
(6)小组同学经过讨论后,提出了Fe2+的检验方法:取待测液于试管中,
______________
_________________________________________________________,证明待测液含有Fe2+。
(7)从上述实验中可以得出结论,在物质性质的检验中,应注意
___________________
___________________________________________(至少写出两条)对实验结果的影响。
【答案】(1)HO 中氧元素为-1价,在反应中可以降为-2价,做氧化剂,FeSO 中铁
2 2 4
元素为+2价,在反应中可以升为+3价,做还原剂
(2)变红
(3)空气中的氧气具有较强的氧化性,会将亚铁离子氧化物为铁离子
(4)能
(5)BaCl 溶液 白色沉淀
2
(6)加入氢氧化钠溶液,生成白色沉淀,白色沉淀迅速变成灰绿色,最后变成红褐色(7)加入物质的顺序、空气对实验的干扰
【解析】(1)HO 中氧元素为-1价,在反应中可以降为-2价,做氧化剂,FeSO 中铁
2 2 4
元素为+2价,在反应中可以升为+3价,做还原剂,因此HO 溶液可以与FeSO 溶液反
2 2 4
应,故答案为:HO 中氧元素为-1价,在反应中可以降为-2价,做氧化剂,FeSO 中铁元
2 2 4
素为+2价,在反应中可以升为+3价,做还原剂;
(2)在试管中加入FeSO 溶液和HO 溶液,反应生成Fe3+,再加入KSCN溶液,发现溶
4 2 2
液变红,故答案为:变红;
(3)盛放FeSO 溶液的试剂瓶中有空气,空气中的氧气具有较强的氧化性,会将亚铁
4
离子氧化物为铁离子,故答案为:空气中的氧气具有较强的氧化性,会将亚铁离子氧化物
为铁离子;
(4)通过实验II,在试管中加入FeSO 溶液,然后加入KSCN溶液,发现溶液无明显
4
变化,说明Fe2+为被氧化,再加入HO 溶液,发现溶液变红,说明生成了铁离子,则可以
2 2
知道过氧化氢能氧化Fe2+,故答案为:能;
(5)HO 可以将SCN-氧化为SO 2-,设计实验III是验证SO 2-的存在,操作为:在试
2 2 4 4
管中加入HO 溶液,加入KSCN溶液,再加入BaCl 溶液,产生白色沉淀,说明SO 2-的存
2 2 2 4
在,故答案为:BaCl 溶液;白色沉淀;
2
(6)Fe2+的检验方法:取待测液于试管中,加入氢氧化钠溶液,生成白色沉淀,白色
沉淀迅速变成灰绿色,最后变成红褐色,证明待测液含有Fe2+,故答案为:加入氢氧化钠
溶液,生成白色沉淀,白色沉淀迅速变成灰绿色,最后变成红褐色;
(7)从上述实验中可以得出结论,在物质性质的检验中,应注意加入物质的顺序、空
气对实验的干扰等对实验结果的影响,故答案为:加入物质的顺序、空气对实验的干扰。