文档内容
第三章 铁 金属材料
第一节 第二课时 铁的氢氧化物 铁盐和亚铁盐
本节是教材高一(必修一)第三章,在这一章学习的过程中,在初中阶段比较肤浅地了解一些
铁的知识,本节要在这些知识的基础上结合;离子反应、氧化还原反应等知识进一步加深学习铁的
有关性质。从本质上了解铁是一种变价金属。 在教学过程中考虑新旧知识的相互衔接,注意充分
发挥理论知识对元素化合物知识的指导作用。学习相关内容时应用理论知识加以解释,应用的过程
也是进一步加深理解这些理论的过程。例如,本节很多的反应都属于氧化还原反应,用电子转移的
观点分析这些反应,既能加深对具体反应的理解,又可以巩固有关氧化还原反应的概念.通过介绍一
些生活中的铁以及氧化物,进一步加深学生对这些知识的理解.
教学目标
1、掌握铁的氢氧化物的主要性质,铁盐和亚铁盐的检验和转化。
2、通过自主学习,自主进行知识网络的构建和知识的归纳整理,培养学生的自学能力和归纳总结
能力。
核心素养
1、 分类、比较、分析、归纳、演绎等整理科学事实的基本方法,学习物质的性质。学会
学习和认识新化学物质的基本思路和方法。
2、 通过铁的化合物的性质与用途的学习,使学生进一步认识化学在促进社会发展、改善
人类的生活条件等方面所起到的重要作用,提高学习化学的兴趣,增强学好化学,服务社会的
责任感和使命感。
重点: 铁的氢氧化物、铁盐和亚铁盐转化
难点: 亚铁离子的检验
查阅铁的氢氧化物、铁盐和亚铁盐相关内容,预习课本。
【过渡】根据前面的学习,由铁的氧化物,可以看出,铁在化合物中主要以哪些价态存在?
【学生回答】+2 、+3【提问】
1、铁的氢氧化物有哪些?什么颜色?
2、能否直接用氧化亚铁、氧化铁溶于水制备氢氧化亚铁和氢氧化铁?
3、能否用铁与水反应制得?
【学生回答】白色氢氧化铁 红褐色氢氧化亚铁 不能用氧化物直接溶于水得到氢氧化物因为铁的
氧化物都不溶于水。也不能用铁和水反应制得。
【教师】那该如何制备铁的氧化物?
【学生回答】用可溶性铝盐和碱。用可溶性铁盐、亚铁盐与碱溶液反应。
【教师】现在每个学习小组都有一个实验筐,里面装有硫酸亚铁溶液,大家看什么颜色,这是+2
价铁离子在溶液当中的颜色。氯化铁溶液,什么颜色?,这是+3价铁离子在溶液当中的颜色。请
大家根据现有的实验药品,分别制备出一份氢氧化亚铁和氢氧化铁。一个同学做实验,其他同学做
好实验记录。将实验现象和结论如实写在表格中。(3min)
实验药品:氯化铁 硫酸亚铁 氢氧化钠
【教师】时间到了,哪一组来展示一下你们小组讨论的结果。
【学生回答】氢氧化铁制备的原理是:Fe3++3OH-=Fe(OH) ↓,所需药品是FeCl 和NaOH。操作
3 3
步骤是,先加入少量FeCl 于试管中,再滴入NaOH振荡。制备氢氧化亚铁的原理是: Fe2++2OH-
3
=Fe(OH) ↓,药品是FeCl 和NaOH。操作步骤是,先加入少量FeCl ,再滴入NaOH振荡。(同
2 2 2
时展示学案结果)
【学生回答】试管一种黄色的溶液和一种无色溶液瞬间就变成了一种红褐色沉淀。(拿着试管展
示)
【学生回答】另一个试管好像看到了灰绿色的沉淀。
【教师】其他同学有没有观察到不一样的现象?我们在制备氢氧化铁时,看到了红褐色的沉淀;制
备氢氧化亚铁时,看到灰绿色的沉淀。氢氧化亚铁原本是什么颜色呢?
【学生回答】白色。
【教师】好,大家把灰绿色试管摇一摇,让绿色沉淀沾在壁上,搁置一边,一边思考出现灰绿色沉
淀的原因,一边观察老师制备氢氧化亚铁的实验,看看我和你的操作有什么不同?
【实验演示】氢氧化亚铁的制备。(油封、溶液煮沸、试管深入到液面以下)
【教师】现在大家看,在胶头滴管最低端有没有白色沉淀?大家观察我的操作和你们的有什么不同?
现在大家观察灰绿色试管的试管壁是什么颜色的物质?推测一下这种物质可能是谁?如何产生?
【学生回答】老师是将胶头滴管插在液面以下滴加氢氧化钠。红褐色。氢氧化铁。
【教师】奇怪了,本来我们要制备的是白色的氢氧化亚铁,但是发现制备出来一种灰绿色沉淀,然
后这个灰绿色沉淀又会变成红褐色氢氧化铁沉淀。(板书)大家从变化前后铁的化合价上分析一下,氢氧化亚铁被还原还是被氧化?
【学生回答】被氧化。
【教师】好,被氧化那一定得有氧化剂,现在大家思考为什么我将胶头滴管插入到液面以下滴加的
时候,可以看见白色沉淀生成?
【学生回答】为了隔绝空气。
【教师】那这个氧化剂很有可能是谁?
【学生回答】氧气
【教师】
氢氧化亚铁中的铁是+2价,我们在讲到还原剂的时候,提到过+2价的铁常常表现出还原性,所以
氢氧化亚铁很容易和氧气水在的条件下发动412政变,转化成红褐色的氢氧化铁。从刚才氧化亚铁
和氢氧化亚铁可以看出,含+2铁的化合物稳定性比较差,容易被氧化。
板书:4Fe(OH) +2H O+O =4Fe(OH)
2 2 2 3
【提问】大家看我刚才制备出来的氢氧化亚铁,还是变成了灰绿色了,怎么回事?
【学生回答】被氧化了。
【教师】可是氢氧化亚铁已经在溶液中了,哪里有氧气?
【学生回答】溶液中有氧气。
【教师】如果我想得到较为纯净的氢氧化亚铁,就必须改进实验方案。大家思考改进的关键在哪?
【学生回答】隔绝氧气
【教师】对!那你现在就想尽办法隔绝氧气,那大家想一想,怎么样才能让溶液当中没有氧气存在?
【学生回答】煮沸水;油封;改进实验装置,反应之前先排出装置中的空气………
【教师】好,大家的想法非常好,老师这有一个实验改进装置,我们来一起分析一下怎么利用这个
装置来制备较为纯净的氢氧化亚铁。
【教师】我们现在看一下这个实验装置,然后回忆氢气还原氧化铜这个实验,开始实验时是先通氢
气还是先加热?
【学生回答】通氢气
【教师】通氢气的目的是什么?
【学生回答】将装置当中的空气排干净。
【教师】大家看A瓶中装有铁和硫酸是干什么的?氢气用来干什么?硫酸亚铁干什么的?
【学生回答】产生氢气和硫酸亚铁,排出实验装置中的空气。
【教师】好!A瓶当中有两个导管,氢气应该从哪个导管出去?
【学生回答】从中间哪个导管出去。
【教师】我们把装置当中的空气赶走以后,还是得不到氢氧化铁,AB两瓶当中的物质碰不上面麽?
怎么办?我们怎样才能让两种液体接触?硫酸亚铁应该从哪个导管出去进到B瓶当中。【学生回答】关闭C,气体不流通,氢气会将硫酸亚铁压到B瓶当中。
【教师】非常好,所以说氢气在这里起到了几个作用?
【学生回答】赶走空气;给硫酸亚铁与氢氧化钠接触提供动力。
【教师】非常好!氢氧化亚铁的制备就讨论到这里,有些同学可能还有更好的方案,我们课下继续
讨论。
好,现在大家根据刚才所学内容以及熟知的碱的性质,归纳总结两种氢氧化物的物理性质和化学性
质,完成学案。2min
【教师】好,我随机抽取一位学生的学案,我们一起看一下。
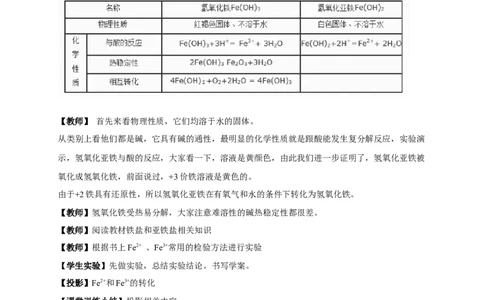
【教师】 首先来看物理性质,它们均溶于水的固体。
从类别上看他们都是碱,它具有碱的通性,最明显的化学性质就是跟酸能发生复分解反应,实验演
示,氢氧化亚铁与酸的反应,大家看一下,溶液是黄颜色,由此我们进一步证明了,氢氧化亚铁被
氧化成氢氧化铁,前面说过,+3价铁溶液是黄色的。
由于+2铁具有还原性,所以氢氧化亚铁在有氧气和水的条件下转化为氢氧化铁。
【教师】氢氧化铁受热易分解,大家注意难溶性的碱热稳定性都很差。
【教师】阅读教材铁盐和亚铁盐相关知识
【教师】根据书上Fe2+ 、Fe3+常用的检验方法进行实验
【学生实验】先做实验,总结实验结论。书写学案。
【投影】Fe2+和Fe3+的转化
【课堂训练小结】投影相关内容