文档内容
课堂检测·素养达标
1.从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平。如
图表示了三种金属被人类开发利用的大致年限,之所以有先后,主要取决于
( )
A.金属的导电性强弱
B.金属在地壳中的含量多少
C.金属的化合价高低
D.金属的活动性强弱
【解析】选D。由于人类掌握科学知识的局限性,越活泼的金属越难以冶炼,故
发现年代越晚。
2.下列说法错误的是 ( )
A.对废旧金属的最好处理方法是回收、再利用
B.提炼金属要经过矿石的富集、冶炼、精炼三步
C.活泼金属的冶炼都是通过电解其盐溶液
D.热还原法中还原剂有焦炭、一氧化碳、氢气和活泼金属等【解析】选C。活泼金属的冶炼是电解其熔融盐(如MgCl 、NaCl等)或熔融氧化
2
物(如Al O 等)制得的,电解其盐溶液得不到金属单质。
2 3
3.把铝粉和氧化亚铁粉末配成铝热剂,分成两等份。一份在高温下恰好完全反
应后,再与足量盐酸反应;另一份直接放入足量的烧碱溶液中充分反应。前后两
种情况下生成的气体的质量比是 ( )
A.3∶2 B.2∶3 C.1∶1 D.28∶9
【解析】选C。本题应分析两个过程中电子转移的数目。铝置换出铁,铁再和盐
酸反应生成H ,和铝直接与烧碱反应生成H 转移的电子数目应该相同,化学方程
2 2
式如下:2Al+3FeO Al O +3Fe,3Fe+6HCl 3FeCl +3H ↑; 2Al+2NaOH+2H O
2 3 2 2 2
2NaAlO +3H ↑;由此可看出两种情况下生成的气体的质量比为1∶1。
2 2
【补偿训练】
下列说法中正确的是 ( )
A.金属的冶炼原理,就是利用氧化还原反应原理,在一定条件下将金属从其化合
物中还原出来
B.冶炼金属时,必须加入一种物质作为还原剂
C.金属由化合态变为游离态,可能被还原,也可能被氧化
D.金属单质被发现和应用得越早,其在地壳中的含量越大【解析】选A。A项,金属冶炼是将金属化合物转化为金属单质,正确;B项,冶炼
金属并不一定要加入还原剂,如电解法制取钠和镁,错误;C项,金属由化合态变
为游离态,都是由高价态降低到0价,故一定被还原,错误;D项,金属被发现的早
晚与其在地壳中的含量无关,如在地壳的金属中铝的含量虽然最大,但被发现的
时间却比铁、铜晚得多,错误。
4.某同学设计了从海水中提取镁单质的四种方法,从化学原理和经济效益角度
分析,最可行的是 ( )
A.海水 Mg(OH) Mg
2
B.海水 MgCl Mg
2
C.海水 Mg(OH) MgO Mg
2
D.海水 Mg(OH) MgCl Mg
2 2
【解析】选D。海水中Mg2+的含量很低,直接蒸发得到的主要成分是NaCl,B不符
合题意;海水中加入碱可生成氢氧化镁沉淀,一般使用比较廉价的石灰乳,而不
用价格较贵的NaOH,A不符合题意;MgO熔点很高,故工业上从经济效益方面考虑,
不采用电解MgO的方法,而采用电解MgCl 的方法,C不符合题意,D符合题意。
2
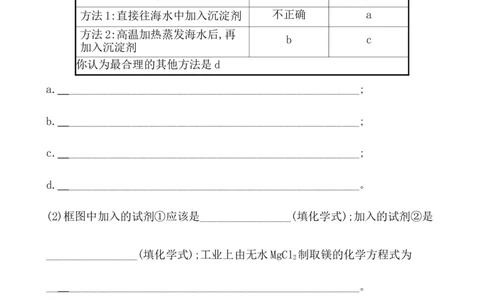
5.(教材变式题)已知海水提取镁的主要步骤如下:(1)关于加入试剂①作沉淀剂,有以下几种不同方法,请完成下列问题。
方法 是否正确 简述理由
方法1:直接往海水中加入沉淀剂 不正确 a
方法2:高温加热蒸发海水后,再
b c
加入沉淀剂
你认为最合理的其他方法是d
a. ___________________________________________________;
b. ___________________________________________________;
c. ___________________________________________________;
d. ___________________________________________________。
(2)框图中加入的试剂①应该是________________(填化学式);加入的试剂②是
________________(填化学式);工业上由无水MgCl 制取镁的化学方程式为
2
__ ___________________________________________________。
【解析】本题考查的是从海水中提取镁的流程。试剂①应是石灰乳,发生的反
应是MgCl +Ca(OH) Mg(OH) ↓+CaCl ;试剂②应是盐酸,反应是Mg(OH) +2HCl
2 2 2 2 2
MgCl +2H O,然后浓缩、结晶、脱水得无水MgCl ,再电解熔融的MgCl 便可制
2 2 2 2
得Mg:MgCl (熔融) Mg+Cl ↑。
2 2答案:(1)a.海水中镁离子浓度较小,沉淀剂用量大,不经济
b.不正确 c.能源消耗大,不经济
d.海滩晒盐后得到的苦卤中,加入沉淀剂
(2)Ca(OH) HCl
2
MgCl (熔融) Mg+Cl ↑
2 2