文档内容
课时素养评价 十三
烷烃的性质
(30分钟 50分)
一、选择题(本题包括4小题,每小题6分,共24分)
1.(2019·烟台高一检测)下列关于甲烷的叙述中不正确的是 ( )
A.甲烷是一种无色、难溶于水的气体
B.将甲烷通入酸性高锰酸钾溶液,溶液褪色
C.甲烷只有1种二氯代物,证明它是正四面体结构
D. CH 和Cl 在光照条件下能发生反应,得到多种产物
4 2
【解析】选B。常温下,甲烷是一种无色无味的气体,难溶于水, A正确;甲烷不
能与高锰酸钾溶液反应使溶液褪色, B错误;甲烷的取代产物二氯甲烷没有同分
异构体,即可说明甲烷是正四面体结构, C正确;甲烷与氯气在光照条件下发生
反应可以生成一氯甲烷、二氯甲烷、三氯甲烷、四氯甲烷四种有机产物,另外
还有HCl气体生成, D正确。
2.在标准状况下,22.4 L CH 与氯气在光照下发生取代反应,待反应完全后,测得
4
四种有机取代物的物质的量相等,则消耗的氯气为( )
A.0.5 mol B.2 mol
C.2.5 mol D.4 mol
【解析】选C。1 mol CH 与氯气发生取代反应,生成CH Cl、CH Cl 、CHCl 、
4 3 2 2 3
CCl 各0.25 mol,该四种取代物中 n(Cl)=0.25 mol×(1+2+3+4)=2.5 mol,根据
4
取代反应特点, 的氯原子进入氯化氢,所以n(HCl)=2.5 mol,故生成物中所含氯
原子共2.5 mol+2.5 mol=5 mol,参加反应的氯气为n(Cl )=2.5 mol。
2
3.液化石油气中含有丙烷,且丙烷中碳原子成键特点与CH 中碳原子相似,性质
4
相似。下列有关丙烷的叙述中不正确的是 ( )
A.分子中碳原子不在一条直线上
B.光照下能够发生取代反应
C.丙烷与甲烷不是同系物
D.丙烷不能使酸性KMnO 溶液褪色
4
【解析】选C。A项,结合CH 中碳原子成键特点知丙烷分子中碳原子不在同一
4
条直线上;B项,光照下与卤素发生取代反应是烷烃的主要性质;C项,丙烷与甲烷均为烷烃,互为同系物;D项,丙烷性质稳定,不能被酸性KMnO 溶液氧化而使其褪
4
色。
4.鉴别CH 、CO、H 三种无色气体的方法是 ( )
4 2
A.点燃——通入澄清石灰水——加入溴的四氯化碳溶液
B.点燃——罩上小烧杯——加入澄清石灰水
C.点燃——通入澄清石灰水
D.点燃——通入酸性KMnO 溶液
4
【解析】选B。根据燃烧后的产物来判断,甲烷燃烧后生成CO 和H O,氢气燃烧
2 2
后生成H O,CO燃烧后生成CO 。在燃烧的火焰上方罩一个干燥的小烧杯,出现水
2 2
雾的是甲烷和氢气,没有水雾的是CO;然后在有水雾的两个小烧杯里加入澄清石
灰水,出现浑浊的是甲烷,无现象的是H 。
2
二、非选择题(本题包括1小题,共10分)
5.甲烷是最简单的有机物。
(1)下列关于天然气的叙述中,不正确的是________(填字母)。
a.天然气和沼气的主要成分都是甲烷
b.天然气是一种清洁能源
c.天然气燃烧的废气中,SO 等污染物的含量少
2d.天然气和空气混合点燃,不会发生爆炸
(2)写出光照条件下CH 与溴蒸气反应时一个氢原子被取代的化学方程式:
4
____________。
(3)完全燃烧一定量的甲烷,其燃烧产物依次通过浓硫酸、碱石灰,使装有碱石
灰的玻璃管增加8.8 g。则原来的甲烷在标准状况下的体积为________L。
(4)CH 和H 混合气体10 mL,完全燃烧后生成6 mL CO 气体(气体的体积在相同
4 2 2
状况下测定),则混合气体中CH 和H 的体积之比为________(填字母)。
4 2
a.2∶3 b.3∶2
c.2∶1 d.1∶2
【解析】(1)天然气和沼气的主要成分都是CH ,甲烷完全燃烧生成CO 和H O,所
4 2 2
以是一种清洁能源;天然气中硫元素等含量低,所以燃烧废气中SO 等污染物的
2
含量少;天然气与空气混合点燃,如果二者比例达到某一范围就可能爆炸。
(2)类似于与氯气的取代反应。
(3)由题意可知m(CO )=8.8 g,n(CO )=0.2 mol,根据碳原子守恒知,n(CH )=0.2
2 2 4
mol,V(CH )=4.48 L。
4
(4) CH +2O CO +2H O
4 2 2 2
1 1V(CH ) 6 mL
4
V(CH )= =6 mL
4
V(H )=10 mL-6 mL=4 mL
2
故V(CH )∶V(H )=6 mL∶4 mL=3∶2。
4 2
答案:(1)d (2)CH +Br CH Br+HBr
4 2 3
(3)4.48 (4)b
【补偿训练】
一定量的甲烷在O 不足的情况下燃烧,得到CO、CO 和H O的总质量为14.4
2 2 2
g,若其中水的质量为7.2 g,则CO的质量是 ( )
A.2.8 g B.4.4 g
C.5.6 g D.在2.8 g~5.6 g之间
【解析】选A。甲烷燃烧时,当O 少量时生成CO和H O,当O 足量时生成CO 和
2 2 2 2
H O;所以在不足量的O 中燃烧生成CO、CO 和H O。由氢原子守恒知CH 的物质
2 2 2 2 4
的量为0.2 mol。设CO和CO 的质量分别为x、y。
2
则
解得x=2.8 g。一、选择题(本题包括1小题,共6分)
6.(2019·郑州高一检测)乙烷与氯气反应得到的有机产物最多有( )
A.10种 B.9种 C.8种 D.7种
【解析】选B。乙烷的一氯取代物和五氯取代物种数相同,各有1种,二氯取代
物和四氯取代物种数相同,各有2种,三氯取代物有2种,六氯取代物1种,所以
共
二、非选择题(本题包括1小题,共10分)
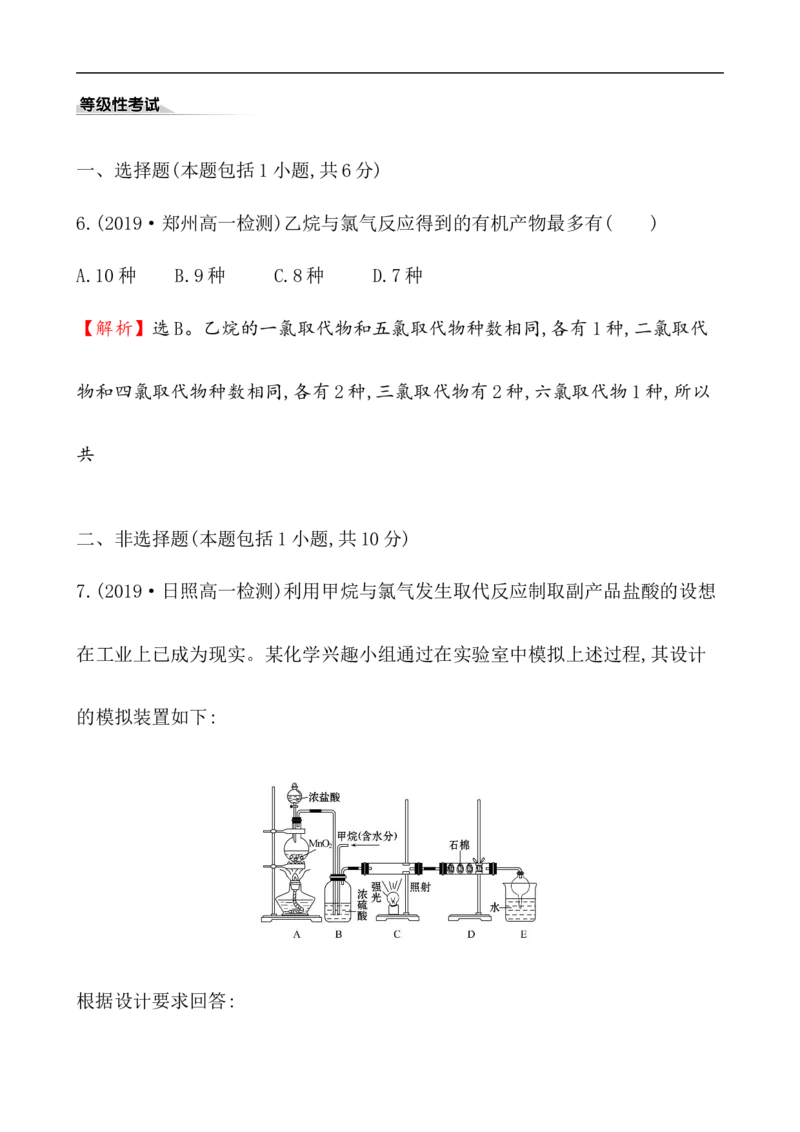
7.(2019·日照高一检测)利用甲烷与氯气发生取代反应制取副产品盐酸的设想
在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计
的模拟装置如下:
根据设计要求回答:(1)B装置有三种功能:①控制气流速度;②均匀混合气体;③______________。
(2)D装置的石棉中均匀混有KI粉末,其作用是____________________________。
(3)E装置的作用是________(填编号)。
A.收集气体 B.吸收氯气
C.防止倒吸 D.吸收氯化氢
(4)在C装置中,经过一段时间的强光照射,发现硬质
玻璃管内壁有黑色小颗粒产生,写出生成黑色小颗粒的化学方程式:_______
_______________________。
(5)E装置除生成盐酸外,还含有有机物,从E中分离出有机物的最佳方法为
______________________________________。该装置还有缺陷,原因是没有进
行尾气处理,其尾气主要成分为________(填编号)。
a.CH b.CH Cl c.CH Cl d.CHCl e.CCl
4 3 2 2 3 4
【解析】(1)B装置的三个作用为:①控制气流速度从而达到合适的反应比例;②
均匀混合气体,便于后续实验;③干燥混合气体。(2)氯气具有强氧化性,能将碘离子氧化生成碘单质,KI的作用是吸收多余的
Cl ,防止过量的氯气排入空气中污染环境,反应的化学方程式为Cl +2KI
2 2
2KCl+I 。
2
(3)E装置既吸收反应生成的HCl气体,同时还防止倒吸。
(4)据信息可知生成的黑色小颗粒为炭黑,说明在强光照射下可发生反应,根据
原子守恒应为CH +2Cl C+4HCl。
4 2
(5)最后从D中分离出的气体有HCl易溶于水,可用分液的方法分离,分离难溶于
水的油状液体可用分液法。
答案:(1)干燥混合气体 (2)吸收过量的氯气 (3)C、D
(4)CH +2Cl C+4HCl (5)分液 a、b
4 2