文档内容
第一章 物质及其变化
第三节 氧化还原反应
第3课时 氧化还原反应的应用
(1)能利用氧化还原反应概念判断物质的氧化性和还原性
(2)氧化还原反应基本规律的应用
【内容分析】
本节内容主要分为两部分:氧化还原反应,氧化剂和还原剂。
本节内容的特点是概念多、抽象,理论性强,所以安排了3个课时进行学习。第一课时建议学习氧化还
原反应的基本特征和本质,概括氧化还原反应和四大基本反应类型的关系。第二课时建议学习氧化还原反
应中电转移的表示方法以及氧化剂、还原剂、氧化产物及还原产物等基本概念,构建氧化还原反应基本概
念间关系的模型。
本节课在氧化还原反应基本概念和原理学习的基础上,进一步深入学习氧化还原反应基本规律的应用,
整节课以“电子得失守恒律”“价态律”为指导思想,从宏观角度——利用元素化合价对物质氧化性和还
原性进行判断,再到实验的角度探究物质的氧化性和还原性,并对物质氧化性和还原性强弱的比较。此外,
利用化合价升降数目相等对氧化还原反应方程式进行配平。
【教学重点和难点】
重点:物质的氧化性和还原性。
难点:利用价态律配平氧化还原方程式
【教学流程】【练习回顾】
1、判断下列反应中的氧化剂,还原剂?
1. H O高+C温==H +CO
2 2
△
2. 2KClO ==2KCl+3O ↑
3 2
3. I2+SO2+2H2O===H2SO4+2HI
4. 2FeCl +2HI===2FeCl +I+2HCl
3 2 2
2、用双向桥法表示下列反应中电子转移方向和数目.
KClO + 6HCl = KCl+3Cl ↑ + 3H O
3 2 2
HS + H SO (浓)= S ↓+ SO ↑ + 2H O
2 2 4 2 2
【设计意图】通过练习复习上一节课学习的氧化还原反应的基本概念和电子转移的表示方法,并对同种元
素的不同价态间发生氧化还原反应时,高价态和低价态变成它们相邻的中间价态的反应规律(只靠拢不交
叉的规律)进行拓展,学生在分析这类特殊反应的电子转移情况时容易出错。
【学习任务一】 物质氧化性和还原性
【引入】
展示一些常见氧化剂在生活中的用途图片,
【问题】生活中常用ClO 、KMnO 、O、HO 物质能杀菌消毒,利用它们的什么性质?
2 4 3 2 2
【设计意图】导入新课——物质的氧化性和还原性
1、概念
氧化性:物质得电子性质,氧化剂具有氧化性。
还原性:物质失电子性质,还原剂具有还原性。
【概念辨析】物质得失电子数目越多,物质的氧化性、还原性就越强?
物质氧化性或还原性的强弱取决于其得失电子的难易程度,与得失电子的多少无关。物质得电子越容易氧
化性越强;失电子越容易还原性越强。
2、物质氧化性、还原性的判断
【宏观辨识】根据元素化合价判断——“价态律”元素处于高价态具有氧化性,最高价态,则只具有氧化性
元素处于低价态具有还原性,最低价态,则只具有还原性
元素处于中间价态,则既有氧化性又有还原性
【练习】考点:根据元素化合价物质是否具有氧化性、还原性
【设计意图】化合价升降是氧化还原反应的重要特征,引导学生从化合价的角度分析物质的氧化性和还原
性是基于宏观辨识的核心素养。
【科学探究】
【实验探究1】生活中常用到双氧水(HO 溶液)杀菌消毒,是利用了过氧化氢的强氧化性,请你设计实
2 2
验方案证明过氧化氢具有氧化性吗?(可选择的实验试剂:HO 溶液、酸性KMnO 溶液,稀硫酸,NaOH
2 2 4
溶液,淀粉KI溶液。)
【实验探究2】从价态上分析,过氧化氢中氧元素处于中间价态,除了体现出氧化性,还能体现出一定的
还原性,请你设计实验方案证明过氧化氢具有还原性?(HO 溶液、酸性KMnO 溶液,氢硫酸(HS溶
2 2 4 2
液),盐酸,NaOH溶液,淀粉KI溶液)
【学生活动】设计实验方案并进行相关实验,观察实验现象,得出结论。
【设计意图】依据化合价预测物质的氧化性和还原性,设计实验进行初步验证,并能分析、解释有关现象。
落实学生科学探究与创新意识的核心素养。
【学习评价】练习1、2
3、物质氧化性与还原性的强弱比较
(1) 根据反应方程式来比较:氧化剂 + 还原剂 = 还原产物 +氧化产物
【理论分析】在氧化还原反应中:氧化剂具有较强的氧化性,还原剂具有较强的还原性;氧化产物具有较
弱的氧化性,还原产物具有较弱的还原性。
氧化性:氧化剂>还原剂;还原性:还原剂>还原产物
【设计意图】利用氧化还原反应概念比较物质的氧化性和还原性。
【科学探究】
【实验探究3】已知Cu2+、Fe2+具有一定的氧化性,你能设计实验方案并进行相关实验比较两者的氧化性强
弱吗?
【实验设计依据】氧化剂 + 还原剂 = 还原产物 +氧化产物
【学生活动】设计实验方案并进行实验探究,根据现象得出结论
【设计意图】基于理论分析的基础上,从实验的角度进行探究,落实学生科学探究与创新意识的核心素养。
(2)根据金属活动顺序:
K Ca Na Mg Al Zn Fe Sn Pb(H) Cu Hg Ag Pt Au金属性逐渐减弱,还原性逐渐减弱。
K+ Ca2+ Na+ Mg2+ Al3+ Zn2+ Fe2+ Sn2+ Pb2+(H+) Cu2+ Fe3+ Hg2+ Ag+
金属性逐渐减弱,对应的阳离子氧化性逐渐增强。
氧化性:F > Cl > O > Br > I > S
2 2 2 2 2
非金属性逐渐减弱,氧化性逐渐减弱。
还原性:F- < Cl- < O2- < Br- < I- < S2-
非金属性逐渐减弱,对应的阴离子还原性逐渐增强。
【学习评价】练习3、4
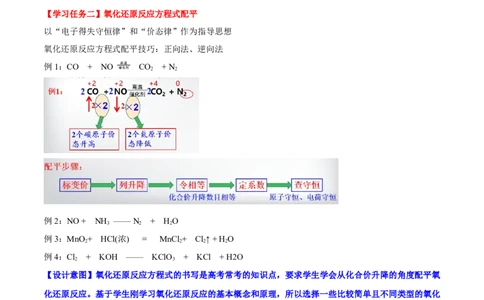
【学习任务二】氧化还原反应方程式配平
以“电子得失守恒律”和“价态律”作为指导思想
氧化还原反应方程式配平技巧:正向法、逆向法
例1:CO + NO 高温 CO + N
催化剂 2 2
例2:NO + NH —— N + H O
3 2 2
例3:MnO + HCl(浓) = MnCl + Cl ↑ + H O
2 2 2 2
例4:Cl + KOH —— KClO + KCl + H2O
2 3
【设计意图】氧化还原反应方程式的书写是高考常考的知识点,要求学生学会从化合价升降的角度配平氧
化还原反应。基于学生刚学习氧化还原反应的基本概念和原理,所以选择一些比较简单且不同类型的氧化
还原反应作为例题,避免加重学生的学习负担,但又要帮助学生掌握好氧化还原反应配平技巧。
【学习评价】练习5【生活情景素材】
生活中常用ClO 、KMnO 、O、HO 物质能杀菌消毒,利用它们的什么性质?
2 4 3 2 2
【使用建议】导入新课——物质氧化性、还原性的学习。
【实验素材】
【实验探究1】生活中常用到双氧水(HO 溶液)杀菌消毒,是利用了过氧化氢的强氧化性,请你设计实
2 2
验方案证明过氧化氢具有氧化性吗?(可选择的实验试剂:HO 溶液、酸性KMnO 溶液,稀硫酸,NaOH
2 2 4
溶液,淀粉KI溶液。)
【实验探究2】从价态上分析,过氧化氢中氧元素处于中间价态,除了体现出氧化性,还能体现出一定的
还原性,请你设计实验方案证明过氧化氢具有还原性?(可选择的实验试剂:HO 溶液、酸性KMnO 溶
2 2 4
液,盐酸,NaOH溶液,淀粉KI溶液。)
【实验探究3】已知Cu2+、Fe2+具有一定的氧化性,你能设计实验方案并进行相关实验比较两者的氧化性强
弱吗?(可选择的实验试剂:Cu片,铁屑,CuSO 溶液、FeSO 溶液,FeCl 溶液,NaOH溶液。)
4 4 3
【使用建议】实验1和实验2用于探究物质的氧化性和还原性,实验3目的是探究物质氧化性、还原性强
弱,通过实验方案的设计和实验活动的开展,可以增强小组合作实验探究、讨论交流等多样化方式解决问
题的能力。
【练习素材】
1、人体正常的血红蛋白中应含有Fe2+。若误食亚硝酸钠,则导致血红蛋白中Fe2+转化为高铁血红蛋白而中
毒。服用维生素C可解除亚硝酸钠中毒。下列叙述中正确的是( )A、亚硝酸钠表现还原性
B、维生素C表现了还原性
C、亚硝酸钠被氧化
D、维生素C作为氧化剂
【答案】B
【解析】血红蛋白中含有的Fe2+有和亚硝酸钠反应转化为高铁血红蛋白,Fe2+化合价升高,作为还原剂,具
有还原性,被氧化;亚硝酸钠体现氧化性,被还原。维生素 C可解除亚硝酸钠中毒,原理是将高铁血红蛋
白中的铁元素还原为Fe2+,维生素C具有还原性。
2.关于物质氧化性及还原性的强弱,下列说法中正确的是( )
A.物质越易失电子,还原性越强
B.原子失电子越多,还原性越强
C.元素化合价降低越多,氧化性越强
D.物质越易被氧化,氧化性越强
【答案】A
【解析】还原性强弱与电子转移数目、化合价升降的多少无关,与失电子能力有关,越易失电子,还原性
越强。
3、根据下列反应判断HSO 、 I- 、 Fe2+ 、 NO的还原性由强到弱的顺序是_____________ 。
2 3
HSO + I + H O = 2HI + H SO
2 3 2 2 2 4
2FeCl + 2HI = 2FeCl + 2HCl + I
3 2 2
3FeCl + 4HNO = 2FeCl + NO↑ + 2H O + Fe(NO )
2 3 3 2 3 3
【答案】HSO > I- > Fe2+ > NO
2 3
【点拨】标化合价,明确变价元素,找出还原剂和还原产物,比较还原性
【使用建议】评价:物质氧化性、还原性的判断
4、已知三个氧化还原反应:①2FeCl +2KI=2FeCl +2KCl+I,②2FeCl +Cl=2FeCl ,
3 2 2 2 2 3
③2KMnO +16HCl(浓)= 2KCl+2MnCl +8HO+5Cl↑。若某溶液中有Fe2+、I-、Cl-共存,要将I-氧化
4 2 2 2
除去而不氧化Fe2+和Cl-,则可加入的试剂是( )
A.Cl B.KMnO C.FeCl D.HCl
2 4 3
【答案】C;
【解析】由信息可知,氧化性由强至弱的顺序为:MnO ->Cl>Fe3+>I,还原性由强至弱的顺序为I->
4 2 2
Fe2+>Cl->Mn2+;
A.氯气能将Fe2+、I-均氧化,故A错误;B.KMnO 能将Fe2+、I-和Cl-均氧化,故B错误;
4
C.FeCl 能氧化除去I-而不影响Fe2+和Cl-,故C正确;
3
D.HCl与三种离子均不反应,故D错误;
【使用建议】评价:物质氧化性、还原性的强弱比较
5、练习:根据化合价升降数目相等配平下列方程式
(1)Fe (SO )+ H O+ SO ——FeSO +H SO
2 4 3 2 2 4 2 4
(2)KMnO +HCl(浓)——KCl+MnCl +Cl↑+HO
4 2 2 2
【答案】(1)Fe (SO )+SO +2HO==2FeSO +2HSO
2 4 3 2 2 4 2 4
(2)2KMnO +16HCl(浓)==2KCl+2MnCl +5Cl↑+8HO
4 2 2 2
【使用建议】评价:氧化还原方程式的配平
附课本习题答案:p25-26
均属于氧化还原反应。
2.氧化 还原
3. Al Fe O
2 3
4.①②③
提示:钟乳石的生成只涉及复分解反应,而所有复分解反应均属于非氧化还原反应。
5.③ ④ ①②
提示:置换反应中既有单质变成化合物,又有化合物变成单质,元素化合价必然发生变化。
6. C
7. C B
提示:HCI中,+1价氢元素具有氧化性,如能氧化活泼金属,本身变为0价(氢气);-1价氯元素具有还
原性,如可以还原二氧化锰,而本身变为0价(氯气)。因此,HCl既有氧化性又有还原性。
8. C
9. D
提示:在NaH中,氢元素的化合价为-1价。10.
11.(1)氧化剂(2)还原剂(3)既是氧化剂,又是还原剂
12.
氧化剂:CIO- 还原剂: Fe3+
13.
年份 代表人物 主要观点
1774年 【法】拉瓦锡 物质与氧结合的反应叫做氧化反应;氧化物失去氧的反
应叫做还原反应。
1852年 【英】弗兰克兰 化合价升高的反应叫做氧化反应;化合价降低的反应叫
做还原反应。
1897年 【英】汤姆孙 原子失去电子(或电子对偏离)的过程叫做氧化;原子得到电子(或电子对偏向)的过程叫做还原。
启示示例:科学概念往往有一定的适用范围,人们对科学概念的认识有一个逐步完善、发展的过程。