文档内容
第 21 讲 难溶电解质的沉淀溶解平衡
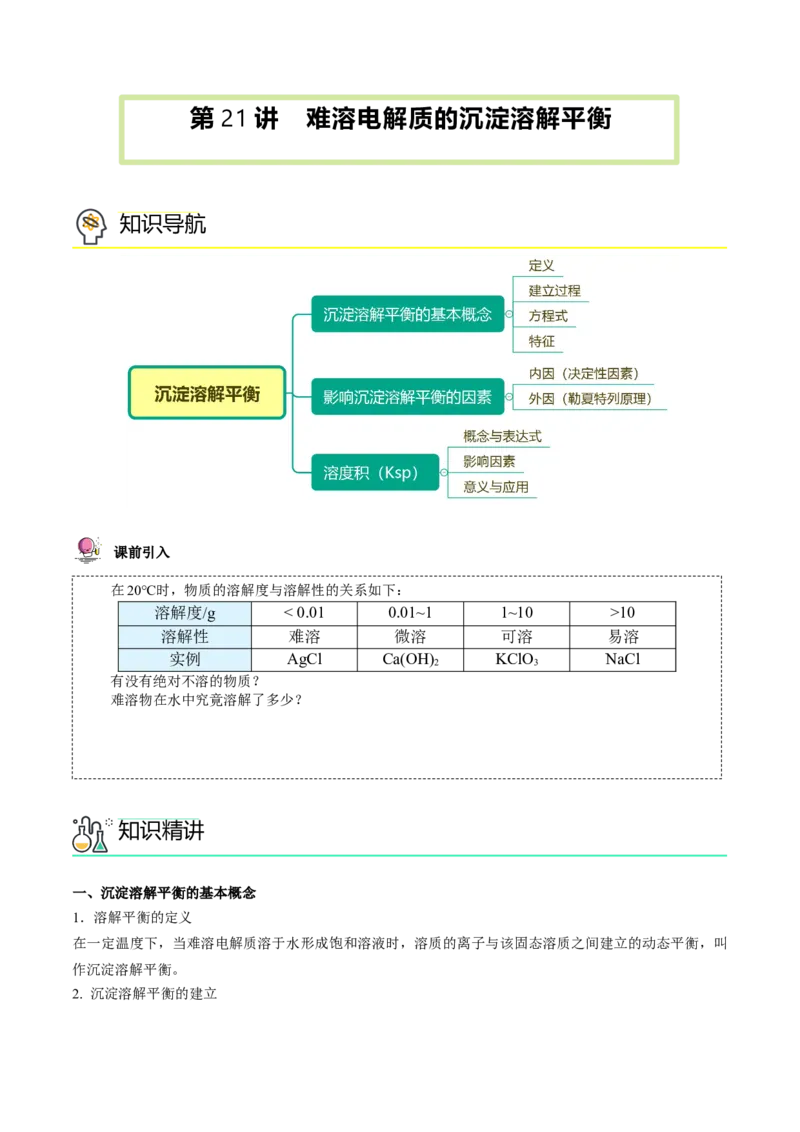
知识导航
小杨老师 15521324728 侵权必究
课前引入
在20℃时,物质的溶解度与溶解性的关系如下:
杨sir化学,侵权必究
溶解度/g < 0.01 0.01~1 1~10 >10
溶解性 难溶 微溶 可溶 易溶
实例 AgCl Ca(OH) KClO NaCl
2 3
有没有绝对不溶的物质?
难溶物在水中究竟溶解了多少?
知识精讲
小杨老师 15521324728 侵权必究
一、沉淀溶解平衡的基本概念
1.溶解平衡的定义
杨sir化学,侵权必究
在一定温度下,当难溶电解质溶于水形成饱和溶液时,溶质的离子与该固态溶质之间建立的动态平衡,叫
作沉淀溶解平衡。
2. 沉淀溶解平衡的建立3. 沉淀溶解平衡方程式
M A(s) mMn+(aq) + nAm-(aq)
m n
如AgCl沉淀溶解平衡:AgCl(s) Ag+(aq) + Cl-(aq)
4. 沉淀溶解平衡的特征
二、影响沉淀溶解平衡的因素
1.内因(决定性因素):难溶电解质本身的性质。
杨sir化学,侵权必究
2.外因:温度、浓度、同离子效应等,其影响符合“勒夏特列原理”。
①温度:一般来说,温度越高,固体物质的溶解度越大。极少数固体物质的溶解度随温度的升高而减小,
如Ca(OH) 。
2
②同离子效应:加入与电解质电离的离子相同的可溶性盐,平衡向生成沉淀的方向移动,溶解度减小。
③外加其他物质(与电解质电离的离子反应),平衡向沉淀溶解的方向移动,溶解度增大。
三、溶度积(K )
sp
1. 概念与表达式
① 在一定温度下,沉淀溶解平衡的平衡常数称为溶度积常数,简称溶度积,用K 表式。
sp
② 对于沉淀溶解平衡:M A(s) ⇌ mMn+(aq) + nAm-(aq),K = cm(Mn+)·cn(Am-)。
m n sp
如Fe(OH) (s) ⇌ Fe3+ (aq) + 3OH- (aq) K = c(Fe3+)·c3(OH-)
3 sp
2.影响因素
① 溶度积K 值的大小只与难溶电解质本身的性质和温度有关。
sp
② 溶解平衡一般是吸热的,温度升高,平衡正移,K 增大,但Ca(OH) 相反。
sp 2
3. 意义
对于相同类型的难溶电解质,K 越大,说明难溶电解质在水中的溶解能力越大。
sp如:K (AgCl) > K (AgBr) > K (AgI),则溶解度:S (AgCl) > S (AgBr) > S (AgI)。
sp sp sp
4.应用
① M A(s) ⇌ mMn+(aq) + nAm-(aq),任意时刻的离子积:Q = cm(Mn+)·cn(Am-)
m n
② 根据K 和Q的相对大小,可以判断给定条件下溶液中难溶电解质的沉淀或溶解情况:
sp
Q > K ,溶液中有沉淀析出
sp 杨sir化学,侵权必究
Q = K ,沉淀与溶解处于平衡状态
sp
Q < K ,溶液中无沉淀析出
sp
对点训练
小杨老师 15521324728 侵权必究
题型一:沉淀溶解平衡的理解
杨sir化学,侵权必究
【变1-1】对“AgCl(s) Ag+(aq)+Cl-(aq)”的理解正确的是
①说明AgCl没有完全电离,AgCl是弱电解质
②说明溶解的AgCl已完全电离,是强电解质
③说明Cl-与Ag+的反应不能完全进行到底
④说明Cl-与Ag+的反应可以完全进行到底
A.③④ B.②③ C.①③ D.②④
【答案】B
【详解】
氯化银在水溶液中存在沉淀溶解平衡:AgCl(s)⇌Ag+(aq)+Cl-(aq),其完整过程为AgCl(s)⇌AgCl(aq)=Ag+(aq)
+Cl-(aq),说明AgCl完全电离,是强电解质,故①错误,②正确;由于存在沉淀溶解平衡,说明Ag+与Cl-
的反应不能完全进行到底,故③正确,④错误;所以只有②③正确;B正确;
综上所述,本题选B。
题型二:沉淀溶解平衡的移动
杨sir化学,侵权必究
【变2-2】将AgCl分别加入盛有:①5mL水②6mL0.5 溶液③10mL0.2 溶液
④5mL0.1 盐酸的烧杯中,均有固体剩余,各溶液中 从大到小的顺序排列正确的是
A.①④③② B.②③④① C.④③②① D.①③②④
杨sir化学,侵权必究
【答案】A
【分析】
在AgCl饱和溶液中存在沉淀溶解平衡:AgCl(s)⇌Ag+(aq)+Cl‒(aq),加入Cl‒平衡逆向移动c(Ag+)会减小,加
入Cl‒的浓度越大,c(Ag+)越小,即c(Ag+)与c(Cl‒)大小顺序相反,据此分析。
【详解】
①水中没有Cl‒,即5mL水对AgCl的沉淀溶解平衡没有抑制作用,①中c(Ag+)最大;②6mL0.5mol/LNaCl溶液中含有Cl‒,且c(Cl‒)=0.5mol/L,对AgCl的沉淀溶解平衡有抑制作用,则②中
c(Ag+)小于①中c(Ag+);
③10mL0.2mol/LCaCl 溶液中含有Cl‒,c(Cl‒)=0.2mol/L×2=0.4mol/L,对AgCl的沉淀溶解平衡有抑制作用,
2
则②中c(Ag+)小于③中c(Ag+);
④5mL0.1mol/L盐酸中含有Cl‒,且c(Cl‒)=0.1mol/L,对AgCl的沉淀溶解平衡有抑制作用,则④中c(Ag+)
大于③中c(Ag+);
综上所述,各溶液中c(Ag+)从大到小的顺序为①④③②,A项正确。
答案选A。
题型三:溶度积K
sp杨sir化学,侵权必究
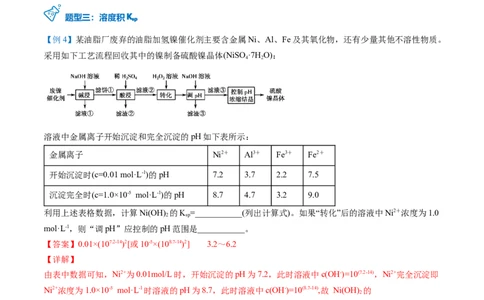
【例4】某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。
采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO ·7H O):
4 2
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Ni2+ Al3+ Fe3+ Fe2+
开始沉淀时(c=0.01 mol·L-1)的pH 7.2 3.7 2.2 7.5
沉淀完全时(c=1.0×10-5 mol·L-1)的pH 8.7 4.7 3.2 9.0
利用上述表格数据,计算Ni(OH) 的K =___________(列出计算式)。如果“转化”后的溶液中Ni2+浓度为1.0
2 sp
mol·L-1,则“调pH”应控制的pH范围是___________。
【答案】0.01×(107.2-14)2[或10-5×(108.7-14)2] 3.2~6.2
【详解】
由表中数据可知,Ni2+为0.01mol/L时,开始沉淀的pH为7.2,此时溶液中c(OH-)=10(7.2-14),Ni2+完全沉淀即
Ni2+浓度为1.0×10-5 mol·L-1时溶液的pH为8.7,此时溶液中c(OH-)=10(8.7-14),故 Ni(OH) 的
2
K =c(Ni2+)c2(OH-)=0.01×[10(7.2-14)]2[或10-5×[10(8.7-14)]2],如果“转化”后的溶液中Ni2+浓度为1.0 mol·L-1,此
sp
时溶液的中OH-浓度为:c(OH-)= = =10-7.8mol/L,故c(H+)=10(7.8-14)=10-
6.2mol/L,即此时pH=6.2,故则“调pH”应控制pH的作用应该是Fe3+完全沉淀,而Ni2+未开始沉淀,故
pH范围是3.2~6.2,故答案为:0.01×[10(7.2-14)]2[或10-5×[10(8.7-14)]2];3.2~6.2。
【变4】已知下列物质在20 ℃时的K 见下表,试回答下列问题:
sp
化学式 AgCl AgBr AgI Ag S Ag CrO
2 2 4颜色 白色 浅黄色 黄色 黑色 砖红色
K 2.0×10-10 5.4×10-13 8.3×10-17 2.0×10-48 2.0×10-12
sp
(1)20 ℃时,上述五种银盐饱和溶液中,Ag+物质的量浓度由大到小的顺序是___________。
(2)向BaCl 溶液中加入AgNO 和KBr,当两种沉淀共存时, =___________。
2 3
(3)测定水体中氯化物的含量,常用标准硝酸银法进行滴定,滴定时,应加入的指示剂是___________(填
字母)。
A.KBr B.KI
C.KS D.KCrO
2 2 4
【答案】
(1)Ag CrO>AgCl>AgBr>AgI>Ag S
2 4 2
(2)2.7×10-3
(3)D
【解析】
(1)
AgCl饱和溶液中,Ag+物质的量浓度 ;AgBr饱和溶液中,Ag+物质的量浓度
;AgI饱和溶液中,Ag+物质的量浓度 ;
Ag S饱和溶液中,Ag+物质的量浓度 ;
2
Ag CrO 饱和溶液中,Ag+物质的量浓度 ;则Ag+物质的量浓度由大到小
2 4
的顺序是Ag CrO>AgCl>AgBr>AgI>Ag S。
2 4 2
(2)
向BaCl 溶液中加入AgNO 和KBr,当两种沉淀共存时,
2 3
。
(3)
测定水体中氯化物的含量,常用标准硝酸银法进行滴定,滴定至终点时,溶液是AgCl的饱和溶液,为了
明显判断最后一滴过量的硝酸银,加入的指示剂应符合现象明显、生成物饱和溶液的Ag+物质的量浓度比
AgCl更大的要求,故答案选D。
【点睛】不同类型的K 不能直接比较数值大小而判断其饱和溶液离子浓度大小。
sp
题型四:沉淀溶解平衡图像
杨sir化学,侵权必究
【例5】不同温度(T 和T)时,硫酸钡在水中的沉淀溶解平衡曲线如图所示,已知硫酸钡在水中溶解时吸
1 2
收热量。下列说法正确的是
A.T>T
1 2
B.加入BaCl 固体,可使溶液由a点变到c点
2
C.c点时,在T、T 两个温度下均没有固体析出
1 2
D.图中c点对应的是T 时硫酸钡的过饱和溶液
1
【答案】D
【详解】
A.硫酸钡在水中溶解时吸收热量,升高温度,BaSO 的溶度积常数增大。根据图象可知温度:T>T,A
4 2 1
错误;
B.硫酸钡在溶液中存在着溶解平衡,a点在平衡曲线上,加入BaCl 固体,会增大c(Ba2+),沉淀溶解平衡
2
逆向移动,导致溶液中c( )降低,所以不能使溶液由a点变到c点,B错误;
C.在T 时c点表示Q>Ksp,溶液为过饱和溶液,有沉淀析出;在T 时c点表示Q<Ksp,溶液不饱和,
1 c 2 c
没有沉淀析出,C错误;
D.根据图象可知:在T 时c点表示Q>Ksp,所以此时的溶液为过饱和溶液,D正确;
1 c
故合理选项是D。
【变6-1】已知:常温下, 。某温度下,饱和溶液中 与 、
的关系如图所示。下列说法正确的是
A.曲线Ⅱ代表 的沉淀溶解平衡曲线
B.常温下, 的
C.常温下,当 时,饱和溶液中
D.加入 固体可使溶液由 点沿直线变为 点
杨sir化学,侵权必究
【答案】BC
【详解】
A.离子浓度的负对数值越大,对应的离子浓度越小,对应的溶度积越小,故曲线Ⅱ代表溴化银的沉淀溶解
平衡曲线,选项A错误;
B.常温下,当 时, ,此时, ,
选项B正确;
C.常温下,当 时, =4.0,饱和溶液中 ,选项C
正确;
D.加入 固体后,饱和溶液中 增大, 减小,可使溶液由 点变为 点,选项D
错误。
答案选BC。
提分特训
小杨老师 15521324728 侵权必究
【题1】常温下,将足量CaCO 加入下列各体系中,溶解度最大的是
3
A.10 mL水 B.10 mL 0.1 mol/L CaCl 溶液
2C.20 mL 0.1 mol/L NaHSO 溶液 D.40 mL 0.1 mol/L Na CO 溶液
4 2 3
【答案】C
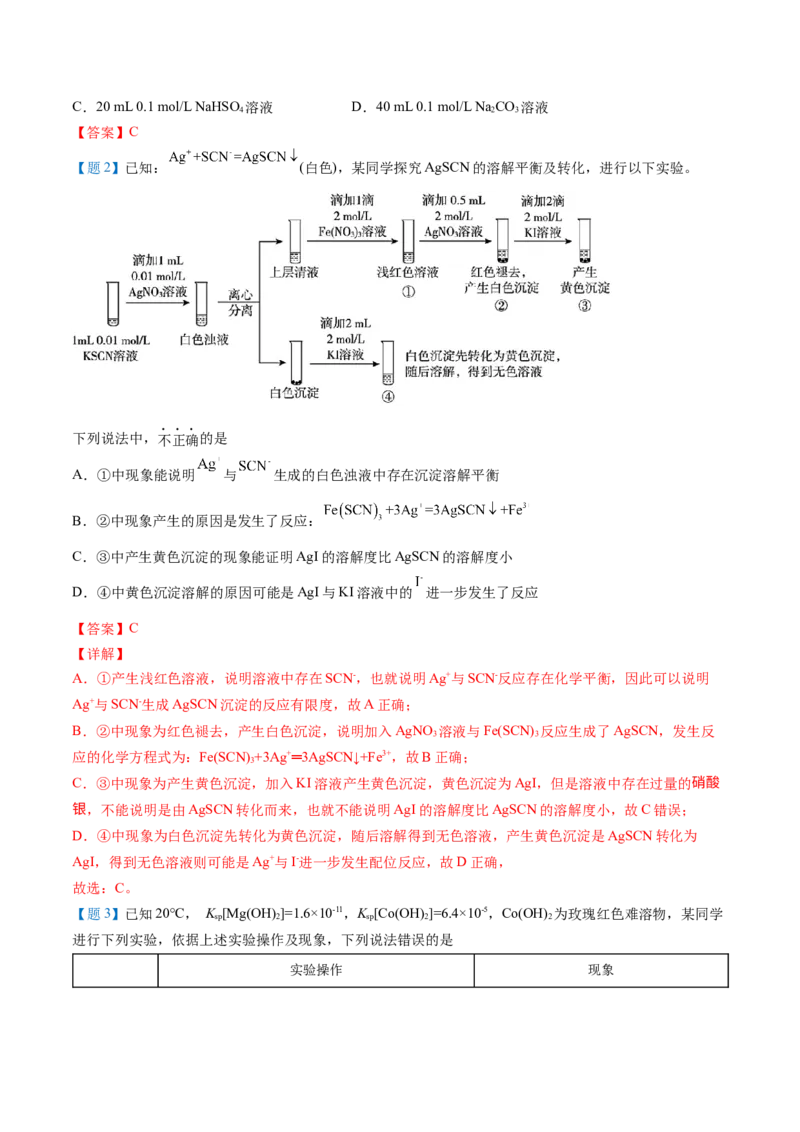
【题2】已知: (白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
下列说法中,不正确的是
A.①中现象能说明 与 生成的白色浊液中存在沉淀溶解平衡
B.②中现象产生的原因是发生了反应:
杨sir化学,侵权必究
C.③中产生黄色沉淀的现象能证明AgI的溶解度比AgSCN的溶解度小
D.④中黄色沉淀溶解的原因可能是AgI与KI溶液中的 进一步发生了反应
【答案】C
【详解】
A.①产生浅红色溶液,说明溶液中存在SCN-,也就说明Ag+与SCN-反应存在化学平衡,因此可以说明
Ag+与SCN-生成AgSCN沉淀的反应有限度,故A正确;
B.②中现象为红色褪去,产生白色沉淀,说明加入AgNO 溶液与Fe(SCN) 反应生成了AgSCN,发生反
3 3
应的化学方程式为:Fe(SCN) +3Ag+═3AgSCN↓+Fe3+,故B正确;
3
C.③中现象为产生黄色沉淀,加入KI溶液产生黄色沉淀,黄色沉淀为AgI,但是溶液中存在过量的硝酸
银,不能说明是由AgSCN转化而来,也就不能说明AgI的溶解度比AgSCN的溶解度小,故C错误;
D.④中现象为白色沉淀先转化为黄色沉淀,随后溶解得到无色溶液,产生黄色沉淀是AgSCN转化为
AgI,得到无色溶液则可能是Ag+与I-进一步发生配位反应,故D正确,
故选:C。
【题3】已知20℃, K [Mg(OH) ]=1.6×10-11,K [Co(OH) ]=6.4×10-5,Co(OH) 为玫瑰红色难溶物,某同学
sp 2 sp 2 2
进行下列实验,依据上述实验操作及现象,下列说法错误的是
实验操作 现象将镁条用砂纸打磨光亮后置于饱和氯化钠溶液中, 有无色气体和较多白色沉淀产生,溶液
实验一
滴加几滴酚酞 变红色
实验二 取出镁条,将悬浊液加热 红色加深
实验三 冷却至20℃后滴加适量CoCl 溶液 部分白色难溶物变成玫瑰红色难溶物
2
A.镁条和水发生置换反应生成H 和 Mg(OH)
2 2
B.由题干信息可知20℃时,饱和 Mg(OH) 溶液中,c(OH-)= mol/L,因此实验一中溶
2
液可变为红色
C.Mg(OH)(s) Mg2+(aq)+2OH-(aq) H>0
D.加入适量 CoCl 溶液后,c(Mg2+):c△(Co2+)=2500:1
2
【答案】B
【详解】
A. 由实验一的现象可知,镁条和水发生置换反应生成H 和 Mg(OH) ,故A正确;
2 2
B. 已知20℃,K [Mg(OH) ]=1.6×10-11,设饱和 Mg(OH) 溶液中,c(OH-)=2x mol/L,c(Mg2+)=x mol/L,则
sp 2 2
K [Mg(OH) ]= c(Mg2+)×c2(OH-)=4x3=1.6×10-11,则20℃时,饱和 Mg(OH) 溶液中,c(OH-)=
sp 2 2
mol/L,故B错误;
C. 由实验二可知,将悬浊液加热,红色加深,说明Mg(OH)(s)在水中的溶解过程是吸热的,故Mg(OH)
(s) Mg2+(aa)+2OH-(aq) H>0,故C正确;
△
D. 加入适量 CoCl 溶液后,发生反应Co2+(aq)+Mg(OH)(s) Mg2+(aq)+ Co(OH)(s),c(Mg2+):c(Co2+)=
2
c(Mg2+) c2(OH-):c(Co2+) c2(OH-)= K [Mg(OH) ]:K [Co(OH) ]=2500:1,故D正确;
sp 2 sp 2
故选B。
【题4】已知25℃时,HCrO 的 K =3.2×10-7,BaCO 的K=2.5×10-9,BaCrO 在水中的沉淀溶解平衡曲线
2 4 a2 3 4
如图所示。下列说法正确的是
A.向m点的悬浊液中通入HCl,能使m点沿mp线向p点方向移动
B.通过蒸发可使q点溶液向p点移动C.25℃时:BaCrO(s)+ (aq) BaCO (s)+ (aq)的K=6.4×10-2
4 3
D.n点时,沉淀溶解的速率大于沉淀生成的速率
杨sir化学,侵权必究
【答案】C
【分析】
BaCrO 在水中的沉淀溶解平衡BaCrO(s) Ba2+(aq)+ (aq),根据图像,m、p为平衡点,n、q不在
4 4
平衡曲线上,其中n点在曲线上方,有c(Ba2+) c( )>K ,q点在曲线下方,有c(Ba2+) c( )<K ,
sp sp
结合溶解平衡的影响因素分析解答。
【详解】
A.m为平衡点,BaCrO(s) Ba2+(aq)+ (aq),向m点的悬浊液中通入HCl,HCrO 的K =3.2×10-
4 2 4 a2
7,存在 +H+ ,使得 浓度减小,平衡正向移动,c(Ba2+)增大,能使m点沿曲线向m点
左上方移动,选项A错误;
B.q点在曲线下方,有c(Ba2+) c( )<K ,蒸发后,c(Ba2+)和 c( )均增大,可使q点溶液向p点
sp
右下方移动,选项B错误;
C.常温下,BaCrO(s)+ (aq) BaCO (s)+ (aq)的K= = = =
4 3
=6.4×10-2,选项C正确;
D.n点在曲线上方,有c(Ba2+) c( )>K ,沉淀溶解的速率小于沉淀生成的速率,选项D错误;
sp
答案选C。
【题5】已知:pCu=-lg c(Cu+),pX=-lg c(X-),式中X-表示卤素阴离子。298 K时,
K (CuCl)≈1.0×10-6,K (CuBr)≈1.0×10-9,K (CuI)≈1.0×10-12。298 K时,CuCl、CuBr、CuI的饱和溶液中
sp sp sp
pCu和pX的关系如图所示。下列说法正确的是A.298 K时,向CuCl饱和溶液中加入少量NaCl固体,c(Cu+)和c(Cl-)都减小
B.图像中曲线X代表CuI 且a=3
C.298 K时,在曲线Y对应的饱和溶液中,增大阴离子浓度曲线Y向曲线Z移动
D.298 K时,反应CuBr(s)+I-(aq) CuI(s)+Br-(aq)的平衡常数K=1000
【答案】D
【分析】
由题目信息,CuCl 的溶解平衡中c(Cl-)=c(Cu+)= =10-3mol/L,pCu=-1gc(Cu+)=3,同理CuBr
的溶解平衡中c(Br-)=c(Cu+)= =10-4.5mol/L,pCu=-1gc(Cu+)=4.5,pBr=-lgc(Br-)=4.5,CuI的
溶解平衡中c(I-)=c(Cu+)= =10-6mol/L,pCu=-1gc(Cu+)=6,pI=-lgc(I-)=6,即曲线x代表
CuCl,则y代表CuBr,z代表CuI,以此解答。
【详解】
A.298 K时,向CuCl饱和溶液中加入少量NaCl固体,沉淀溶解平衡逆向移动,c(Cu+)减小,但c(Cl-)增
大,故A错误;
B.由分析可知,X代表CuCl,Y代表CuBr,Z代表CuI,a=6,故B错误;
C.298K时,在曲线Y对应的饱和溶液中,增大阴离子浓度,温度不变,K (CuBr)不变,则c(Cu+)减小,
sp
pCu=-1gc(Cu+)增大,即y上的点向点(4.5,4.5)的斜下方移动,故C错误;
D.298K时CuBr(s)+I-(aq) CuI(s)+Br-(aq)的平衡常数K= = = ,故D正确;
故选D。
【题6】Ⅰ.我国《生活饮用水卫生标准》中规定生活用水中锅的排放量不超过0.005mg/L。处理含镉废水
可采用化学沉淀法。试回答下列问题:
(1)磷酸镉[Cd (PO )]沉淀溶解平衡常数的表达式为Ksp=___________。
3 4 2
(2)一定温度下, 的 , 的 ,那么它们在水中的溶解量
___________较大。
杨sir化学,侵权必究
(3)向某含镉废水中加入 ,当 浓度达到 时,废水中 的浓度为
___________mol/L[已知: , ],此时是否符合生活饮用水卫生标准?
___________(填“是”或“否”)。
Ⅱ.根据题目提供的溶度积数据进行计算并回答下列问题:
(4)已知25℃时, ;酸碱指示剂百里酚蓝变色的pH范围如下:8.0~96
颜色 黄色 绿色 蓝色
25℃时,向 饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为___________。
(5)25℃向 的 溶液中加入 的盐酸,生成沉淀。已知该温度下,
AgCl的 ,忽略溶液的体积变化,请计算:
杨sir化学,侵权必究
①完全沉淀后,溶液中 =___________,
②完全沉淀后,溶液的pH=___________。
③如果向完全沉淀后的溶液中继续加入 的盐酸,是否有白色沉淀生成?___________(填
“是”或“否”)。
【答案】
(1)c3(Cd2+)•c2(PO 3-)
4
(2)Cd(OH)
2
(3) 1.0×10-19 是
(4)蓝色
(5) 1.0×10-7 2 否
【分析】
(1)
根据磷酸镉的溶解平衡反应式为:Cd (PO )(s) 3Cd2+(aq)+2 (aq),磷酸镉[Cd (PO )]沉淀溶解平衡常
3 4 2 3 4 2
数的表达式K =c3(Cd2+)•c2 (PO 3-),故答案为:c3(Cd2+)•c2(PO 3-);
sp 4 4
(2)
当CdCO 达到沉淀溶解平衡时有CdCO(s) Cd2++CO 2-,则其平衡时摩尔溶解度为s= =
3 3 3
⇌
=2×10-6mol/L,当Cd(OH) 达到沉淀溶解平衡时有Cd(OH) (s) Cd2++2OH-,则其平衡时摩尔溶解
2 2
⇌
度为s= = =2×10-5mol/L,则它们在水中的溶解能力较大的是Cd(OH) , 故答案
2
为:Cd(OH) ;
2
(3)当S2-浓度达到7.9×10-8mol•L-1时,Cd2+浓度为 =1.0×10-19mol•L-1= <
0.005mg•L-1,是符合水源标准,故答案为:1.0×10-19; 是;
(4)
Mg(OH) 的溶度积Ksp=5.6×10-12,则c(Mg2+)c2(OH-)=5.6×10-12;c(OH-)=2c(Mg2+)=x,得到0.5x×x2=5.6×10-
2
12;计算得到x=2.24×10-4mol/L;c(H+)= =4.5×10-11mol/L,pH=10.4>9.6,所以溶液呈蓝色,故答
案为:蓝色;
(5)
①起始时为50mL 0.018mol/L的AgNO 溶液中加入50mL 0.020mol/L的HCl发生反应,反应后溶液中
3
c(Cl-)= mol/L=10-3mol/L,则溶液中c(Ag+)= =1.0×10-7mol/L,故答案为:
1.0×10-7;
②完全沉淀后盐酸过量,溶液中c(H+)= =0.010mol/L,则溶液的pH=-lgc(H+)=2,故答案为:
2;
③再向反应后的溶液中加入50mL 0.001mol•L-1盐酸,不发生反应时c(Ag+)= ×1.0×10-7mol•L-1=0.67×10-
7mol•L-1、c(Cl-)= ×[(0.001+1.0×10-7+0.001]mol•L-1≈0.001mol•L-1,而离子浓度积=0.001×0.67×10-7=0.67×10-10
<1.0×10-10,故不能沉淀产生,故答案为:否。
提分作业
小杨老师 15521324728 侵权必究
【练1】25 ℃时,在含有PbI 晶体的饱和溶液中存在平衡:PbI (s)⇌Pb2+(aq)+2I-(aq),加入KI固体时,下
2 2
列说法错误的是
A.溶液中PbI (s)质量增大 B.PbI 的溶度积常数不变
2 2
C.溶液中Pb2+的浓度不变 D.沉淀溶解平衡向左移动
【答案】C
【详解】
A.加入少量 KI 固体, I− 浓度增大,平衡逆向移动,溶液中 PbI 质量增大,A正确;
2
B.溶度积常数只与温度有关系,温度不变,溶度积常数 K 不变,B正确;
sp
C.加入少量 KI 固体, I− 浓度增大,平衡逆向移动,Pb2+的浓度减小,C错误;
D.加入少量 KI 固体, I− 浓度增大,沉淀溶解平衡向左移动,D正确;答案选C。
【练2】石灰乳中存在下列平衡:Ca(OH) (s) Ca2+(aq)+2OH-(aq);加入下列溶液,可使固体明显减少的是
2
A.NaCO 溶液 B.KCl溶液
2 3
C.NaOH溶液 D.CaCl 溶液
2 杨sir化学,侵权必究
【答案】B
【详解】
A.加入NaCO 溶液,碳酸根离子与钙离子反应,平衡Ca(OH) (s) Ca2+(aq)+2OH-(aq)正向移动,
2 3 2
Ca(OH) (s)减小,但生成碳酸钙,碳酸钙的摩尔质量大于氢氧化钙的摩尔质量,固体量不会减少,A不符
2
题意;
B.加入KCl溶液,溶液总体积增大,相当于加水稀释,平衡Ca(OH) (s) Ca2+(aq)+2OH-(aq)正向移动,
2
Ca(OH) (s)减小,固体明显减少,B符合题意;
2
C.加入NaOH溶液,氢氧根离子浓度增大,平衡Ca(OH) (s) Ca2+(aq)+2OH-(aq)逆向移动,Ca(OH) (s)增
2 2
多,C不符题意;
D.加入CaCl ,c(Ca2+)增大,平衡逆向移动,Ca(OH) 增多,固体增多,D不符题意;
2 2
选B。
【练3】升高温度,下列数据不一定增大的是
A.溶度积常数K B.弱电解质的电离平衡常数K
sp a
C.水解平衡常数K D.水的离子积常数K
h w
【答案】A
【详解】
A.溶度积常数,还与难容电解质的溶解性有关,并不是所有的难容电解质的溶解性都随温度升高而升高,
故温度升高,溶度积常数K 不一定增大,故A正确;
sp
B.电解质的电离需要吸收热量,温度升高,电离程度一定增大,故B错误;
C.水解是中和反应的逆反应,是吸热反应,温度升高,水解平衡常数一定增大,故C错误;
D.水的电离是吸热反应,故温度升高,电离程度一定增大,水的离子积常数一定增大,故D错误;
本题答案A。
【练4】已知25 ℃时,AgCl的溶度积K =1.8×10-10 mol2·L-2,则下列说法正确的是
sp
A.向饱和AgCl水溶液中加入盐酸,K 值变大
sp
B.AgNO 溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-)
3
C.温度一定,当溶液中c(Ag+)·c(Cl-)=K 时,此溶液为AgCl饱和溶液
sp
D.将固体AgCl加入到KI溶液中,固体由白色变为黄色,AgCl完全转化为AgI,AgCl的溶解度小于AgI
的溶解度
【答案】C
【详解】
A.向饱和AgCl水溶液中加入盐酸,溶解度减小,但K 不变,K 只受温度影响,故A错误;
sp sp
B.两种溶液混合,因为各溶液的浓度未知,所以c(Ag+)不一定等于c(Cl-),故B错误;
C.温度一定,当溶液中c(Ag+)·c(Cl-)=K 时,说明此溶液为AgCl饱和溶液,故C正确;
spD.沉淀转化时是溶解度较小的沉淀转化为溶解度更小的沉淀,AgCl的溶解度大于AgI的溶解度,故D错
误;
故答案为C。
【练5】已知常温下:K (AgCl)=1.8×10-10,K (Ag CrO)=1.9×10-12,下列叙述正确的是
sp sp 2 4
A.AgCl在饱和NaCl溶液中的K 比在纯水中的小
sp
B.向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明K (AgCl)K (AgBr),B错误;
sp sp
C.AgCl的悬浊液存在AgCl(s) Ag+(aq)+Cl-(aq),滴加浓氨水,沉淀溶解,说明AgCl(s) Ag+(aq)+Cl-
(aq)正向移动,C正确;
D.产生AgCl沉淀的最小c(Ag+)= =1.8×10-7mol/L,产生Ag CrO 沉淀的最小
2 4
c(Ag+)= ,形成AgCl所需c(Ag+)较小,因此先形成AgCl
沉淀,D错误;
答案选C。
【练6】已知K (AgCl)=1.8×10-10。向盛有0.1 mol/L AgNO 溶液的试管中滴加等体积0.1 mol/L NaCl溶液,
sp 3
静置沉降,取上层清液和下层悬浊液分别进行实验。下列判断正确的是
A.上层清液为AgCl的饱和溶液
B.向清液中滴加0.1 mol/L AgNO 溶液,c(Cl-)不变
3
C.向悬浊液中滴加0.1 mol/L KI溶液,不会有明显变化
D.向悬浊液中加入适量浓氨水,混合液变澄清,说明AgCl可溶于强碱
【答案】A
【详解】
A项、0.1 mol/L AgNO 溶液与等体积0.1 mol/L NaCl溶液反应生成氯化银沉淀和硝酸钠,静置沉降,上层
3
清液为氯化银的饱和溶液,下层为氯化银悬浊液,故A正确;
B项、向清液中滴加0.1 mol/L AgNO 溶液,溶液中银离子浓度增大,由K (AgCl)=c(Ag+) c(Cl-)可知,溶
3 sp
液中氯离子浓度减小,故B错误;C项、碘化银的溶度积小于氯化银,向氯化银悬浊液中滴加0.1 mol/L KI溶液,氯化银白色沉淀会转化为
黄色碘化银沉淀,故C错误;
D项、向悬浊液中加入适量浓氨水,氯化银与氨水反应生成溶于水的银氨络离子,混合液变澄清,但氯化
银不能与氢氧根离子反应,不溶于强碱,故D错误;
故选A。
【练7】t℃时, 在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
A.t℃时, 的Ksp数量级是10-9
B.t℃时: 的平衡常数 (t℃时 )
C.t℃时,用 液滴定 和 的混合液, 先沉
淀
D.在饱和 溶液中加入 固体可使溶液由Y点到X点
杨sir化学,侵权必究
【答案】B
【详解】
A. 的沉淀溶解平衡为 ,根据图像曲线上的数据结合溶度积
常数概念计算得到 ,A项错误;
B.在 时, 的平衡常数
,B项正确;
C.混合溶液中 , ,向其中滴加 溶液,开始生成 沉淀时所需 ,开始生成 沉淀时所
需 ,故先析出氯化银沉淀,C项错
误;
D.在 饱和溶液中加入 固体,可使沉淀溶解平衡逆向移动,则溶液中 增大,
减小,不可能由Y点到X点,D项错误;
答案选B。
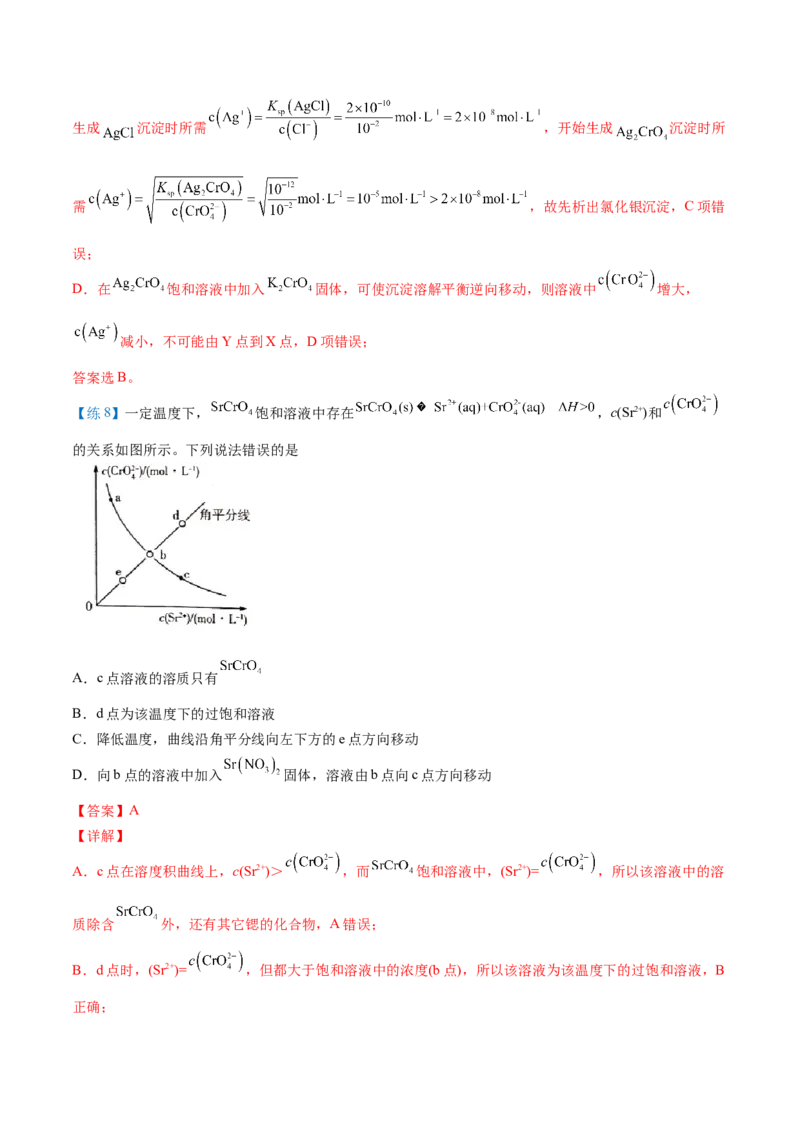
【练8】一定温度下, 饱和溶液中存在 ,c(Sr2+)和
的关系如图所示。下列说法错误的是
A.c点溶液的溶质只有
B.d点为该温度下的过饱和溶液
C.降低温度,曲线沿角平分线向左下方的e点方向移动
杨sir化学,侵权必究
D.向b点的溶液中加入 固体,溶液由b点向c点方向移动
【答案】A
【详解】
A.c点在溶度积曲线上,c(Sr2+)> ,而 饱和溶液中,(Sr2+)= ,所以该溶液中的溶
质除含 外,还有其它锶的化合物,A错误;
B.d点时,(Sr2+)= ,但都大于饱和溶液中的浓度(b点),所以该溶液为该温度下的过饱和溶液,B
正确;C.降低温度, 的溶解平衡逆向移动,虽然(Sr2+)= 但都比b点时小,所以曲线沿角平分线
向左下方的e点方向移动,C正确;
D.向b点的溶液中加入 固体,增大溶液中的c(Sr2+),使 的溶解平衡逆向移动,达平衡时,
c(Sr2+)> ,所以溶液由b点向c点方向移动,D正确;
故选A。
【练9】已知常温下,AgCl的K =1.8×10-10,AgBr的K =4.9×10-13。
sp sp
(1)现向AgCl的悬浊液中:
①加入AgNO 固体,则c(Cl-)_______(填“变大”、“变小”或“不变”,下同);
3
②若改加更多的AgCl固体,则c(Ag+)_______;
③若改加更多的KBr固体,则c(Ag+)_______;
(2)有关难溶盐的溶度积及溶解度有以下叙述,其中错误的是_______;
A.将难溶电解质放入纯水中,溶解达到平衡时,升高温度,K 一定增大
sp
B.两种难溶盐电解质,其中K 小的溶解度也一定小
sp
C.难溶盐电解质的K 与温度有关
sp
D.向AgCl的悬浊液中加入适量的水,使AgCl再次达到溶解平衡,AgCl的K 不变,其溶解度也不变
sp
【答案】变小 不变 变小 AB
【详解】
(1)AgCl的悬浊液中存在, 所以:
①加入AgNO 固体,平衡 逆向移动,则c(Cl-)变小,故答案为:变小;
3
②AgCl的悬浊液已经为饱和溶液,所以若加更多的AgCl固体,溶液中离子浓度不发生变化,故答案为:
不变;
③由已知常温下,AgCl的K =1.8×10-10,AgBr的K =4.9×10-13.,可知AgCl的溶解平衡常数大于AgBr的溶
sp sp
解平衡常数,则AgCl易转化为AgBr,所以若加KBr固体则溶液中c(Ag+)变小,故答案为:变小;
(2)
A.升高温度,电解质溶于水为吸热还是放热未知,所以将难溶电解质放入纯水中,溶解达到平衡时,升
高温度,K 不一定增大,故A错误;
sp
B.K 小溶解度不一定小,取决于物质的构成是否相似,如AgCl与AgBr,组成相似,溶度积越小,则溶
sp
解度越小,故B错误;
C.K 与温度有关,属于温度函数,所以难溶盐电解质的K 与温度有关,故C正确;
sp sp
D.K 与温度有关,属于温度函数,温度不变,溶度积不变,所以向AgCl的悬浊液中加入适量的水,使
sp
AgCl再次达到溶解平衡,AgCl的K 不变,其溶解度也不变,故D正确。
sp
答案选AB。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育