文档内容
2010年黄高优录考试选拔赛试卷2
可能用到的相对原子质量:C—12 H—1 O—16 N—14 Na—23 Fe—56 Ca—40
一. 选择题(: 本题包括15个小题,每小题2分,共30分.每小题有1个或2个选项符合题
意.若有两个答案的错1个不得分,漏选1个扣1分.请将答案填在下表相应题号的空格
内.)
1.下列物质的哪些用途与它的物理性质有关:①氩气和氮气作灯泡的保护气 ②用铝做炊
具 ③用氧气作助燃剂 ④用碳作燃料 ⑤用花岗岩铺地面,以上说法正确的是( )
A.①②③④ B.①③⑤ C.②⑤ D.②④⑤
2.我国大力发展水力发电站建设,如葛洲坝,年发电量相当于每年燃烧3000万吨煤的火力
发电站了出的电量,水力发电和火力发电相比,下列说法中正确的是( )
①减少CO 的排放有利于减轻温室效应 ②减少 SO 的排放有利于减少降酸雨 ③减少废
2 2
渣排放有利减少对土壤、水体污染 ④减轻白色污染
A.①②③④ B.①②③ C.①② D.①
3.甲基橙(指示剂)是种酸的钠盐,含C、H、N、S、O、Na 等元素,定量分析得到下列元素的质
量分数:C为51.4%;H为4.3%;N为12.8%;S为9.8%;Na 为7.0%。则甲基橙的相对分子质
量至少不低于( )
A.98 B.109 C.327 D.82
4.一位遇上海难的水手,随着木排在海上漂流,他用完了淡水,仍感到异常的口渴,虽然周围
的海水十分清澈,但他不喝海水,因为他知道海水会致命。理由是( )
A.海水有苦涩味,根本喝不下去
B.海水中含有各种盐类,能使人肠胃腐烂,致人死亡
C.海水中有许多微生物,有些微生物能致人死亡
D.海水会造成水分从血液和组织内脱离出来进入肠胃,使人脱水死亡
5.某可燃性气体在空气中燃烧能生成水,则下列推断正确的是( )
A.该气体一定是氢气 B.该气体中一定含有氢氧两种元素
C.该气体不一定含有氢气 D.该气体中一定含有氢元素
6.农业及城市生活污水中含磷,家用洗涤剂(含磷酸钠)就是污水中磷的一个重要来源,处理
污水时要不要除去磷,有以下几种意见,你认为正确的是( )
A.磷是生物的营养元素,不必除去
B.含磷的污水是很好的肥料,不必处理
C.含磷的污水排放能引起藻类增殖,使水变质,必须除去
D.磷对人无毒害,除去与否无关紧要
7.硫酸铵的化学式是(NH ) SO ,其中各元素都不存在的化合价是( )
4 2 4
A.-2 B.-3 C.+5 D.+6
8.小明同学做探究性实验:用称量法测定铁在氧气中燃烧的产物。发现5.6g铁在充足的氧气
中燃烧得到7.82g固体.小明排除了其它因素可能产生的误差,则实验中得到的固体产物可能
是( )
A.只有Fe O 固体 B .Fe O 和FeO的混合物
3 4 3 4
C. Fe O 和Fe O 的混合物 D.Fe O、FeO和Fe的混合物
2 3 3 4 3 4
9.如图表示等质量的金属Mg和Al分别与足量且质量分数相等的稀硫酸反应,下列叙述正
确的是
A、X表示反应所用时间,Y表示生成氢气的质量
B、X表示生成氢气的质量,Y表示反应所用时间C、X表示滴加稀硫酸的质量,Y表示生成氢气的质量
D、X表示参加反应的金属的质量,Y表示生成氢气质量
10.日常生活中所用自来水管,你认为选用下面哪种既经济又耐用( )
A.普通钢管 B.铜管 C.不锈钢管 D.镀锌管
11.大气中二氧化碳增多会引起温室效应,现有五个反应:
Y Al
① CO 2 + H 2 O == H 2 CO 3 ②CO 2 + Ca(OH) 2 == CaCO 3 ↓+ H 2 O Y
Mg
阳光
③6nCO + 5nH O (C H O)n + 6nO
2 2 6 10 5 2
叶绿素
高温
④ CO
2
+ C 2CO ⑤CO
2
+ CaCO
3
+ H
2
O == Ca(HCO
3
)
2
X
能说明自然界中消耗CO 的反应是 ( )
2
A.①② B.②③ C.①③⑤ D.①②⑤
12.在我国干旱严重的华北地区,近年来利用飞机、高炮或火箭等运载工具向过冷云层中播
撒碘化银或干冰,实现人工增雨,达到减灾的目的。下列有关人工增雨的评述中,你认为不太
合理的是( )
A.它对农业生产和大气环境的改善有一定的效果
B.它使用的碘化银中的重金属元素将对地表土壤造成污染
C.它使用的碘化银如换成干冰,可避免重金属元素对土壤的污染
D.它是人类彻底战胜自然的表现,体现了人类的力量是无穷的
13.煤坑道内的“瓦斯“爆炸往往造成重大矿难事故,“瓦斯”的要成分是甲烷气体。以下措
施不能防止煤矿坑道内“瓦斯”爆炸的是( )
A.及时通风 B.杜绝明火 C.监测温度 D.监测甲烷浓度
14.国庆50周年,我国导弹部队展示了我国最先进的导弹,这些导弹装备的都是固体燃料,
这些固体燃料一定不是( )
A.固体H B.固体碳氢化合物
2
C.固体碳 氢 氧化合物 D.固体O
2
15.2000年5月,保利集团在香港拍卖会上花费3000多万港元购回在火烧圆明园时流失的
国宝:铜铸的牛首、猴首和虎首。普通铜器时间稍久容易出现铜绿,其主要成分是Cu (OH)
2
CO。这三种1760年铜铸的国宝在240年后看上去仍然熠熠生辉不生锈。下列对其原因的分
2 3
析,最可能的是( )
A.它们的表面都电镀上了一层抗腐蚀的黄金
B.环境污染日趋严重,它们表面的铜绿被酸雨溶解洗去
C.铜的金属活动性比氢小,因此不易被氧化
D.它们是含有一定比例金、银、锡、锌的铜合金
二.填空题(本题包括个小题,共41分)
16.冶金技术在中国有着修久的历史。我国古代将炉甘石(ZnCO )、赤铜矿(主要成分为
3
Cu O)和木炭粉混合加热至800℃左右,即可得到金光闪闪与黄金外观相似的“药金”。
2
(1)用上述方法不能制得黄金是因为_____________________________.
(2)药金的主要成分是______________________
.
17.元素分成金属元素、非金属元素;物质可分成有机物、无机物……分类都有一定的原则。
下列化学式各表示一种物质,请按你的原则,将下列物质分成各有五种的A、B两类,并写出
你的分类原则。
Ca、NH 、MgO、NaOH、CH、HO、KH、SiC、HF、Ne
3 4 2A:_________________________;B:_________________________。
分类原则是__________________________________________________。
18.高温烧制黏土砖时,当砖已烧成且窑温较高时,往砖上浇水得到的是青砖,而不浇水得到
的是红砖。成砖的颜色主要是由砖中铁的氧化物决定的。青砖中所含铁的氧化物________
(填化学式),红砖中所含铁的氧化物___________(填化学式)
19.广义的氧化还原反应概念是:凡是化合价有升降的反应就是氧化还原反应。在氧化还原
反应中,元素化合价的升降数相等。已知ROn- 氧化I(- 碘离子)的反应方程式ROn- +6I- +6H+
3 3
= 3I + 3H O + R- 。则在ROn-中,R元素的化合价是________,R原子的最外层电子数是
2 2 3
______ 。
20.在法庭医学分析上常用马氏砷法来证明受害者是否为砒霜(As O)中毒。用锌和盐酸与
2 3
试样混合在一起,若试样中有砒霜,就会发生反应生成砷化氢(AsH )、氯化锌和水。写出该
3
反应的化学方程式__________________________________________________________。
21.化学电池在通信、交通和日常生活中有着广泛的应用,但是,废弃电池所带来的环境污染
问题也日益突出。已知镍镉(Ni-Cd)电池中发生的化学反应为:
Cd + 2NiO(OH) + 2H O
放
2
电
N i(OH) + Cd(OH)
2 2 2
充电
其中2Ni(OH) 和Cd(OH) 均难溶于水,但能溶于酸。请回答:
2 2
(1)镍镉电池充电时,其能量的转化是由_________能转化为________能;
(2)一节废镍镉电池会使1m2的耕地失去使用价值,要酸性土壤中,这种污染尤为严重。这是
因为_________________________________。
(3)废弃的镍镉电池所产生的Cd2+污染,可导致人体患骨痛病及肝、肾、肺的病变,其中,
Cd2+进入人体的途径如下图所示:
A、B、C代表Cd2+污染传递的载体,如果A代表土壤; 废弃电池 A C 人体
则B代表_____________;C代表____________。
(4)你认为减少甚至消除废弃电池污染,应采取的措施是:
B
________________________________________________。
22.分子中仅含C、H两种元素的有机物叫烃,可用通式C H 表示,且y≤2x+2。汽油的主要
x y
成分是含碳原子5~11个的烃,柴油以含碳原子15~18个的烃为主,而压缩天然气的主要成分
是甲烷,液化石油气主要是含3~4个碳原子的烃。烃类在燃烧时,含碳量(质量分数)越高,就
越易造成不完全燃烧,产生一氧化碳甚至冒黑烟!
( 1 ) 写 出 烃 ( C H ) 在 空 气 中 完 全 燃 烧 的 化 学 方 程 式
x y
__________________________________________.
(2)很多机动车在行驶中不仅噪音巨大,而且还排放大量黑烟。若某机动车燃料为C H,写
x y
出 不 完 全 燃 烧 分 别 生 成 “ 黑 烟 ” 和 一 氧 化 碳 的 两 个 化 学 方 程 式 :
_______________________________________。
(3)资料显示,在非采暖期,北京大气中79%的烃、80%的一氧化碳和55%的氮氧化物主要来
自汽车尾气,而在采暖期,上述三种污染物的比例却降低到74%、63%和37%。在冬季采暖期,
汽 车 尾 气 排 放 的 三 种 污 染 物 的 比 例 下 降 的 原 因 可 能 是
____________________________________________。
采暖期大气污染程度是有所减轻还是有所加重?_____________________________________。
(4)若改用新型燃料作为机动车的动力来源,以此减轻城市大气污染,最好用
________________(填序号)
A.无烟煤 B.压缩天然气 C.电瓶 D.液化石油气
23.药物康力龙属于国际奥委会宣布禁用的合成类固醇,结构简式如下图所示。此药物对肝
功能有明显损害作用,过量使用还会产生女子男性化,男子过早秃顶,肝中毒,甚至患肝癌等毒副作用。已知康力龙的相对分子质量为328,在康力龙分子中,w(C) =76.83%,
w(H)=9.76%, w(N)=8.85%
w(O)=4.56%。设康力龙的化学式为C HNO ,已知x=32, y=2, z=1, 则q= 。
q x y z
24.已知CHOH、 C HOH、 HO的混合物
3 2 5 2
中,C、H、O的质量比为3:1:4,若甲醇与乙醇充
分燃烧所消耗的氧气量相等,求混合物中甲醇、
乙醇、水的质比为__________________.
三.实验题(本题包括2小题,共20分)
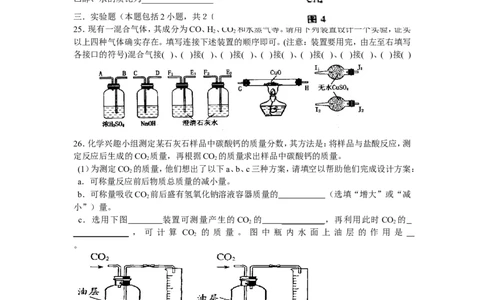
25.现有一混合气体,其成分为CO、H、CO 和水蒸气等。请用下列装置设计一个实验,证实
2 2
以上四种气体确实存在。填写连接下述装置的顺序即可。(注意:装置要用完,由左至右填写
各接口的符号)混合气接( )、( )接( )、( )接( )、( )接( )、( )接( )、( )接( )、( )接( )
26.化学兴趣小组测定某石灰石样品中碳酸钙的质量分数,其方法是:将样品与盐酸反应,测
定反应后生成的CO 质量,再根据CO 的质量求出样品中碳酸钙的质量。
2 2
(1)为测定CO 的质量,他们想出了以下a、b、c三种方案,请填空以帮助他们完成设计方案:
2
a.可称量反应前后物质总质量的减小量。
b.可称量吸收CO 前后盛有氢氧化钠溶液容器质量的 (选填“增大”或“减
2
小”)量。
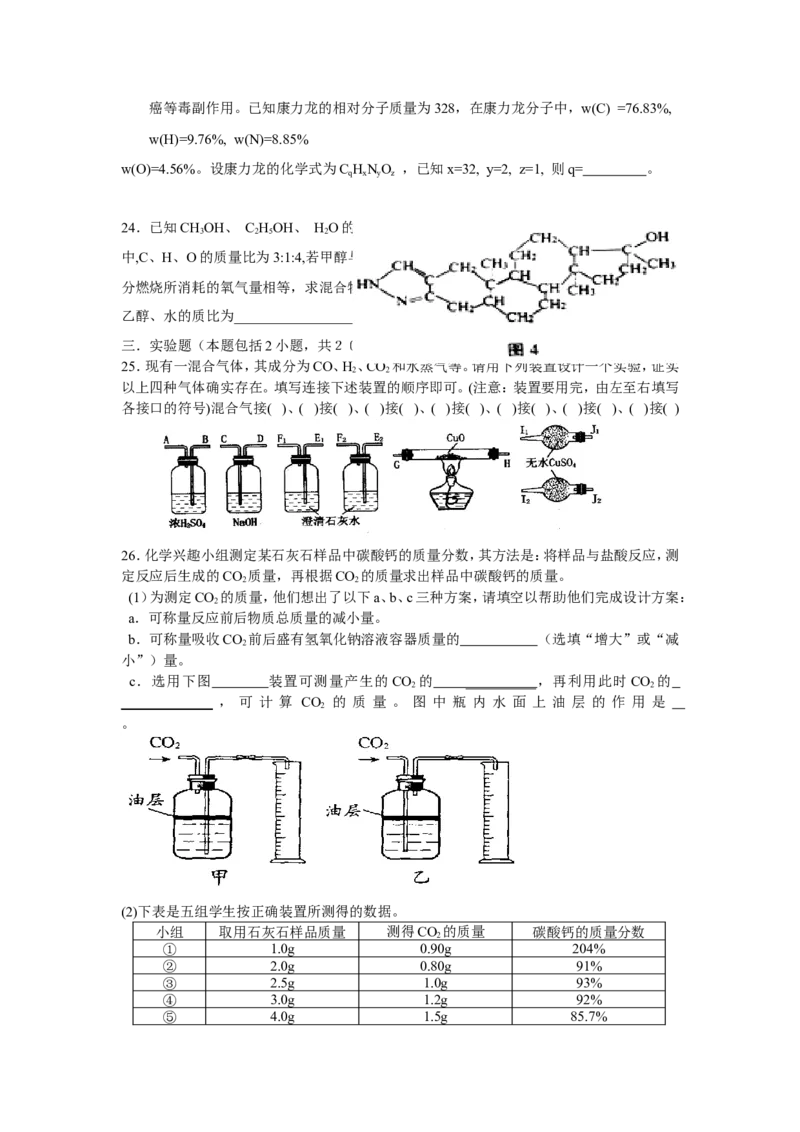
c.选用下图 装置可测量产生的CO 的 __________ ,再利用此时CO 的
2 2
_____________ , 可 计 算 CO 的 质 量 。 图 中 瓶 内 水 面 上 油 层 的 作 用 是
2
。
(2)下表是五组学生按正确装置所测得的数据。
小组 取用石灰石样品质量 测得CO 的质量 碳酸钙的质量分数
2
① 1.0g 0.90g 204%
② 2.0g 0.80g 91%
③ 2.5g 1.0g 93%
④ 3.0g 1.2g 92%
⑤ 4.0g 1.5g 85.7%根据上表所得数据,该样品中碳酸钙质量分数的平均值为 ;在
此 实 验 中 , 导 致 碳 酸 钙 质 量 分 数 比 实 际 值 偏 高 的 可 能 原 因
, 碳 酸 钙 质 量 分 数 比 实 际 值 偏 低 的 可 能 原 因 有
。
参考答案:
一..........................................................选择题:
1.C 2.B 3. C 4.D 5 .C D 6.C 7 .C 8.C 9C 10.D 11.C 12.D 13.C 14.D
15.D
二.填空题
16.(1)根据质量守恒定律知道,反应物中没有金元素,反应后不可能的金生成.
(2)铜锌合金
17. A. Ca MgO NaOH KH SiC
B. NH CH HO HF Ne
3 4 2
每组每个分子中所含质子数相等
18. Fe O (或FeO或FeO 和Fe O) Fe O
3 4 3 4 2 3
19. .+5 7
20. As O+6Zn+12HCI===2AsH +6ZnCI +3H O
2 3 3 2 2
21.(1)电 化学
(2)电池中Ni(OH) Ca(OH) 与酸反应生成可溶性有重金属有毒镍,镉离子,所以污染土地.
2 2
(3)水体 植物或生物体
(4)回收集中处理
22.(1)4C H+(4x+y)O ===4xCO +2yH O
x y 2 2 2
(2) 4C H+yO ==4xC+2yH O 4C H+(2x+y)O ==4xCO+2yHO
x y 2 2 x y 2 2
(3)采暖期,居民使用煤等化石燃料增多,排放到空气中污染物比例增大,而汽车尾气相对比例
下降.
加重 B
23. 21 24. 32:23:9
25.J 、I 接 E、F 接C、D 接B、A 接G、H 接J、I 接E
1 1 1 1 2 2 2
26.(1)增大 甲 体积 密度 阻止二氧化碳溶于水中。
(2)92% 混有其它杂质也能与酸液反应放出气体。
试样不充分反应或装置漏气。