文档内容
黄浦区 2022 年九年级适应性调研
综 合 测 试 卷
化学部分
(满分50分)
考生注意:
1.本试卷化学部分含二个大题。
2.答题时,考生务必按答题要求在答题纸规定的位置上作答,在草稿纸、本试卷上答题一律
无效。
相对原子质量:H-1 C-12 O-16 Na-23 S-32 Cl-35.5 Ca-40 Fe-56 Cu-64
五、选择题(共20分)
请将正确选项的代号用2B铅笔填涂在答题纸的相应位置上,更改答案时,用橡皮擦去,重新
填涂。21~34每题均只有一个正确选项
1. 下列物质中,金属活动性最弱的是
A. 钙 B. 镁 C. 汞 D. 铝
2. 灼烧NaCl时,火焰的颜色是
.
A 红色 B. 绿色 C. 紫色 D. 黄色
3. 下列可作钾肥的物质是
A. CO(NH ) B. KCl C. Ca(HPO ) D. NH Cl
2 2 2 4 2 4
4. 以下含有氮分子的物质是
A. N B. NO C. NO D. N O
2 2 2 5
5. 以下各物质的用途是利用了其化学性质的是
A. 木炭用作燃料 B. 金刚石切割玻璃
C. 石墨制作铅笔芯 D. 活性炭吸附异味
6. 磷燃烧的化学方程式书写正确的是
A. P+O PO B. 4P+5O=2P O
2 2 2 2 5
C. 4P+5O 2PO↑ D. 4P+5O 2PO
2 2 5 2 2 5
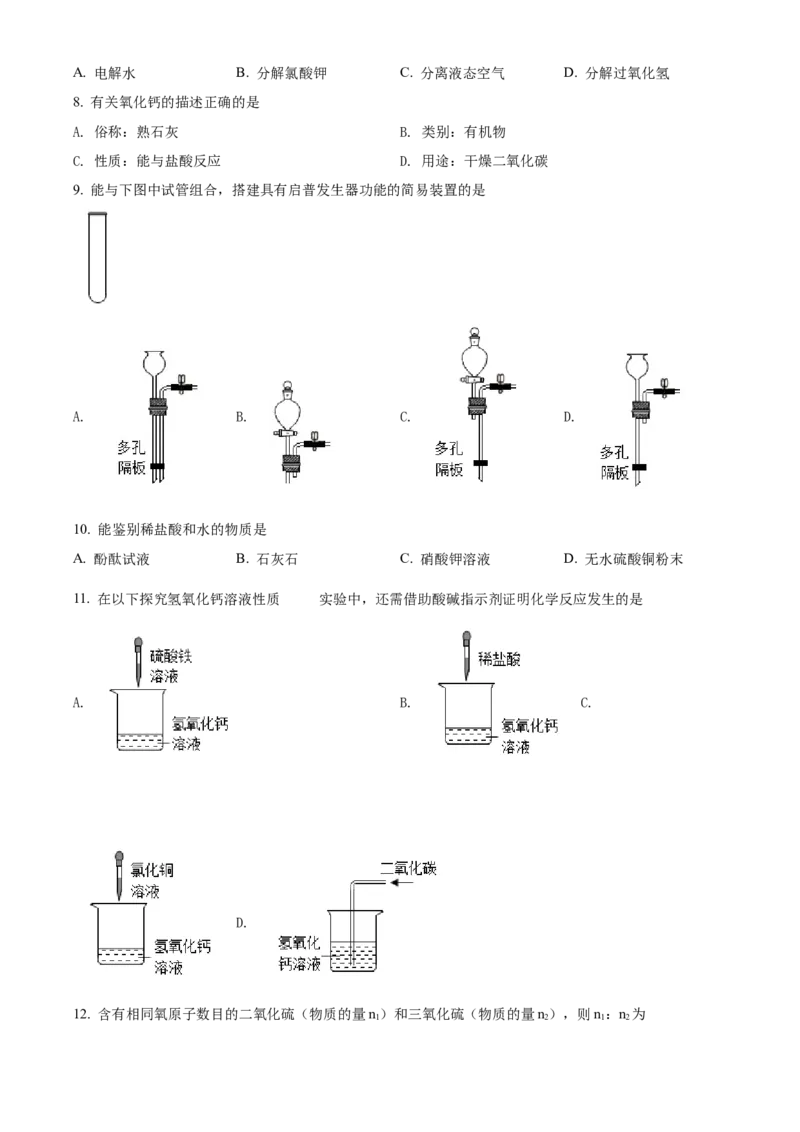
7. 以下得到氧气的过程属于物理变化的是A. 电解水 B. 分解氯酸钾 C. 分离液态空气 D. 分解过氧化氢
8. 有关氧化钙的描述正确的是
A. 俗称:熟石灰 B. 类别:有机物
C. 性质:能与盐酸反应 D. 用途:干燥二氧化碳
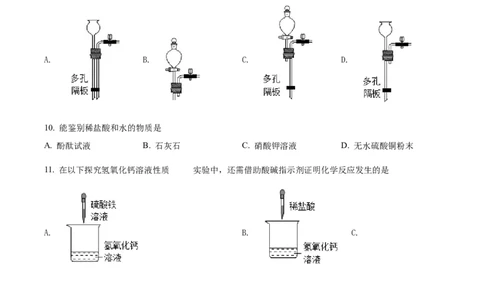
9. 能与下图中试管组合,搭建具有启普发生器功能的简易装置的是
A. B. C. D.
10. 能鉴别稀盐酸和水的物质是
A. 酚酞试液 B. 石灰石 C. 硝酸钾溶液 D. 无水硫酸铜粉末
的
11. 在以下探究氢氧化钙溶液性质 实验中,还需借助酸碱指示剂证明化学反应发生的是
A. B. C.
D.
12. 含有相同氧原子数目的二氧化硫(物质的量n)和三氧化硫(物质的量n),则n:n 为
1 2 1 2A. 1:1 B. 2:3 C. 3:2 D. 4:5
13. 某物质的微观示意图如下所示(用“ ”“ ”分别表示不同的原子),有关说法一定
正确的是
A. 该物质不可能是碱
B. 该物质由三种元素组成
C. 每个分子中含3 mol原子
D. 和 质量比为2:1
14. 以下反应类型,一定有单质生成的反应是
A. 复分解反应 B. 置换反应 C. 化合反应 D. 分解反应
35~37每题均有1~2个正确选项
15. 稀硫酸与物质X反应,生成硫酸铁和水,则X可能是
A. 铁 B. 氧化铁 C. 氯化铁 D. 氢氧化铁
16. 科学上,常用数学方法来表示某些量的关系。下列图像中能用阴影部分面积表示相应的量是
A. 物质的量 B. 溶质质量
C. 元素质量 D. 溶剂质量
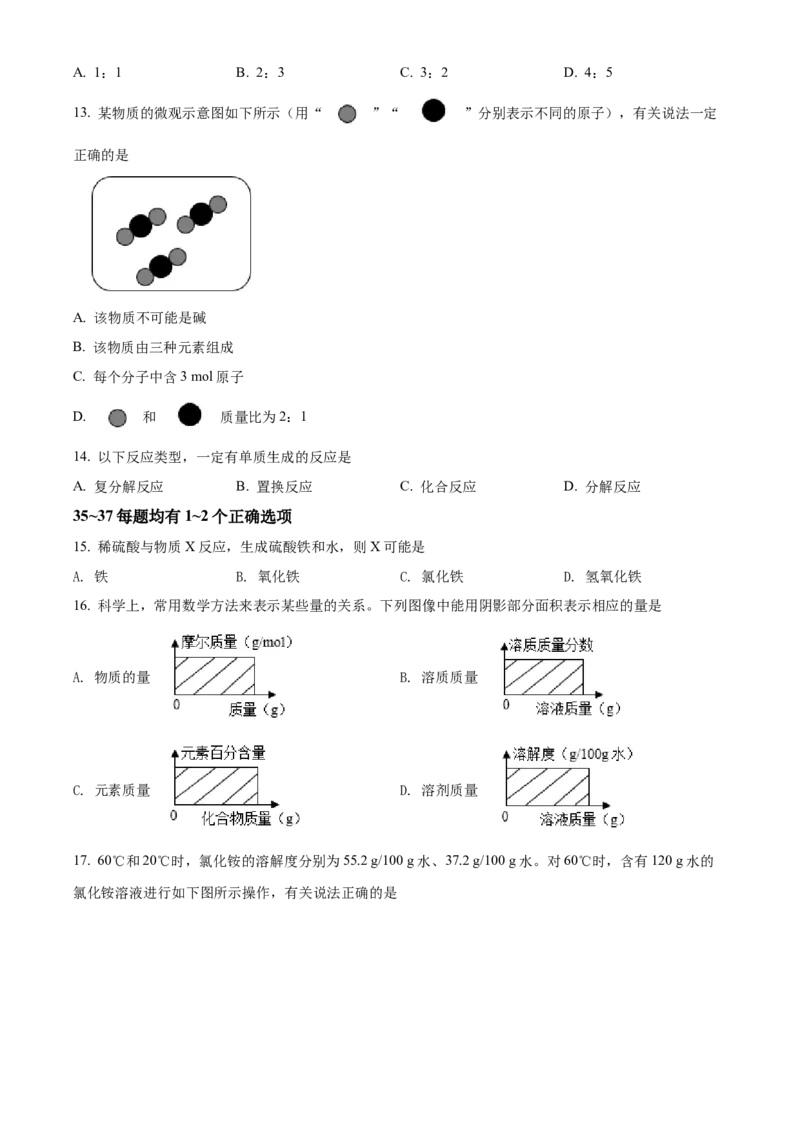
17. 60℃和20℃时,氯化铵的溶解度分别为55.2 g/100 g水、37.2 g/100 g水。对60℃时,含有120 g水的
氯化铵溶液进行如下图所示操作,有关说法正确的是A. 溶液①的溶质质量分数小于溶液②
B. 溶液②为60℃时,氯化铵的不饱和溶液
C. 溶液④中含氯化铵19.2 g
D. 若溶液①蒸发25 g水,仍无氯化铵析出
六、简答题(共30分)
的
18. 北宋《千里江山图》是我国 十大传世名画之一。全画以青绿色调为主,石青、石绿等矿石为作
画的主要颜料。
(1)蓝铜矿在我国古代被称为“石青”,可作为铜矿石来提炼铜。蓝铜矿中铜元素的存在形态是______。
(2)孔雀石也是一种铜矿石,古称为“石绿”,主要成分是Cu (OH)CO。孔雀石属于______(选填
2 2 3
“混合物”或“纯净物”)。1 mol Cu (OH)CO 中约含______个铜原子。我国在3000多年前就将孔雀
2 2 3
石与木炭混合加热炼铜,过程中生成的氧化铜再与木炭反应得到铜。氧化铜与木炭反应的现象是______,
若参加反应的氧化铜为800 g,能生成______mol铜。
(3)《千里江山图》绘制过程中,还使用了赭石。赭石的主要成分是氧化铁,氧化铁中铁元素的化合价
为______,铁元素的百分含量为______。
19. 实验室将一定量的铁粉加入含硝酸银的废液中,用于回收其中的银。
(1)反应完全,为判断银是否全部被铁置换,同学设计了两种不同的实验方案:
方案I:将反应后的混合物进行过滤,取少量滤渣,滴入稀盐酸,产生气泡,由此判断银全部被置换。滴
入盐酸发生反应的化学方程式是______。
方案II:将反应后的混合物进行过滤,______(请将实验方案补充完整),由此判断银全部被置换。
(2)本实验______(选填“能”或“不能”)用锌代替铁,用于回收废液中的银。
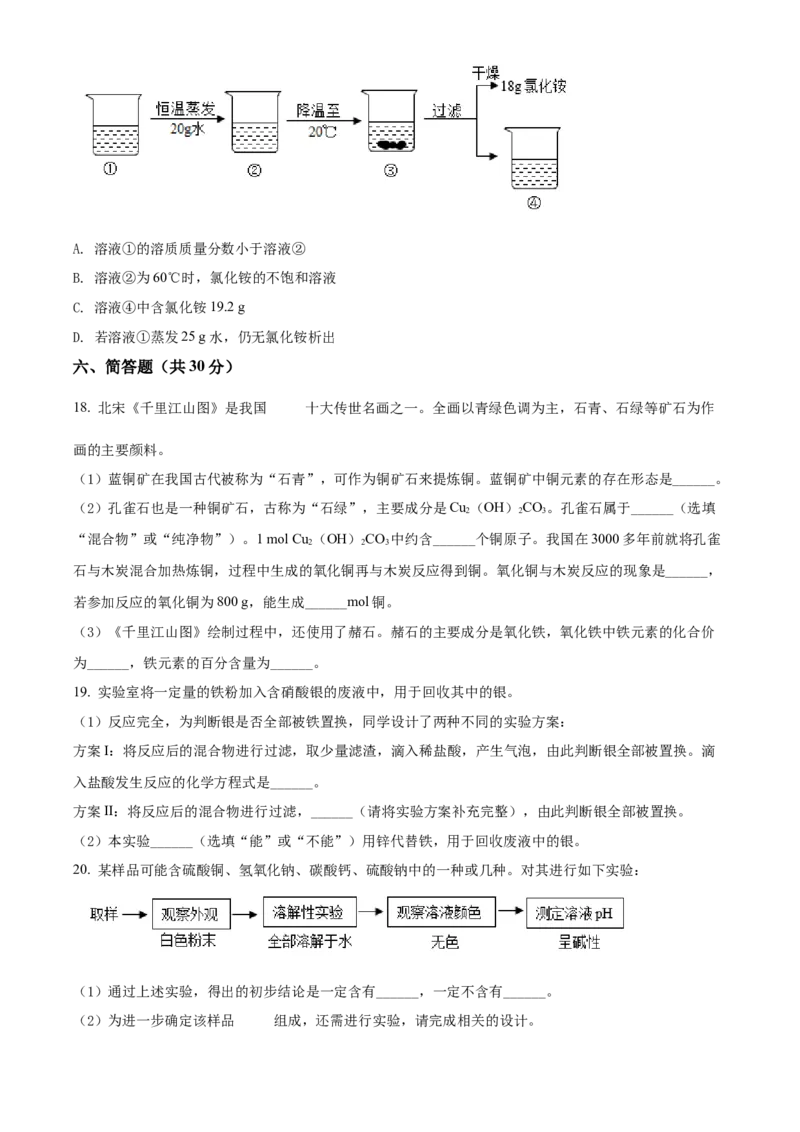
20. 某样品可能含硫酸铜、氢氧化钠、碳酸钙、硫酸钠中的一种或几种。对其进行如下实验:
(1)通过上述实验,得出的初步结论是一定含有______,一定不含有______。
(2)为进一步确定该样品 的组成,还需进行实验,请完成相关的设计。步骤 预测的现象及对应的结论
______ ______
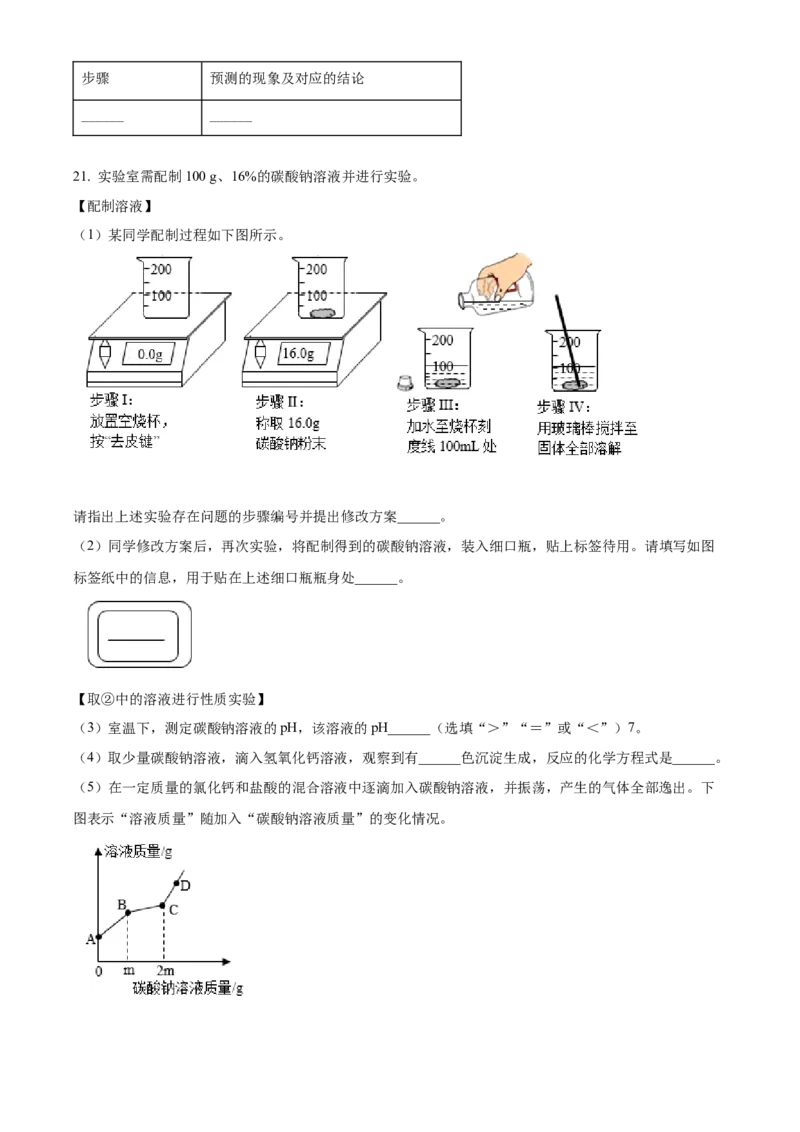
21. 实验室需配制100 g、16%的碳酸钠溶液并进行实验。
【配制溶液】
(1)某同学配制过程如下图所示。
请指出上述实验存在问题的步骤编号并提出修改方案______。
(2)同学修改方案后,再次实验,将配制得到的碳酸钠溶液,装入细口瓶,贴上标签待用。请填写如图
标签纸中的信息,用于贴在上述细口瓶瓶身处______。
【取②中的溶液进行性质实验】
(3)室温下,测定碳酸钠溶液的pH,该溶液的pH______(选填“>”“=”或“<”)7。
(4)取少量碳酸钠溶液,滴入氢氧化钙溶液,观察到有______色沉淀生成,反应的化学方程式是______。
(5)在一定质量的氯化钙和盐酸的混合溶液中逐滴加入碳酸钠溶液,并振荡,产生的气体全部逸出。下
图表示“溶液质量”随加入“碳酸钠溶液质量”的变化情况。的
①AB段发生反应 化学方程式是______。
②D点溶液中溶质的成分是______。
③解释上图中AB段和BC段溶液质量呈现不同增重趋势的原因______。