文档内容
专练 29 晶体结构与性质
授课提示:对应学生用书57页
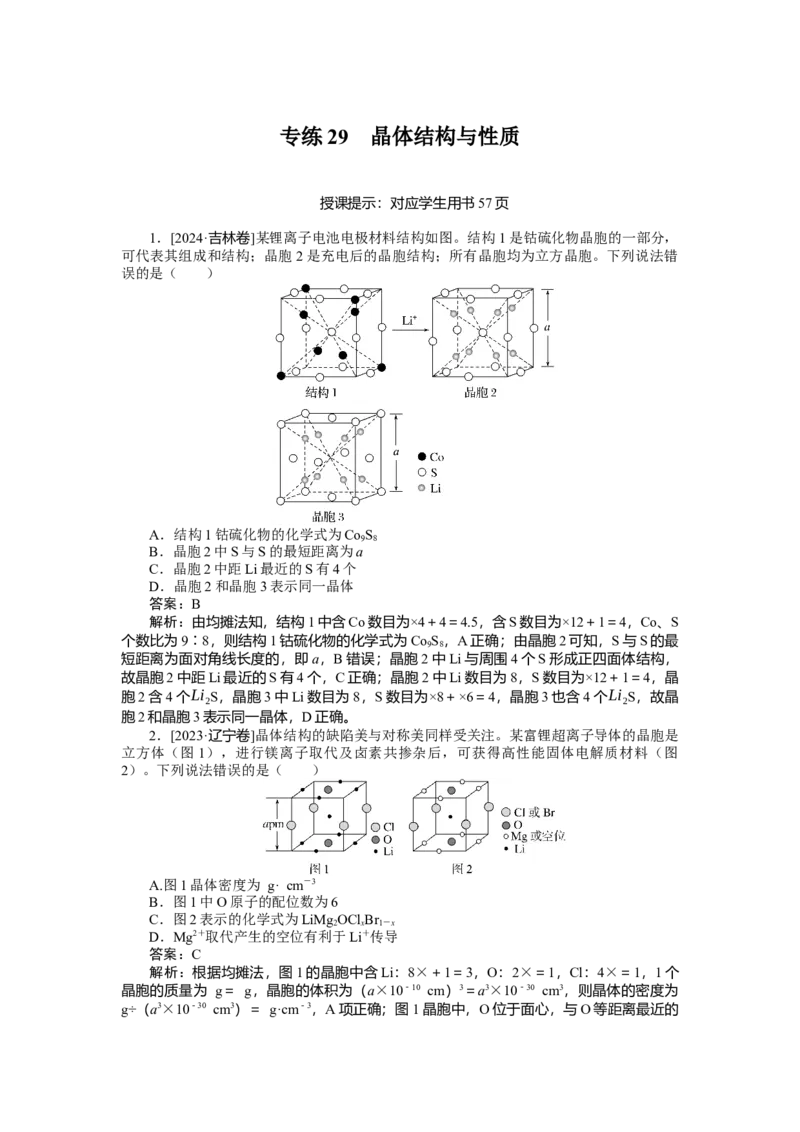
1.[2024·吉林卷]某锂离子电池电极材料结构如图。结构1是钴硫化物晶胞的一部分,
可代表其组成和结构;晶胞2是充电后的晶胞结构;所有晶胞均为立方晶胞。下列说法错
误的是( )
A.结构1钴硫化物的化学式为Co S
9 8
B.晶胞2中S与S的最短距离为a
C.晶胞2中距Li最近的S有4个
D.晶胞2和晶胞3表示同一晶体
答案:B
解析:由均摊法知,结构1中含Co数目为×4+4=4.5,含S数目为×12+1=4,Co、S
个数比为9∶8,则结构1钴硫化物的化学式为Co S ,A正确;由晶胞2可知,S与S的最
9 8
短距离为面对角线长度的,即a,B错误;晶胞2中Li与周围4个S形成正四面体结构,
故晶胞2中距Li最近的S有4个,C正确;晶胞2中Li数目为8,S数目为×12+1=4,晶
胞2含4个Li S,晶胞3中Li数目为8,S数目为×8+×6=4,晶胞3也含4个Li S,故晶
2 2
胞2和晶胞3表示同一晶体,D正确。
2.[2023·辽宁卷]晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是
立方体(图1),进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图
2)。下列说法错误的是( )
A.图1晶体密度为 g· cm-3
B.图1中O原子的配位数为6
C.图2表示的化学式为LiMg OClBr
2 x 1-x
D.Mg2+取代产生的空位有利于Li+传导
答案:C
解析:根据均摊法,图1的晶胞中含Li:8×+1=3,O:2×=1,Cl:4×=1,1个
晶胞的质量为 g= g,晶胞的体积为(a×10-10 cm)3=a3×10-30 cm3,则晶体的密度为
g÷(a3×10-30 cm3)= g·cm-3,A项正确;图1晶胞中,O位于面心,与O等距离最近的Li有6个,O原子的配位数为6,B项正确;根据均摊法,图2中Li:1,Mg或空位为8×
=2,O:2×=1,Cl或Br:4×=1,Mg的个数小于2,根据正负化合价的代数和为0,图
2的化学式为LiMgOClBr ,C项错误;进行镁离子取代及卤素共掺杂后,可获得高性能
x 1-x
固体电解质材料,说明Mg2+取代产生的空位有利于Li+的传导,D项正确;答案选C。
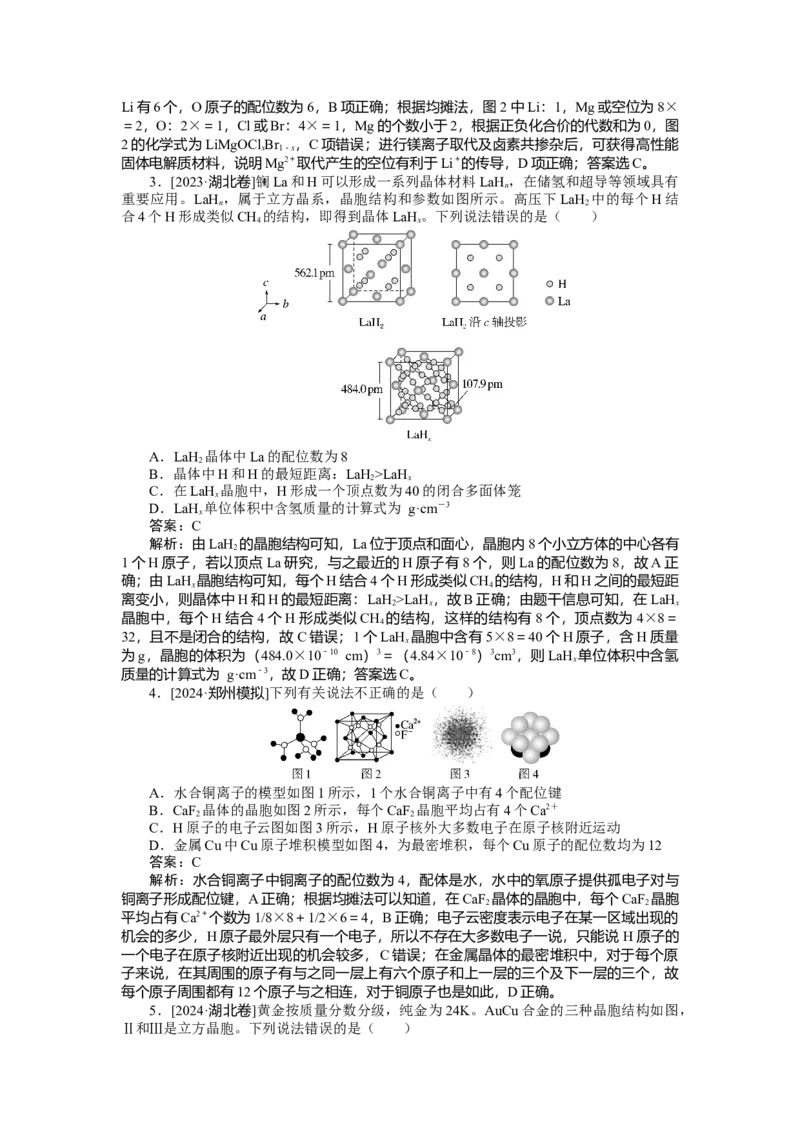
3.[2023·湖北卷]镧La和H可以形成一系列晶体材料LaH ,在储氢和超导等领域具有
n
重要应用。LaH ,属于立方晶系,晶胞结构和参数如图所示。高压下LaH 中的每个H结
n 2
合4个H形成类似CH 的结构,即得到晶体LaH。下列说法错误的是( )
4 x
A.LaH 晶体中La的配位数为8
2
B.晶体中H和H的最短距离:LaH >LaH
2 x
C.在LaH 晶胞中,H形成一个顶点数为40的闭合多面体笼
x
D.LaH 单位体积中含氢质量的计算式为 g·cm-3
x
答案:C
解析:由LaH 的晶胞结构可知,La位于顶点和面心,晶胞内8个小立方体的中心各有
2
1个H原子,若以顶点La研究,与之最近的H原子有8个,则La的配位数为8,故A正
确;由LaH 晶胞结构可知,每个H结合4个H形成类似CH 的结构,H和H之间的最短距
x 4
离变小,则晶体中H和H的最短距离:LaH >LaH,故B正确;由题干信息可知,在LaH
2 x x
晶胞中,每个H结合4个H形成类似CH 的结构,这样的结构有8个,顶点数为4×8=
4
32,且不是闭合的结构,故C错误;1个LaH 晶胞中含有5×8=40个H原子,含H质量
x
为g,晶胞的体积为(484.0×10-10 cm)3=(4.84×10-8)3cm3,则LaH 单位体积中含氢
x
质量的计算式为 g·cm-3,故D正确;答案选C。
4.[2024·郑州模拟]下列有关说法不正确的是( )
A.水合铜离子的模型如图1所示,1个水合铜离子中有4个配位键
B.CaF 晶体的晶胞如图2所示,每个CaF 晶胞平均占有4个Ca2+
2 2
C.H原子的电子云图如图3所示,H原子核外大多数电子在原子核附近运动
D.金属Cu中Cu原子堆积模型如图4,为最密堆积,每个Cu原子的配位数均为12
答案:C
解析:水合铜离子中铜离子的配位数为4,配体是水,水中的氧原子提供孤电子对与
铜离子形成配位键,A正确;根据均摊法可以知道,在CaF 晶体的晶胞中,每个CaF 晶胞
2 2
平均占有Ca2+个数为1/8×8+1/2×6=4,B正确;电子云密度表示电子在某一区域出现的
机会的多少,H原子最外层只有一个电子,所以不存在大多数电子一说,只能说 H原子的
一个电子在原子核附近出现的机会较多,C错误;在金属晶体的最密堆积中,对于每个原
子来说,在其周围的原子有与之同一层上有六个原子和上一层的三个及下一层的三个,故
每个原子周围都有12个原子与之相连,对于铜原子也是如此,D正确。
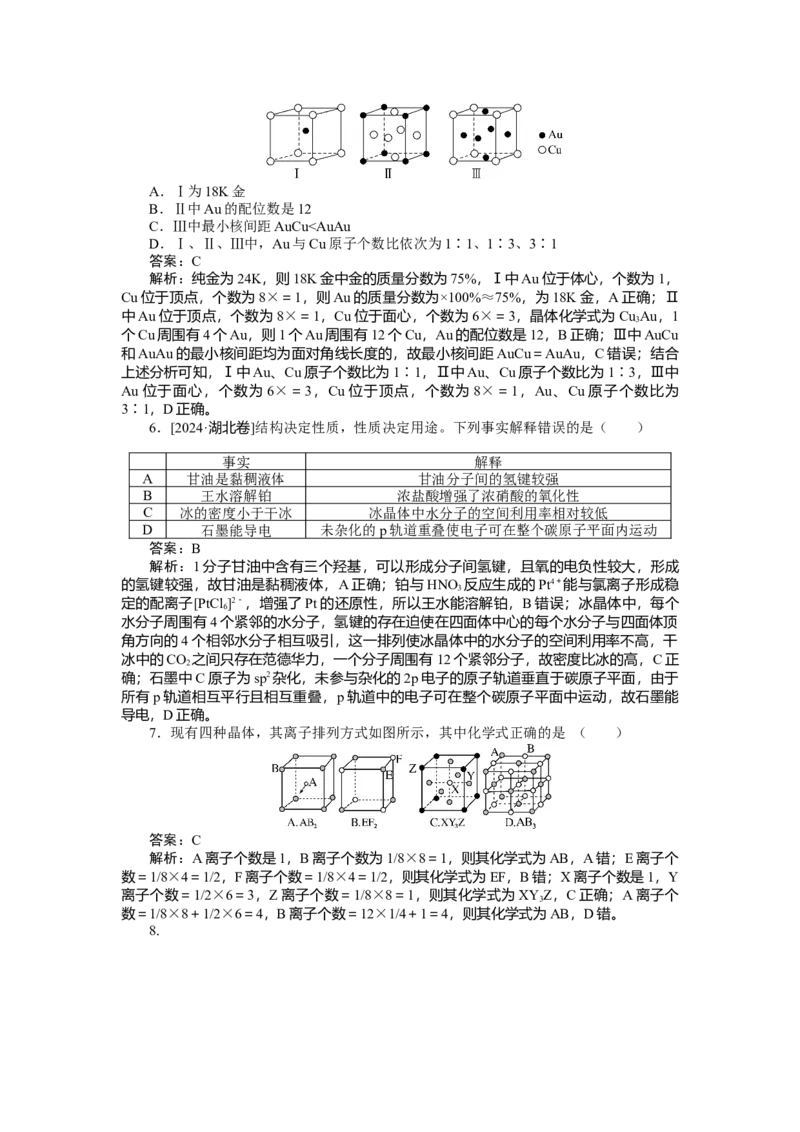
5.[2024·湖北卷]黄金按质量分数分级,纯金为24K。AuCu合金的三种晶胞结构如图,
Ⅱ和Ⅲ是立方晶胞。下列说法错误的是( )A.Ⅰ为18K金
B.Ⅱ中Au的配位数是12
C.Ⅲ中最小核间距AuCu离
子晶体>分子晶体;在共价晶体中,原子半径越大熔点越低;在离子晶体中,离子半径越
大,熔点越低,电荷越多,熔点越高;在分子晶体中,相对分子质量越大,熔点越高(含
有氢键的物质除外),所以这几种物质的熔点高低顺序是金刚石、SiC、NaF、NaCl、
HO、HS,故③正确;④离子晶体中可能有共价键,如氯化铵中氮氢键属于共价键,分子
2 2
晶体中肯定没有离子键,故④错误;⑤由晶胞结构可知CaTiO 晶体中Ti的配位数为12,
3
所以每个Ti4+和12个O2-紧邻,故⑤正确;⑥SiO 晶体中每个硅原子与4个氧原子以共价
2
键相结合,故⑥错误;⑦分子稳定性与分子内共价键的强弱有关,与分子间作用力无关,
故⑦错误;⑧离子晶体熔化时离子键被破坏,氯化钠是离子晶体,故⑧正确。故正确序号
为③⑤⑧。综上所述,本题正确答案为D。
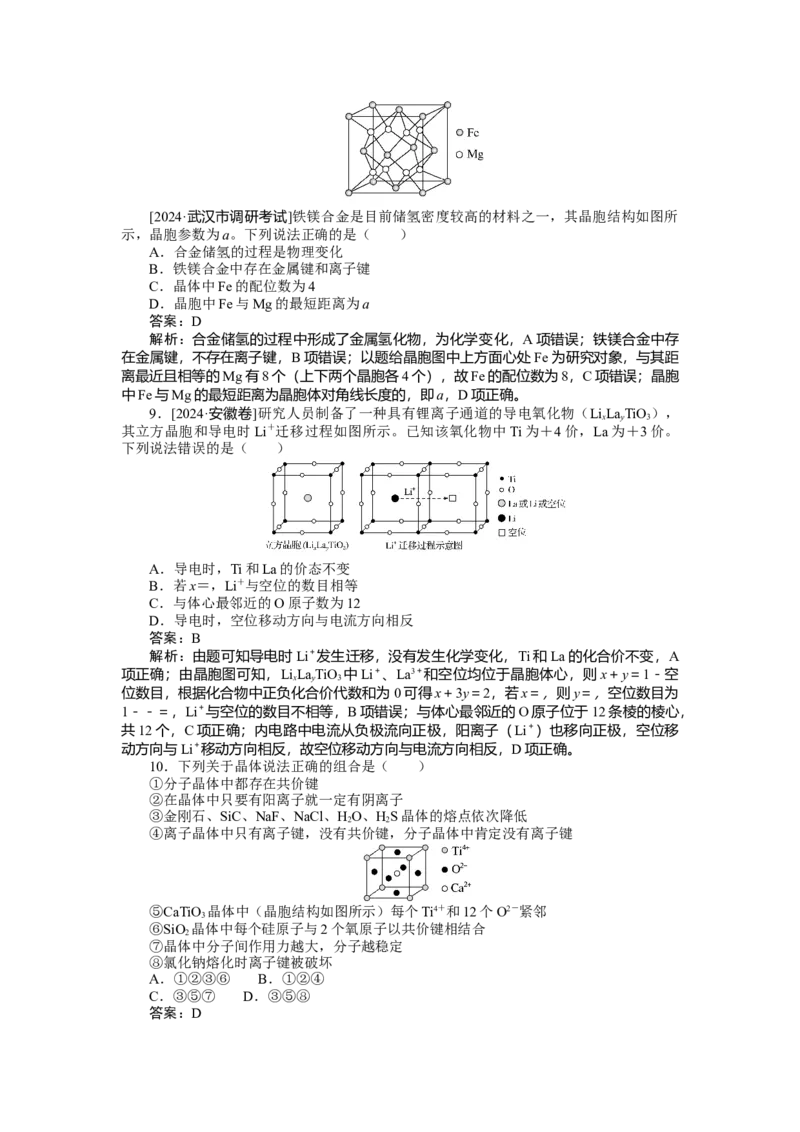
11.[2024·石家庄市质量检测]某晶体由镁、铝、氧三种元素组成,若将其晶胞按图1
方式切成8个体积相同的小立方体,Mg2+、Al3+和O2-在小立方体中的分布如图2、图3所
示。已知Mg2+之间的最小间距为a pm。下列说法错误的是( )
A.晶体的化学式为MgAlO
2 4
B.晶体中三种元素的第一电离能:O>Mg>Al
C.晶胞的体积为a3×10-30 cm3
D.晶体中Mg2+的配位数为4
答案:C
解析:立方体A中,Mg2+位于4个顶点和体心,根据均摊法,Mg2+个数为4×+1
=,O2-位于体内,个数为4,立方体B中,Mg2+位于4个顶点,个数为,Al3+位于体内,
个数为4,O2-位于体内,个数为4,图1晶胞由4个立方体A、4个立方体B构成,所以晶
胞中Mg2+个数为(+)×4=8,Al3+个数为4×4=16,O2-个数为(4+4)×4=32,所
以该晶体的化学式为MgAlO ,A项正确;同周期元素自左向右第一电离能呈增大的趋势,
2 4
但第ⅡA族元素的第一电离能大于第ⅢA族元素的,同一主族元素第一电离能自上而下逐
渐减小,则晶体中三种元素的第一电离能:O>Mg>Al,B项正确;两个最近的Mg2+在体对
角线上,二者的距离为体对角线长度的,设晶胞的棱长为x cm,则a×10-10=,x=,晶
胞的体积为( cm)3= cm3,C项错误;由立方体A的结构可知,每个Mg2+与4个O2-紧
邻,则Mg2+的配位数为4,D项正确。
12.[2024·湖北鄂东南省级示范高中期中]下列叙述不正确的是( )A.LiS晶胞结构如图甲,S2-的配位数是8
2
B.某镍白铜合金的立方晶胞结构如图乙,晶胞中铜原子与镍原子的数量比为3∶1
C.氯化钠晶胞如图丙,离钠离子最近的钠离子有6个
D.铜与氧形成的晶胞如图丁,晶胞中Cu均匀地分散在立方体内部,a、b的坐标参数
分别为(0,0,0)、,则d的坐标参数为
答案:C
解析:由LiS的晶胞结构可知,S2-的配位数是8,A项正确;根据“均摊法”,晶胞
2
中Ni原子的个数为8×=1,Cu原子的个数为6×=3,则晶胞中铜原子与镍原子的数量比
为3∶1,B项正确;以顶点Na+为研究对象,在图示晶胞中离其最近的Na+为位于面心上
的Na+,顶点Na+与3个面的面心上的Na+紧邻,每个顶点参与形成8个晶胞,每个面参
与形成2个晶胞,因此氯化钠晶胞中离钠离子最近的钠离子有12个,C项错误;由晶胞图
可知Cu原子位于体对角线上,与体心O原子的距离为体对角线长的,a、b的坐标参数分
别为(0,0,0)、,则d的坐标参数为,D项正确。