文档内容
专练 34 原电池原理及应用(一)
授课提示:对应学生用书67页
一、选择题
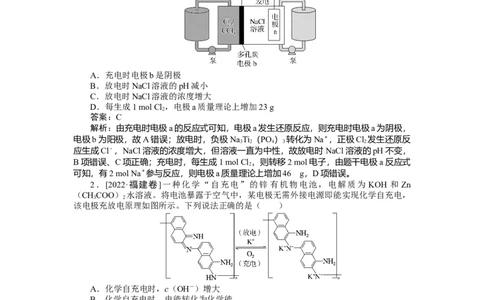
1.[2022·广东卷]科学家基于Cl 易溶于CCl 的性质,发展了一种无需离子交换膜的新
2 4
型氯流电池,可作储能设备(如图)。充电时电极 a的反应为: NaTi (PO ) +2Na++
2 4 3
2e-===Na Ti (PO )。下列说法正确的是( )
3 2 4 3
A.充电时电极b是阴极
B.放电时NaCl溶液的pH减小
C.放电时NaCl溶液的浓度增大
D.每生成1 mol Cl ,电极a质量理论上增加23 g
2
答案:C
解析:由充电时电极a的反应式可知,电极a发生还原反应,则充电时电极a为阴极,
电极b为阳极,故A错误;放电时,负极NaTi (PO ) 转化为Na+,正极Cl 发生还原反
3 2 4 3 2
应生成Cl-,NaCl溶液的浓度增大,但溶液一直为中性,故放电时NaCl溶液的pH不变,
B项错误、C项正确;充电时,每生成1 mol Cl ,则转移2 mol电子,由题干电极a反应式
2
可知,有2 mol Na+参与反应,则电极a质量理论上增加46 g,D项错误。
2.[2022·福建卷]一种化学“自充电”的锌有机物电池,电解质为 KOH 和 Zn
(CHCOO) 水溶液。将电池暴露于空气中,某电极无需外接电源即能实现化学自充电,
3 2
该电极充放电原理如图所示。下列说法正确的是( )
A.化学自充电时,c(OH-)增大
B.化学自充电时,电能转化为化学能
C.化学自充电时,锌电极反应式:
Zn2++2e-===Zn
D.放电时,外电路通过0.02 mol电子,正极材料损耗0.78 g
答案:A
解析:由图示可知,化学自充电时,O 得电子转化为 OH-,OH-与K+结合形成
2
KOH,c(OH-)增大,A正确;该电池为自充电电池,无需外接电源,因此化学自充电时,
没有电能转化为化学能,B错误;由图示可知,化学自充电时,阳极反应为有机物之间的
转化,阴极反应为 O 转化为 OH-,没有发生 Zn2++2e-===Zn,C 错误;放电时,
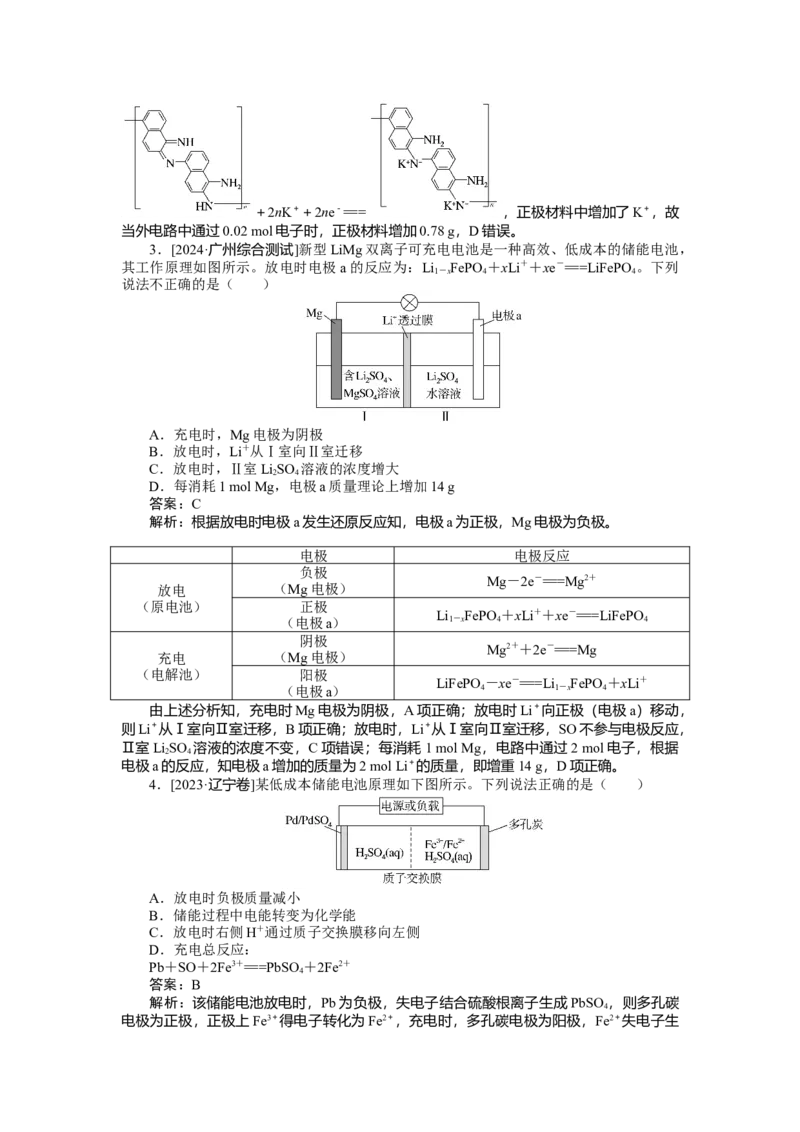
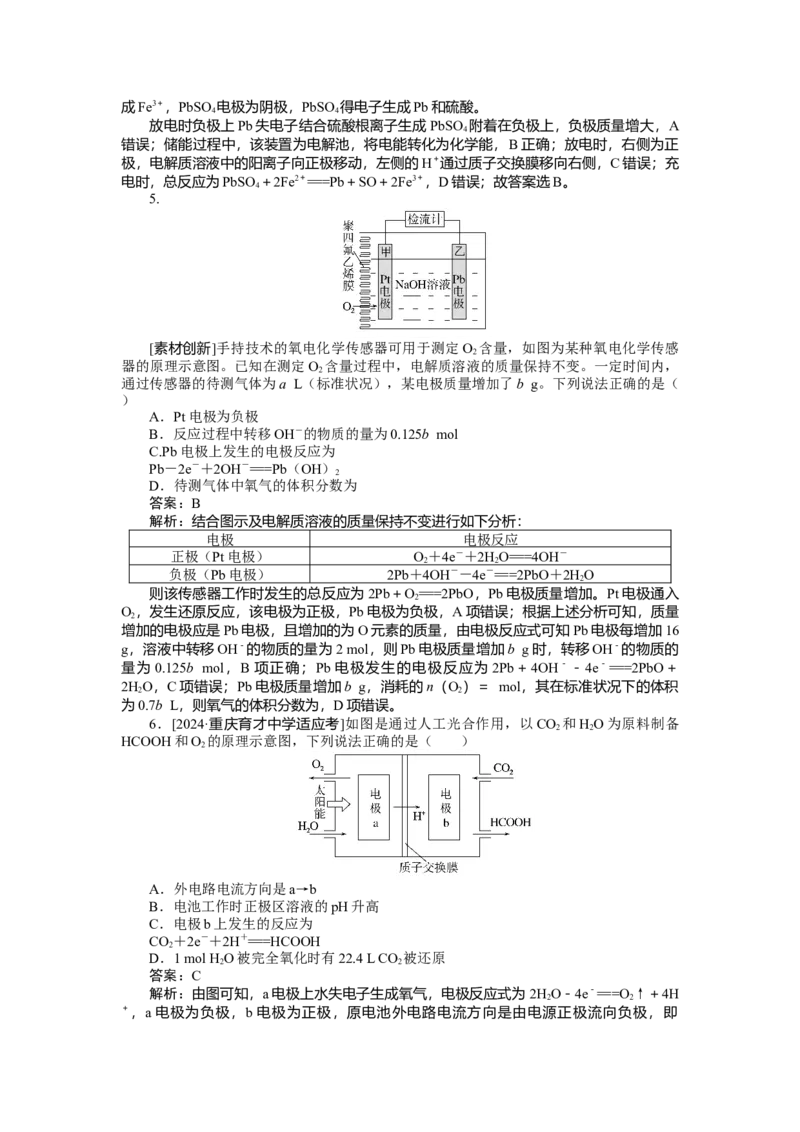
2+2nK++2ne-=== ,正极材料中增加了K+,故
当外电路中通过0.02 mol电子时,正极材料增加0.78 g,D错误。
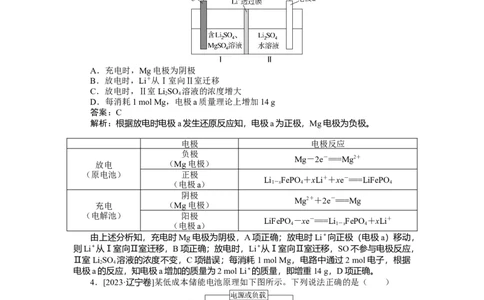
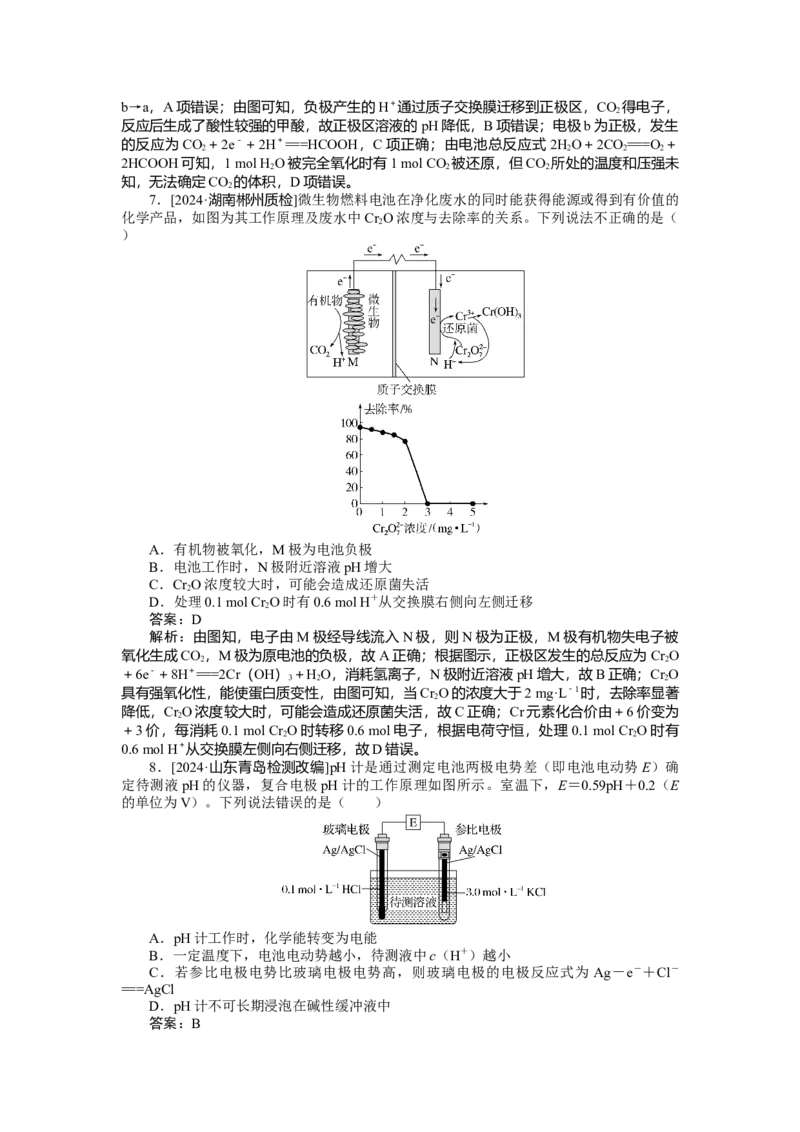
3.[2024·广州综合测试]新型LiMg双离子可充电电池是一种高效、低成本的储能电池,
其工作原理如图所示。放电时电极a的反应为:Li FePO +xLi++xe-===LiFePO 。下列
1-x 4 4
说法不正确的是( )
A.充电时,Mg电极为阴极
B.放电时,Li+从Ⅰ室向Ⅱ室迁移
C.放电时,Ⅱ室LiSO 溶液的浓度增大
2 4
D.每消耗1 mol Mg,电极a质量理论上增加14 g
答案:C
解析:根据放电时电极a发生还原反应知,电极a为正极,Mg电极为负极。
电极 电极反应
负极
Mg-2e-===Mg2+
放电 (Mg电极)
(原电池) 正极
Li FePO +xLi++xe-===LiFePO
(电极a) 1-x 4 4
阴极
Mg2++2e-===Mg
充电 (Mg电极)
(电解池) 阳极
LiFePO -xe-===Li FePO +xLi+
(电极a) 4 1-x 4
由上述分析知,充电时Mg电极为阴极,A项正确;放电时Li+向正极(电极a)移动,
则Li+从Ⅰ室向Ⅱ室迁移,B项正确;放电时,Li+从Ⅰ室向Ⅱ室迁移,SO不参与电极反应,
Ⅱ室LiSO 溶液的浓度不变,C项错误;每消耗1 mol Mg,电路中通过2 mol电子,根据
2 4
电极a的反应,知电极a增加的质量为2 mol Li+的质量,即增重14 g,D项正确。
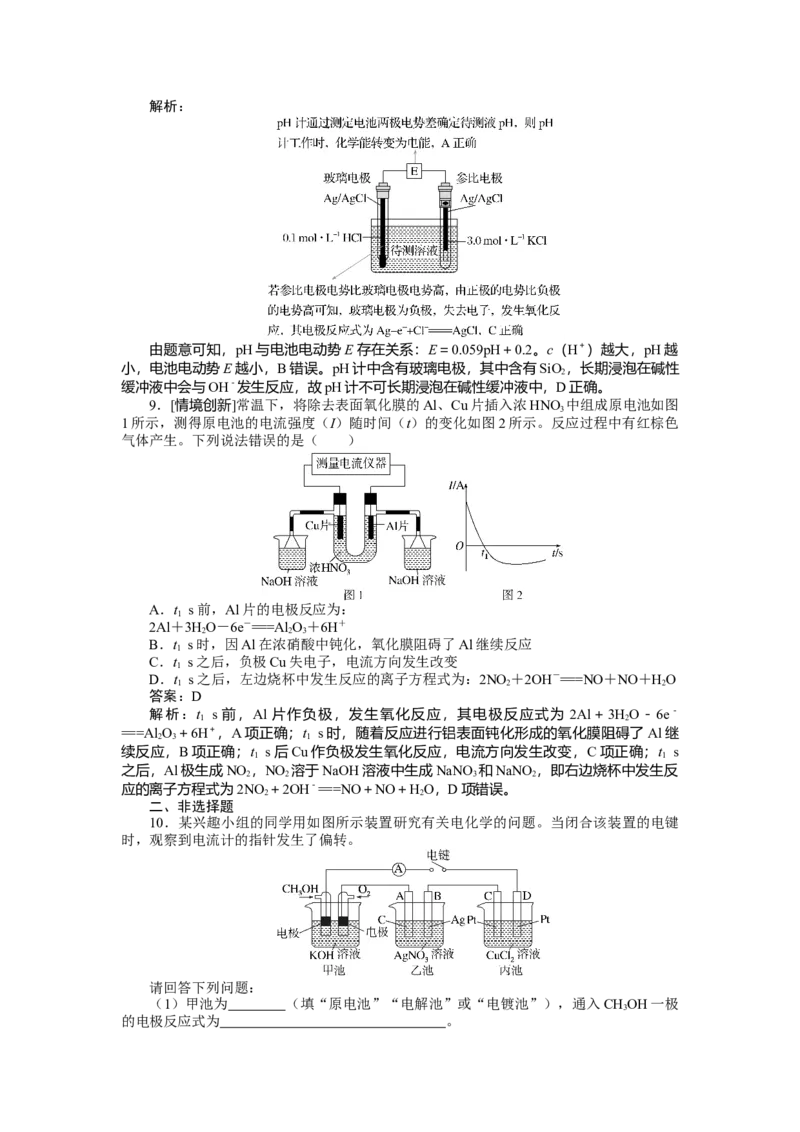
4.[2023·辽宁卷]某低成本储能电池原理如下图所示。下列说法正确的是( )
A.放电时负极质量减小
B.储能过程中电能转变为化学能
C.放电时右侧H+通过质子交换膜移向左侧
D.充电总反应:
Pb+SO+2Fe3+===PbSO+2Fe2+
4
答案:B
解析:该储能电池放电时,Pb为负极,失电子结合硫酸根离子生成PbSO ,则多孔碳
4
电极为正极,正极上Fe3+得电子转化为Fe2+,充电时,多孔碳电极为阳极,Fe2+失电子生成Fe3+,PbSO 电极为阴极,PbSO 得电子生成Pb和硫酸。
4 4
放电时负极上Pb失电子结合硫酸根离子生成PbSO 附着在负极上,负极质量增大,A
4
错误;储能过程中,该装置为电解池,将电能转化为化学能,B正确;放电时,右侧为正
极,电解质溶液中的阳离子向正极移动,左侧的H+通过质子交换膜移向右侧,C错误;充
电时,总反应为PbSO +2Fe2+===Pb+SO+2Fe3+,D错误;故答案选B。
4
5.
[素材创新]手持技术的氧电化学传感器可用于测定O 含量,如图为某种氧电化学传感
2
器的原理示意图。已知在测定O 含量过程中,电解质溶液的质量保持不变。一定时间内,
2
通过传感器的待测气体为a L(标准状况),某电极质量增加了b g。下列说法正确的是(
)
A.Pt电极为负极
B.反应过程中转移OH-的物质的量为0.125b mol
C.Pb电极上发生的电极反应为
Pb-2e-+2OH-===Pb(OH)
2
D.待测气体中氧气的体积分数为
答案:B
解析:结合图示及电解质溶液的质量保持不变进行如下分析:
电极 电极反应
正极(Pt电极) O+4e-+2HO===4OH-
2 2
负极(Pb电极) 2Pb+4OH--4e-===2PbO+2HO
2
则该传感器工作时发生的总反应为2Pb+O===2PbO,Pb电极质量增加。Pt电极通入
2
O ,发生还原反应,该电极为正极,Pb电极为负极,A项错误;根据上述分析可知,质量
2
增加的电极应是Pb电极,且增加的为O元素的质量,由电极反应式可知Pb电极每增加16
g,溶液中转移OH-的物质的量为2 mol,则Pb电极质量增加b g时,转移OH-的物质的
量为 0.125b mol,B 项正确;Pb 电极发生的电极反应为 2Pb+4OH--4e-===2PbO+
2HO,C项错误;Pb电极质量增加b g,消耗的n(O )= mol,其在标准状况下的体积
2 2
为0.7b L,则氧气的体积分数为,D项错误。
6.[2024·重庆育才中学适应考]如图是通过人工光合作用,以CO 和HO为原料制备
2 2
HCOOH和O 的原理示意图,下列说法正确的是( )
2
A.外电路电流方向是a→b
B.电池工作时正极区溶液的pH升高
C.电极b上发生的反应为
CO+2e-+2H+===HCOOH
2
D.1 mol H O被完全氧化时有22.4 L CO 被还原
2 2
答案:C
解析:由图可知,a电极上水失电子生成氧气,电极反应式为2HO-4e-===O ↑+4H
2 2
+,a电极为负极,b电极为正极,原电池外电路电流方向是由电源正极流向负极,即b→a,A项错误;由图可知,负极产生的H+通过质子交换膜迁移到正极区,CO 得电子,
2
反应后生成了酸性较强的甲酸,故正极区溶液的 pH降低,B项错误;电极b为正极,发生
的反应为CO +2e-+2H+===HCOOH,C项正确;由电池总反应式2HO+2CO===O +
2 2 2 2
2HCOOH可知,1 mol H O被完全氧化时有1 mol CO 被还原,但CO 所处的温度和压强未
2 2 2
知,无法确定CO 的体积,D项错误。
2
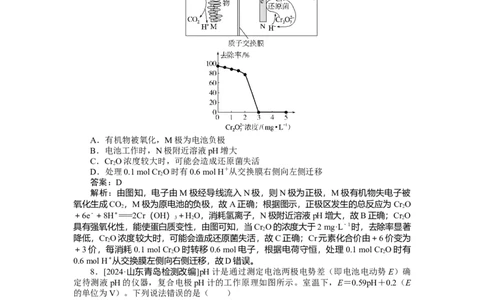
7.[2024·湖南郴州质检]微生物燃料电池在净化废水的同时能获得能源或得到有价值的
化学产品,如图为其工作原理及废水中Cr O浓度与去除率的关系。下列说法不正确的是(
2
)
A.有机物被氧化,M极为电池负极
B.电池工作时,N极附近溶液pH增大
C.Cr O浓度较大时,可能会造成还原菌失活
2
D.处理0.1 mol Cr O时有0.6 mol H+从交换膜右侧向左侧迁移
2
答案:D
解析:由图知,电子由M极经导线流入N极,则N极为正极,M极有机物失电子被
氧化生成CO ,M极为原电池的负极,故A正确;根据图示,正极区发生的总反应为Cr O
2 2
+6e-+8H+===2Cr(OH)+HO,消耗氢离子,N极附近溶液pH增大,故B正确;Cr O
3 2 2
具有强氧化性,能使蛋白质变性,由图可知,当Cr O的浓度大于2 mg·L-1时,去除率显著
2
降低,Cr O浓度较大时,可能会造成还原菌失活,故C正确;Cr元素化合价由+6价变为
2
+3价,每消耗0.1 mol Cr O时转移0.6 mol电子,根据电荷守恒,处理0.1 mol Cr O时有
2 2
0.6 mol H+从交换膜左侧向右侧迁移,故D错误。
8.[2024·山东青岛检测改编]pH计是通过测定电池两极电势差(即电池电动势E)确
定待测液pH的仪器,复合电极pH计的工作原理如图所示。室温下,E=0.59pH+0.2(E
的单位为V)。下列说法错误的是( )
A.pH计工作时,化学能转变为电能
B.一定温度下,电池电动势越小,待测液中c(H+)越小
C.若参比电极电势比玻璃电极电势高,则玻璃电极的电极反应式为 Ag-e-+Cl-
===AgCl
D.pH计不可长期浸泡在碱性缓冲液中
答案:B解析:
由题意可知,pH与电池电动势E存在关系:E=0.059pH+0.2。c(H+)越大,pH越
小,电池电动势E越小,B错误。pH计中含有玻璃电极,其中含有SiO ,长期浸泡在碱性
2
缓冲液中会与OH-发生反应,故pH计不可长期浸泡在碱性缓冲液中,D正确。
9.[情境创新]常温下,将除去表面氧化膜的Al、Cu片插入浓HNO 中组成原电池如图
3
1所示,测得原电池的电流强度(I)随时间(t)的变化如图2所示。反应过程中有红棕色
气体产生。下列说法错误的是( )
A.t s前,Al片的电极反应为:
1
2Al+3HO-6e-===AlO+6H+
2 2 3
B.t s时,因Al在浓硝酸中钝化,氧化膜阻碍了Al继续反应
1
C.t s之后,负极Cu失电子,电流方向发生改变
1
D.t s之后,左边烧杯中发生反应的离子方程式为:2NO +2OH-===NO+NO+HO
1 2 2
答案:D
解析:t s 前,Al 片作负极,发生氧化反应,其电极反应式为 2Al+3HO-6e-
1 2
===AlO +6H+,A项正确;t s时,随着反应进行铝表面钝化形成的氧化膜阻碍了Al继
2 3 1
续反应,B项正确;t s后Cu作负极发生氧化反应,电流方向发生改变,C项正确;t s
1 1
之后,Al极生成NO ,NO 溶于NaOH溶液中生成NaNO 和NaNO ,即右边烧杯中发生反
2 2 3 2
应的离子方程式为2NO +2OH-===NO+NO+HO,D项错误。
2 2
二、非选择题
10.某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键
时,观察到电流计的指针发生了偏转。
请回答下列问题:
(1)甲池为 (填“原电池”“电解池”或“电镀池”),通入CHOH一极
3
的电极反应式为 。(2)乙池中A(石墨)电极的名称为 (填“正极”“负极”“阴极”或“阳
极”),总反应式为 。
(3)当乙池中B极质量增加5.40 g时,甲池中理论上消耗O 的体积为 mL
2
(标准状况),丙池中 极析出 g铜。
(4)若丙池中电极不变,将其溶液换成NaCl溶液,电键闭合一段时间后,甲池中溶
液的pH将 (填“增大”“减小”或“不变”,下同);丙池中溶液的pH将
,若要将丙池中溶液复原,需加入 。
答案:(1)原电池 CHOH-6e-+8OH-===CO+6HO
3 2
(2)阳极 4AgNO+2HO=====4Ag+O↑+4HNO
3 2 2 3
(3)280 D 1.6 (4)减小 增大 HCl
解析:(1)甲池为原电池,通入CHOH的电极为负极,电极反应式为CHOH-6e-
3 3
+8OH-===CO+6HO。(2)乙池中为用惰性电极电解AgNO 溶液,其中A作阳极,B作
2 3
阴极,总反应式为4AgNO+2HO=====4Ag+O↑+4HNO。(3) 乙池中B极质量增加
3 2 2 3
5.40 g为银的质量,则银的物质的量为=0.05 mol,根据电子转移守恒n(Ag)=4n(O )
2
=2n(Cu),故V(O )=×22.4 L·mol-1=0.28 L=280 mL,m(Cu)=×64 g·mol-1=1.6
2
g。(4)若丙池中电极不变,将其溶液换成 NaCl溶液,根据丙池中总反应式2NaCl+
2HO=====2NaOH+H↑+Cl↑可知,溶液pH增大,而甲池中总反应式为2CHOH+3O
2 2 2 3 2
+4KOH===2K CO+6HO,溶液pH减小。
2 3 2