文档内容
机密★启用前
2025 年河北省初中学业水平考试
化学
注意事项:1.本试卷共6页,总分60分,考试时间60分钟。
2.答题前,考生务必将姓名、准考证号填写在试卷和答题卡的相应位置。
3.所有答案均在答题卡上作答,在本试卷或草稿纸上作答无效。答题前,请仔细阅读答题卡
上的“注意事项”,按照“注意事项”的规定答题。
4.答选择题时,用2B铅笔将答题卡上对应题目的答案标号涂黑;答非选择题时,请在答题卡
上对应题目的答题区域内答题。
5.考试结束时,请将答题卡、试卷和草稿纸一并交回。
可能用到的相对原子质量:H1 C12 O16 S32 Zn65
一、选择题(本大题共10小题,每小题2分,共20分。在每小题给出的四个选项中,只有一
项符合题意)
1. 2025年《政府工作报告》提出,持续加强生态环境保护。从绿色低碳的角度考虑,下列能源中最理想
的是
A. 氢能 B. 煤 C. 石油 D. 天然气
【答案】A
【解析】
煤、石油、天然气属于化石燃料,燃烧时会产生大量的二氧化碳气体,以及二氧化硫、二氧化氮、可吸
入颗粒物等污染物, 不符合绿色低碳要求; 氢气燃烧只产生水,无二氧化碳和其他污染物产生,符合绿
色低碳要求。
故选A。
2. 如图所示为探究空气中氧气含量的实验,其中没有用到的仪器是
A. 集气瓶 B. 试管 C. 燃烧匙 D. 烧杯
【答案】B【解析】
由图可知,用到的仪器有集气瓶、燃烧匙、烧杯等,没有用到试管。故选B。
3. “中国水周”期间,学生制作了简易净水器,其中主要用于吸附水中色素的材料是
A. 小卵石 B. 石英砂 C. 活性炭 D. 塑料瓶
【答案】C
【解析】
A. 小卵石在简易净水器中主要起过滤较大颗粒不溶性杂质的作用,不能吸附色素。选项错误;
B. 石英砂主要是进一步过滤较小颗粒的不溶性杂质,不具备吸附色素的功能。选项错误;
C. 活性炭具有疏松多孔的结构,有很强的吸附性,能够吸附水中的色素和异味,可用于简易净水器中吸
附色素,选项正确;
D. 塑料瓶是简易净水器的容器,不参与吸附色素等净水过程。选项错误;
故选C。
4. 我国“神舟”系列载人飞船的发射均取得圆满成功,飞船使用的某种发动机利用了反应:
,该反应属于
A. 分解反应 B. 化合反应 C. 置换反应 D. 复分解反应
【答案】A
【解析】
,该反应符合“一变多”的特点,属于基本反应类型中的分解
反应,故选:A。
5. 我国科研团队设计的一种锂载体分子 可无损修复废旧锂离子电池。 由碳、氟、
硫、氧、锂元素组成,上述元素属于非金属元素的有
A. 2种 B. 3种 C. 4种 D. 5种
【答案】C
【解析】
CF SO Li由碳、氟、硫、氧、锂元素组成,其中锂带“钅”字旁,属于金属元素;碳、硫带“石”字
3 3
旁,属于固态非金属元素;氟、氧带“气”字头,属于非金属元素;故上述元素属于非金属元素的有4种,
故选:C。
6. 我国科研人员在二氧化钛( )里混入 的稀土元素钪,制备出新型光解水催化材料,如图为元素周期表中钪元素的信息。下列说法错误的是
A. 中钛元素的化合价为+4 B. 属于氧化物
C. 钪的相对原子质量为44.96g D. 钪的原子序数为21
【答案】C
【解析】
A、 中O元素为-2价,设Ti化合价为x,根据化合物中各元素正负化合价代数和为0,则x +
2×(-2)=0 , x=+4,选项正确;
B、氧化物是由两种元素组成,其中一种是氧元素的化合物, 由钛和氧两种元素组成,属于氧化物,
选项正确;
C、在元素周期表的一格中,名称下方的数字为相对原子质量,故钪的相对原子质量为44.96,相对原子质
量的单位是“1”,省略不写,不是“g”,选项错误;
D、元素周期表单元格中,左上角数字表示原子序数,钪的原子序数为21,选项正确;
故选C。
7. 如图所示为一种多灯头便携式热源,罐内装有环保矿物油,使用时点燃灯头。下列说法错误的是
A. 矿物油具有可燃性
B. 点燃灯头过程中提高了矿物油的着火点
C. 点燃不同数量的灯头可调控火力大小
D. 将火焰盖灭应用的灭火原理是隔绝空气
【答案】B
【解析】
A、矿物油属于可燃物,具有可燃性,选项正确;
B、点燃灯头过程,是提供热量,使温度达到矿物油的着火点,着火点是物质的固有属性,不会因点燃过
程而改变。选项错误;C、多灯头设计通过控制点燃数量来调节总热量输出,实现火力调控。选项正确;
D、燃烧需要可燃物与氧气接触,盖灭火焰是通过隔绝氧气(空气)的灭火原理,选项正确;
故选B。
8. 如图所示为某班学生用废旧金属制作班徽的过程。下列说法错误的是
A. ①中利用了铁能被磁铁吸引的性质 B. ②中稀盐酸可用氯化钠溶液替代
C. ④中铁板上会出现红色图案 D. ⑤中塑封是为了防止班徽生锈
【答案】B
【解析】
A、用磁铁选出废铁板,利用了铁能被磁铁吸引的性质,故选项说法正确。
B、铁不能与氯化钠反应,②中稀盐酸不能用氯化钠溶液替代,故选项说法错误。
C、铁和硫酸铜反应生成硫酸亚铁和铜,④中铁板上会出现红色图案,故选项说法正确。
D、铁与氧气、水充分接触时容易生锈,⑤中塑封能隔绝氧气和水,是为了防止班徽生锈,故选项说法正
确。
故选B。
9. 下列实验方案不能达到实验目的的是
选
实验目的 实验方案
项
A 鉴别白醋和食盐水 闻气味
B 鉴别硝酸铵和氢氧化钠 加水溶解,测量温度变化
C 除去氮气中的水蒸气 通过足量浓硫酸
D 除去氧化铜中的铜粉 加入足量稀硫酸,过滤
A. A B. B C. C D. D
【答案】D
【解析】
A、白醋有刺激性气味,食盐水无特殊气味,闻气味可鉴别二者,A 能达到实验目的;
B、硝酸铵溶于水吸热,温度降低;氢氧化钠溶于水放热,温度升高,加水溶解测温度变化可鉴别,B 能
达到实验目的;C、浓硫酸具有吸水性,且不与氮气反应,通过足量浓硫酸可除去氮气中的水蒸气,C 能达到实验目的;
D、氧化铜能与稀硫酸反应生成硫酸铜和水( ),铜粉不与稀硫酸反应。加
入足量稀硫酸会把原物质氧化铜除去,不能达到除去氧化铜中铜粉的目的,D不能达到实验目的。
故选D。
10. 常温下,某小组同学向氢氧化钠溶液a中加水,向氢氧化钠溶液b中逐滴加稀盐酸,利用pH传感器分
别测得溶液pH的变化如图1、图2所示。下列说法正确的是
A. 图1:M点时的溶液能使石蕊溶液变红
的
B. 图1:向N点时 溶液中加大量水可使溶液的
C. 图2:向P点时的溶液中加入锌粒能产生气泡
D. 图2:Q→S过程中溶液中氯化钠的质量分数逐渐减小
【答案】D
【解析】
A、M点时的溶液pH>7,显碱性,能使紫色石蕊溶液变蓝,选项错误;
B、M点时的溶液pH>7,显碱性,向其中加大量水,溶液碱性逐渐减弱,pH逐渐减小,但pH始终大于
7,选项错误;
C、氢氧化钠溶液显碱性,pH大于7,稀盐酸显酸性,pH小于7,氢氧化钠与盐酸反应生成氯化钠和水,
氯化钠溶液显中性,pH等于7,P点溶液pH等于7,此时氢氧化钠与盐酸恰好完全反应,溶液中只含有一
种溶质氯化钠,加入锌粒不会产生气体,选项错误;
D、Q→S过程盐酸过量,没有反应发生,溶液中氯化钠质量不变,但溶液质量随着盐酸的加入而逐渐增大,
故溶液中氯化钠的质量分数逐渐减小,选项正确;
故选D。
二、非选择题(本大题共8小题,共40分)
11. 河北省在盐碱地治理与利用方面持续发力,让盐碱地成为农业发展的新沃土。
(1)培肥“控”盐、节水“阻”盐是常用的盐碱地治理方法。磷酸二氢钙 是一种土壤改良剂,属于___________(填“氮肥”“磷肥”或“钾肥”);写出一种节水灌溉的方法:___________。
(2)河北省持续培育旱碱麦新品种,亩产大幅度提高。旱碱麦富含的淀粉和蛋白质均属于___________(填
“无机物”或“有机物”);旱碱麦还富含多种元素,其中___________(填“铁”“锌”或“钾”)元素的
适量摄入有利于血红蛋白的合成,可预防贫血。
【答案】
(1)①.磷肥 ②.滴灌(或喷灌)
(2)①.有机物 ②.铁
【解析】
【小问1详解】
磷酸二氢钙 是一种土壤改良剂,属于磷肥;节水灌溉的方法有滴灌、喷灌等;
【小问2详解】
旱碱麦富含的淀粉和蛋白质均属于有机物;.
旱碱麦还富含多种元素,其中铁元素的适量摄入有利于血红蛋白的合成,可预防贫血。
12. 文字的载体——甲骨、青铜器、简牍、丝帛和纸张等,在中华文明传承过程中发挥了重要作用。
(1)在甲骨和青铜器上刻字,属于___________(填“物理”或“化学”)变化。
(2)简牍探中华,帛书藏春秋。竹简、丝帛中的纤维都属于___________(填“天然”或“合成”)纤维;
用墨在竹简、丝帛上书写的文字历经千年而不变色,其主要原因是常温下碳单质的化学性质___________。
(3)纸书《天工开物》中有锻造铁器的记载,“受锻之时,十耗其三为铁华、铁落”。“铁华、铁落”
中含有四氧化三铁,铁燃烧生成四氧化三铁的化学方程式为___________。
【答案】
(1)物理
(2)①.天然 ②. 稳定(或不活泼)
(3)
【解析】
【小问1详解】
在甲骨和青铜器上刻字,只是形状发生改变,没有新物质生成,属于物理变化。
【小问2详解】
竹简、丝帛中的纤维均是自然界原有的或经人工培植的植物上、人工饲养的动物上直接取得的纺织纤维,
都属于天然纤维;
墨是用炭黑制成的,炭黑的主要成分是碳,用墨在竹简、丝帛上书写的文字历经千年而不变色,其主要原因是常温下碳单质的化学性质不活泼。
【小问3详解】
铁燃烧生成四氧化三铁,化学方程式为 。
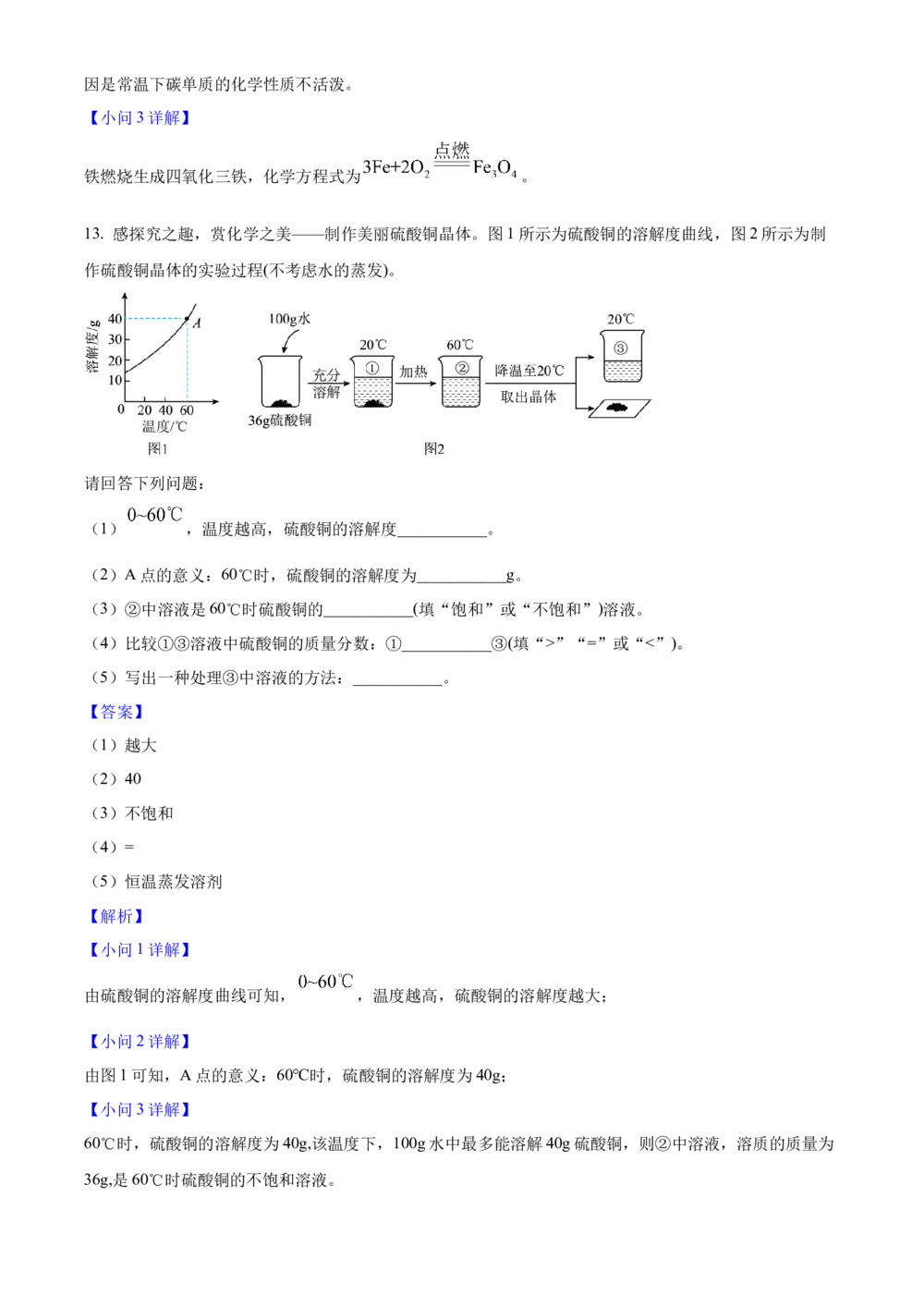
13. 感探究之趣,赏化学之美——制作美丽硫酸铜晶体。图1所示为硫酸铜的溶解度曲线,图2所示为制
作硫酸铜晶体的实验过程(不考虑水的蒸发)。
请回答下列问题:
(1) ,温度越高,硫酸铜的溶解度___________。
(2)A点的意义:60℃时,硫酸铜的溶解度为___________g。
(3)②中溶液是60℃时硫酸铜的___________(填“饱和”或“不饱和”)溶液。
(4)比较①③溶液中硫酸铜的质量分数:①___________③(填“>”“=”或“<”)。
(5)写出一种处理③中溶液的方法:___________。
【答案】
(1)越大
(2)40
(3)不饱和
(4)=
(5)恒温蒸发溶剂
【解析】
【小问1详解】
由硫酸铜的溶解度曲线可知, ,温度越高,硫酸铜的溶解度越大;
【小问2详解】
由图1可知,A点的意义:60℃时,硫酸铜的溶解度为40g;
【小问3详解】
60℃时,硫酸铜的溶解度为40g,该温度下,100g水中最多能溶解40g硫酸铜,则②中溶液,溶质的质量为
36g,是60℃时硫酸铜的不饱和溶液。【小问4详解】
由图2可知,20℃时向36g硫酸铜中加入100g水,充分溶解后得到①,升温至60℃得到②,再降温至
20℃过滤出晶体得到③,则③中溶液与①中溶液均为20℃时硫酸铜的饱和溶液,因此①③溶液中硫酸铜的
质量分数:①=③;
【小问5详解】
③中溶液为20℃时硫酸铜的饱和溶液,则处理③中溶液的方法可以是恒温蒸发溶剂,使硫酸铜结晶析出。
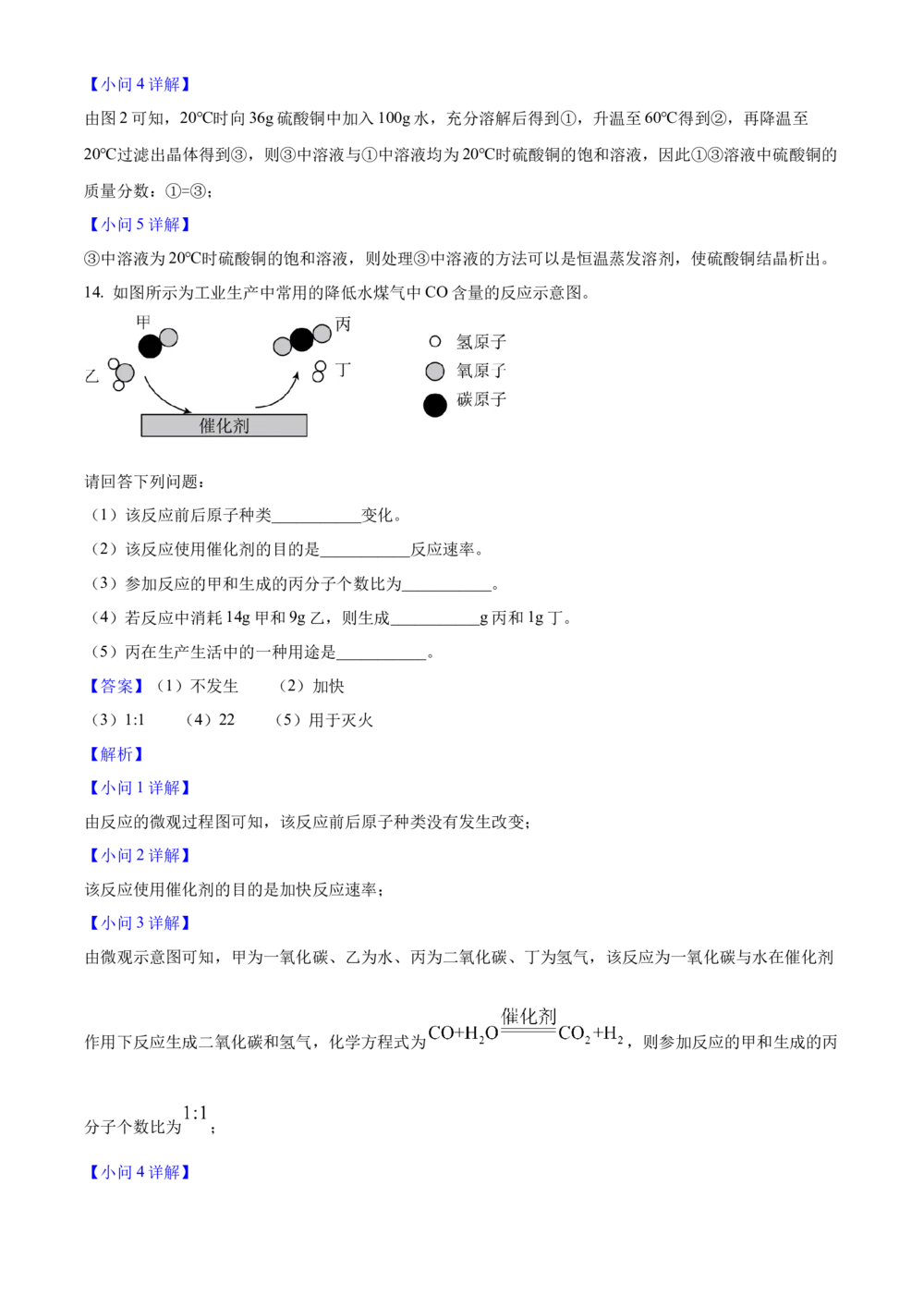
14. 如图所示为工业生产中常用的降低水煤气中CO含量的反应示意图。
请回答下列问题:
(1)该反应前后原子种类___________变化。
(2)该反应使用催化剂的目的是___________反应速率。
(3)参加反应的甲和生成的丙分子个数比为___________。
(4)若反应中消耗14g甲和9g乙,则生成___________g丙和1g丁。
(5)丙在生产生活中的一种用途是___________。
【答案】(1)不发生 (2)加快
(3)1:1 (4)22 (5)用于灭火
【解析】
【小问1详解】
由反应的微观过程图可知,该反应前后原子种类没有发生改变;
【小问2详解】
该反应使用催化剂的目的是加快反应速率;
【小问3详解】
由微观示意图可知,甲为一氧化碳、乙为水、丙为二氧化碳、丁为氢气,该反应为一氧化碳与水在催化剂
作用下反应生成二氧化碳和氢气,化学方程式为 ,则参加反应的甲和生成的丙
分子个数比为 ;
【小问4详解】由第(3)小问分析可知,甲为一氧化碳、乙为水、丙为二氧化碳、丁为氢气,该反应的化学方程式为
,一氧化碳、水、二氧化碳、氢气的质量比为
,因此若反应中消耗14g甲和9g乙,则生成22g
丙和1g丁;
【小问5详解】
由微观示意图可知,丙为二氧化碳,二氧化碳不能燃烧且不支持燃烧,可用于灭火。
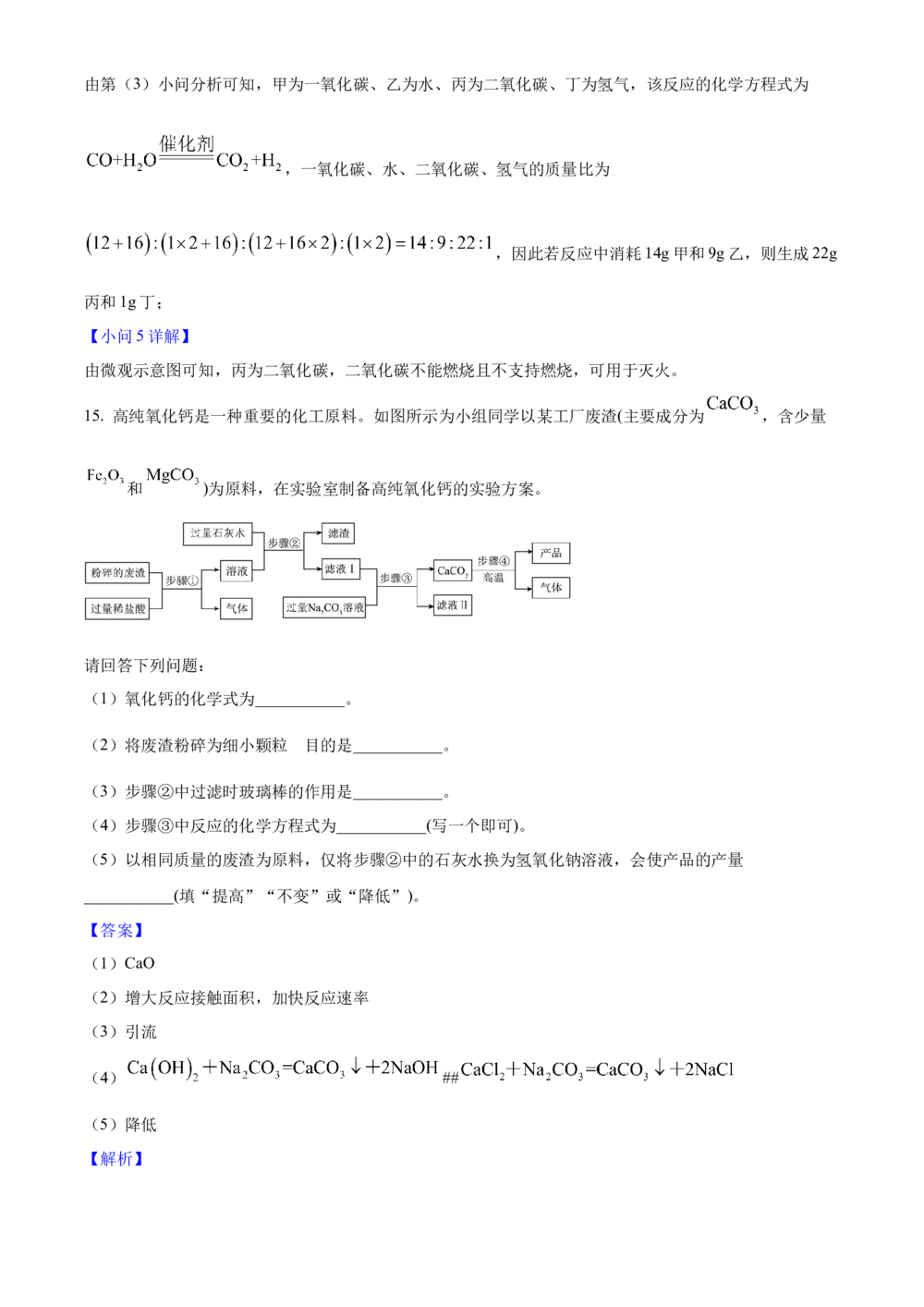
15. 高纯氧化钙是一种重要的化工原料。如图所示为小组同学以某工厂废渣(主要成分为 ,含少量
和 )为原料,在实验室制备高纯氧化钙的实验方案。
请回答下列问题:
(1)氧化钙的化学式为___________。
的
(2)将废渣粉碎为细小颗粒 目的是___________。
(3)步骤②中过滤时玻璃棒的作用是___________。
(4)步骤③中反应的化学方程式为___________(写一个即可)。
(5)以相同质量的废渣为原料,仅将步骤②中的石灰水换为氢氧化钠溶液,会使产品的产量
___________(填“提高”“不变”或“降低”)。
【答案】
(1)CaO
(2)增大反应接触面积,加快反应速率
(3)引流
(4) ##
(5)降低
【解析】【小问1详解】
氧化钙中钙元素显+2价,氧元素显-2价,根据化合物中正负化合价代数和为零,其化学式为CaO;
【小问2详解】
将废渣粉碎为细小颗粒的目的是增大反应物之间的接触面积,能使反应更充分;
【小问3详解】
过滤时玻璃棒的作用是引流,防止液体洒出;
【小问4详解】
步骤①中加入过量的盐酸,盐酸与碳酸钙反应生成氯化钙、水和二氧化碳,与碳酸镁反应生成氯化镁、水
和二氧化碳,与氧化铁反应生成氯化铁和水,溶液中含有氯化钙、氯化镁、氯化铁和盐酸;步骤②加入过
量的石灰水,氢氧化钙与氯化镁反应生成氢氧化镁沉淀和氯化钙,与氯化铁反应生成氢氧化铁沉淀和氯化
钙,过滤得到的滤液中含有氯化钙、氢氧化钙,碳酸钠与氢氧化钙反应生成碳酸钙和氢氧化钠,与氯化钙
反应生成碳酸钙和氯化钠,方程式分别为: 、
;
【小问5详解】
石灰水与二氧化碳、氯化镁等反应会生成沉淀等物质,而氢氧化钠溶液与二氧化碳反应生成碳酸钠和水,
与氯化镁反应生成氢氧化镁沉淀和氯化钠,没有将废渣中的钙元素完全转化为碳酸钙沉淀,所以以相同质
量的废渣为原料,仅将步骤②中的石灰水换为氢氧化钠溶液,会使产品的产量降低。
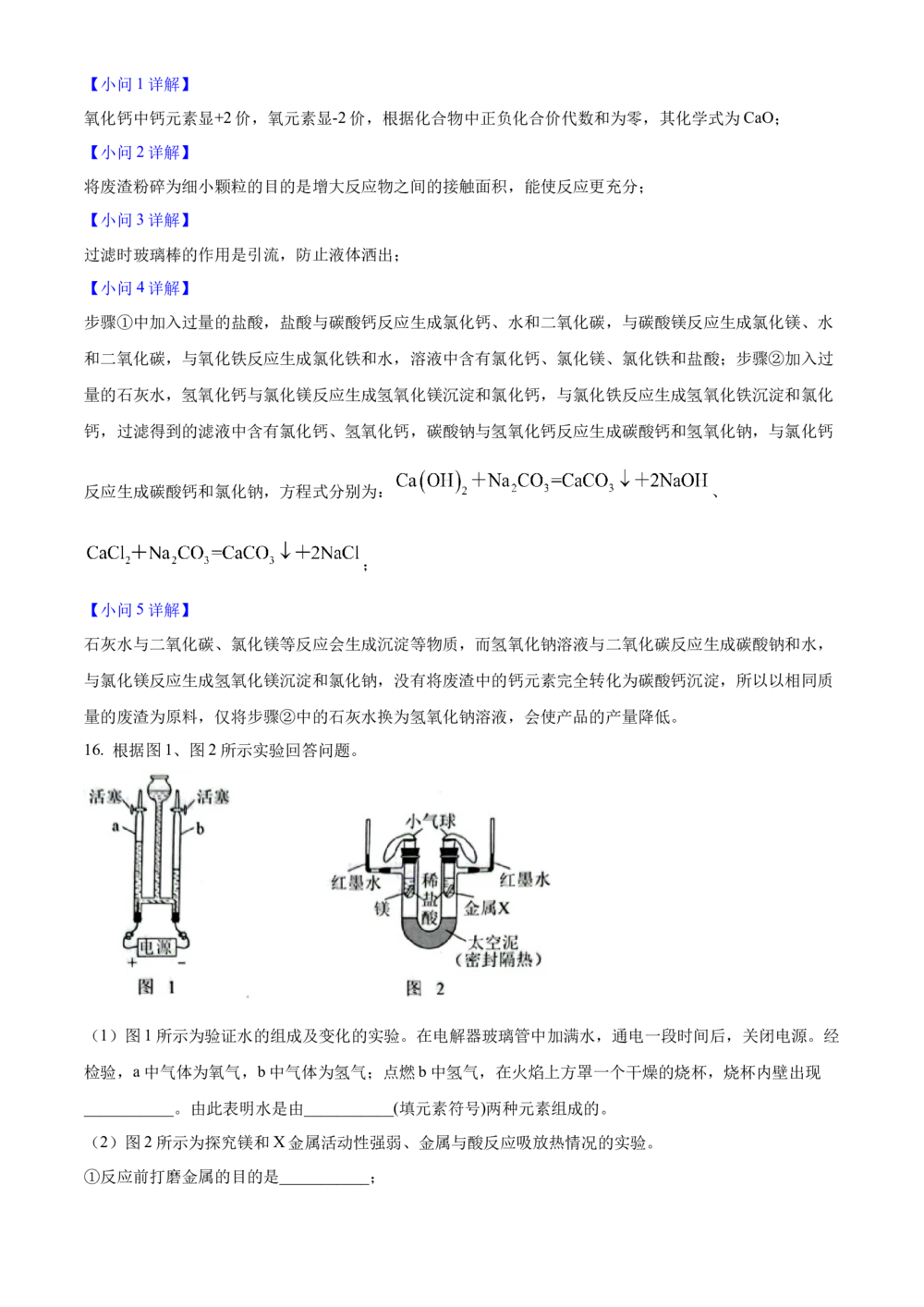
16. 根据图1、图2所示实验回答问题。
(1)图1所示为验证水的组成及变化的实验。在电解器玻璃管中加满水,通电一段时间后,关闭电源。经
检验,a中气体为氧气,b中气体为氢气;点燃b中氢气,在火焰上方罩一个干燥的烧杯,烧杯内壁出现
___________。由此表明水是由___________(填元素符号)两种元素组成的。
(2)图2所示为探究镁和X金属活动性强弱、金属与酸反应吸放热情况的实验。
①反应前打磨金属的目的是___________;②左侧有气泡,右侧无气泡,说明镁的金属活动性比X___________;
③得出镁和稀盐酸反应放热,依据的现象:一是左侧小气球先胀大后轻微缩小,二是___________。
【答案】
(1) ①. 水雾 ②. H、O
(2) ①. 除去金属表面氧化物及污物,防止干扰实验 ②. 强 ③. 左侧红墨水液面先上升后恢
复至原状
【解析】
【小问1详解】
氢气在氧气中燃烧生成水,则点燃b中氢气,在火焰上方罩一个干燥的烧杯,烧杯内壁出现水雾;
电解水生成氢气和氧气,根据质量守恒定律,化学反应前后元素种类不变,氢气由氢元素组成,氧气由氧
的
元素组成,由此表明水是由H、O两种元素组成 ;
【小问2详解】
①反应前打磨金属的目的是除去金属表面氧化物及污物,防止干扰实验;
②左侧有气泡,说明镁能与稀盐酸反应生成氢气,则金属活动性 ;右侧无气泡,说明金属X与稀
盐酸不反应,则金属活动性 ,由此说明镁的金属活动性比X强;
③得出镁和稀盐酸反应放热,依据的现象:一是左侧小气球先胀大后轻微缩小,二是左侧红墨水液面先上
升后恢复至原状。
17. 供氧自救器可用于生产生活中遇到有害气体时应急自救,某兴趣小组探究并自制了供氧自救器。
活动I:探究供氧自救器
【分析原理】为防止人体吸入有害气体,使用自救器时夹住鼻子,只用嘴呼吸,使气体在“气囊 人体
清洁罐 气囊”间形成循环(如图1所示)。
【交流讨论】
(1)用氧气瓶为人体提供氧气,是因为氧气能供给___________。
(2)氧气经压缩储存于氧气瓶中,从微观角度分析,氧气可被压缩是因为___________。(3) 清洁罐中填充有 吸收剂。小组同学讨论后认为:氢氧化钠和氢氧化钙均可吸收 ,理由
是___________。资料显示:氢氧化钠比氢氧化钙价格高,且具有强烈的腐蚀性。故实际选用氢氧化钙作
吸收剂。
活动II:自制简易供氧自救器
小组同学利用化学方法提供氧气,制作简易供氧自救器。
【回忆旧知】
(4)获取氧气的化学方法:
一是加热高锰酸钾,反应的化学方程式为___________;
二是混合过氧化氢溶液和二氧化锰,反应的化学方程式为 。
小组同学经讨论选择了第二种方法。
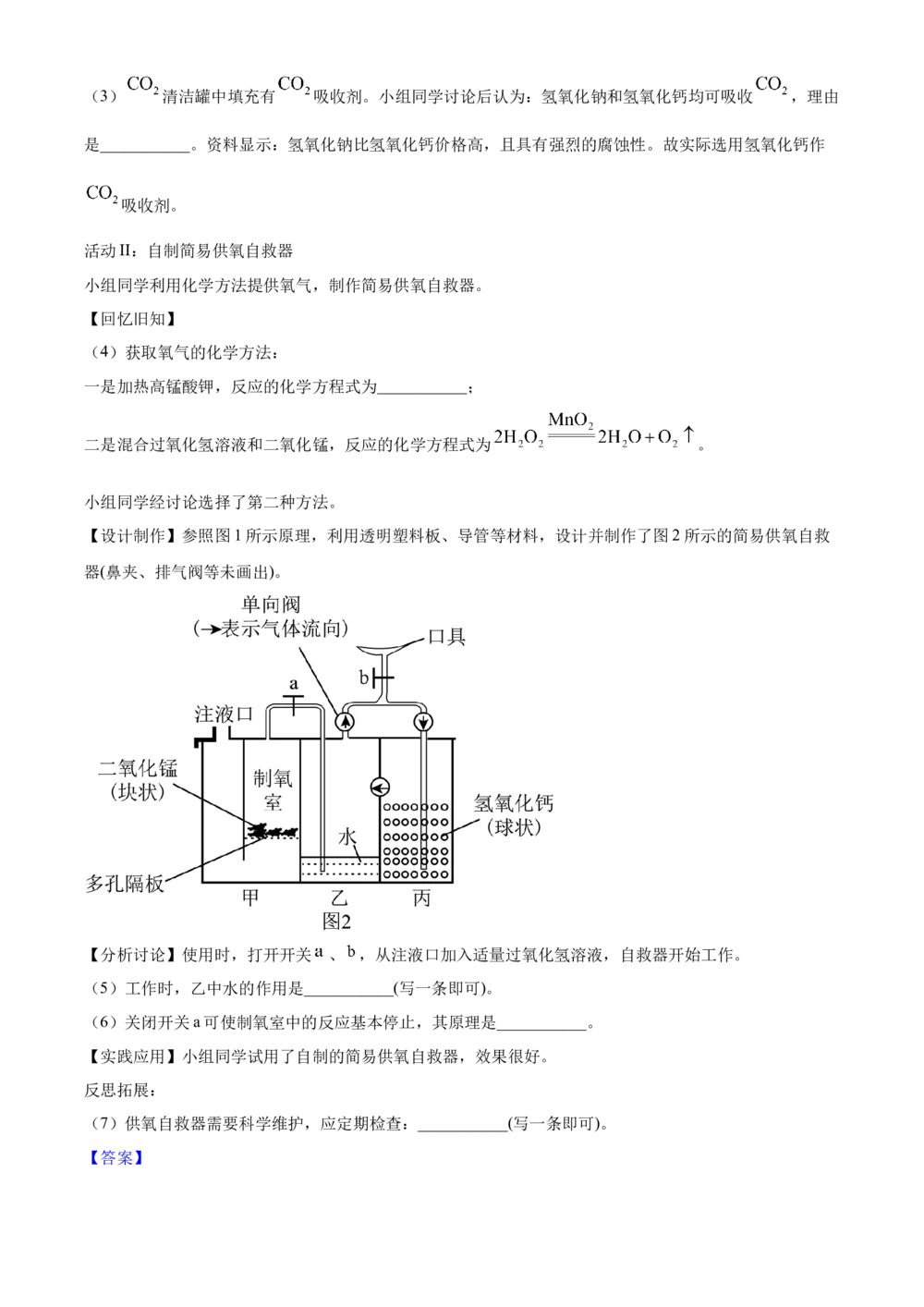
【设计制作】参照图1所示原理,利用透明塑料板、导管等材料,设计并制作了图2所示的简易供氧自救
器(鼻夹、排气阀等未画出)。
【分析讨论】使用时,打开开关 、 ,从注液口加入适量过氧化氢溶液,自救器开始工作。
(5)工作时,乙中水的作用是___________(写一条即可)。
(6)关闭开关a可使制氧室中的反应基本停止,其原理是___________。
【实践应用】小组同学试用了自制的简易供氧自救器,效果很好。
反思拓展:
(7)供氧自救器需要科学维护,应定期检查:___________(写一条即可)。
【答案】(1)
(2)分子之间有间隔,压缩时分子间隔减小
(3)氢氧化钠和氢氧化钙都能与二氧化碳发生化学反应
(4)
(5)湿润氧气(或冷却氧气、观察氧气流速等)
(6)制氧仓中压强增大,将液体逐渐下降到隔板下方,固液分离,从而反应停止
(7)氧气瓶的气密性(开关是否灵活等)
【解析】
【小问1详解】
用氧气瓶为人体提供氧气,是因为氧气能供给呼吸;
【小问2详解】
氧气经压缩储存于氧气瓶中,从微观角度分析,氧气可被压缩是因为分子间有间隔;
【小问3详解】
氢氧化钠与二氧化碳反应生成碳酸钠和水,氢氧化钙与二氧化碳反应生成碳酸钙和水,两者都能与二氧化
碳反应,故都能用于吸收二氧化碳;
【小问4详解】
高锰酸钾加热生成锰酸钾、二氧化锰和氧气,方程式为: ;
【小问5详解】
工作时,乙中水的作用是液封、观察氧气的输出速率和给氧气降温除去氧气中的杂质等;
【小问6详解】
关闭开关a可使制氧室中的反应基本停止,其原理是关闭开关a,制氧室中压强增大,使过氧化氢溶液和二
氧化锰分离,反应基本停止;
【小问7详解】
供氧自救器需要科学维护,应定期检查氧气瓶 的气密性、开关是否灵活、二氧化碳吸收剂是否有效等合理
即可。
18. 炉甘石洗剂可用于皮肤止痒,其中的炉甘石主要成分为 。为测定某炉甘石洗剂中 的质
量分数,从混合均匀的洗剂中取出100g,向其中加入过量稀硫酸,充分反应后,生成4.4g二氧化碳(只有
与稀硫酸反应生成二氧化碳,且二氧化碳全部逸出)。请回答:(1)稀硫酸过量时,所得溶液中溶质主要为 和___________(写化学式)。
(2)该洗剂中 的质量分数。(要求有必要的化学方程式和计算步骤)
【答案】
(1)
(2)解:设100g洗剂中碳酸锌的质量为x。
则该洗剂中 的质量分数为
答:该洗剂中 的质量分数为12.5%。
【解析】
【小问1详解】
炉甘石主要成分为ZnCO 和稀硫酸反应生成硫酸锌、二氧化碳和水,由于稀硫酸过量,则所得溶液中溶
3
质主要为生成的ZnSO 和过量的H SO ;
4 2 4
【小问2详解】
计算过程见答案。