文档内容
机密★启用前
注意事项:
1.本试赛分试题客和答题卡两部分。考试时间为120分钟。满分140分。其中物理80分,
化学60分。
2.考生在答题前请阅读答题卡中的“注意事项“,然后按要求答题。
3.所有答案均确微在答题卡相应区城,做在其他区城无效。
4.可能用到的相对原于质量:H-1 C-12 O-16 C1-35.5 N-23 Fe-56 Ca-40
第I卷(选择题共50分)
1.空气中体职分数约占21%的是
A.氮气 B.氧气 C.二氧化碳 D.稀有气体
2.合理施用化学肥料是农作物增产的途径之一,下列化学肥料属于复合肥料的是
A. Ca(PO) B. CO(NH ) C. KCO D.NH HPO
4 2 2 2 2 3 4 4
3.在水转化为水蒸气的过程中,发生改变的是
A.分子间距 B.分子大小 C.分子数量 D.原子大小
4.下列物质中富含蛋白质的是
A.葡萄干 B.白砂糖 C.鲜鸡蛋 D.植物油
5.下列描述中,属于物质的化学性质的是
A.盐酸易挥发 B.金属具有导电性 C.酒精易溶于水 D.常温下,氮气很稳定
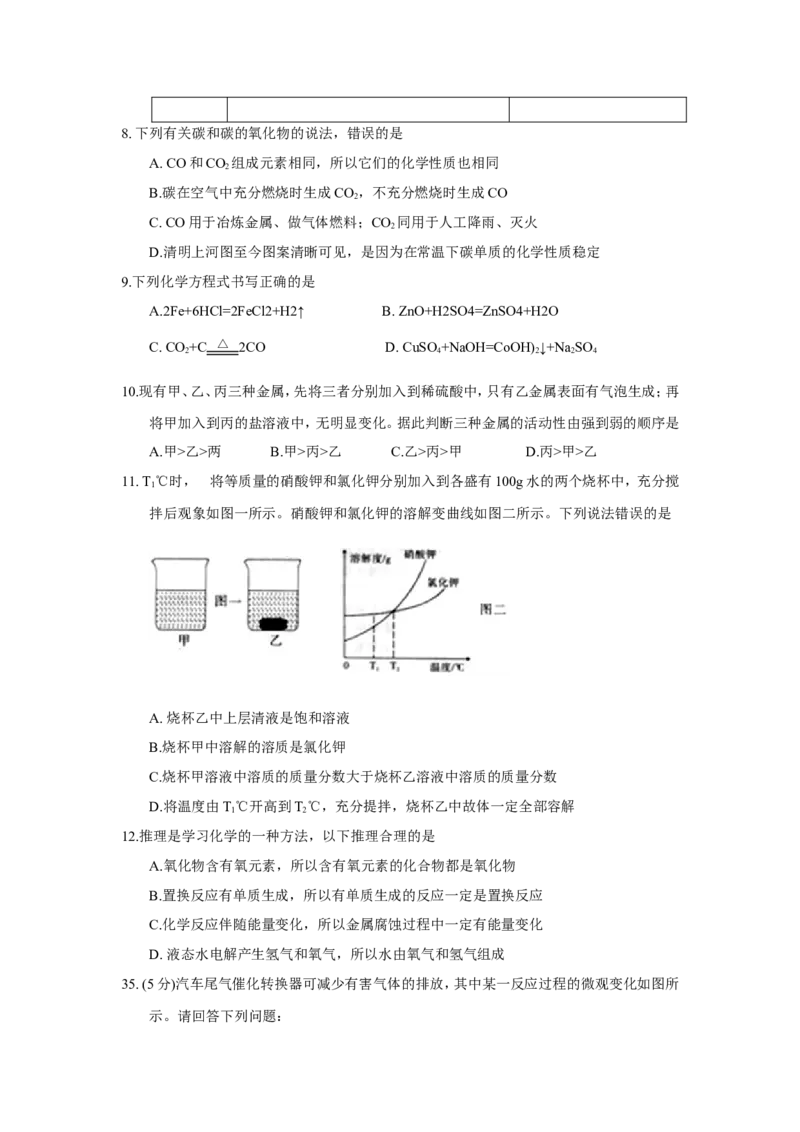
6. 小明从下列某粒于结构示意图中,获取了下列信息,其中错误的是
A.表示阴离子 B.核电荷数为12 C.有两个电子层 D. 表示相对稳定结构
7.下列物质的分类正确的是
选项 物质 分类
A 石油、煤、氢气 化石燃料
B C 、H、水银 单质
60 2
C 纯碱、烧碱、Ba(OH) 碱
2
D CH、Fe O、醋酸 有机物
4 3 48. 下列有关碳和碳的氧化物的说法,错误的是
A. CO和CO 组成元素相同,所以它们的化学性质也相同
2
B.碳在空气中充分燃烧时生成CO,不充分燃烧时生成CO
2
C. CO用于冶炼金属、做气体燃料;CO 同用于人工降雨、灭火
2
D.清明上河图至今图案清晰可见,是因为在常温下碳单质的化学性质稳定
9.下列化学方程式书写正确的是
A.2Fe+6HCl=2FeCl2+H2↑ B. ZnO+H2SO4=ZnSO4+H2O
C. CO+C △ 2 C O D. CuSO +NaOH=CoOH) ↓+NaSO
2 4 2 2 4
10.现有甲、乙、丙三种金属,先将三者分别加入到稀硫酸中,只有乙金属表面有气泡生成;再
将甲加入到丙的盐溶液中,无明显变化。据此判断三种金属的活动性由强到弱的顺序是
A.甲>乙>两 B.甲>丙>乙 C.乙>丙>甲 D.丙>甲>乙
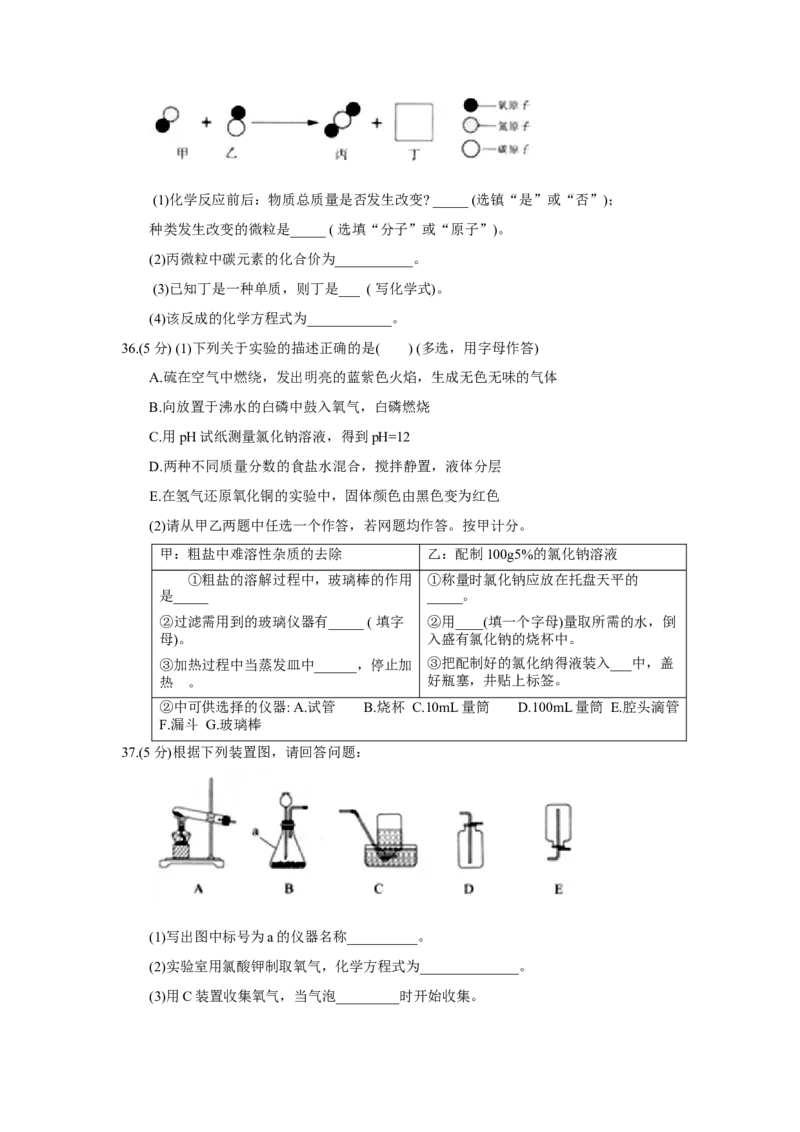
11. T℃时, 将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅
1
拌后观象如图一所示。硝酸钾和氯化钾的溶解变曲线如图二所示。下列说法错误的是
A. 烧杯乙中上层清液是饱和溶液
B.烧杯甲中溶解的溶质是氯化钾
C.烧杯甲溶液中溶质的质量分数大于烧杯乙溶液中溶质的质量分数
D.将温度由T℃开高到T℃,充分提拌,烧杯乙中故体一定全部容解
1 2
12.推理是学习化学的一种方法,以下推理合理的是
A.氧化物含有氧元素,所以含有氧元素的化合物都是氧化物
B.置换反应有单质生成,所以有单质生成的反应一定是置换反应
C.化学反应伴随能量变化,所以金属腐蚀过程中一定有能量变化
D. 液态水电解产生氢气和氧气,所以水由氧气和氢气组成
35. (5分)汽车尾气催化转换器可减少有害气体的排放,其中某一反应过程的微观变化如图所
示。请回答下列问题:(1)化学反应前后:物质总质量是否发生改变? _____ (选镇“是”或“否”);
种类发生改变的微粒是_____ ( 选填“分子”或“原子”)。
(2)丙微粒中碳元素的化合价为___________。
(3)已知丁是一种单质,则丁是___ ( 写化学式)。
(4)该反成的化学方程式为____________。
36.(5分) (1)下列关于实验的描述正确的是( ) (多选,用字母作答)
A.硫在空气中燃绕,发出明亮的蓝紫色火焰,生成无色无味的气体
B.向放置于沸水的白磷中鼓入氧气,白磷燃烧
C.用pH试纸测量氯化钠溶液,得到pH=12
D.两种不同质量分数的食盐水混合,搅拌静置,液体分层
E.在氢气还原氧化铜的实验中,固体颜色由黑色变为红色
(2)请从甲乙两题中任选一个作答,若网题均作答。按甲计分。
甲:粗盐中难溶性杂质的去除 乙:配制100g5%的氯化钠溶液
①粗盐的溶解过程中,玻璃棒的作用 ①称量时氯化钠应放在托盘天平的
是_____ _____。
②过滤需用到的玻璃仪器有_____ ( 填字 ②用____(填一个字母)量取所需的水,倒
母)。 入盛有氯化钠的烧杯中。
③加热过程中当蒸发皿中______,停止加 ③把配制好的氯化纳得液装入___中,盖
热 。 好瓶塞,井贴上标签。
②中可供选择的仪器: A.试管 B.烧杯 C.10mL量筒 D.100mL量筒 E.腔头滴管
F.漏斗 G.玻璃棒
37.(5分)根据下列装置图,请回答问题:
(1)写出图中标号为a的仪器名称__________。
(2)实验室用氯酸钾制取氧气,化学方程式为______________。
(3)用C装置收集氧气,当气泡_________时开始收集。(4)实验室制取二氧化碳应选择的收果装置是_____ (填字母序号)。
(5)用B装置制气体时,长颈漏斗的下端管口要______ ,以防止生成的气体逸用。
38. (5分)松花皮蛋是黄石八珍之一。腌制皮置的一种原料是由NaC1、CaO和NaCO 组成的
2 3
固体混合物。某化学兴题小组用该原料,在实验室进行如下实验:将该固体混合物放入
烧杯中,加入足量的蒸馏水。充分溶解后过滤,得到白色沉淀和无色澄清滤液。同学们对
滤液的溶质成分进行了探究。
请完成以下探究过程,并将①~⑤处答案填入答题卡相应位置。
固体溶解过程中发生了两个化学反应: CaO+H O=Ca(OH) _______。
2 2
【提出问题】滤液中的溶质成分是什么?
【作出猜想】I.解质为: NaC1、NaOH、 Ca(OH) ;
2
II.溶质为: NaC1、NaOH;
III.溶质为:___ ②___。
【设计方案】
实验操作 现象 结论
取少量滤液于试管中, ___ ③ ___ 猜想I正确
向其中滴加碳酸钠钠溶液
另取少量滤液于试管中,向 有气泡产生 猜想III正确
其中滴加__④___溶液。(填
化学式)
【交流反思】兴趣小组经过讨论认为:
若猜想II正确,该原料中CaO与NaCO 的质量比为_____⑤______。
2 3
39. (5分)某兴题小组用铝简制备A1 O 及明矾大晶体,具体流程如下:
2 3
已知:明矾在水中的溶解度随着温度的升高而增大,请回答下列问题:
(1)步骤II中发生反应的化学方程式为:NaAlO+CO +2H O= Al(OH) ↓+X(方程式已
2 2 2 3
配平)。X的化学式为_____________。
(2)少骤III中发生的反应,其基本反应类型为__________。
(3)写出Al(OH) 与硫酸反应的化学方程式____________。
3
(4)在培养明矾大晶体的过程中,其操作的先后顺序为__________。
A. 自然冷却至室温
B. 选规则明矾小晶体,并用一根细线悬挂在溶液中央C. 配制45℃的明矾饱和溶液
(5)写出明矾的一种用途__________。
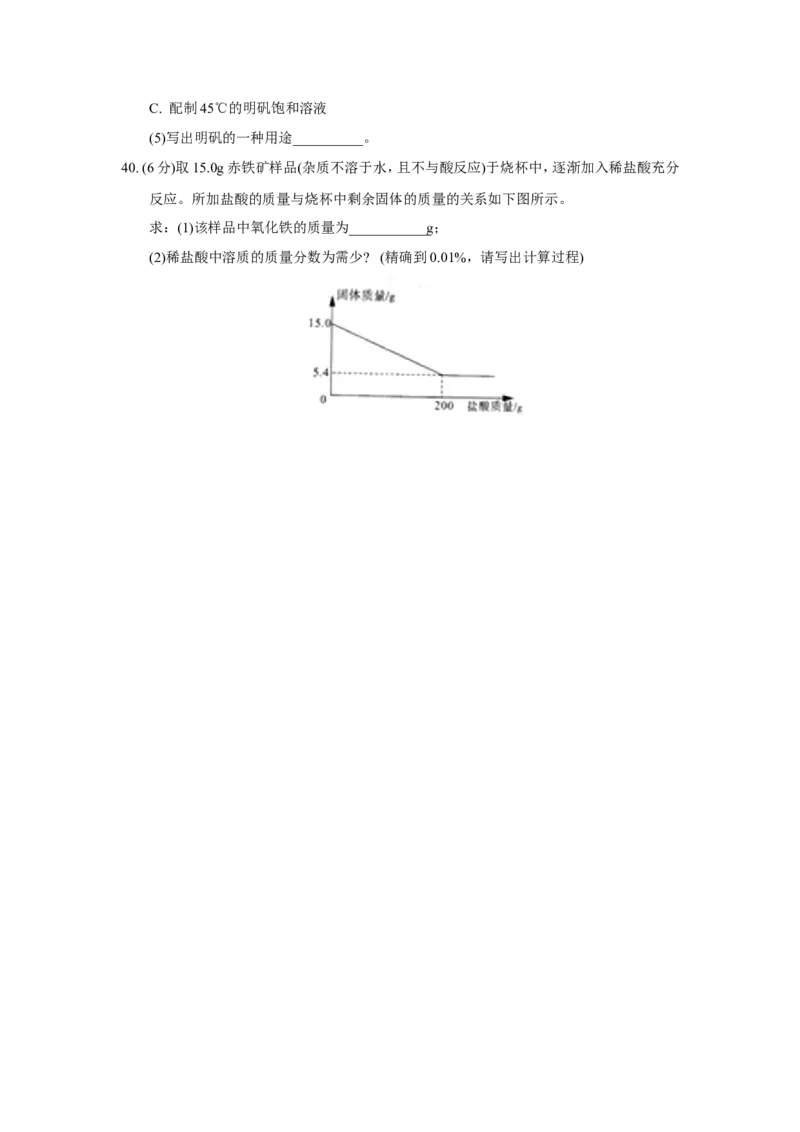
40. (6分)取15.0g赤铁矿样品(杂质不溶于水,且不与酸反应)于烧杯中,逐渐加入稀盐酸充分
反应。所加盐酸的质量与烧杯中剩余固体的质量的关系如下图所示。
求:(1)该样品中氧化铁的质量为___________g;
(2)稀盐酸中溶质的质量分数为需少? (精确到0.01%,请写出计算过程)1-10:BDACD ABABC 11-12:DC
35.(1)否;分子 (2)+4 (3)N ;(4)2NO+2CO 2CO+N
2 2 2
36.(1)B E
(2)甲 ①搅拌 ②B FG ③出现较多固体时,乙 ①左盘 ②D ③试剂瓶
37. (1)锥形瓶 (错别字0分)
(2)KC1O 2KCl+3O↑
3 2
(3)连续并比较均匀地放出时
(4) D
(5)伸入液面下
38. ①Ca(OH)+NaCO=CaCO ↓+2NaOH ②NaCl、NaOH、NaCO
2 2 3 3 2 3
③有白色沉能产生 ④HCl或HSO
2 4
⑤28:53. (或56: 106)
39. (NaHCO ;(2)分解反应;(3)2A1 (OH) +3HSO = A1 (S0 )+6HO
3 3 2 4 2 4 3 2
(4)CBA (5净水剂
40. (1)9.6 (2) 6.579%