文档内容
届高三年级阶段训练
2026
化学试卷参考答案与评分细则
一、选择题:本题共15小题,每小题3分,共45分。
题号
1 2 3 4 5 6 7 8
答案
C C B B C A A B
题号
9 10 11 12 13 14 15
答案
D D C D A D C
二、非选择题:本题共4小题,共55分。
注 有关反应方程式的书写中 化学式错误或未配平 不得分
: , , ;
同一反应中的 条件 等一处或多处错误合计扣 分
“ 、、↑、↓” 1 。
分
16.(13 )
1 2 分
(1)3d 4s (1 )
300℃ 分
(2)Sc2O3+6NH4HF2 2ScF3+6NH4F+3H2O (2 )
确保 完全氟化 提高钪的产率 分
Sc2O3 , (2 )
n 加热会水解 而后分解生成 分
(3)ScF3· H2O , Sc2O3 (2 )
分
(4)< (2 )
分
(5)①CaF2 (2 )
27 3 或 分
② ×10 ( 6750) (2 )
4
分
17.(14 )
阴阳离子的体积很大 离子键较弱 分
(1) , (2 )
加热反应不能在密闭体系进行 分
(2) (2 )
分液漏斗 烧杯 分 溶液 稀 分
(3) 、 (2 ) AgNO3 、 HNO3 (2 )
% 分
(4)75 (2 )
O
[Bmin]SO4
(5)CH3COOH+CH3CH(OH)CH3 CH3 C
△
化学试卷参考答案与解析 第 页 共 页
1 ( 8 )
CH3
分
O CHCH3 +H2O (2 )
有机物易被浓硫酸氧化 碳化 腐蚀生产设备 分
、 , (2 )分
18.(14 )
分
(1) (2 )
羰基 醚键 分
(2) 、 (2 )
取代反应 分
(3) (2 )
分
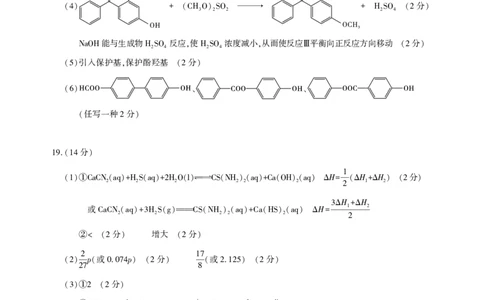
(4) + (CH3O)2SO2 → + H2SO4 (2 )
能与生成物 反应 使 浓度减小 从而使反应 平衡向正反应方向移动 分
NaOH H2SO4 , H2SO4 , Ⅲ (2 )
引入保护基 保护酚羟基 分
(5) , (2 )
(6) 、 、
任写一种 分
( 2 )
分
19.(14 )
H 1 H H 分
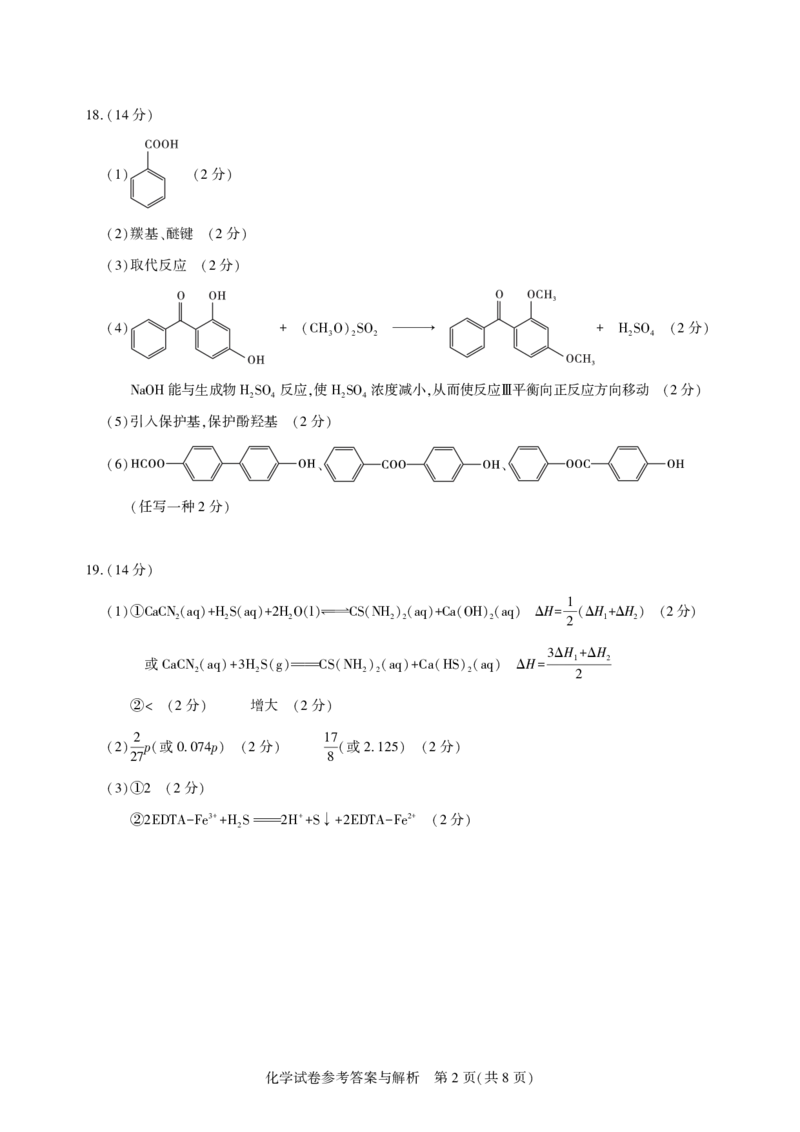
(1)①CaCN2(aq)+H2S(aq)+2H2O(l)CS(NH2)2(aq)+Ca(OH)2(aq) Δ = (Δ 1+Δ 2) (2 )
2
H H
或 H 3Δ 1+Δ 2
CaCN2(aq)+3H2S(g)CS(NH2)2(aq)+Ca(HS)2(aq) Δ =
2
分 增大 分
②< (2 ) (2 )
2 p 或 p 分 17 或 分
(2) ( 0.074 ) (2 ) ( 2.125) (2 )
27 8
分
(3)①2 (2 )
3+ + 2+ 分
②2EDTA-Fe +H2S2H +S↓+2EDTA-Fe (2 )
化学试卷参考答案与解析 第 页 共 页
2 ( 8 )届高三年级阶段训练
2026
化学试卷参考答案与解析
答案
1.【 】C
解析 为无氧酸盐 不符合 为含氧酸 不符合 为无氧酸 符合
【 】A.Na2S ,A ;B. H3PO2 ,B ;C. HCN ,C ;D.
为碱性气体 不符合
NH3 ,D 。
答案
2.【 】C
解析 乙二醇溶液用作汽车防冻液 正确 碘酸钾用作食盐中的营养强化剂 正确 牙膏中
【 】A. ,A ;B. ,B ;C.
添加的氟化物为氟化钠和氟化钙 有毒 错误 维生素 用作水果罐头中的抗氧化剂 正确
,HF ,C ;D. C ,D 。
答案
3.【 】B
F F
解析 为共价化合物 错误 的名称为顺 二氟乙烯 且为结构式 正
【 】A.H2O2 ,A ;B. CC -1,2- , ,B
H H
确 系统命名 甲基丁烷 错误 冶炼金属镁为电解熔融的氯化镁
;C.CH3CH(CH2CH3)CH3 :2- ,C ;D. ,D
错误
。
答案
4.【 】B
解析 杜瓦苯中含碳碳双键能使溴水褪色 正确 杜瓦苯分子中含单键碳原子 所有原子不共
【 】A. ,A ;B. ,
平面 错误 棱晶烷中 个氢原子等效 只含一种氢 正确 三者结构不同 分子式相同 互为同
,B ;C. 6 , ,C ;D. , ,
分异构体 正确
,D 。
答案
5.【 】C
解析 反应为可逆反应 不可能完全转化 正确 氨气催化氧化生成 正确 可根据价层
【 】A. , ,A ;B. NO,B ;C.
电子对理论判断硝酸根中氮原子为 2 杂化 分子中 原子也为 2 杂化 错误 产生的尾
sp ,HNO3 N sp ,C ;D.
气可用碱液吸收 正确
,D 。
答案
6.【 】A
解析 根据题目可推断 为氧 为硫 为氯 没有其它可能 氧元素主要为 和 价 一般无
【 】 X ,Y ,Z , 。 A. -2 -1 ,
正价 错误 电负性 正确 原子半径最大为硫原子 正确 键角
,A ;B. O>Cl>S,B ;C. ,C ;D. :H2O>H2S,D
正确
。
答案
7.【 】A
解析 重油比轻质油黏稠 因重油相对分子质量更大 范德华力更大 重油和轻质油的成分几乎都
【 】A. , , ,
是烃 不存在分子间氢键 故 错误 键能 因 原子半径小 与 间排斥力大
, , A ;B. :F—FO2, C ;D.—CH3 ,CH3NH2·H2O N ,
更容易结合质子 碱性 故 正确
, :CH3NH2·H2O>NH3·H2O, D 。
答案
8.【 】B
解析 氨气密度比空气小 应采用向下排空气法收集 图中收集氨气的导管应深入试管底部 故
【 】A. , , , A
错误 实验装置和操作符合葡萄糖的银镜反应实验 故 正确 溴水腐蚀橡胶 应使用酸式滴定
;B. , B ;C.① ,
管 溴水和碘化钾溶液开始反应生成 溶液即变成蓝色 无法指示反应终点 故 错误 为了避
;② I2, , ; C ;D.
免 与 -反应 电解饱和食盐水应使用阳离子交换膜 故 错误 综上 正确答案为
Cl2 OH , , D 。 , B。
答案
9.【 】D
解析 从 +和 3-的正视图 俯视图以及 点 3-的坐标可以看出 +和 3-处在 个小立方体的
【 】 Li As 、 M As ,Li As 8
体心 交错排列 上下底面的面心 棱心 顶点都是 2+ 均摊法可得晶胞中有 个 由此得到
, 。 、 、 Fe , 4 LiFeAs,
均正确 个晶胞中有 个 2+ 个 3- 个 + 当 个 3-被 2-取代后 总负电荷减少
ABC 。 1 4 Fe ,4 As ,4 Li 。 1 As Se , 1,
则 2+通过降价成 使得正负电荷代数和为 则 个 2+中有 个降为 价 因此 2+
Fe Fe 0, 4 Fe 0.5 0 , Fe =3.5,Fe=
与 的个数比为 故 错误
0.5,Fe(Ⅱ) Fe(0) 7 ∶ 1, D 。
答案
10.【 】D
解析 电极 为阴极 +由电极 向电极 迁移 正确 转移 -时 电极 表面 +
【 】A. b ,H a b ,A ;B. 1 mol e , b 1 mol H
放电 同时 +通过质子交换膜迁移到右池 故溶液 几乎不变 若不考虑电解中温度升高导致
, 1 mol H , pH (
的溶液体积增大 正确 因为 难溶于水 所以电极 应对具有好的吸附性 电极 作阳极且不
),B ;C. N2 , a ; a
放电 因为惰性电极 正确 该装置直接制备 左池溶液应为酸性溶液 -
, ,C ;D. HNO3, :N2-10e +6H2O
- + 错误
2NO3 +12H ,D 。
答案
11.【 】C
解析 根据题目可推断 分别为
【 】 M、N、Q、R、E、F CaC2、H2O、Ca(OH)2、C2H2、CH3CHO、CH3COOH。
催化剂
该反应先发生加成反应生成乙烯醇 后异构化生成乙醛 正确
A.CH≡CH+H2O →CH3CHO , ,A ;
△
分子中含 个 键和 个 键 个数比为 正确 中含离子键和非极性共价
B.CH3CHO 6 σ 1 π , 6 ∶ 1,B ;C.CaC2
键 中含离子键和极性共价键 错误 炔氧焰的温度可达 可用于切割和焊接金
、Ca(OH)2 ,C ;D. 3000℃,
属 正确
,D 。
答案
12.【 】D
解析
【 】
该历程中 有 价 价两种价态 正确 2+与乙烯配位时 利用的是乙烯的 键 与
A. ,Pd 0 、+2 ,A ;B.Pd , p-pπ ,
催化剂
2+的空轨道形成配位键 正确 总反应式 其中 2+ 2+作
Pd ,B ;C. :2CH2 CH2+O2 →2CH3CHO, Cu 、Pd
催化剂 正确 强碱性溶液中 2+形成了 沉淀 不能与乙烯形成配合物 形成的
,C ;D. ,Pd Pd(OH)2 , ; Cu
化学试卷参考答案与解析 第 页 共 页
4 ( 8 )沉淀不能氧化 错误
(OH)2 Pd,D 。
答案
13.【 】A
解析 根据题目可知 为蒸馏水 为稀硝酸 为浓硝酸 为氢氧化钠溶液 为蒸馏
【 】 ,②⑤ ,③ ,④ ,⑥ 。 A. ②⑤
水 错误 开始前通氮气驱赶空气避免影响 正确 为氢氧化钠溶液吸收尾气 正确
,A ;B. ,B ;C.⑥ NO2,C ;
中气体不变色 中气体由无色变为红棕色为实验结果 正确
D.③ ,④ ,D 。
答案
14.【 】D
解析 该胶束的液体为胶体有丁达尔现象 错误 若该液体的 时 其所带电荷计算过程
【 】A. ,A ;B. pH=7 ,
K K
+ 2 a
为δ + (CH ) -7 δ - a1 2 -3
(H2A )= (CH + ) 2 +(CH + ) K a1+ K a1 K a 2 =9.9×10 , (A )= (CH + ) 2 +(CH + ) K a1+ K a1 K a 2 =9.9×10 ,
则每个盘状双层胶束所带电荷为 -3 -7 - - 错误 形成该胶束
1000×(9.9×10 -9.9×10 )= 9.9 e ≈10 e ,B ;C.
过程体现了分子自组装的超分子特征 错误 随 从 变大 携带电荷增加 胶束表面单位面积
,C ;D. pH 7 , ,
电荷增加 胶束头部与头部斥力增大 头部距离变大 尾部距离变小 向球形转变 正确
, , , , ,D 。
答案
15.【 】C
解析 根据题目可知 亚硫酸分子 为亚硫酸氢根 为亚硫酸根 为亚硫酸根 正确
【 】 ,① ,② ,③ 。 A. ③ ,A ;
根据题意 时 c - 与 c 2- 相等 约为 正确 的
B. ,pH=7. 2 , (HSO3) (SO3 ) , 0. 05 mol/L,B ;C. 0. 10 mol/L
1
溶液的 约为 K - 2 错误 + 2- 的平衡常数 K K
NaHSO3 pH -lg(0.1× a2) =4.1,C ;D. H2SO3 2H +SO3 = a1×
K -9.1 正确
a2=10 ,D 。
二、非选择题:本题共4小题,共55分。
分
16.(13 )
答案
【 】
1 2 分
(1)3d 4s (1 )
300℃ 分
(2)Sc2O3+6NH4HF2 2ScF3+6NH4F+3H2O (2 )
确保 完全氟化 提高钪的产率 分
Sc2O3 , (2 )
n 加热会水解 而后分解生成 分
(3)ScF3· H2O , Sc2O3 (2 )
分
(4)< (2 )
分
(5)①CaF2 (2 )
27 3 或 分
② ×10 ( 6750) (2 )
4
解析
【 】
为 号元素 其基总原子价层电子排布式为 1 2
(1)Sc 21 , 3d 4s ;
通过流程分析 氧化的产物为 和 还有 其化学方程式为 300℃
(2) , ScF3 NH4F, H2O, Sc2O3+6NH4HF2
化学试卷参考答案与解析 第 页 共 页
5 ( 8 )需过量的目的是使 完全氟化 提高产率
2ScF3+6NH4F+3H2O;NH4HF2 Sc2O3 , ;
类比 n 加热 会发生水解而
(3) TiCl4· H2O , Sc2O3;
后蒸出来 故沸点高
(4)Sc , ;
-11 3 -18
2.7×10 4.0×10 故 先析出
(5)① <
-6
, CaF2 ;
0.1 1.0×10
-11
2.7×10
-3 2 -5
(1.0×10 ) 2.7×10 27 3
② = = ×10 。
-18 -9
4.0×10 4.0×10 4
-3 3
(1.0×10 )
分
17.(14 )
答案
【 】
阴阳离子的体积很大 离子键较弱 分
(1) , (2 )
加热反应不能在密闭体系进行 分
(2) (2 )
分液漏斗 烧杯 分 溶液 稀 分
(3) 、 (2 ) AgNO3 、 HNO3 (2 )
% 分
(4)75 (2 )
O
[Bmin]SO4
(5)CH3COOH+CH3CH(OH)CH3 CH3 C
△
化学试卷参考答案与解析 第 页 共 页
6 ( 8 )
CH3
分
O CHCH3 +H2O (2 )
有机物易被浓硫酸氧化 碳化 腐蚀生产设备 分
、 , (2 )
解析
【 】
根据离子液体特点答案为 阴阳离子体积大 离子键较弱
(1) : , ;
该反应为密闭体系 易产生安全事故
(2) , ;
分液漏斗 烧杯 检验 - 故试剂为 溶液 稀硝酸
(3) , ; Br , AgNO3 , ;
44.73 g
284 g/mol % %
(4) ×100 =75 ;
0.21 mol
O
[Bmin]SO4
(5)CH3COOH+CH3CH(OH)CH3 CH3 C
△
CH3
有机物易被浓硫酸氧化
O CHCH3 +H2O; 、
碳化 腐蚀生产设备
, 。
分
18.(14 )
答案
【 】
分
(1) (2 )羰基 醚键 分
(2) 、 (2 )
取代反应 分
(3) (2 )
分
(4) + (CH3O)2SO2 → + H2SO4 (2 )
能与生成物 反应 使 浓度减小 从而使反应 平衡向正反应方向移动 分
NaOH H2SO4 , H2SO4 , Ⅲ (2 )
引入保护基 保护酚羟基 分
(5) , (2 )
(6) 、 、
任写一种 分
( 2 )
解析
【 】
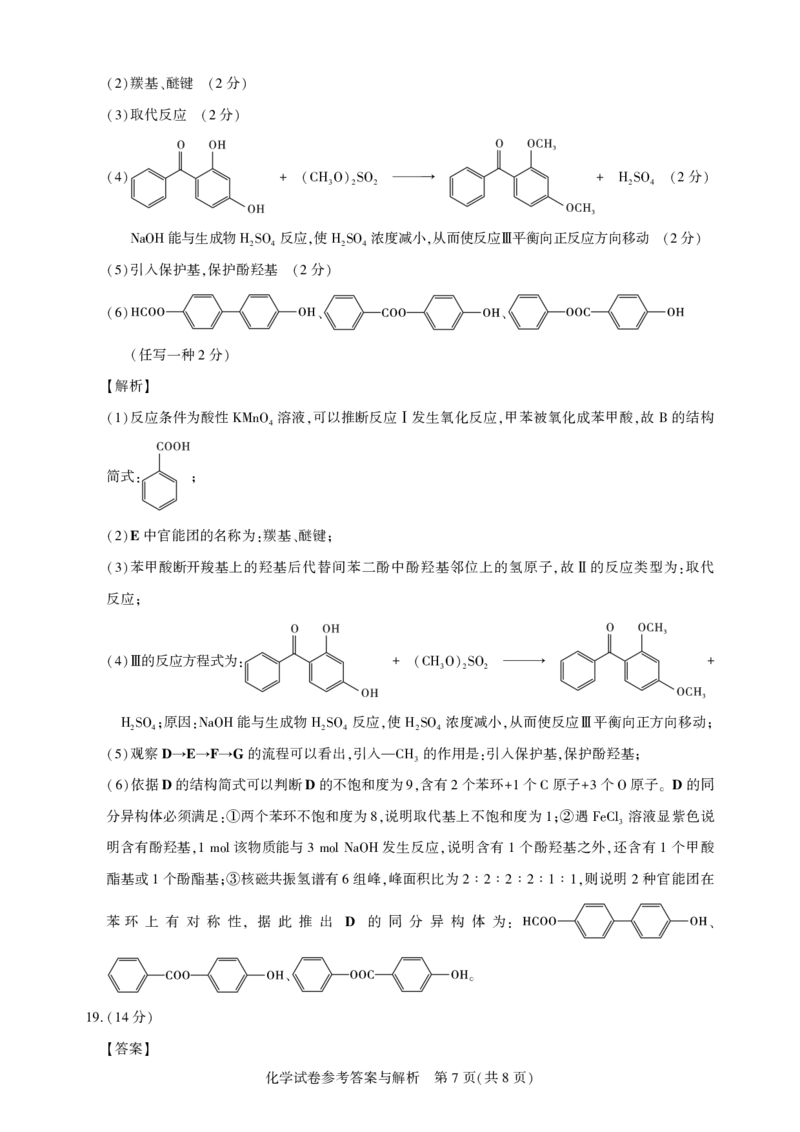
反应条件为酸性 溶液 可以推断反应 发生氧化反应 甲苯被氧化成苯甲酸 故 的结构
(1) KMnO4 , Ⅰ , , B
简式
: ;
E中官能团的名称为 羰基 醚键
(2) : 、 ;
苯甲酸断开羧基上的羟基后代替间苯二酚中酚羟基邻位上的氢原子 故 的反应类型为 取代
(3) , Ⅱ :
反应
;
的反应方程式为
(4)Ⅲ : + (CH3O)2SO2 → +
原因 能与生成物 反应 使 浓度减小 从而使反应 平衡向正方向移动
H2SO4; :NaOH H2SO4 , H2SO4 , Ⅲ ;
观察D E F G的流程可以看出 引入 的作用是 引入保护基 保护酚羟基
(5) → → → , —CH3 : , ;
依据D的结构简式可以判断D的不饱和度为 含有 个苯环 个 原子 个 原子 D的同
(6) 9, 2 +1 C +3 O 。
分异构体必须满足 两个苯环不饱和度为 说明取代基上不饱和度为 遇 溶液显紫色说
:① 8, 1;② FeCl3
明含有酚羟基 该物质能与 发生反应 说明含有 个酚羟基之外 还含有 个甲酸
,1 mol 3 mol NaOH , 1 , 1
酯基或 个酚酯基 核磁共振氢谱有 组峰 峰面积比为 则说明 种官能团在
1 ;③ 6 , 2 ∶ 2 ∶ 2 ∶ 2 ∶ 1 ∶ 1, 2
苯环 上 有 对 称 性 据 此 推 出 D 的 同 分 异 构 体 为
, : 、
、 。
分
19.(14 )
答案
【 】
化学试卷参考答案与解析 第 页 共 页
7 ( 8 )H 1 H H 分
(1)①CaCN2(aq)+H2S(aq)+2H2O(l)CS(NH2)2(aq)+Ca(OH)2(aq) Δ = (Δ 1+Δ 2) (2 )
2
H H
或 H 3Δ 1+Δ 2
CaCN2(aq)+3H2S(g)CS(NH2)2(aq)+Ca(HS)2(aq) Δ =
2
分 增大 分
②< (2 ) (2 )
2 p 或 p 分 17 或 分
(2) ( 0.074 ) (2 ) ( 2.125) (2 )
27 8
分
(3)①2 (2 )
3+ + 2+ 分
②2EDTA-Fe +H2S2H +S↓+2EDTA-Fe (2 )
解析
【 】
通入 过量时 H 3 H 1 H
(1)① H2S ,Δ = Δ 1+ Δ 2;
2 2
随着1 的减小 温度升高 k 增大的倍数更大 故逆反应是吸热反应 故 H 升高温度 平衡逆
② T , , 逆 , ; Δ 3<0; ,
n
移 [CS(NH2)2]的值增大
, n ;
(NH4SCN)
.
0.2 p 0 4 p 2
× ×( . × )
平衡时 n n n K 1.2 1 2 2 p 恒压
(2) , (H2S)= 0.6 mol, (H2)= 0.4 mol, (S2)= 0.2 mol; p= . = ;
0 6 p 2 27
( . × )
1 2
时 充入 设为x 且平衡时 n n n K
, Ar( mol), , (H2S)= 0. 5 mol, (H2)= 0. 5 mol, (S2)= 0. 25 mol; p =
.
0.25 p 0 5 p 2
x× ×( . x× )
1.25+ 1 25+ 2p 解得x 18或者
. = , = 2.125 mol;
0 5 p 2 27 8
( . x× )
1 25+
阳极处理 即 转移 - 质子交换膜转移电荷 即 + 阳极区反应
(3) 34 g H2S( 1 mol H2S) 2 mol e , , 2 mol H ;
2+ - 3+ 反应 3+ 2+ + 阴极区的
Ⅰ:2EDTA-Fe -2e 2EDTA-Fe ; Ⅱ:2EDTA-Fe +H2S=2EDTA-Fe +2H +S↓;
反应 - +
:CO2+2e +2H CO+H2O
化学试卷参考答案与解析 第 页 共 页
8 ( 8 )