文档内容
2025-2026 学年上期高 2026届一诊模拟测试
化学 试卷
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Mn-55 Cu-64
一、选择题:本题共 15 小题,每小题3 分,共 45 分。每小题给出的四个选项中,只有一项是符合题目要求
的。
1. 材料是人类赖以生存和发展的物质基础,关于材料正确的是
A.化学纤维是石油、天然气和煤等为原料制成的
B. 硫化程度最高的橡胶可用于生产医用乳胶手套
C. 水玻璃具有黏结力强、耐高温等特性,可以用作黏合剂和防火剂,属于电解质
D.聚乳酸易降解,可用作手术缝合线
2. 化学与社会生活密切相关。下列有关说法错误的是
A.超市中食用油中添加入2-叔丁基对苯二酚作为抗氧化剂
B.燃料油、石蜡油都是碳数较多的烷烃,可通过石油减压蒸馏获得
C.向鸡蛋清溶液中加入几滴浓硝酸溶液,直接变为黄色沉淀
D.焰色试验中涉及图标含有 和
3. 下列化学用语或图示正确的是
A. 的系统命名:邻甲基苯酚
B.反式聚异戊二烯的结构简式:
C.BF 的空间填充模型:
3
D.CH NH 的电子式:
3 2
4.M、N、P三种有机物的转化关系如图所示。下列说法错误的是( )
A.M 中所有碳原子不可能共平面
B.M 加成过量氢气后,能形成两个手性碳
C.M 转化N 发生了加成反应
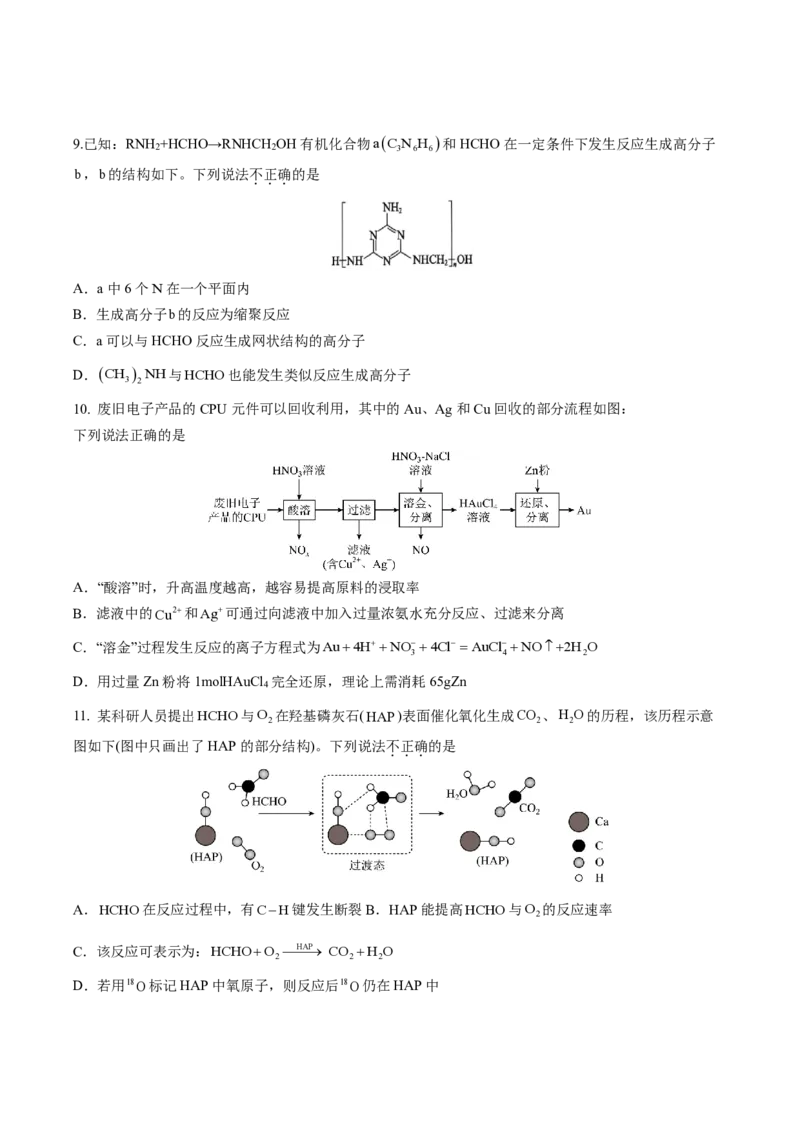
D.苯环上含1 个取代基能与碳酸氢钠反应的 N 的同分异构体有 5 种(不考虑立体异构)9.已知:RNH +HCHO→RNHCH OH有机化合物
2 2
a ( C
3
N
6
H
6
) 和HCHO在一定条件下发生反应生成高分子
b,b的结构如下。下列说法不
.
正
.
确
.
的是
A.a中6个 N 在一个平面内
B.生成高分子 b 的反应为缩聚反应
C.a可以与HCHO反应生成网状结构的高分子
D.(CH ) NH与
3 2
H C H O 也能发生类似反应生成高分子
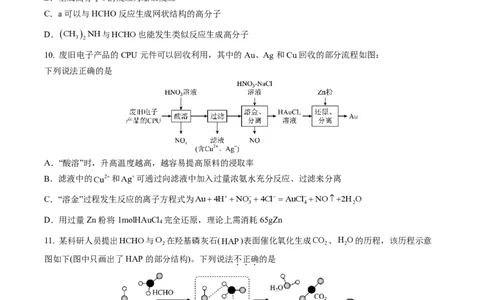
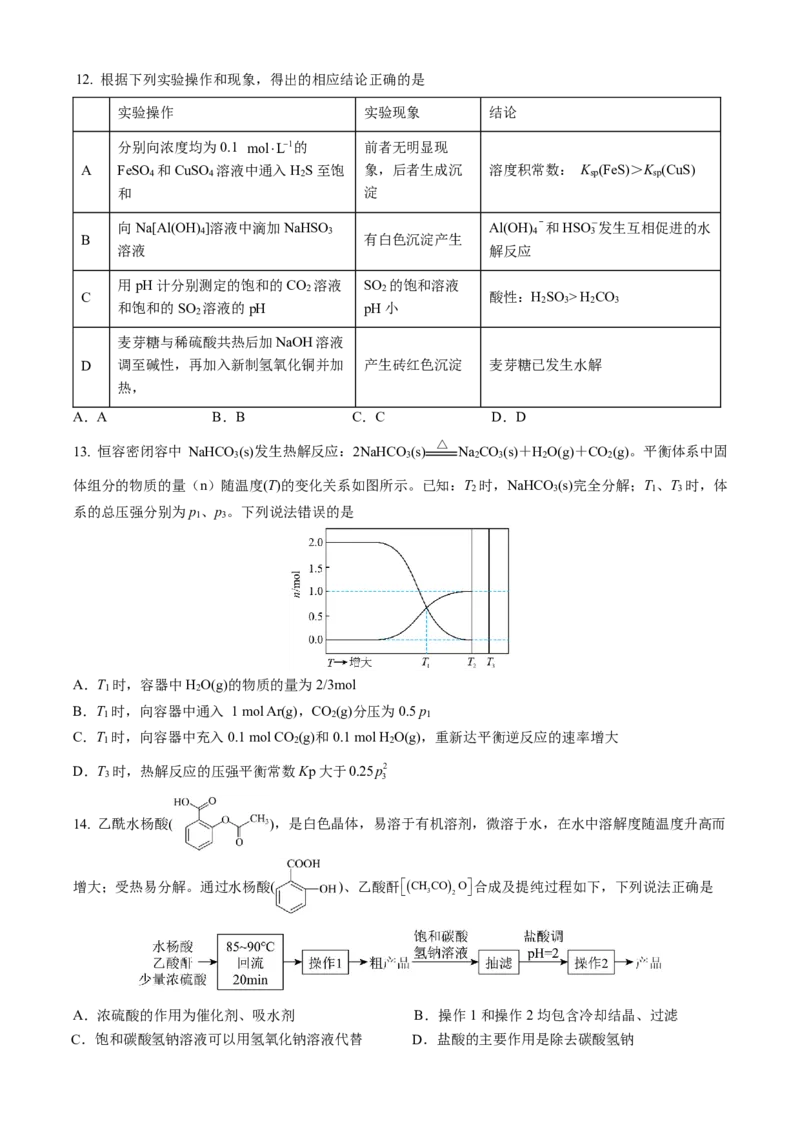
10. 废旧电子产品的CPU元件可以回收利用,其中的Au、Ag和Cu回收的部分流程如图:
下列说法正确的是
A.“酸溶”时,升高温度越高,越容易提高原料的浸取率
B.滤液中的Cu2+和 A g + 可通过向滤液中加入过量浓氨水充分反应、过滤来分离
C.“溶金”过程发生反应的离子方程式为Au+4H++NO−+4Cl− =AuCl−+NO+2H O
3 4 2
D.用过量Zn粉将1molHAuCl 完全还原,理论上需消耗65gZn
4
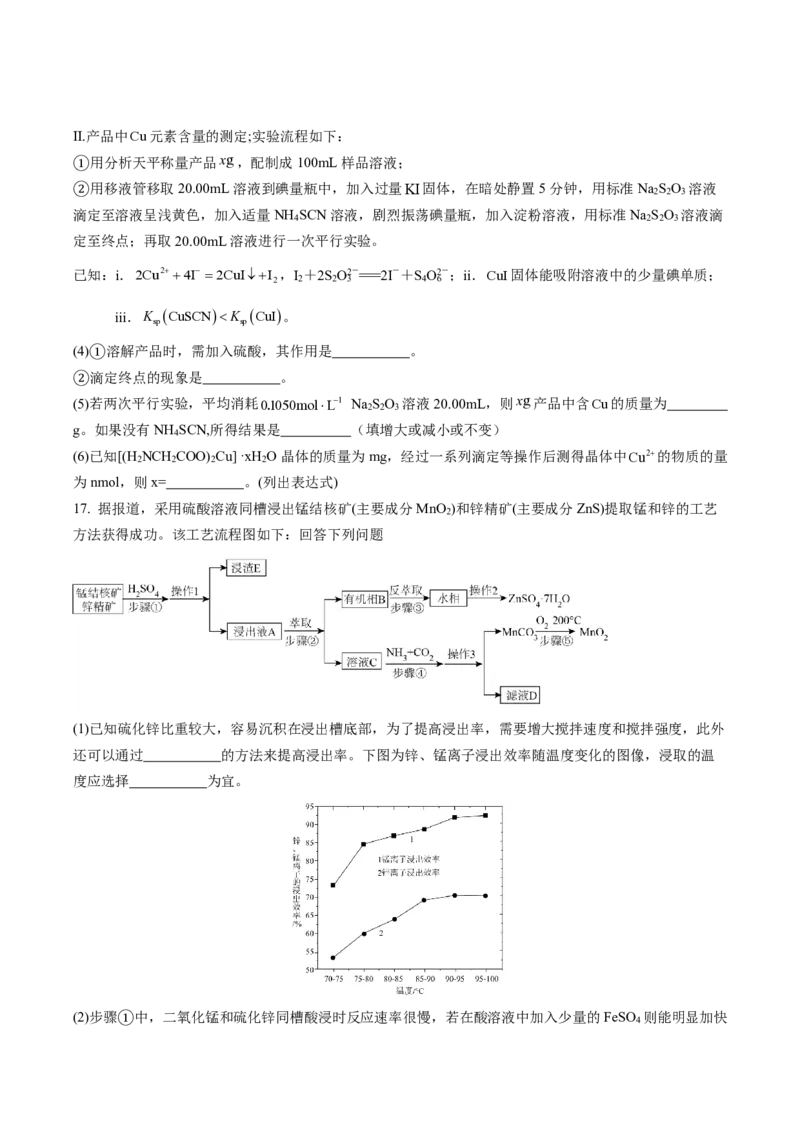
11. 某科研人员提出 H C H O 与 O
2
在羟基磷灰石( H A P )表面催化氧化生成 C O
2
、 H
2
O 的历程,该历程示意
图如下(图中只画出了HAP的部分结构)。下列说法不
.
正
.
确
.
的是
A.HCHO在反应过程中,有C−H键发生断裂B.HAP能提高HCHO与 O
2
的反应速率
C.该反应可表示为:HCHO+O ⎯ H⎯A⎯→P CO +H O
2 2 2
D.若用18O标记HAP中氧原子,则反应后18O仍在HAP中实验操作 实验现象 结论
分别向浓度均为0.1
A
m o l L − 1 的 前者无明显现
FeSO 4 和CuSO 4 溶液中通入H 2 S至饱 象,后者生成沉 溶度积常数: K sp (FeS)>K sp (CuS)
和 淀
向Na[Al(OH) ]溶液中滴加NaHSO Al(OH) -和HSO-发生互相促进的水
4 3 4 3
B 有白色沉淀产生
溶液 解反应
用pH计分别测定的饱和的CO 溶液 SO 的饱和溶液
2 2
C 酸性:H 2 SO 3 > H 2 CO 3
和饱和的SO 溶液的pH pH小
2
麦芽糖与稀硫酸共热后加
D
N a O H 溶液
调至碱性,再加入新制氢氧化铜并加 产生砖红色沉淀 麦芽糖已发生水解
热,
A.A B.B C.C D.D
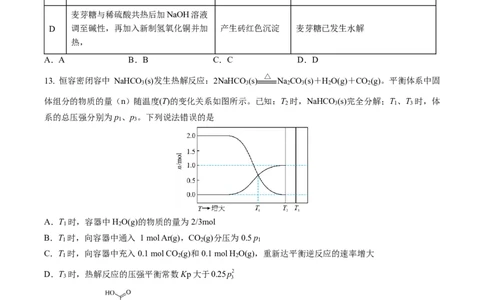
13. 恒容密闭容中 NaHCO (s)发生热解反应:2NaHCO (s) Na CO (s)+H O(g)+CO (g)。平衡体系中固
3 3 2 3 2 2
体组分的物质的量(n)随温度(T)的变化关系如图所示。已知:T 时,NaHCO (s)完全分解;T 、T 时,体
2 3 1 3
系的总压强分别为p 、p 。下列说法错误的是
1 3
A.T 时,容器中H O(g)的物质的量为2/3mol
1 2
B.T 时,向容器中通入 1 mol Ar(g),CO (g)分压为0.5 p
1 2 1
C.T 时,向容器中充入0.1 mol CO (g)和0.1 mol H O(g),重新达平衡逆反应的速率增大
1 2 2
D.T 时,热解反应的压强平衡常数Kp大于0.25p2
3 3
14. 乙酰水杨酸( ),是白色晶体,易溶于有机溶剂,微溶于水,在水中溶解度随温度升高而
增大;受热易分解。通过水杨酸( )、乙酸酐 (CH 3 CO) 2 O 合成及提纯过程如下,下列说法正确是
A.浓硫酸的作用为催化剂、吸水剂 B.操作1和操作2均包含冷却结晶、过滤
△
12. 根据下列实验操作和现象,得出的相应结论正确的是
C.饱和碳酸氢钠溶液可以用氢氧化钠溶液代替 D.盐酸的主要作用是除去碳酸氢钠15.一价金属元素M的两种弱酸盐MA和MB均为难溶电解质。室温下,MA与MB的溶液中M+离子浓度
值的负对数pM随溶液pH的变化曲线如图所示。已知:M+离子不水解,K (HA)>K (HB)。曲线L 和L
a a 1 2
与纵轴的交点分别为2.0和1.0。下列说法正确的是( )
L
pM 1
L
2
pH
A. 曲线L 表示的是MA的变化图线
2
B. 室温时MA溶度积常数的数量级为10-4
C. 室温时MA(s)+B-(ag) MB(s)+A-(ag)的反应限度接近完全
D. 室温下,0.10 mol/L NaB溶液的pH约为9.5
二、非选择题:本题共4小题,共55分
16.某研究小组制备配合物顺式一二甘氨酸合铜[(H NCH COO) Cu]并测定所得产品中铜的含量。回答下列问
2 2 2
题:
I.制备顺式一二甘氨酸合铜(H NCH COO) Cu]
2 2 2
步骤1:取5.0g CuSO ·5H O固体,加水溶解,再慢慢加入体积比1:1氨水并不断搅拌,直至Cu(OH) 沉
4 2 2
淀恰好溶解,得深蓝色溶液,再加入足量较浓NaOH溶液,使沉淀完全。抽滤、洗涤,得沉淀备用。
步骤2:称取4.5g甘氨酸,溶解,控制反应温度为65~70℃,边搅拌边加入步骤I中制得的沉淀,直至沉
淀溶解,趁热抽滤,向滤液中加入10mL95%乙醇,冷却直至析出蓝色针状晶体,在冰水浴上继续冷却20
分钟。
步骤3:冷却后,抽滤,用体积比为1:3的酒精溶液洗涤晶体一次,再用丙酮洗涤两次并干燥,制得顺式
[(H NCH COO) Cu] ·xH O晶体。
2 2 2 2
已知:①二甘氨酸合铜易溶于水,微溶于乙醇,难溶于丙酮,加热至130℃脱水,228℃分解;②二甘氨
酸合铜在水中溶解度:顺式(蓝色针状晶体)>反式(蓝紫色鳞片状结晶);热稳定性:反式>顺式;
(1)写出Cu(OH) 与甘氨酸反应的化学方程式: 。。
2
(2)在步骤Ⅲ洗涤采用先1:3酒精溶液后丙酮洗涤的优点 。
(3)下列说法不正确的是___________。
A.步骤1为了加快实验速度,也可以用NaOH溶液直接与CuSO 溶液反应制备氢氧化铜
4
B.实验中多次采取抽滤操作,其中可能的优点是可以加快固液分离的速度,获得较为干燥的产品
C.步骤2中,加入95%乙醇的目的是减小溶剂的极性,抑制晶体在水中的溶解,有利于晶体析出
D.65~70℃优先析出顺式二甘氨酸合铜,原因是该反应的活化能大II.产品中 C u 元素含量的测定;实验流程如下:
①用分析天平称量产品 x g ,配制成100mL样品溶液;
②用移液管移取20.00mL溶液到碘量瓶中,加入过量KI固体,在暗处静置5分钟,用标准Na S O 溶液
2 2 3
滴定至溶液呈浅黄色,加入适量NH SCN溶液,剧烈振荡碘量瓶,加入淀粉溶液,用标准Na S O 溶液滴
4 2 2 3
定至终点;再取20.00mL溶液进行一次平行实验。
已知:i.2Cu2++4I− =2CuI+I ,I +2S O2-===2I-+S O2-;ii.
2 2 2 3 4 6
C u I 固体能吸附溶液中的少量碘单质;
iii.K (CuSCN)K (CuI)。
sp sp
(4)①溶解产品时,需加入硫酸,其作用是 。
②滴定终点的现象是 。
(5)若两次平行实验,平均消耗 0 .1 0 5 0 m o l L − 1 Na S O 溶液20.00mL,则
2 2 3
x g 产品中含 C u 的质量为
g。如果没有NH SCN,所得结果是 (填增大或减小或不变)
4
(6)已知[(H NCH COO) Cu] ·xH O晶体的质量为mg,经过一系列滴定等操作后测得晶体中
2 2 2 2
C u 2 + 的物质的量
为nmol,则x= 。(列出表达式)
17. 据报道,采用硫酸溶液同槽浸出锰结核矿(主要成分MnO )和锌精矿(主要成分ZnS)提取锰和锌的工艺
2
方法获得成功。该工艺流程图如下:回答下列问题
(1)已知硫化锌比重较大,容易沉积在浸出槽底部,为了提高浸出率,需要增大搅拌速度和搅拌强度,此外
还可以通过 的方法来提高浸出率。下图为锌、锰离子浸出效率随温度变化的图像,浸取的温
度应选择 为宜。
(2)步骤①中,二氧化锰和硫化锌同槽酸浸时反应速率很慢,若在酸溶液中加入少量的FeSO 则能明显加快
4反应速率,发生反应的离子方程式为2Fe2++MnO +4H+=2Fe3++Mn2++2H O和 , FeSO 在该反
2 2 4
应中的作用为 。
(3)研究发现,步骤①中两种矿物同槽酸浸4小时后,锰和锌的浸出率只有约80%,在实际工艺中,需将
浸渣E用四氯乙烷处理后再做二次酸浸,四氯乙烷的作用是 。
(4)操作2的具体步骤是 ,过滤,洗涤,干燥。
(5)步骤④沉淀锰的离子反应方程式为 。
(6)步骤⑤中的产物在不同温度下分解可得到锰的不同氧化物。加热到1000℃时,可得一种固体纯净物,
根据下图数据计算其化学式为 。
18. 甲烷催化氧化偶联制乙烯是提高甲烷附加值的一项重要研究课题,其涉及的反应如下:
反应 I: 4CH (g)+ O (g) 2 C H (g)+2H O (g) ΔH=-354kJ·mol-1 ;
4 2 2 6 2
反应II. 2CH (g)+ O (g) C H (g)+2H O (g) ΔH=-282 kJ·mol-1
4 2 2 4 2
n(C H )
已知:①C H (g)的选择性= 2 6 100%;
2 6 n(C H )+n(C H )
2 6 2 4
②K :用平衡分压代替平衡浓度计算;分压
p
= 总压物质的量分数。
回答下列问题:
(1) 反应III:2 C H (g)+ O (g) 2C H (g)+2H O (g)的H = 2 6 2 2 4 2 3 k J m o l − 1 ,反应III能够自发进
行的原因是 。
(2)向刚性容器中充入4mol CH (g)和2mol O (g),起始压强为
4 2
p
0
k P a 、温度为TK条件下发生反应I、反应
II,达到平衡后,测得反应体系总压强为 0 .9 5 p
0
k P a ,CH (g)的分压为p /15kPa,则C H (g)的选择性
4 0 2 4
为 ,反应I的分压表示的平衡常数K = kPa−1(用含p 代数式表示),若再向刚性容器中充
p 0
p(C H )
入一定量的O (g),重新达平衡后,则分压p(CH )将 (填“增大”“减小”或“不变”), 2 4 将
2 4 p(C H )
2 6
(填“增大”“减小”或“不变”)。
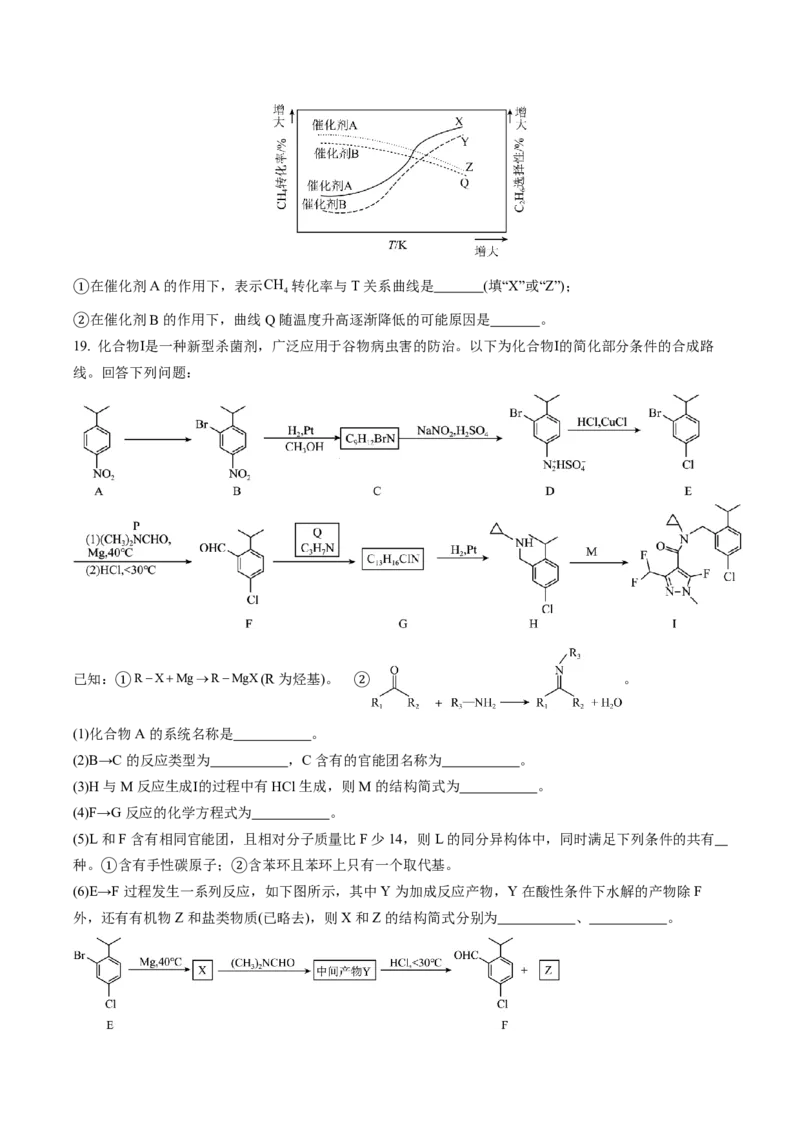
(3)向刚性容器中,充入4mo CH (g)和2mol O (g),分别在催化剂A、催化剂B作用下发生反应I、反应
4 2
II,反应tmin时测得CH 转化率、C H 选择性与温度关系如图所示:
4 2 6①在催化剂A的作用下,表示CH 转化率与T关系曲线是 (填“X”或“Z”);
4
②在催化剂B的作用下,曲线Q随温度升高逐渐降低的可能原因是 。
19. 化合物Ⅰ是一种新型杀菌剂,广泛应用于谷物病虫害的防治。以下为化合物Ⅰ的简化部分条件的合成路
线。回答下列问题:
已知:①R−X+Mg→R−MgX(R为烃基)。 ② 。
(1)化合物A的系统名称是 。
(2)B→C的反应类型为 ,C含有的官能团名称为 。
(3)H与M反应生成Ⅰ的过程中有HCl生成,则M的结构简式为 。
(4)F→G反应的化学方程式为 。
(5)L和F含有相同官能团,且相对分子质量比F少14,则L的同分异构体中,同时满足下列条件的共有
种。①含有手性碳原子;②含苯环且苯环上只有一个取代基。
(6)E→F过程发生一系列反应,如下图所示,其中Y为加成反应产物,Y在酸性条件下水解的产物除F
外,还有有机物Z和盐类物质(已略去),则X和Z的结构简式分别为 、 。