文档内容
2 0 2 5 年 上 教 师 资 格 · 化 学 学 科 笔 试
主讲老师 岳筱涵
粉笔教师教育 粉笔教师铁、铜及其化合物P55
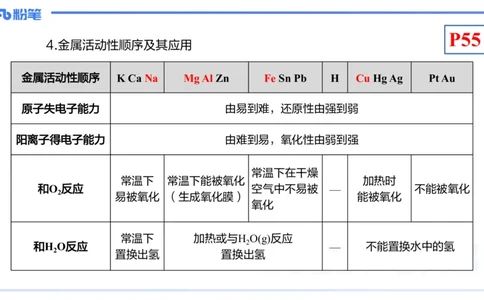
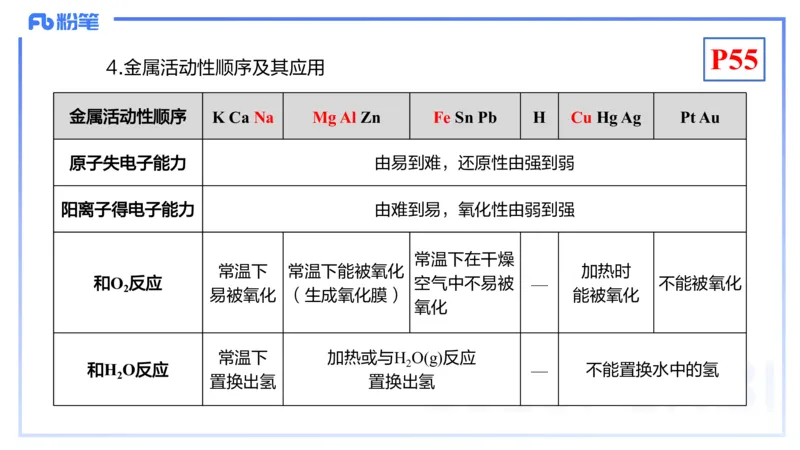
4.金属活动性顺序及其应用
金属活动性顺序 K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au
原子失电子能力 由易到难,还原性由强到弱
阳离子得电子能力 由难到易,氧化性由弱到强
常温下在干燥
常温下 常温下能被氧化 加热时
和O 反应 空气中不易被 — 不能被氧化
2
易被氧化 (生成氧化膜) 能被氧化
氧化
常温下 加热或与H O(g)反应
2
和H O反应 — 不能置换水中的氢
2
置换出氢 置换出氢P55
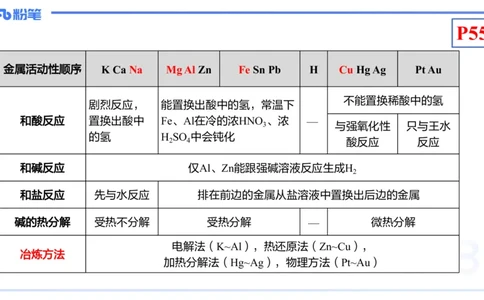
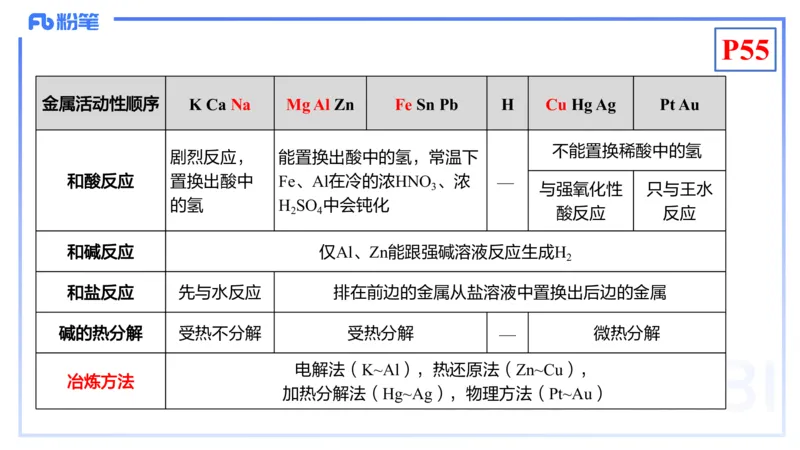
金属活动性顺序 K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au
不能置换稀酸中的氢
剧烈反应, 能置换出酸中的氢,常温下
和酸反应 置换出酸中 Fe、Al在冷的浓HNO 、浓 —
3 与强氧化性 只与王水
的氢 H SO 中会钝化
2 4 酸反应 反应
和碱反应 仅Al、Zn能跟强碱溶液反应生成H
2
和盐反应 先与水反应 排在前边的金属从盐溶液中置换出后边的金属
碱的热分解 受热不分解 受热分解 — 微热分解
电解法(K~Al),热还原法(Zn~Cu),
冶炼方法
加热分解法(Hg~Ag),物理方法(Pt~Au)碳、硅及其化合物P56
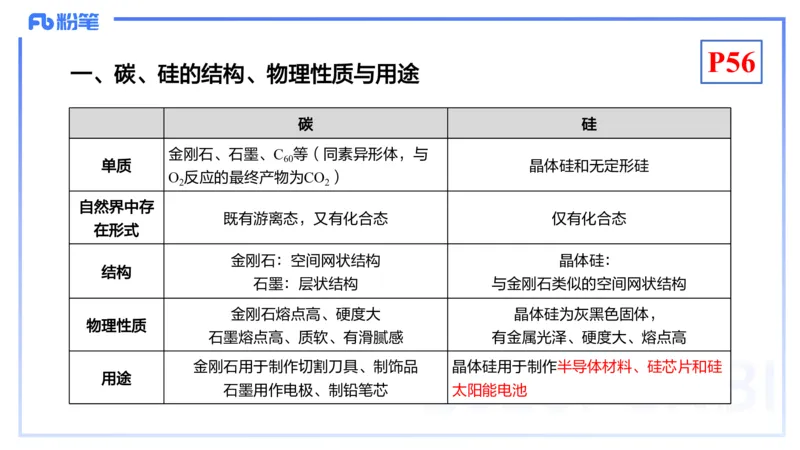
一、碳、硅的结构、物理性质与用途
碳 硅
金刚石、石墨、C 等(同素异形体,与
60
单质 晶体硅和无定形硅
O 反应的最终产物为CO )
2 2
自然界中存
既有游离态,又有化合态 仅有化合态
在形式
金刚石:空间网状结构 晶体硅:
结构
石墨:层状结构 与金刚石类似的空间网状结构
金刚石熔点高、硬度大 晶体硅为灰黑色固体,
物理性质
石墨熔点高、质软、有滑腻感 有金属光泽、硬度大、熔点高
金刚石用于制作切割刀具、制饰品 晶体硅用于制作半导体材料、硅芯片和硅
用途
石墨用作电极、制铅笔芯 太阳能电池P57
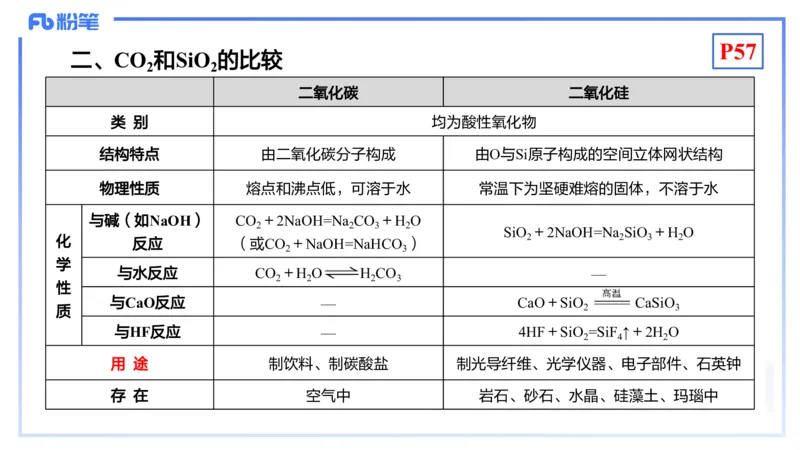
二、CO 和SiO 的比较
2 2
二氧化碳 二氧化硅
类 别 均为酸性氧化物
结构特点 由二氧化碳分子构成 由O与Si原子构成的空间立体网状结构
物理性质 熔点和沸点低,可溶于水 常温下为坚硬难熔的固体,不溶于水
与碱(如NaOH) CO +2NaOH=Na CO +H O
2 2 3 2
SiO +2NaOH=Na SiO +H O
化 2 2 3 2
反应 (或CO +NaOH=NaHCO )
2 3
学
与水反应 CO +H O H CO —
2 2 2 3
性
与CaO反应 — CaO+SiO CaSiO
质 2 3
与HF反应 — 4HF+SiO =SiF ↑+2H O
2 4 2
用 途 制饮料、制碳酸盐 制光导纤维、光学仪器、电子部件、石英钟
存 在 空气中 岩石、砂石、水晶、硅藻土、玛瑙中P57
三、碳、硅元素单质及其化合物的特性
1.一般情况,非金属元素单质熔、沸点低,硬度小,但硅和金刚
石熔、沸点高,硬度大,其中金刚石为天然存在的硬度最大的物质。
2.一般情况,非金属元素单质为绝缘体,但硅为半导体,石墨为
电的良导体。
3.一般情况,氧化还原反应遵循“剂强物弱”的原则,而碳却能还
原出比它更强的还原剂:
SiO +2C Si+2CO↑,FeO+ C Fe+CO↑。
2P57
4.非金属单质一般不能生成H ,但C、Si均可:
2
C+H O(g) CO+H (水蒸气通过灼热的碳层,生成水煤气
2 2
的反应);
Si+2NaOH+H O Na SiO +2H ↑ 。
2 2 3 2
5.一般情况,较活泼金属+酸 = 盐+氢气,然而Si是非金属,却
能与氢氟酸发生反应:
Si+4HF SiF ↑+2H ↑。
4 2
但生成的SiF 不属于盐。
4P57
6.一般情况,酸性氧化物+碱 = 盐+水,SiO 是酸性氧化物,却
2
能与氢氟酸反应:
SiO +4HF SiF ↑+2H O
2 4 2
7.无机酸一般能溶于水,而H SiO 却难溶于水。
2 3
8.H CO 的酸性强于H SiO 且生成的硅酸为沉淀,
2 3 2 3
所以有 Na SiO +CO +H O H SiO ↓+Na CO ,
2 3 2 2 2 3 2 3
但反应Na CO +SiO Na SiO +CO ↑ 也能发生 。
2 3 2 2 3 2P58
9. 制粗硅:SiO +2C Si+2CO↑。
2
粗硅提纯:Si(粗)+2Cl SiCl ,SiCl +2H Si(纯)+4HCl。
2 4 4 2
C Cl H
工业制取纯硅的工艺流程为 SiO 粗硅 2 SiCl 2 纯硅,
2 4
用焦炭还原SiO ,产物是 CO 而不是 CO 。
2 2P58
四、实验:硅酸的制备
硅酸是一种很弱的酸(酸性比碳酸还弱),溶解度很小。由于 SiO
2
不溶于水,所以硅酸是通过可溶性硅酸盐与其他酸反应制得的。所生成
的 H SiO 逐渐聚合而形成胶体溶液——硅酸溶胶,硅酸浓度较大时,则
2 3
形成软而透明的、胶冻状的硅酸凝胶。硅酸凝胶经干燥脱水后就形成硅
酸干胶,称为“硅胶”。硅胶多孔,吸附水分能力强,常用作实验室和袋装
食品、瓶装药品等的干燥剂,也可以用作催化剂的载体。P58
(一)实验步骤
在试管中加入3~5mLNa SiO 溶液(饱和Na SiO 溶液按1:2或1:3的体
2 3 2 3
积比用水稀释),滴入1~2滴酚酞溶液,再用胶头滴管逐滴加入稀盐酸,边
加边振荡,至溶液红色变浅并接近消失时停止。静置,仔细观察变化过程
及现象。
(二)实验现象
滴入酚酞溶液变红色(SiO 2-水解使溶液显碱性,从而使酚酞溶液呈
3
红色),加入稀盐酸后,有透明的硅酸凝胶形成。
Na SiO +2HCl H SiO (胶体)+2NaCl
2 3 2 3P58
五、硅酸盐
硅酸盐是由硅、氧和金属元素组成的化合物的总称。
硅酸盐在自然界中分布极广,是一大类结构复杂的固态物质,大
多数不溶于水,化学性质稳定。P59
(一)最简单的硅酸盐——硅酸钠(Na SiO )
2 3
最简单的硅酸盐是Na SiO ,是白色、可溶于水的粉末状固体,其水溶液
2 3
俗称水玻璃或泡花碱,有黏性,溶液显碱性,硅酸钠长期暴露在空气中会变
质,因此要密封保存且盛放硅酸钠的试剂瓶不能用玻璃塞。
1.能与酸性比硅酸强的酸反应
与盐酸反应:Na SiO +2HCl 2NaCl+H SiO ↓
2 3 2 3
与CO 水溶液反应:Na SiO +CO +H O H SiO ↓+Na CO
2 2 3 2 2 2 3 2 3
2.用途:制作黏合剂(矿物胶)、耐火阻燃材料。P59
(二)硅酸盐表示方法
硅酸盐种类繁多,结构复杂,组成各异,通常用二氧化硅和金属氧
化物的组合形式表示其组成。
如硅酸钠(Na SiO ):Na O·SiO 。
2 3 2 2
复杂硅酸盐改写成氧化物的规则:
1.格式:金属氧化物•二氧化硅•水
2.顺序:金属氧化物按金属活动性顺序(或低价在前,高价在后,
若价态相同按活动性顺序)
如钾长石(KAlSi O ):K O·Al O ·6SiO ;
3 8 2 2 3 2
钾云母(KH Al Si O ):K O·3Al O ·6SiO ·2H O。
2 3 3 12 2 2 3 2 2P59
(三)硅酸盐工业
以含硅物质为原料经加热而制成硅酸盐产品的工业,叫作硅酸盐
工业。如制造水泥、玻璃、陶瓷等的工业都属于硅酸盐工业。陶瓷是
人类最早使用的硅酸盐材料。P59
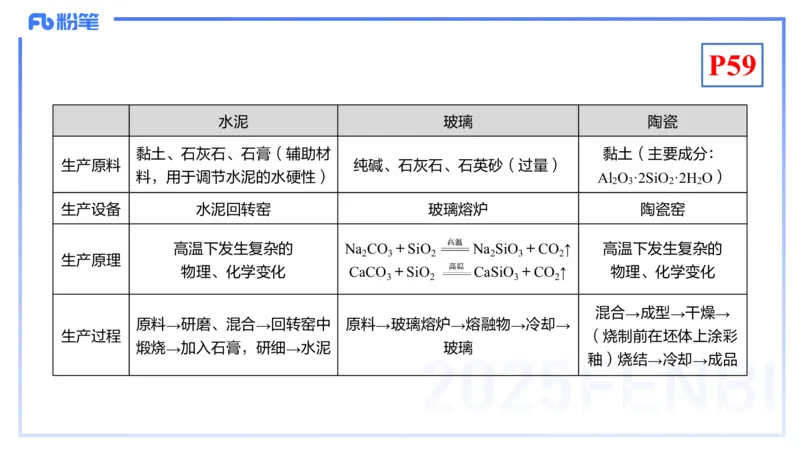
水泥 玻璃 陶瓷
黏土、石灰石、石膏(辅助材 黏土(主要成分:
生产原料 纯碱、石灰石、石英砂(过量)
料,用于调节水泥的水硬性) Al O ·2SiO ·2H O)
2 3 2 2
生产设备 水泥回转窑 玻璃熔炉 陶瓷窑
高温下发生复杂的 Na CO +SiO Na SiO +CO ↑ 高温下发生复杂的
2 3 2 2 3 2
生产原理
物理、化学变化 CaCO +SiO CaSiO +CO ↑ 物理、化学变化
3 2 3 2
混合→成型→干燥→
原料→研磨、混合→回转窑中 原料→玻璃熔炉→熔融物→冷却→
生产过程 (烧制前在坯体上涂彩
煅烧→加入石膏,研细→水泥 玻璃
釉)烧结→冷却→成品P60
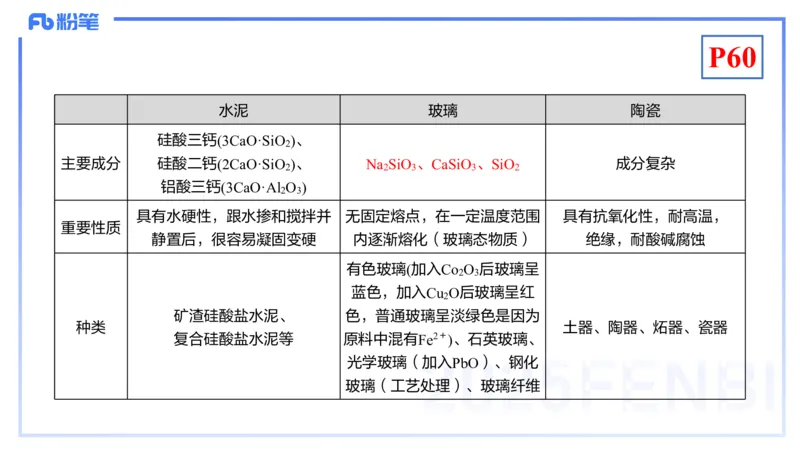
水泥 玻璃 陶瓷
硅酸三钙(3CaO·SiO )、
2
主要成分 硅酸二钙(2CaO·SiO )、 Na SiO 、CaSiO 、SiO 成分复杂
2 2 3 3 2
铝酸三钙(3CaO·Al O )
2 3
具有水硬性,跟水掺和搅拌并 无固定熔点,在一定温度范围 具有抗氧化性,耐高温,
重要性质
静置后,很容易凝固变硬 内逐渐熔化(玻璃态物质) 绝缘,耐酸碱腐蚀
有色玻璃(加入Co O 后玻璃呈
2 3
蓝色,加入Cu O后玻璃呈红
2
矿渣硅酸盐水泥、 色,普通玻璃呈淡绿色是因为
种类 土器、陶器、炻器、瓷器
复合硅酸盐水泥等 原料中混有Fe2+ )、石英玻璃、
光学玻璃(加入PbO)、钢化
玻璃(工艺处理)、玻璃纤维P60
(四)新型无机非金属材料
传统的无机非金属材料(硅酸盐材料) 新型无机非金属材料
高温结构陶瓷、生物陶瓷、
种类 普通水泥、普通玻璃、黏土质陶瓷等
压电陶瓷、光导纤维等
①能承受高温,强度大;
①耐腐蚀、耐高温; ②具有电学特性;
特性
②质脆、经不起热冲击 ③具有光学特性;
④具有生物功能P61
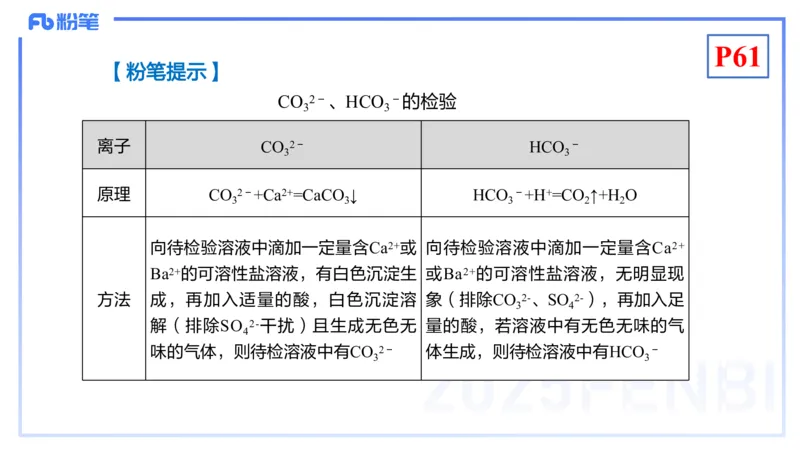
【粉笔提示】
CO 2-、HCO -的检验
3 3
离子 CO 2- HCO -
3 3
原理 CO 2-+Ca2+=CaCO ↓ HCO -+H+=CO ↑+H O
3 3 3 2 2
向待检验溶液中滴加一定量含Ca2+或 向待检验溶液中滴加一定量含Ca2+
Ba2+的可溶性盐溶液,有白色沉淀生 或Ba2+的可溶性盐溶液,无明显现
方法 成,再加入适量的酸,白色沉淀溶 象(排除CO 2-、SO 2-),再加入足
3 4
解(排除SO 2-干扰)且生成无色无 量的酸,若溶液中有无色无味的气
4
味的气体,则待检溶液中有CO 2- 体生成,则待检溶液中有HCO -
3 3P61
1. 不能用 Ca(OH) 溶液和 Ba(OH) 溶液检验 CO 2−和 HCO −,原因
2 2 3 3
是 OH– 能将 HCO −转化为 CO 2−。
3 3
2. 加酸后可根据气体是否有气味排除 SO 2−、HSO −的干扰。
3 3
3. 不能用加酸看是否有无色气体产生的方法检验 CO 2−和 HCO −,
3 3
因为 CO 2−与 HCO −两种离子都有该现象发生。
3 3P61
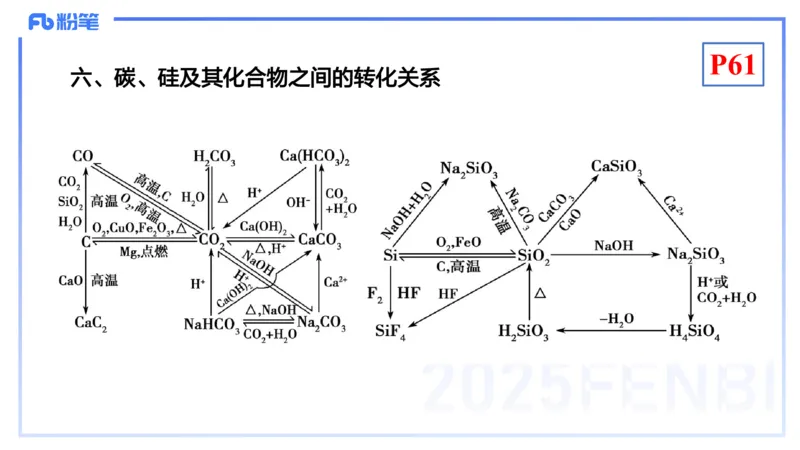
六、碳、硅及其化合物之间的转化关系P61
化学与社会生活密切相关,下列说法正确的是( )。
A. 菜籽油都是利用萃取方法制取的
B. 造纸的主要原料是纤维素和低聚糖
C. 高纯度晶体硅被广泛用于制作光导纤维
D. 煤经过气化和液化等处理可转变为清洁能源氯、溴、碘及其化合物P62
一、氯气的性质和用途
(一)物理性质
通常氯气为黄绿色、有强烈刺激性气味、密度比空气大的有毒气
体,易液化。25 ℃时,1体积水约溶解2体积氯气,其水溶液俗称氯水,
为淡黄绿色。P62
(二)化学性质
氯原子的结构:
氯气是一种活泼的非金属单质,化学性质很活泼,是强氧化剂。1.与金属反应(与变价金属反应,将金属氧化至高价态)
P62
2Na+Cl 2NaCl(白烟)
2
2Fe+3Cl 2FeCl (棕褐色烟)
2 3
Cu+Cl CuCl (棕黄色烟)
2 2
注意:常温下干燥的氯气或液氯不能与铁发生反应,所以工业上
常把干燥的液氯储存在钢瓶中。2.与非金属反应
P63
H +Cl 2HCl(苍白色火焰、白雾)
2 2
2P+3Cl 2PCl (Cl 不足)(白雾)
2 3 2
2P+5Cl 2PCl (Cl 充足)(白烟)
2 5 2
3.与水反应
Cl +H O HCl+HClO(强氧化性)
2 2
2HClO 2HCl+O ↑(HClO不稳定,见光易分解)
2【粉笔提示】 P63
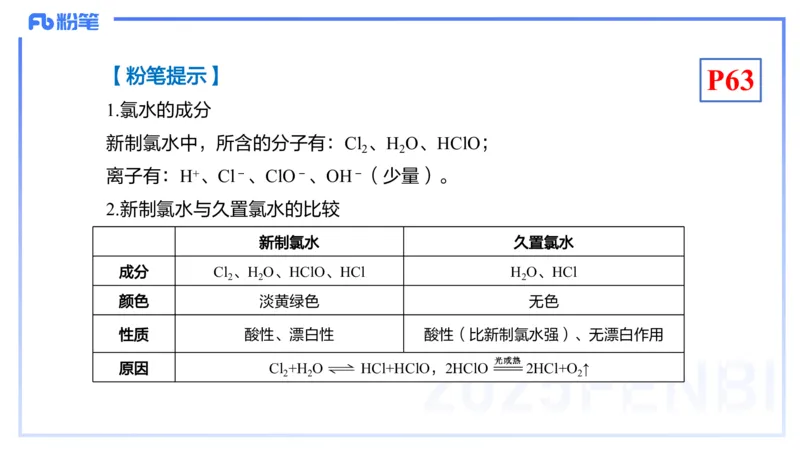
1.氯水的成分
新制氯水中,所含的分子有:Cl 、H O、HClO;
2 2
离子有:H+、Cl-、ClO-、OH-(少量)。
2.新制氯水与久置氯水的比较
新制氯水 久置氯水
成分 Cl 、H O、HClO、HCl H O、HCl
2 2 2
颜色 淡黄绿色 无色
性质 酸性、漂白性 酸性(比新制氯水强)、无漂白作用
原因 Cl +H O HCl+HClO,2HClO 2HCl+O ↑
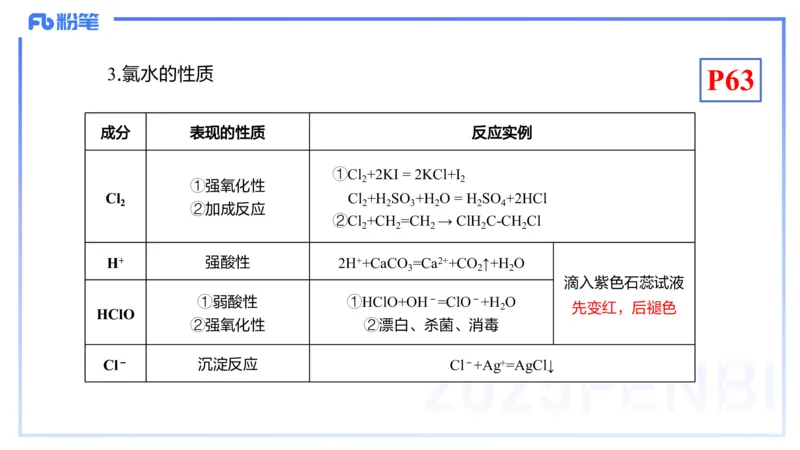
2 2 23.氯水的性质
P63
成分 表现的性质 反应实例
①Cl +2KI = 2KCl+I
2 2
①强氧化性
Cl Cl +H SO +H O = H SO +2HCl
2 2 2 3 2 2 4
②加成反应
②Cl +CH =CH → ClH C-CH Cl
2 2 2 2 2
H+ 强酸性 2H++CaCO =Ca2++CO ↑+H O
3 2 2
滴入紫色石蕊试液
①弱酸性 ①HClO+OH-=ClO-+H O
2 先变红,后褪色
HClO
②强氧化性 ②漂白、杀菌、消毒
Cl- 沉淀反应 Cl-+Ag+=AgCl↓P64
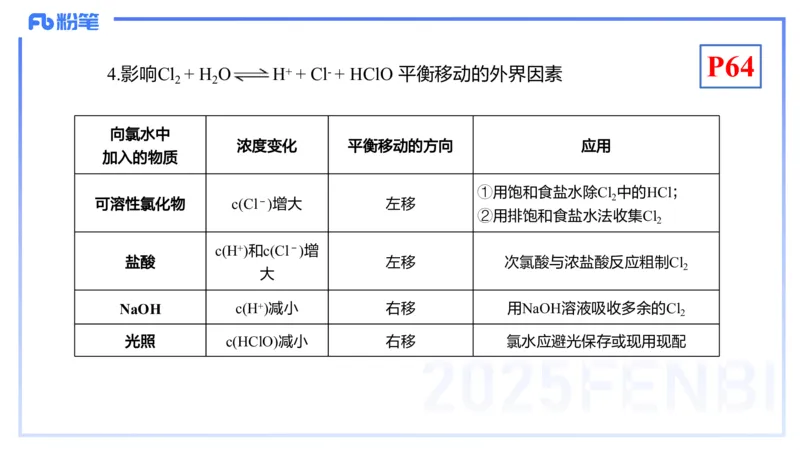
4.影响Cl + H O H+ + Cl- + HClO 平衡移动的外界因素
2 2
向氯水中
浓度变化 平衡移动的方向 应用
加入的物质
①用饱和食盐水除Cl 中的HCl;
2
可溶性氯化物 c(Cl-)增大 左移
②用排饱和食盐水法收集Cl
2
c(H+)和c(Cl-)增
盐酸 左移 次氯酸与浓盐酸反应粗制Cl
2
大
NaOH c(H+)减小 右移 用NaOH溶液吸收多余的Cl
2
光照 c(HClO)减小 右移 氯水应避光保存或现用现配4.与碱反应
P64
Cl +2NaOH NaCl+NaClO+H O
2 2
2Cl +2Ca(OH) CaCl +Ca(ClO) +2H O
2 2 2 2 2
补充:实质是氯气先与水反应生成酸,酸再与碱反应
①Cl +H O HCl+HClO
2 2
②HCl+NaOH NaCl+H O
2
③HClO+NaOH NaClO+H O
2
漂白粉发挥作用或失效的原理为:
CO +Ca(ClO) +H O CaCO +2HClO
2 2 2 35.与还原性物质反应
P64
Cl +SO +2H O H SO +2HCl
2 2 2 2 4
2KI+Cl 2KCl+I
2 2
2FeCl +Cl 2FeCl
2 2 3
6.与有机物反应
CH +Cl CH Cl+HCl
4 2 3(三)氯离子的检验 P64
在用AgNO 溶液检验Cl-时,一般先在被检测的溶液中滴入少量
3
稀硝酸使其酸化,以排除干扰离子。
(四)氯气的用途
制漂粉精,消毒,制盐酸、农药、氯仿等。P68
1. 已知甲、乙、丙、丁、戊均为中学化学常见物质,其中甲为非金属
单质,常温下为黄绿色气体,乙为金属单质,丙为含甲元素的酸,它们在
一定条件下能发生如下转化:
下列说法正确的是( )。
A. 甲是常用的还原剂 B. 丙是常用的氧化剂
C. 丁比戊中所含元素种类多 D. 乙与丁反应可得到戊粉笔教师教育 粉笔教师