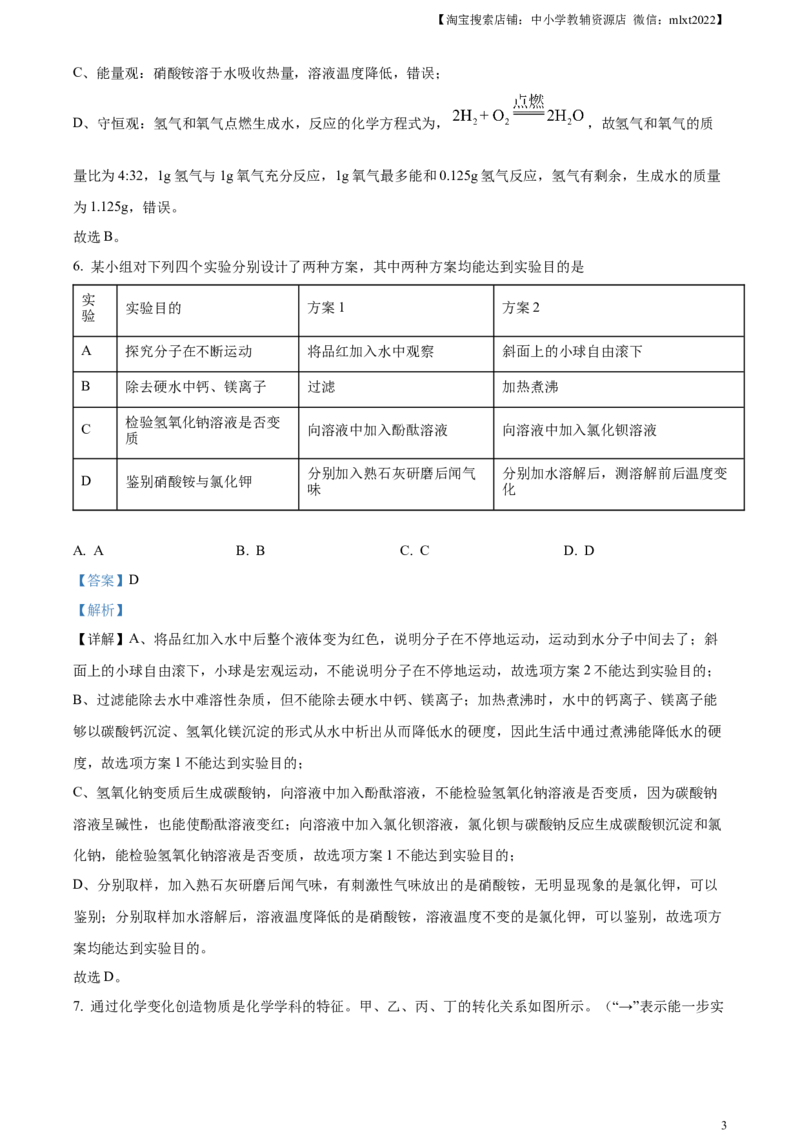文档内容
【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
贵州省 2023 年初中学业水平考试
化学部分
可能用到的相对原子质量:H-1 C-12 O-16 Zn-65
一、化学选择题:本题共7个小题,每小题2分,共14分。每题只有一个选项符合题意.
1. “绿水青山就是金山银山”体现了生态文明思想。下列不符合这一思想的做法是
A. 生活垃圾分类处理,节约资源能源 B. 合理使用农药化肥,增加粮食产量
C. 化石燃料取之不尽,提倡大量使用 D. 使用公共交通出行,减少尾气污染
【答案】C
【解析】
【详解】A、生活垃圾分类处理,节约资源能源,减少污染,体现了生态文明思想,故A不符合题意;
B、合理使用农药化肥,增加粮食产量,减少污染,避免浪费,体现了生态文明思想,故B不符合题意;
C、化石燃料的储量有限,短时间内不会再生,不能大量使用,故C符合题意;
D、使用公共交通出行,减少尾气污染,体现了生态文明思想,故D不符合题意。
故选C。
的
2. 下列实验安全规范或基本操作正确 是
A. 将未用完的药品放回原试剂瓶 B. 稀释浓硫酸时,将水倒入浓硫酸
C. 制取气体前应检查装置的气密性 D. 将pH试纸直接放入待测液测试
【答案】C
【解析】
【详解】A、不能将未用完的药品放回原试剂瓶中,以防止污染试剂,应放入指定的容器中,不符合题意;
B、稀释浓硫酸时,应将浓硫酸沿烧杯内壁缓慢倒入水中,并不断用玻璃棒搅拌,使产生的热量及时散发
出去,不符合题意;
C、实验室制取气体,装药品前先检查装置的气密性,否则会漏气,造成药品浪费,符合题意;
D、用pH试纸测定溶液pH的具体操作为:将一小片pH试纸放在白瓷板或玻璃片上,用干净的玻璃棒蘸
取被测溶液并滴在pH试纸上,把pH试纸显示的颜色与标准比色卡比较,读出该溶液的pH,将pH试纸直
接放入待测液测试会污染待测液,不符合题意;
故选C。
3. 下列变化中不涉及化学变化的是
A. 用体温计测量体温 B. 用黄豆酿造酱油
C. 用生石灰作干燥剂 D. 用食醋去除水垢
1【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
【答案】A
【解析】
【详解】A、用体温计测量体温,没有新物质生成,属于物理变化;
B、用黄豆酿造酱油,发生缓慢氧化,有新物质生成,属于化学变化;
C、用生石灰作干燥剂,有新物质氢氧化钙生成,属于化学变化;
D、用食醋去除水垢,有二氧化碳等新物质生成,属于属于化学变化。
故选A。
4. 答题卡上条形码的黏性主要来源于胶黏剂—丙烯酸(化学式为 ),下列说法正确的是
A. 丙烯酸的物质类别是氧化物
B. 丙烯酸中碳元素与氧元素的质量比为9:8
C. 丙烯酸的相对分子质量为72g
D. 丙烯酸由3个碳原子、4个氢原子和2个氧原子构成
【答案】B
【解析】
【详解】A、丙烯酸(化学式为 C HO )是由C、H、O元素组成的,不属于氧化物,故A错误;
3 4 2
B、丙烯酸中碳元素与氧元素的质量比为: =9:8,故B正确;
C、相对分子质量的单位不是“g”,故C错误;
D、丙烯酸是由丙烯酸分子构成的,1个丙烯酸分子是由3个碳原子、4个氢原子和2个氧原子构成,故D
错误。
故选B。
5. 构建化学基本观念是学好化学的基础,下列认识正确的是
A. 微粒观:构成氯化钠的微粒是氯化钠分子
B. 结构观: 和 的分子构成不同,化学性质不同
C. 能量观:硝酸铵溶于水吸收热量,溶液温度升高
D. 守恒观:1g氢气与1g氧气充分反应,生成2g水
【答案】B
【解析】
【详解】A、微粒观:构成氯化钠的微粒是氯离子和钠离子,错误;
B、结构观: 由水分子构成, 由过氧化氢分子构成,二者的分子构成不同,化学性质不同,正
确;
2【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
C、能量观:硝酸铵溶于水吸收热量,溶液温度降低,错误;
D、守恒观:氢气和氧气点燃生成水,反应的化学方程式为, ,故氢气和氧气的质
量比为4:32,1g氢气与1g氧气充分反应,1g氧气最多能和0.125g氢气反应,氢气有剩余,生成水的质量
为1.125g,错误。
故选B。
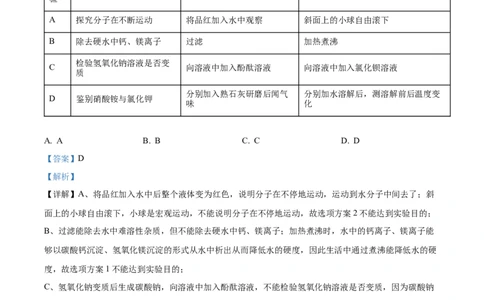
6. 某小组对下列四个实验分别设计了两种方案,其中两种方案均能达到实验目的是
实
实验目的 方案1 方案2
验
A 探究分子在不断运动 将品红加入水中观察 斜面上的小球自由滚下
B 除去硬水中钙、镁离子 过滤 加热煮沸
检验氢氧化钠溶液是否变
C 向溶液中加入酚酞溶液 向溶液中加入氯化钡溶液
质
分别加入熟石灰研磨后闻气 分别加水溶解后,测溶解前后温度变
D 鉴别硝酸铵与氯化钾
味 化
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A、将品红加入水中后整个液体变为红色,说明分子在不停地运动,运动到水分子中间去了;斜
面上的小球自由滚下,小球是宏观运动,不能说明分子在不停地运动,故选项方案2不能达到实验目的;
B、过滤能除去水中难溶性杂质,但不能除去硬水中钙、镁离子;加热煮沸时,水中的钙离子、镁离子能
够以碳酸钙沉淀、氢氧化镁沉淀的形式从水中析出从而降低水的硬度,因此生活中通过煮沸能降低水的硬
度,故选项方案1不能达到实验目的;
C、氢氧化钠变质后生成碳酸钠,向溶液中加入酚酞溶液,不能检验氢氧化钠溶液是否变质,因为碳酸钠
溶液呈碱性,也能使酚酞溶液变红;向溶液中加入氯化钡溶液,氯化钡与碳酸钠反应生成碳酸钡沉淀和氯
化钠,能检验氢氧化钠溶液是否变质,故选项方案1不能达到实验目的;
D、分别取样,加入熟石灰研磨后闻气味,有刺激性气味放出的是硝酸铵,无明显现象的是氯化钾,可以
鉴别;分别取样加水溶解后,溶液温度降低的是硝酸铵,溶液温度不变的是氯化钾,可以鉴别,故选项方
案均能达到实验目的。
故选D。
7. 通过化学变化创造物质是化学学科的特征。甲、乙、丙、丁的转化关系如图所示。(“→”表示能一步实
3【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
现反应,部分物质和反应条件已略去),下列说法中错误的是
A. 若甲为 ,则丁可以是Fe或
B. 若甲为 ,则丁→甲不可以是复分解反应
C. 若甲为 ,则丙可以是水
D. 若甲为NaOH,则丙可以是
【答案】D
【解析】
【详解】A、若甲为H,丁可以是铁或水,铁和酸反应生成氢气,水通电生成氢气和氧气,不符合题意;
2
B、复分解反应是两种化合物互相交换成分生成另外两种化合物的反应,其产物均是化合物,而氢气属于
单质,故若甲为 ,则丁→甲不可以是复分解反应,不符合题意;
C、若甲为 ,乙可以是碳酸,则丙可以是水,丁可以是碳酸氢钙,不符合题意;
D、若甲为NaOH,则丙不可以是 ,因为丙若是硝酸铁,则乙是氧化铁或亚铁盐,而氢氧化钠
不能一步转化为氧化铁或亚铁盐,符合题意;
故选:D。
二、化学非选择题:本题共7个小题,共46分.
8. 生活中处处有化学。
(1)我们的生活离不开空气,请写出空气中所含的一种物质的名称______。
(2)人体需要营养物质。请写出贵阳肠旺面、花溪牛肉粉、遵义豆花面、都匀冲冲糕、毕节汤圆、镇宁
波波糖等贵州著名小吃中所含有的营养素______(写一种)。
(3)山药中含有碱性皂角素,皮肤沾上会奇痒难忍,可以涂抹厨房中的_______选填(“食醋”或者“食
盐”)来止痒。
(4)水果、蔬菜常用塑料保鲜膜进行保鲜 。塑料属于_______(选填“天然”或“合成”)有机高分子材
4【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
料。
(5)粮食增产在一定程度上依赖肥料的使用。常用的化学肥料有尿素[ ]、硝酸铵(
)、硫酸钾( )、磷酸氢二铵[ ]等,其中属于钾肥的是________。
(6)用木炭烧烤,木炭充分燃烧时的化学方程式为________。
【答案】(1)氮气(合理即可)
(2)糖类(合理即可)
(3)食醋 (4)合成
(5)硫酸钾##
(6)
【解析】
【小问1详解】
空气中的成分按体积计算,由多到少的顺序依次是氮气、氧气、稀有气体、二氧化碳、其它气体等,故可
填氮气、氧气、二氧化碳等,不可填稀有气体、其它气体,其属于混合物,不是一种物质(纯净物);
【小问2详解】
贵阳肠旺面、遵义豆花面、都匀冲冲糕、毕节汤圆、镇宁波波糖中富含糖类,花溪牛肉粉中富含蛋白质、
糖类;
【小问3详解】
碱性皂角素可以与食醋发生反应,以减弱皂角素对人体皮肤的刺激;
【小问4详解】
日常生活中使用最多的塑料、合成纤维和合成橡胶等则属于合成有机高分子材料,简称有机合成材料;
【小问5详解】
[ ]中含有N营养元素,属于氮肥;
硝酸铵( )中含有N营养元素,属于氮肥;
硫酸钾( )中含有K营养元素,属于钾肥;
磷酸氢二铵[ ]中含有N、P两种营养元素,属于复合肥;
【小问6详解】
5【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
碳与氧气发生充分燃烧反应生成二氧化碳,化学方程式 。
为
9. 从微观的角度研究物质的组成、结构、性质及其变化规律是化学学科的特色。
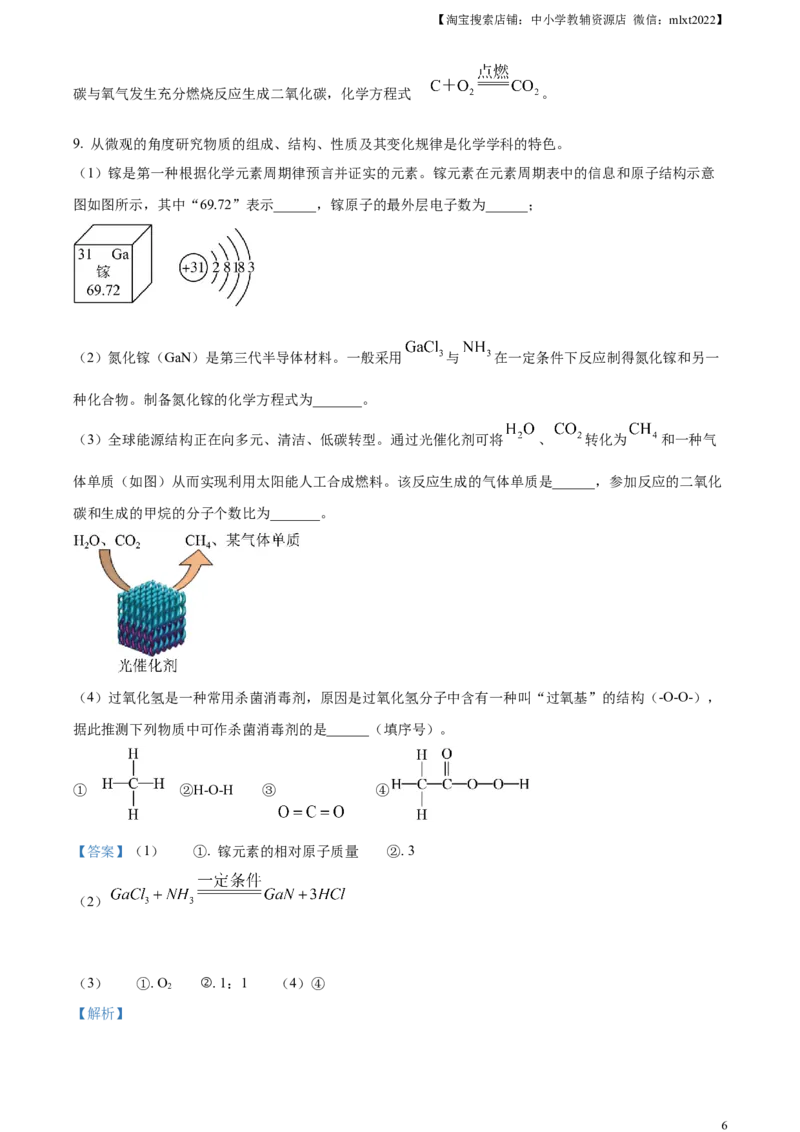
(1)镓是第一种根据化学元素周期律预言并证实的元素。镓元素在元素周期表中的信息和原子结构示意
图如图所示,其中“69.72”表示______,镓原子的最外层电子数为______;
(2)氮化镓(GaN)是第三代半导体材料。一般采用 与 在一定条件下反应制得氮化镓和另一
种化合物。制备氮化镓的化学方程式为_______。
(3)全球能源结构正在向多元、清洁、低碳转型。通过光催化剂可将 、 转化为 和一种气
体单质(如图)从而实现利用太阳能人工合成燃料。该反应生成的气体单质是______,参加反应的二氧化
碳和生成的甲烷的分子个数比为_______。
(4)过氧化氢是一种常用杀菌消毒剂,原因是过氧化氢分子中含有一种叫“过氧基”的结构(-O-O-),
据此推测下列物质中可作杀菌消毒剂的是______(填序号)。
① ②H-O-H ③ ④
【答案】(1) ①. 镓元素的相对原子质量 ②. 3
(2)
(3) ①. O ②. 1:1 (4)④
2
【解析】
6【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
【小问1详解】
周期表中下面的数字表示相对原子质量,则“69.72”表示镓元素的相对原子质量;根据镓原子的结构示意
图可知,镓原子的最外层电子数为3;
【小问2详解】
GaCl 与NH 在一定条件下反应制得氮化镓和另一种化合物,依据质量守恒定律,反应前后元素的种类不
3 3
变,另一种化合物为HCl,反应的化学方程式为: ;
【小问3详解】
依据质量守恒定律,反应前后元素的种类不变,反应物中有H、O、C元素,生成物中有C、H元素,所以
该反应生成的气体单质是O;反应的化学方程式为: ,所以参加反应
2
的二氧化碳和生成的甲烷的分子个数比为1:1;
【小问4详解】
根据物质的结构,①②③中没有“过氧基”的结构(-O-O-),④中有“过氧基”的结构(-O-O-),故④
可作杀菌消毒剂。
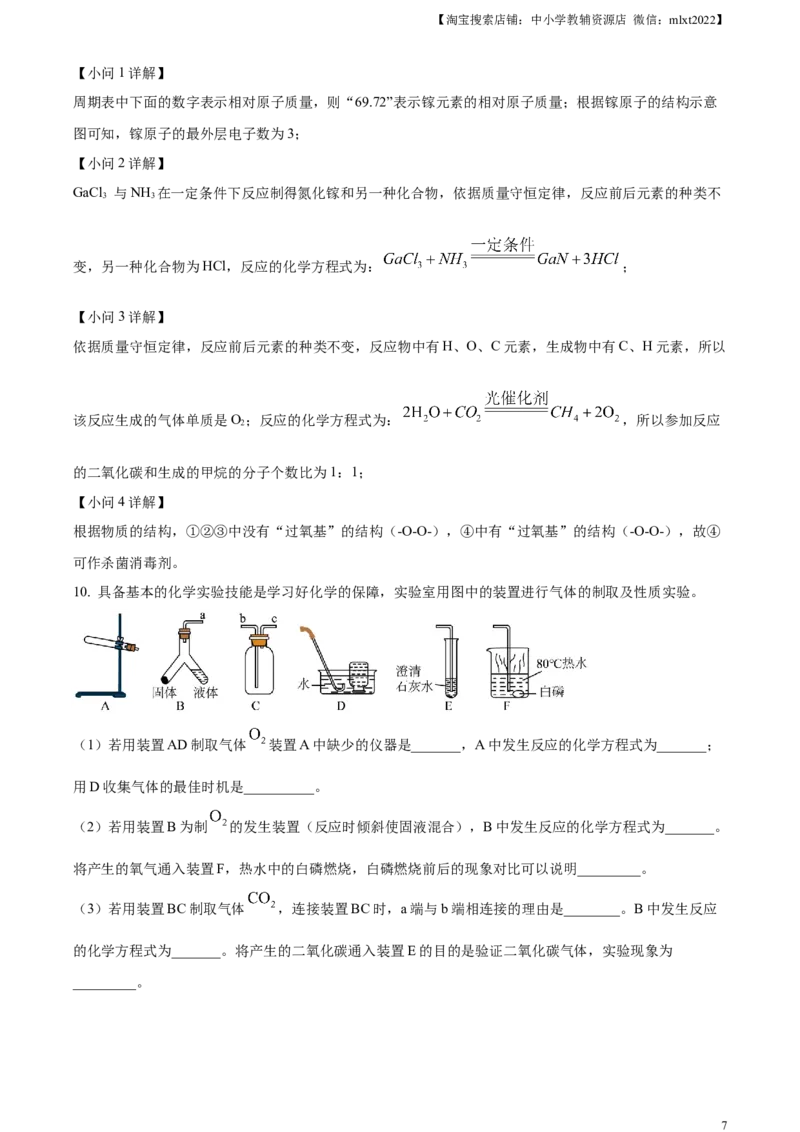
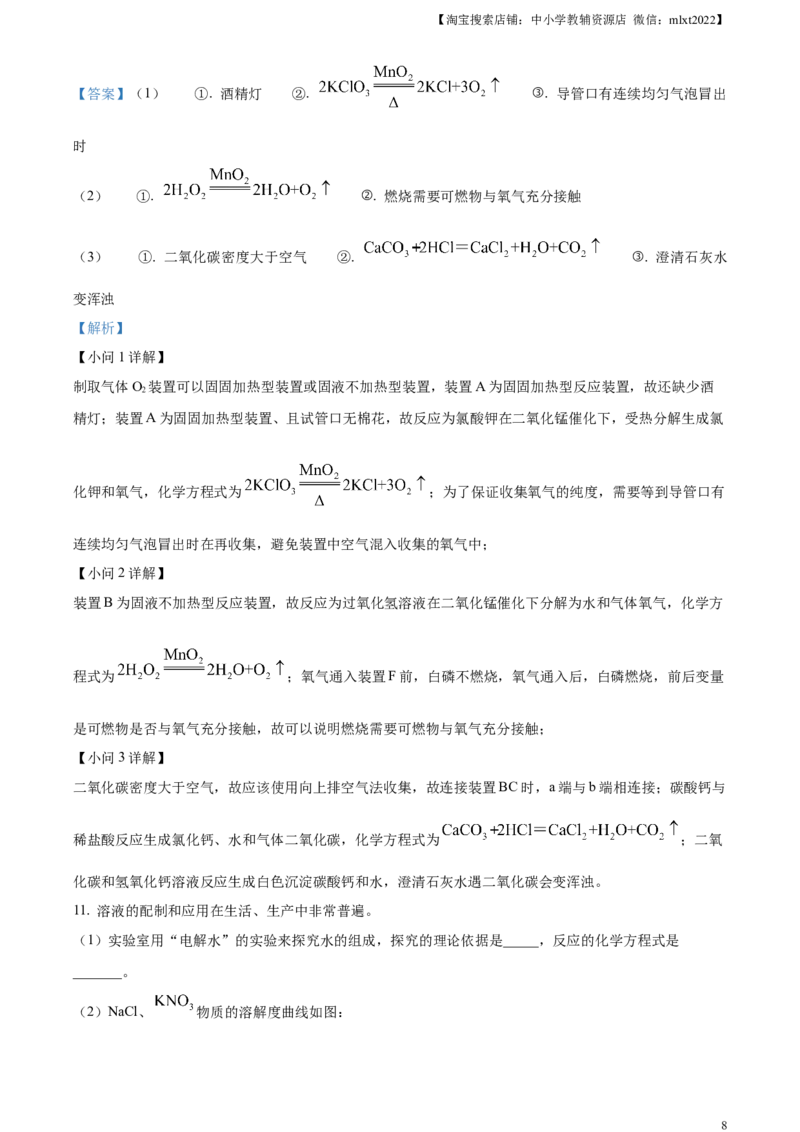
10. 具备基本的化学实验技能是学习好化学的保障,实验室用图中的装置进行气体的制取及性质实验。
(1)若用装置AD制取气体 装置A中缺少的仪器是_______,A中发生反应的化学方程式为_______;
用D收集气体的最佳时机是__________。
(2)若用装置B为制 的发生装置(反应时倾斜使固液混合),B中发生反应的化学方程式为_______。
将产生的氧气通入装置F,热水中的白磷燃烧,白磷燃烧前后的现象对比可以说明_________。
(3)若用装置BC制取气体 ,连接装置BC时,a端与b端相连接的理由是________。B中发生反应
的化学方程式为_______。将产生的二氧化碳通入装置E的目的是验证二氧化碳气体,实验现象为
_________。
7【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
【答案】(1) ①. 酒精灯 ②. ③. 导管口有连续均匀气泡冒出
时
(2) ①. ②. 燃烧需要可燃物与氧气充分接触
(3) ①. 二氧化碳密度大于空气 ②. ③. 澄清石灰水
变浑浊
【解析】
【小问1详解】
制取气体O 装置可以固固加热型装置或固液不加热型装置,装置A为固固加热型反应装置,故还缺少酒
2
精灯;装置A为固固加热型装置、且试管口无棉花,故反应为氯酸钾在二氧化锰催化下,受热分解生成氯
化钾和氧气,化学方程式为 ;为了保证收集氧气的纯度,需要等到导管口有
连续均匀气泡冒出时在再收集,避免装置中空气混入收集的氧气中;
【小问2详解】
装置B为固液不加热型反应装置,故反应为过氧化氢溶液在二氧化锰催化下分解为水和气体氧气,化学方
程式为 ;氧气通入装置F前,白磷不燃烧,氧气通入后,白磷燃烧,前后变量
是可燃物是否与氧气充分接触,故可以说明燃烧需要可燃物与氧气充分接触;
【小问3详解】
二氧化碳密度大于空气,故应该使用向上排空气法收集,故连接装置BC时,a端与b端相连接;碳酸钙与
稀盐酸反应生成氯化钙、水和气体二氧化碳,化学方程式为 ;二氧
化碳和氢氧化钙溶液反应生成白色沉淀碳酸钙和水,澄清石灰水遇二氧化碳会变浑浊。
11. 溶液的配制和应用在生活、生产中非常普遍。
(1)实验室用“电解水”的实验来探究水的组成,探究的理论依据是_____,反应的化学方程式是
_______。
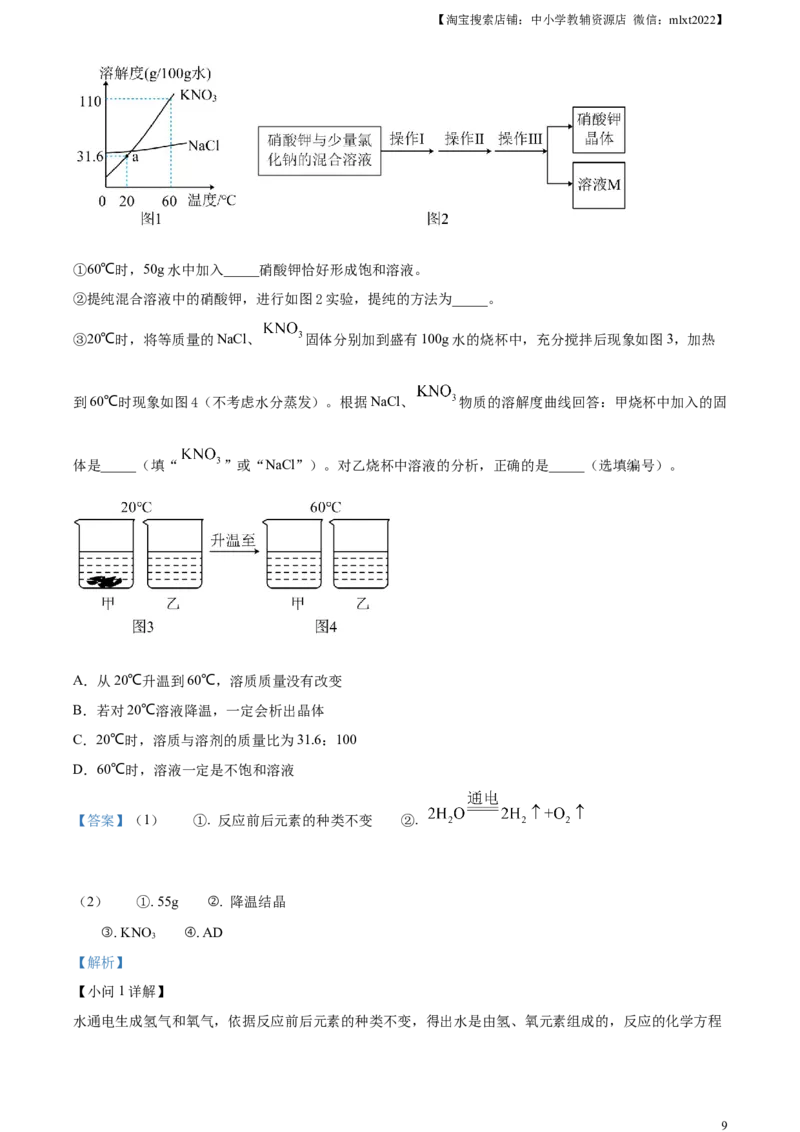
(2)NaCl、 物质的溶解度曲线如图:
8【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
①60℃时,50g水中加入_____硝酸钾恰好形成饱和溶液。
②提纯混合溶液中的硝酸钾,进行如图2实验,提纯的方法为_____。
③20℃时,将等质量的NaCl、 固体分别加到盛有100g水的烧杯中,充分搅拌后现象如图3,加热
到60℃时现象如图4(不考虑水分蒸发)。根据NaCl、 物质的溶解度曲线回答:甲烧杯中加入的固
体是_____(填“ ”或“NaCl”)。对乙烧杯中溶液的分析,正确的是_____(选填编号)。
A.从20℃升温到60℃,溶质质量没有改变
B.若对20℃溶液降温,一定会析出晶体
C.20℃时,溶质与溶剂的质量比为31.6:100
D.60℃时,溶液一定是不饱和溶液
【答案】(1) ①. 反应前后元素的种类不变 ②.
(2) ①. 55g ②. 降温结晶
③. KNO ④. AD
3
【解析】
【小问1详解】
水通电生成氢气和氧气,依据反应前后元素的种类不变,得出水是由氢、氧元素组成的,反应的化学方程
9【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
式是: ;
【小问2详解】
①60℃时,硝酸钾的溶解度为110g,所以50g水中加入55g硝酸钾恰好形成饱和溶液;
②由图可知,硝酸钾和氯化钠的溶解度均随温度升高而增大,硝酸钾的溶解度受温度影响较大,氯化钠的
溶解度受温度影响较小,提纯硝酸钾可用冷却热饱和溶液的方法,故操作Ⅰ是蒸发浓缩,操作Ⅱ是降温结
晶,再经操作Ⅲ过滤将硝酸钾晶体和溶液分开,故操作II的名称为降温结晶;
③20℃时,将等质量的NaCl、KNO 固体分别加入到盛有100g水的烧杯中,甲部分溶解,乙全部溶解,说
3
明乙溶解度大,由图1可知,甲为硝酸钾,乙为氯化钠,故填:KNO;
3
A、从20℃升温到60℃,氯化钠溶解度缓慢变大,溶质质量没有改变,正确;
B、乙烧杯中溶液可能是不饱和溶液,若对20℃溶液降温,不一定会析出晶体,错误;
C、20℃时,硝酸钾有固体不溶解,说明加入溶质质量大于31.6g,故该温度下,乙烧杯中溶质与溶剂的质
量比大于31.6:100,错误;
D、20℃时,乙烧杯中溶液可能是不饱和溶液,也可能是刚刚饱和,升高温度,溶解度变大,60℃时,溶
液一定是不饱和溶液,正确。
故填AD。
12. 对于金属材料,我们应该从多角度了解。
Ⅰ金属冶炼
(1)《天工开物》中记载了炼锡的场景:“凡煎炼亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞴
(指鼓入空气)熔化。”
①鼓入足量空气的目的是_______,从而提高炉温。
②“点铅勾锡”是炼锡的关键步骤,加铅能使锡较易熔化流出,其原因是________。
Ⅱ金属的活动性
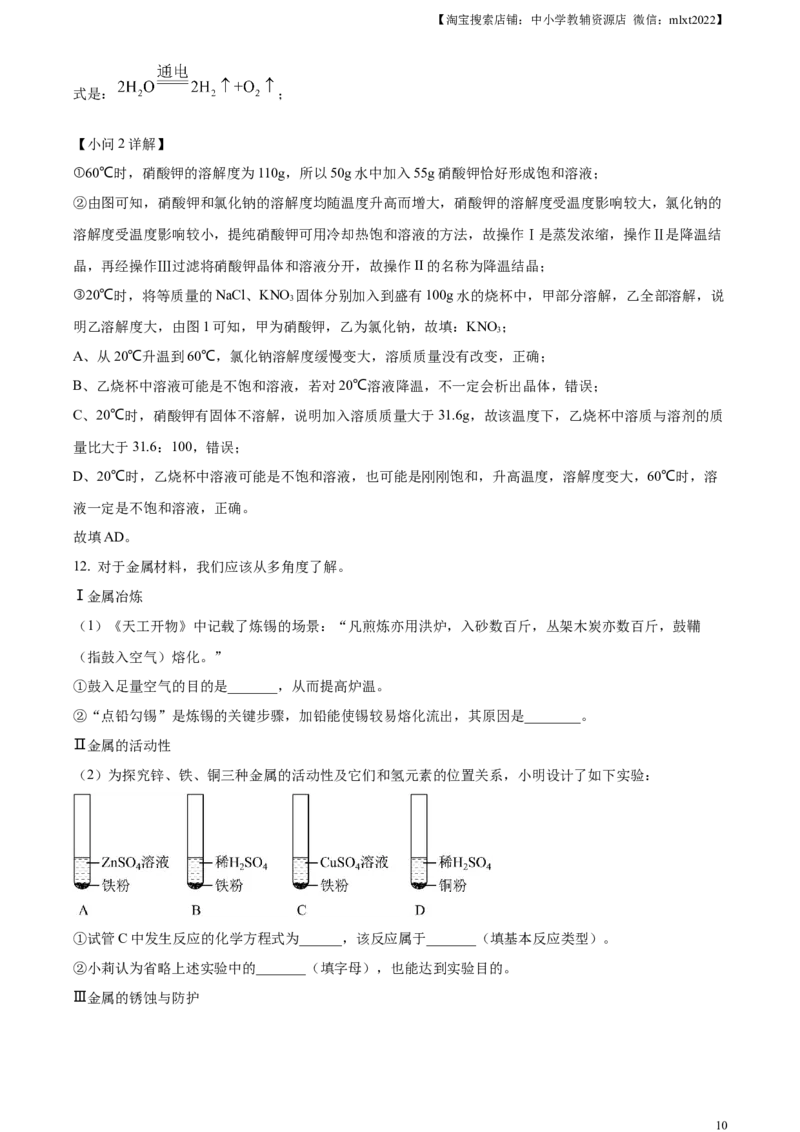
(2)为探究锌、铁、铜三种金属的活动性及它们和氢元素的位置关系,小明设计了如下实验:
①试管C中发生反应的化学方程式为______,该反应属于_______(填基本反应类型)。
②小莉认为省略上述实验中的_______(填字母),也能达到实验目的。
Ⅲ金属的锈蚀与防护
10【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
(3)对钢铁制品进行“发蓝”处理,使其表面生成一层致密的氧化膜,能有效防止钢铁锈蚀。
①“发蓝”过程属于______(填“物理”或“化学”)变化。
的
②“发蓝”能防止钢铁锈蚀 原因是_________。
Ⅳ金属的回收再利用
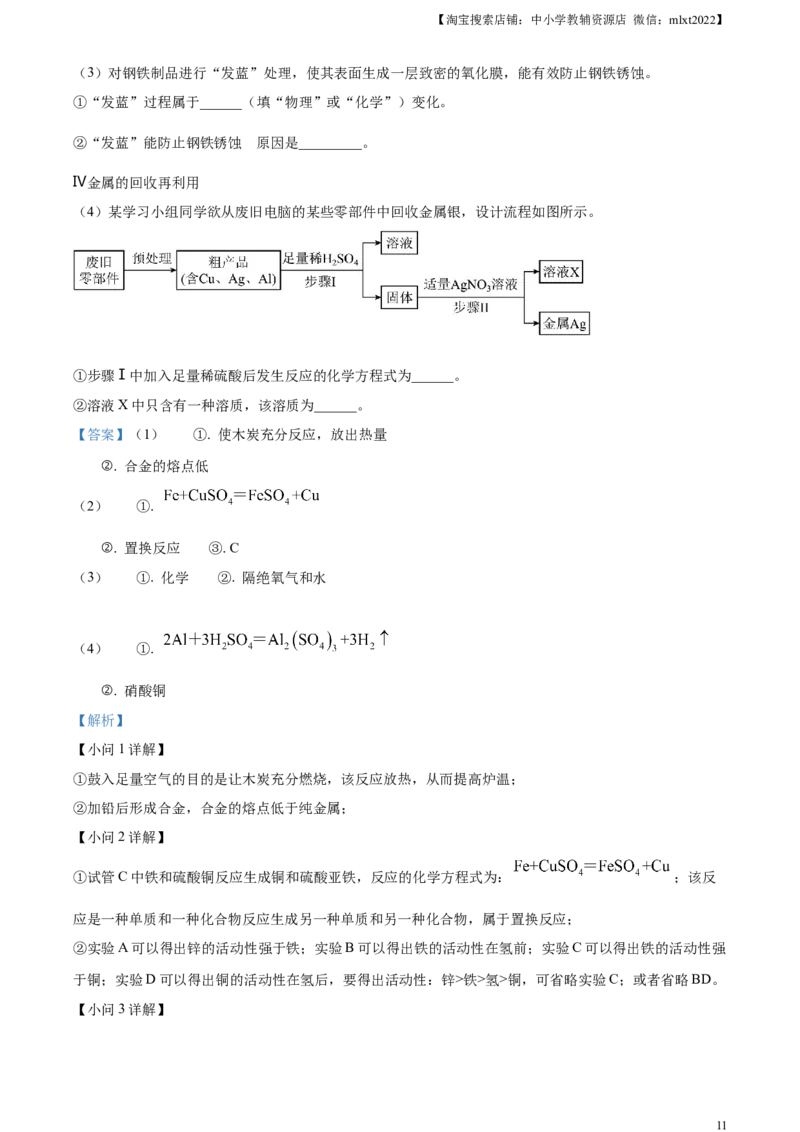
(4)某学习小组同学欲从废旧电脑的某些零部件中回收金属银,设计流程如图所示。
①步骤Ⅰ中加入足量稀硫酸后发生反应的化学方程式为______。
②溶液X中只含有一种溶质,该溶质为______。
【答案】(1) ①. 使木炭充分反应,放出热量
②. 合金的熔点低
(2) ①.
②. 置换反应 ③. C
(3) ①. 化学 ②. 隔绝氧气和水
(4) ①.
②. 硝酸铜
【解析】
【小问1详解】
①鼓入足量空气的目的是让木炭充分燃烧,该反应放热,从而提高炉温;
②加铅后形成合金,合金的熔点低于纯金属;
【小问2详解】
①试管C中铁和硫酸铜反应生成铜和硫酸亚铁,反应的化学方程式为: ;该反
应是一种单质和一种化合物反应生成另一种单质和另一种化合物,属于置换反应;
②实验A可以得出锌的活动性强于铁;实验B可以得出铁的活动性在氢前;实验C可以得出铁的活动性强
于铜;实验D可以得出铜的活动性在氢后,要得出活动性:锌>铁>氢>铜,可省略实验C;或者省略BD。
【小问3详解】
11【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
①“发蓝”过程是使其表面生成一层致密的氧化膜,有新物质生成,属于化学变化;
②铁生锈是与氧气和水共同作用,“发蓝”能防止钢铁锈蚀的原因是隔绝了氧气和水;
【小问4详解】
①步骤Ⅰ中加入足量稀硫酸后,铜、银不反应,铝和硫酸反应生成硫酸铝和氢气,反应的化学方程式为:
;
②步骤Ⅰ过滤出的固体中含有铜、银,加入适量硝酸银溶液,铜和硝酸银反应生成银和硝酸铜,故溶液X
中含有硝酸铜。
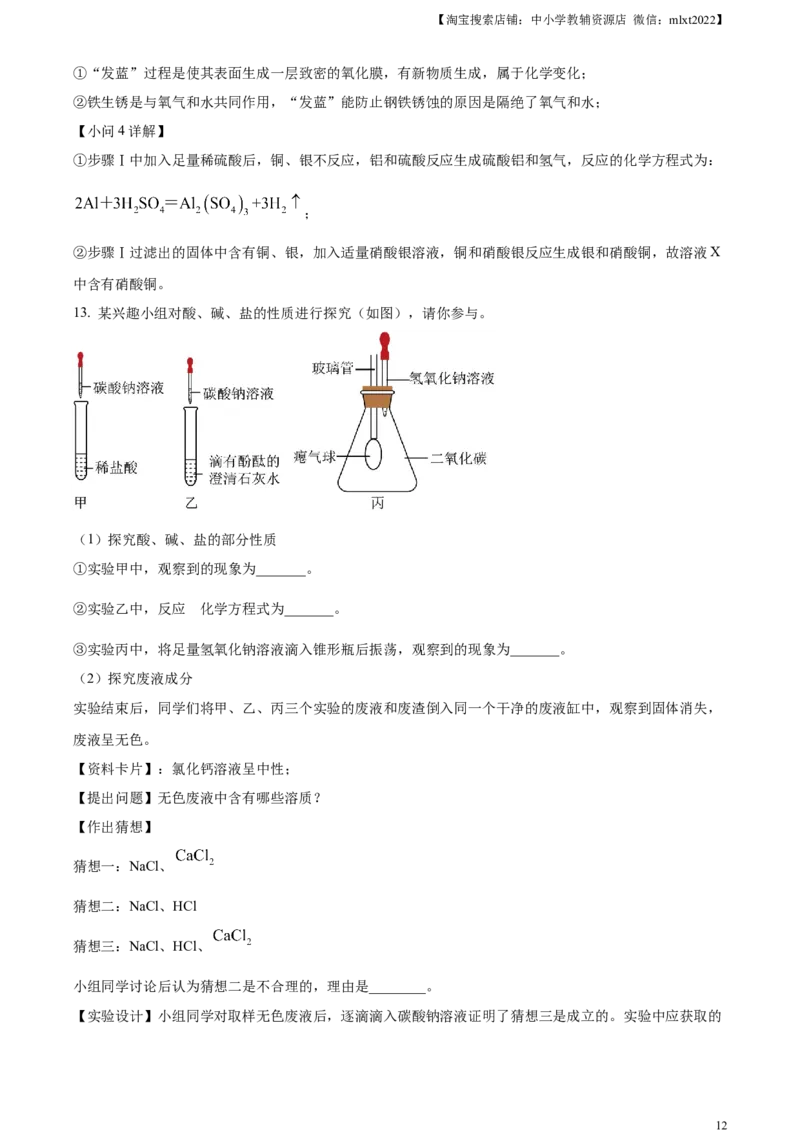
13. 某兴趣小组对酸、碱、盐的性质进行探究(如图),请你参与。
(1)探究酸、碱、盐的部分性质
①实验甲中,观察到的现象为_______。
的
②实验乙中,反应 化学方程式为_______。
③实验丙中,将足量氢氧化钠溶液滴入锥形瓶后振荡,观察到的现象为_______。
(2)探究废液成分
实验结束后,同学们将甲、乙、丙三个实验的废液和废渣倒入同一个干净的废液缸中,观察到固体消失,
废液呈无色。
【资料卡片】:氯化钙溶液呈中性;
【提出问题】无色废液中含有哪些溶质?
【作出猜想】
猜想一:NaCl、
猜想二:NaCl、HCl
猜想三:NaCl、HCl、
小组同学讨论后认为猜想二是不合理的,理由是________。
【实验设计】小组同学对取样无色废液后,逐滴滴入碳酸钠溶液证明了猜想三是成立的。实验中应获取的
12【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
证据为_______,发生的化学方程式为______。
【反思总结】通过以上探究实验,可归纳出碱的化学性质有________。
【答案】(1) ①. 有气泡产生 ②.
③. 气球膨胀
(2) ①. 一定存在氯化钙 ②. 先有气泡产生,后有白色沉淀生成 ③.
、
④. 能与盐、非金属氧化物、酸反应
【解析】
【小问1详解】
①实验甲中,碳酸钠和盐酸反应生成氯化钠、水、二氧化碳,观察到有气泡产生;
②实验乙中,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:
;
③实验丙中,氢氧化钠和二氧化碳反应,气体减少,压强减小,能观察到气球膨胀;
【小问2详解】
作出猜想:观察到固体消失,说明碳酸钙和盐酸反应生成氯化钙、水、二氧化碳,则废液中一定含有氯化
钙,所以猜想二不合理;
实验设计:碳酸钠先与盐酸反应生成氯化钠、水、二氧化碳气体,盐酸完全反应后,碳酸钠再与氯化钙反
应生成碳酸钙沉淀和氯化钠,故能观察到先有气泡产生,后有白色沉淀生成,则证明猜想三成立,发生的
化学方程式为: 、 ;
反思总结:通过以上探究实验,由乙实验得出碱能与盐反应,由丙实验得出碱能与非金属氧化物反应,丙
中氢氧化钠足量,混合后废液呈无色,说明氢氧化钠与盐酸发生了反应,能得出碱能与酸反应。
14. 6.5克锌与稀硫酸恰好完全反应,生成氢气的质量是多少?
【答案】解:设生成氢气的质量是x
13【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
x=0.2g
答:生成氢气的质量是0.2g。
【解析】
【详解】过程见答案。
14