文档内容
重庆市高 2024 届高三第五次质量
化 学 试 题
2023.1
考生注意:
1.本试卷满分100分,考试时间75分钟。
2.考生作答时,请将答案答在答题卡上。必须在题号所指示的答题区域作答,超
.
出
.
答
.
题
.
区
.
域
.
书
.
写
.
的
.
答
.
案
.
无
.
效,在试题卷、草稿纸上答题无效。
...............
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Ca—40 Ba—137
一、选择题:本题共 14 小题,每小题 3分,共 42 分。在每小题给出的四个选项中,只有一项是符合题目要求
的。
1.下列说法不正确的是
A.DNA分子中的双螺旋链通过共价键相互结合
B.用聚乳酸塑料代替聚氯乙烯塑料可以减少白色污染
C.乙炔在氧气中燃烧剧烈放热,可以用于焊接或切割金属
D.血液中存在 的缓冲体系,为维持血液pH的稳定发挥着重要作用
2.工业上制备NaHSO₃的原理−为: 反应涉及的微粒中空间构型为Ⅴ形且含有
H2CO3/HCO3
π键的是
2SO₂+Na₂CO₃+H₂O=CO₂+2NaHSO₃,
A.SO₂ C.H₂O
2−
3.若用N 表示阿伏加B.德CO罗3常数的值,下列说法正确的是D.CO₂
A
A.用足量NaOH溶液吸收46gNO₂,转移的电子数目为
B.高温下12g石墨完全转化为金刚石,σ键的数目增加2NA
C.将 溶液蒸干所得的固体中 的N数A目为
D.将110m0oml甲L0酸.1钠mo固l/体LF溶eC于l₃甲酸溶液所得的中性溶液Cl中⁻ 00⁻的.03数N目A 为
4.钢中添加硅可提高其强度、硬度以及高温时的抗氧化性H。C下OO列⁻相关化学术语NA的使用正确的是
A.工业制粗硅的化学方程式:
B.SiO₂的结构式:O=Si=O
C.钢铁发生吸氧腐蚀的负极方程式:
的价层电子排布式: Fe−2e⁻=Fe²⁺
5.关
D.
于
Fe
下
²⁺
列实验仪器使用的说法
3d
正
⁵4
确
s¹
的是
① ② ③ ④ ⑤ ⑥
A.①②均不能用酒精灯直接加热,可垫陶土网加热
B.④的冷凝效果比③更好,可用于蒸馏装置
第1页共7页C.⑤可用于贮存浓硝酸
D.⑥可用于配制并贮存一定物质的量浓度的溶液
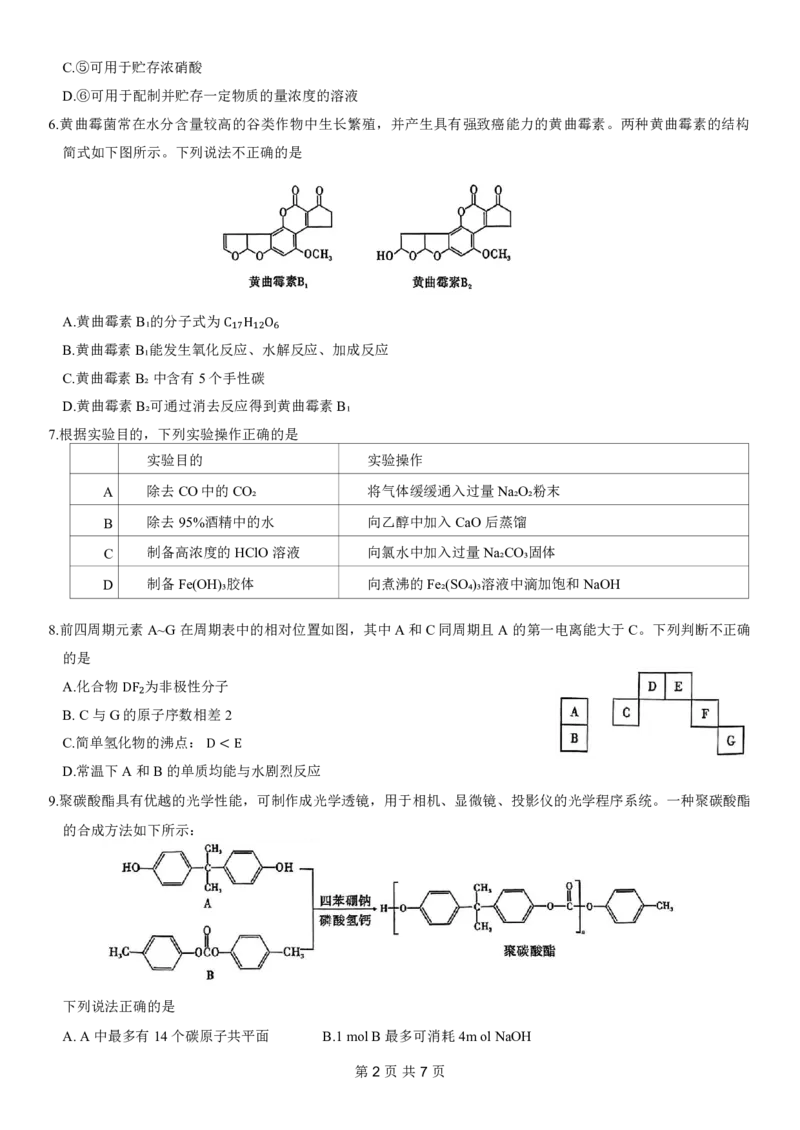
6.黄曲霉菌常在水分含量较高的谷类作物中生长繁殖,并产生具有强致癌能力的黄曲霉素。两种黄曲霉素的结构
简式如下图所示。下列说法不正确的是
A.黄曲霉素B₁的分子式为
B.黄曲霉素B₁能发生氧化反
C₁
应
₇H
、
₁₂
水
O₆
解反应、加成反应
C.黄曲霉素B₂中含有5个手性碳
D.黄曲霉素B₂可通过消去反应得到黄曲霉素B₁
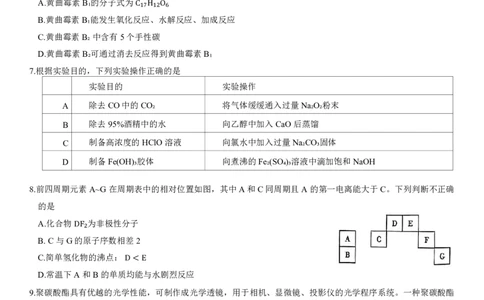
7.根据实验目的,下列实验操作正确的是
实验目的 实验操作
A 除去CO中的CO₂ 将气体缓缓通入过量Na₂O₂粉末
B 除去95%酒精中的水 向乙醇中加入CaO后蒸馏
C 制备高浓度的HClO溶液 向氯水中加入过量Na₂CO₃固体
D 制备Fe(OH)₃胶体 向煮沸的Fe₂(SO₄)₃溶液中滴加饱和NaOH
8.前四周期元素A~G在周期表中的相对位置如图,其中A和C同周期且A的第一电离能大于C。下列判断不正确
的是
A.化合物 为非极性分子
B.C与GD 的
F
原
₂
子序数相差2
C.简单氢化物的沸点:
D.常温下A和B的单质
D
均
<
能
E
与水剧烈反应
9.聚碳酸酯具有优越的光学性能,可制作成光学透镜,用于相机、显微镜、投影仪的光学程序系统。一种聚碳酸酯
的合成方法如下所示:
下列说法正确的是
A.A中最多有14个碳原子共平面 B.1molB最多可消耗4molNaOH
第2页共7页C.可用酸性高锰酸钾溶液鉴别A D.该合成反应的原子利用率为100%
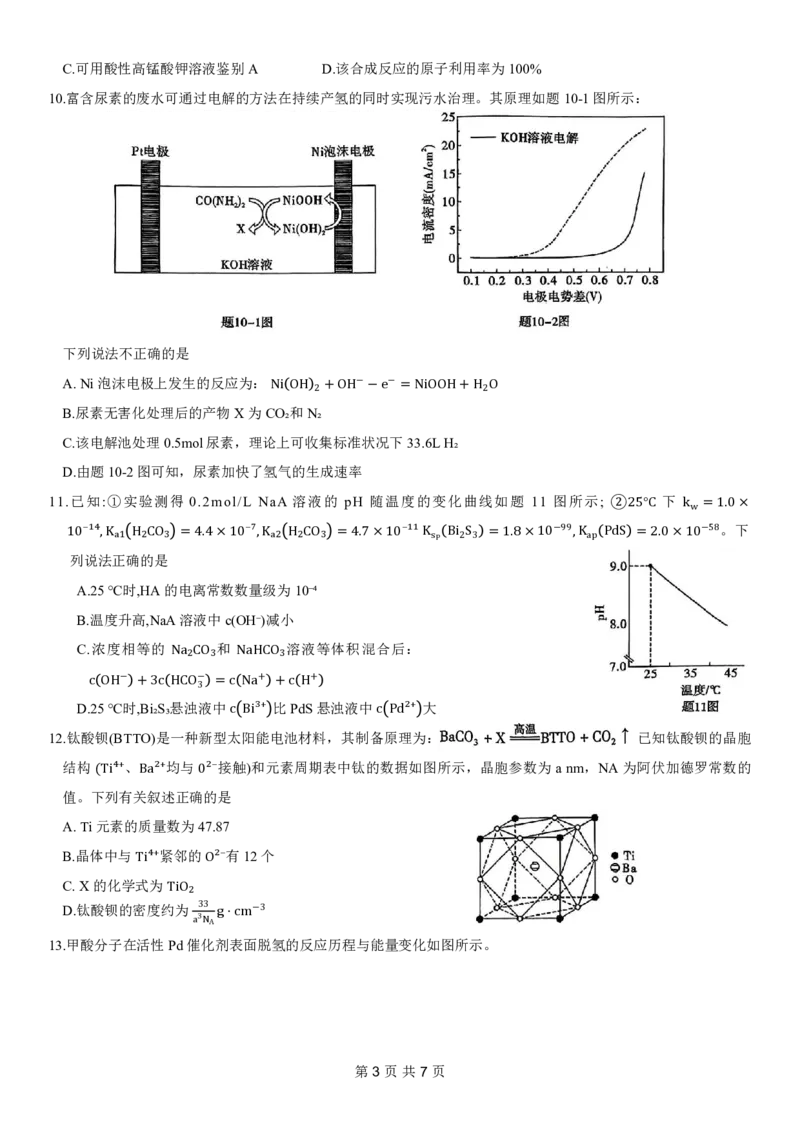
10.富含尿素的废水可通过电解的方法在持续产氢的同时实现污水治理。其原理如题10-1图所示:
下列说法不正确的是
A.Ni泡沫电极上发生的反应为:
− −
B.尿素无害化处理后的产物X为CNOi₂和OHN2₂+OH −e =NiOOH+H2O
C.该电解池处理0.5mol尿素,理论上可收集标准状况下33.6LH₂
D.由题10-2图可知,尿素加快了氢气的生成速率
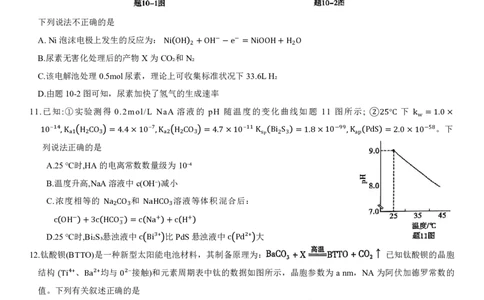
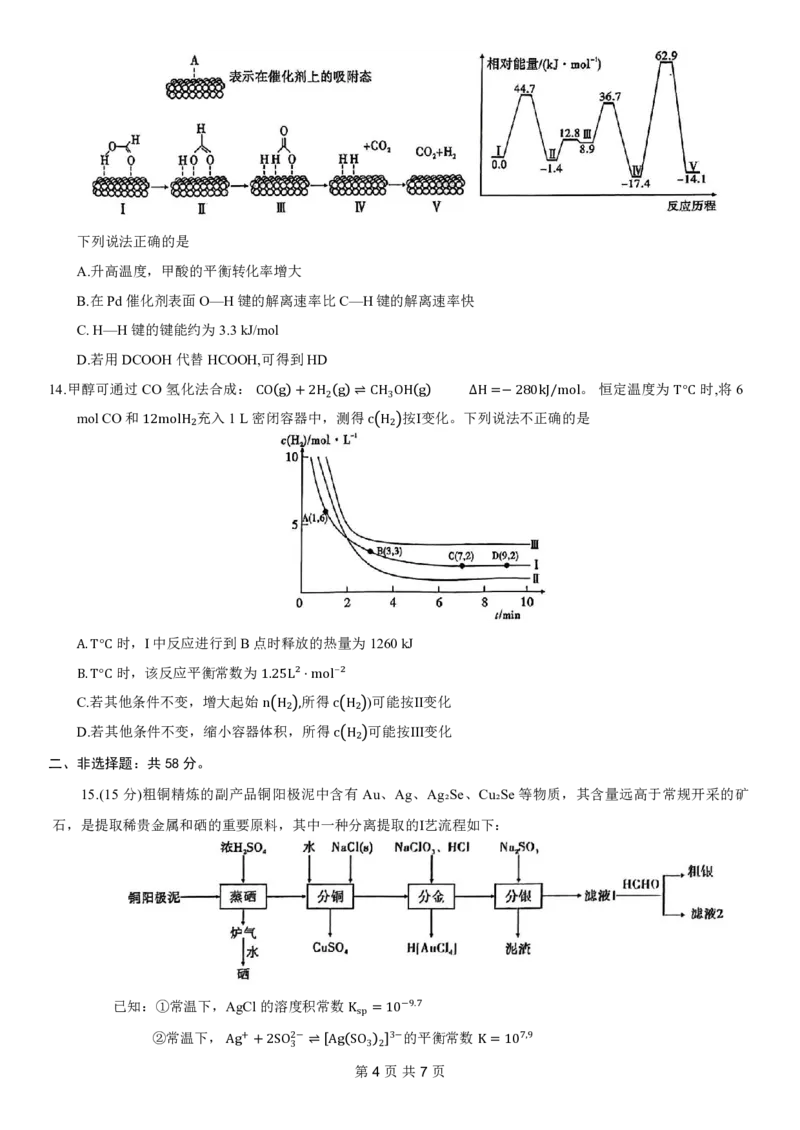
11.已知:①实验测得 0.2mol/L NaA 溶液的 pH 随温度的变化曲线如题 11 图所示; 下
②25°C kw =1。.0下×
−99 −58
1列0⁻说¹⁴法,K正ₐ₁确H的₂C是O₃ =4.4×10⁻⁷,Kₐ₂ H₂CO₃ =4.7×10⁻¹¹KsP Bi2S3 =1.8×10 ,Kap PdS =2.0×10
A.25℃时,HA的电离常数数量级为10⁻⁴
B.温度升高,NaA溶液中c(OH⁻)减小
C.浓度相等的 和 溶液等体积混合后:
Na₂CO₃ NaHCO₃
− − + +
D.c25O℃H时,+Bi3₂Sc₃悬HC浊O3液中=c Na 比+cPdHS悬浊液中 大
12.钛酸钡(BTTO)是一种新型太c 阳Bi³能⁺电池材料,其制备c原Pd理²⁺为: 已知钛酸钡的晶胞
结构 、 均与 接触)和元素周期表中钛的数据如图所示,晶胞参数为a nm,NA 为阿伏加德罗常数的
值。下(T列i⁴⁺有关B叙a²⁺述正确0的²⁻是
A.Ti元素的质量数为47.87
B.晶体中与 紧邻的 有12个
C.X的化学式Ti⁴为⁺ O²⁻
D.钛酸钡的密度约为
TiO₂
33 −3
3
13.甲酸分子在活性Pd催a化NA剂g⋅表cm面脱氢的反应历程与能量变化如图所示。
第3页共7页下列说法正确的是
A.升高温度,甲酸的平衡转化率增大
B.在Pd催化剂表面O—H键的解离速率比C—H键的解离速率快
C.H—H键的键能约为3.3kJ/mol
D.若用DCOOH代替HCOOH,可得到HD
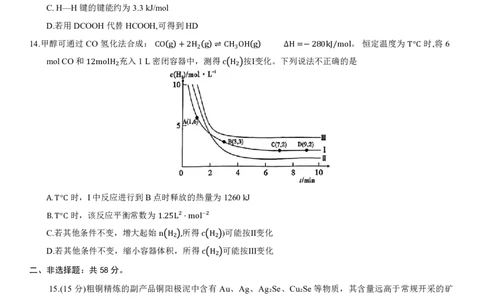
14.甲醇可通过CO 氢化法合成: 。 恒定温度为 时,将6
molCO和 充入1L密CO闭g容器+中2H,2 测g 得⇌ CH3O按HⅠg变化。下∆H列=说−法2不80正kJ确/m的o是l T°C
12molH₂ c H₂
时,I中反应进行到B点时释放的热量为1260kJ
A.T°C 时,该反应平衡常数为
BC..若T°其C 他条件不变,增大起始1.25L²所⋅m得ol⁻² )可能按Ⅱ变化
D.若其他条件不变,缩小容器体n积H₂,,所得c H₂ 可能按Ⅲ变化
二、非选择题:共58分。 c H₂
15.(15 分)粗铜精炼的副产品铜阳极泥中含有Au、Ag、Ag₂Se、Cu₂Se等物质,其含量远高于常规开采的矿
石,是提取稀贵金属和硒的重要原料,其中一种分离提取的Ⅰ艺流程如下:
已知:①常温下,AgCl的溶度积常数
−9.7
②常温下, Ksp =10的平衡常数
+ 2− 3− 7,9
Ag +2SO3 ⇌ Ag S第O3 4 2 页共7页 K= 10(1)Se与O同族,其基态原子价层电子的运动状态有 种。
(2)“蒸硒”时将铜阳极泥与浓硫酸混合于 下焙烧,浓硫酸将硒元素氧化为 并蒸出,写出
与浓硫酸反应的化学方程式 450。∼将5炉00气°C通入水中可得硒单质和 (写Se化O₂学式)。
Cu₂Se (3)“分金”时应控制 的用量以减少 (写化学式)的产生。
(4)“分银”原理为 NaClO₃ 常温下该反应的平衡常数为 ,
2− 3− −
若加入 溶液溶解AagmClolsA+gC2lS,理O3论上aql ⇌ Ag S溶O液3 2的浓度aq须+达C到l aq ; mol/L(忽略溶解前后溶液的体积
变化)。1LNa₂SO₃ Na₂SO₃
(5)HCHO的作用为 ;将滤液2返回“分银”工序循环使用,发现循环多次后银的浸出率降低,可能
的原因是 。
(6)粗银电解精炼时需控制电解液的pH为1.5~2,其原因是 。
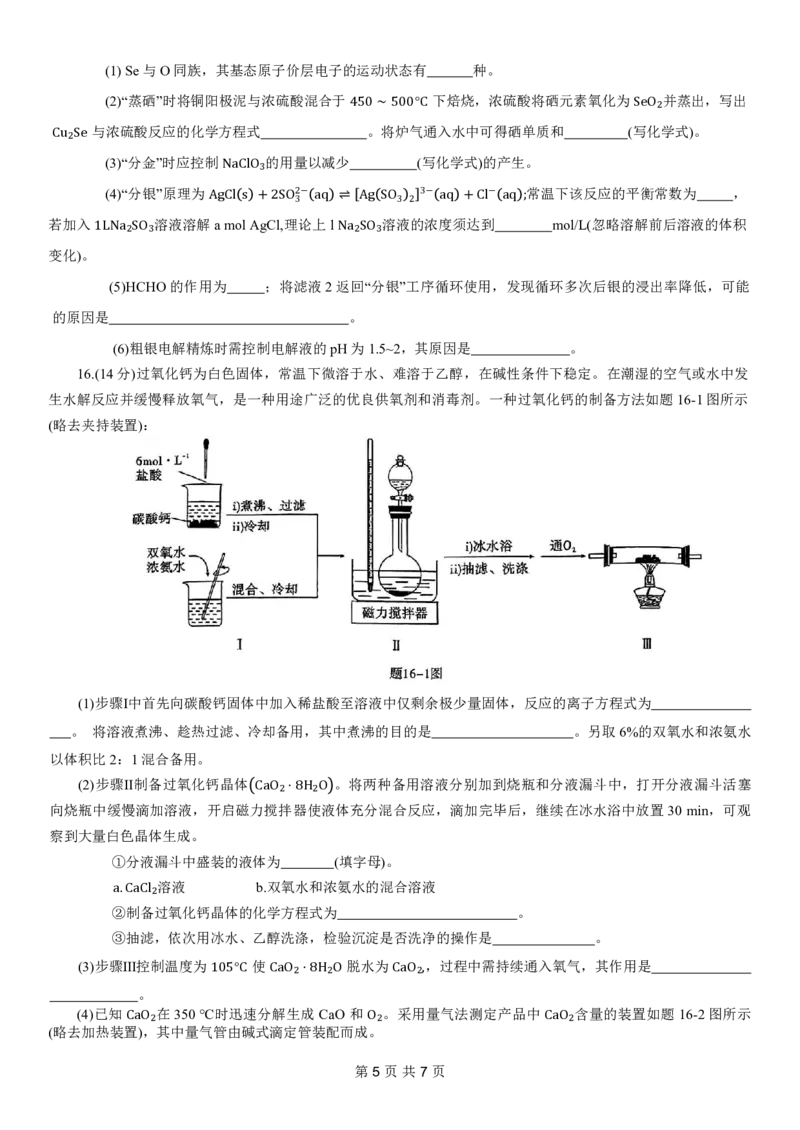
16.(14分)过氧化钙为白色固体,常温下微溶于水、难溶于乙醇,在碱性条件下稳定。在潮湿的空气或水中发
生水解反应并缓慢释放氧气,是一种用途广泛的优良供氧剂和消毒剂。一种过氧化钙的制备方法如题16-1图所示
(略去夹持装置):
(1)步骤Ⅰ中首先向碳酸钙固体中加入稀盐酸至溶液中仅剩余极少量固体,反应的离子方程式为
。 将溶液煮沸、趁热过滤、冷却备用,其中煮沸的目的是 。另取6%的双氧水和浓氨水
以体积比2:1混合备用。
(2)步骤Ⅱ制备过氧化钙晶体 。将两种备用溶液分别加到烧瓶和分液漏斗中,打开分液漏斗活塞
向烧瓶中缓慢滴加溶液,开启磁力搅拌器使液体充分混合反应,滴加完毕后,继续在冰水浴中放置30 min,可观
CaO₂⋅8H₂O
察到大量白色晶体生成。
①分液漏斗中盛装的液体为 (填字母)。
溶液 b.双氧水和浓氨水的混合溶液
②制备过氧化钙晶体的化学方程式为 。
a.CaCl₂
③抽滤,依次用冰水、乙醇洗涤,检验沉淀是否洗净的操作是 。
(3)步骤Ⅲ控制温度为 使 脱水为 ,过程中需持续通入氧气,其作用是
。
105°C CaO₂⋅8H₂O CaO₂,
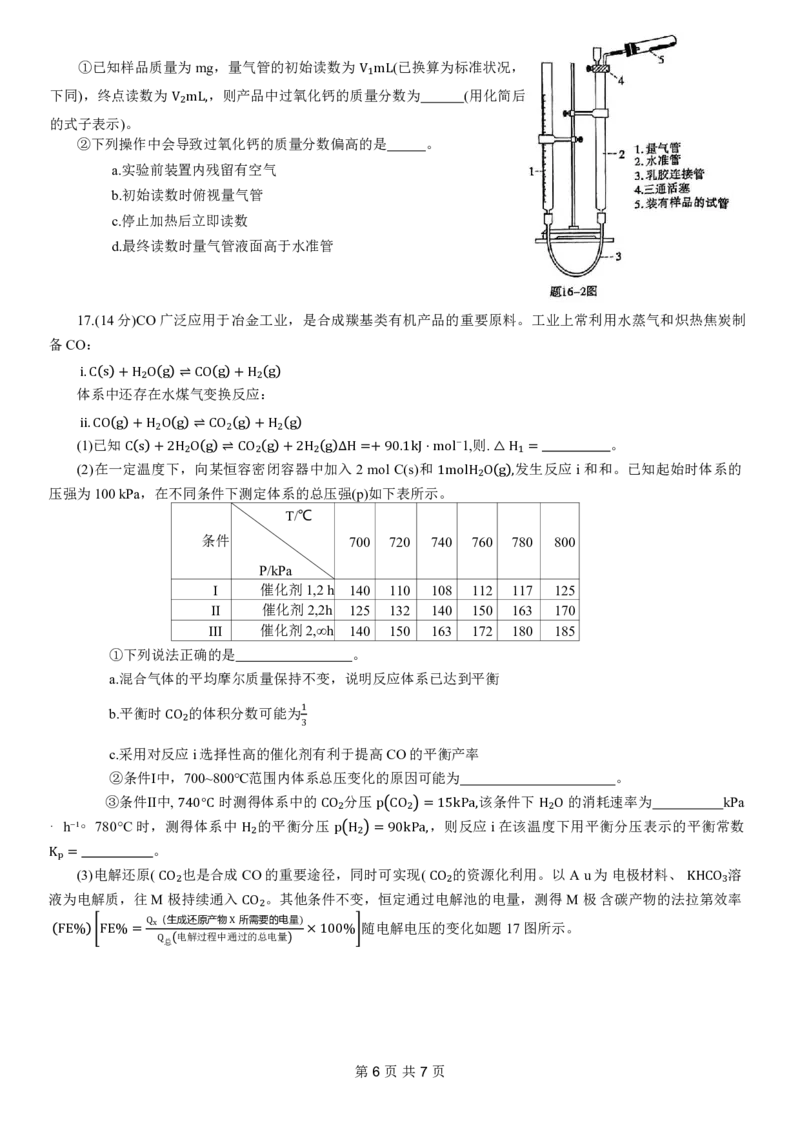
(4)已知 在350 ℃时迅速分解生成CaO 和 。采用量气法测定产品中 含量的装置如题16-2图所示
(略去加热装置),其中量气管由碱式滴定管装配而成。
CaO₂ O₂ CaO₂
第5页共7页①已知样品质量为mg,量气管的初始读数为 (已换算为标准状况,
下同),终点读数为 ,则产品中过氧化钙的质
V
量
₁m
分
L
数为 (用化简后
的式子表示)。
V₂mL,
②下列操作中会导致过氧化钙的质量分数偏高的是 。
a.实验前装置内残留有空气
b.初始读数时俯视量气管
c.停止加热后立即读数
d.最终读数时量气管液面高于水准管
17.(14分)CO广泛应用于冶金工业,是合成羰基类有机产品的重要原料。工业上常利用水蒸气和炽热焦炭制
备CO:
体系中还存在水煤气变换反应:
i.C s +H₂O g ⇌CO g +H₂ g
( i 1 i. )已 CO 知 g +H2O g ⇌CO2 g +H2 g 1,则. 。
(2)在一定温度下,向某恒容密闭容器中加入2 mol C(s)和 发生反应 i和和。已知起始时体系的
C s +2H₂O g ⇌CO₂ g +2H₂ g ΔH=+90.1kJ⋅mol⁻ △H₁=
压强为100kPa,在不同条件下测定体系的总压强(p)如下表所示。
1molH₂O g ,
T/℃
条件 700 720 740 760 780 800
P/kPa
I p 催化剂1,2h 140 110 108 112 117 125
Ⅱ 催化剂2,2h 125 132 140 150 163 170
Ⅲ 催化剂2,∞h 140 150 163 172 180 185
①下列说法正确的是 。
a.混合气体的平均摩尔质量保持不变,说明反应体系已达到平衡
b.平衡时 的体积分数可能为
1
CO₂ 3
c.采用对反应i选择性高的催化剂有利于提高CO的平衡产率
②条件Ⅰ中,700~800℃范围内体系总压变化的原因可能为 。
③条件Ⅱ中, 时测得体系中的 分压 该条件下 的消耗速率为 kPa
⋅ h⁻¹∘ 780°C时,测得体系中 的平衡分压 ,则反应i在该温度下用平衡分压表示的平衡常数
740°C CO₂ p CO₂ =15kPa, H₂O
。
H₂ p H₂ =90kPa,
(3)电解还原( 也是合成CO的重要途径,同时可实现( 的资源化利用。以Au为电极材料、 溶
Kₚ=
液为电解质,往M极持续通入 。其他条件不变,恒定通过电解池的电量,测得M极含碳产物的法拉第效率
CO₂ CO₂ KHCO₃
(生成还原产物 所需要的电量
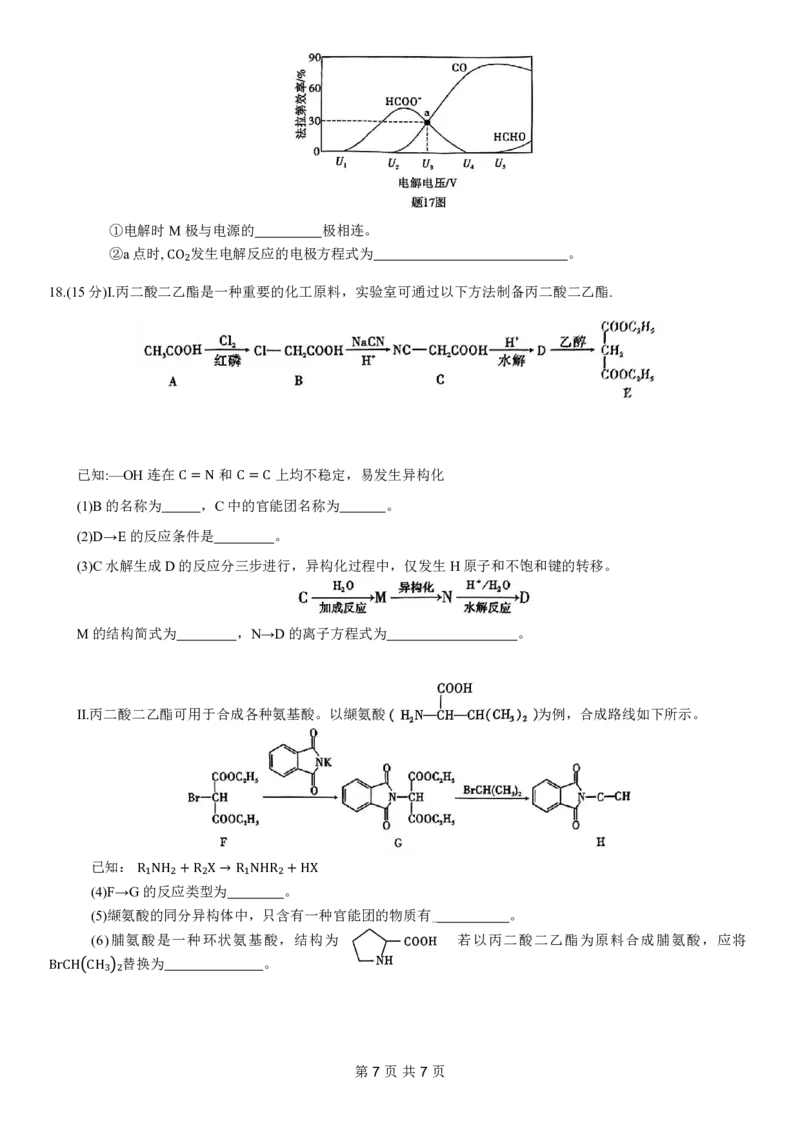
CO₂ 随电解电压的变化如题17图所示。
电解过程中通过的总电量
Qx 总 X )
FE% FE%= Q ×100%
第6页共7页①电解时M极与电源的 极相连。
②a点时, 发生电解反应的电极方程式为 。
CO₂
18.(15分)Ⅰ.丙二酸二乙酯是一种重要的化工原料,实验室可通过以下方法制备丙二酸二乙酯.
已知:—OH连在 和 上均不稳定,易发生异构化
(1)B的名称为 C=,NC中C的=官C能团名称为 。
(2)D→E的反应条件是 。
(3)C水解生成D的反应分三步进行,异构化过程中,仅发生H原子和不饱和键的转移。
M的结构简式为 ,N→D的离子方程式为 。
Ⅱ.丙二酸二乙酯可用于合成各种氨基酸。以缬氨酸 为例,合成路线如下所示。
已知:
(4)F→G的反应类型为 。
R₁NH₂+R₂X→ R₁NHR₂+HX
(5)缬氨酸的同分异构体中,只含有一种官能团的物质有 。
(6)脯氨酸是一种环状氨基酸,结构为 若以丙二酸二乙酯为原料合成脯氨酸,应将
替换为 。
BrCH CH₃ ₂
第7页共7页