文档内容
2024-2025 学年高一化学上学期第一次月考卷
一、选择题:本题共15个小题,每小题4分,共60分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.制作豆腐过程一般有如图六步操作,其中操作⑤用CaSO 或MgCl 作凝固剂。根据图示,下列说法不正
4 2
确的是
A.操作①与操作②的目的是为了更多的蛋白质溶解于水
B.操作③属于固液分离,取其袋子内的固体作为操作④的原料
C.在适宜温度下,操作⑤用MgCl ,作凝固剂可使蛋白质沉淀
2
D.操作⑥使豆腐“成形”,此过程主要发生的是物理变化
【答案】B
【解析】A.操作①即浸泡豆子与操作②即磨豆浆的目的是为了更多的蛋白质溶解于水,以提供豆浆的产
量,A正确;
B.操作③属于固液分离,袋内的固体为豆渣,流出的液体才是豆浆,故应取过滤出的液体作为操作④的
原料,B错误;
C.经过步骤④后得到蛋白质胶体,在适宜温度下,操作⑤用MgCl ,作凝固剂可使蛋白质沉淀,C正确;
2
D.操作⑥使豆腐“成形”,此过程主要使失去更多的水分,故发生的是物理变化,D正确;
故答案为:B。
2.下列有关物质分类的说法正确的是
A.明矾[ ]属于纯净物
学科网(北京)股份有限公司 学科网(北京)股份有限公司B.根据盐溶液的酸碱性,可将盐分为酸式盐、碱式盐和正盐
C.根据是否有丁达尔效应,可将分散系分为溶液、胶体和浊液
D.根据能否与酸或碱反应,可将氧化物分为酸性氧化物和碱性氧化物
【答案】A
【解析】A.明矾[ ]是盐,属于纯净物,A正确;
B.根据是否是由酸与碱完全反应生成的盐,可将盐分为酸式盐、碱式盐和正盐,B错误;
C.根据分散质离子直径大小可将分散系分为溶液、胶体和浊液,C错误;
D.根据能否与酸或碱反应生成盐和水,可将氧化物分为酸性氧化物、碱性氧化物、两性氧化物以及不成
盐氧化物,D错误;
故选A。
3.利用 与 制备 胶体,新制 胶体的胶团结构为
(如图所示)。下列说法错误的是
A.胶粒的直径介于1~100nm之间
B. 胶体带正电
C.胶体能够稳定存在的主要原因是胶粒间存在静电斥力
D. 胶体的电泳现象的原因是扩散层与吸附层分离,带正电的胶粒向阴极移动
【答案】B
【解析】A.依据分散系定义可知,胶体粒子的直径介于1~100 nm之间,故A正确;
B.Fe(OH) 胶体不带电,其胶粒带正电,故B错误;
3
C.胶体整体上不带电,氢氧化铁胶体稳定存在的主要原因是氢氧化铁胶粒带正电荷,相互排斥,不能聚
沉,故C正确;
D.Fe(OH) 胶粒带正电,通电发生电泳,带正电的胶粒向阴极移动,故D正确;
3
学科网(北京)股份有限公司 学科网(北京)股份有限公司故选B。
4.以下物质间的转化,在一定条件下均能一步实现的是
①C→CO→CO ②Fe→Fe O →Fe (SO )
2 2 3 2 4 3
③K CO →KCl→KNO ④CaCO →CaO→Ca(OH)
2 3 3 3 2
A.①②③④ B.①②④ C.①③④ D.①②③
【答案】A
【解析】根据分析:①中: ,②中: ,③中:
,④中: 。故①②③④都能实现一
步转化,故BCD错误,选A。
5.电视节目《中国诗词大会》显示了中国传统文化的博大精深,下列诗词中涉及化学变化的是
A.八月秋高风怒号,卷我屋上三重茅 B.梅须逊雪三分白,雪却输梅一段香
C.无边落木萧萧下,不尽长江滚滚来 D.千锤万凿出深山,烈火焚烧若等闲
【答案】D
【解析】A.八月秋高风怒号,卷我屋上三重茅,是指八月的秋风把屋上的茅草卷走,没有生成新物质,
是物理变化,不符合题意;
B.梅须逊雪三分白,雪却输梅一段香,是指梅花比不上雪的白,而雪却比不上梅花的香气浓,没有生成
新物质,是物理变化,不符合题意;
C.无边落木萧萧下,不尽长江滚滚来,是指无边无际的树木萧萧地飘下落叶,长江滚滚涌来奔腾不息,
过程中没有生成新物质,是物理变化,不符合题意。
D.千锤万凿出深山,是将石头开采出来,烈火焚烧若等闲过程中包含着:碳酸钙分解生成氧化钙和二氧
化碳,是化学变化,符合题意;
故选:D。
6.导体中自由的带电微粒在电场作用下发生定向移动从而形成电流,如金属铜、熔融的NaCl、NaCl溶液
都是导体。下列说法正确的是
A.因为金属有较好的导电性,所以它属于电解质
B.电解质都能电离产生离子,因此都属于导体
C.水分子或加热至熔融态都会使氯化钠发生电离
D.液态氯化氢不能导电,故氯化氢不属于电解质
【答案】C
学科网(北京)股份有限公司 学科网(北京)股份有限公司【解析】A.电解质一定是化合物,金属是单质,不属于电解质,A错误;
B.电解质没有电离时不导电,不属于导体,B错误;
C.氯化钠溶于水或熔融状态下都能导电,即都能发生电离,C正确;
D.虽然液态氯化氢不能导电,但其溶于水能导电,故HCl属于电解质,D错误;
故答案选C。
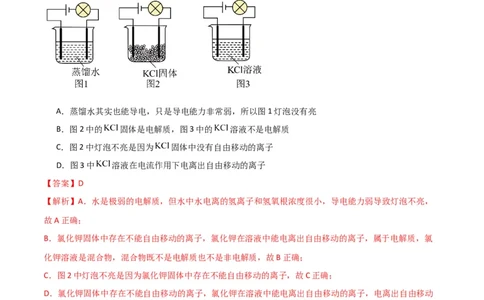
7.某化学兴趣小组按照如图所示装置进行实验,闭合开关后,发现图1、图2灯泡不亮,图3灯泡亮,下
列说法不正确的是
A.蒸馏水其实也能导电,只是导电能力非常弱,所以图1灯泡没有亮
B.图2中的 固体是电解质,图3中的 溶液不是电解质
C.图2中灯泡不亮是因为 固体中没有自由移动的离子
D.图3中 溶液在电流作用下电离出自由移动的离子
【答案】D
【解析】A.水是极弱的电解质,但水中水电离的氢离子和氢氧根浓度很小,导电能力弱导致灯泡不亮,
故A正确;
B.氯化钾固体中存在不能自由移动的离子,氯化钾在溶液中能电离出自由移动的离子,属于电解质,氯
化钾溶液是混合物,混合物既不是电解质也不是非电解质,故B正确;
C.图2中灯泡不亮是因为氯化钾固体中存在不能自由移动的离子,故C正确;
D.氯化钾固体中存在不能自由移动的离子,氯化钾在溶液中能电离出自由移动的离子,电离出自由移动
的离子不需要电流的作用,故D错误;
故选D。
8.向 溶液中滴入几滴酚酞溶液,然后匀速逐滴加入稀硫酸,测得混合溶液的电导率变化的曲线
如图。下列说法不正确的是
学科网(北京)股份有限公司 学科网(北京)股份有限公司A.若向原 溶液中滴加和硫酸浓度相同的硫酸钠溶液,预测电导率变化图相同
B.实验中观察到溶液由红色变成无色,并产生白色沉淀
C.B点时 溶液与稀硫酸恰好完全反应
D.B点之后电导率增加的原因是混合溶液中H+和 的浓度增加
【答案】A
【解析】A.用硫酸钠溶液代替重复上述实验,生成的氢氧化钠溶于水完全电离成自由移动的离子能导电,
溶液导电能力随时间变化与图2不同,A错误;
B.硫酸和氢氧化钡反应生成硫酸钡沉淀和水,碱性变弱直至为酸性,故观察到溶液由红色变成无色,并
产生白色沉淀,B正确;
C.B时刻溶液与稀硫酸恰好完全反应,C正确;
D.B点两者恰好反应,之后硫酸过量,故电导率增加的原因是混合溶液中H+和 的浓度增加,D正确;
故选A。
9.下列化学用语表达正确的是
A.硫酸钠在水溶液中的电离方程式:
B.水的电离方程式:
C.稀硫酸和氢氧化钡反应的离子方程式:
学科网(北京)股份有限公司 学科网(北京)股份有限公司D.稀盐酸滴在铜片上的离子反应:
【答案】B
【解析】A.硫酸钠是强电解质,在溶液中完全电离出钠离子和硫酸根离子,电离方程式为
,故A错误;
B.水是极弱的电解质,能微溶电离出氢离子和氢氧根离子,电离方程式为 ,故B正确;
C.稀硫酸和氢氧化钡溶液反应生成硫酸钡沉淀和水,反应的离子方程式为
,故C错误;
D.铜是不活泼金属,不能与稀盐酸反应,故D错误;
故选B。
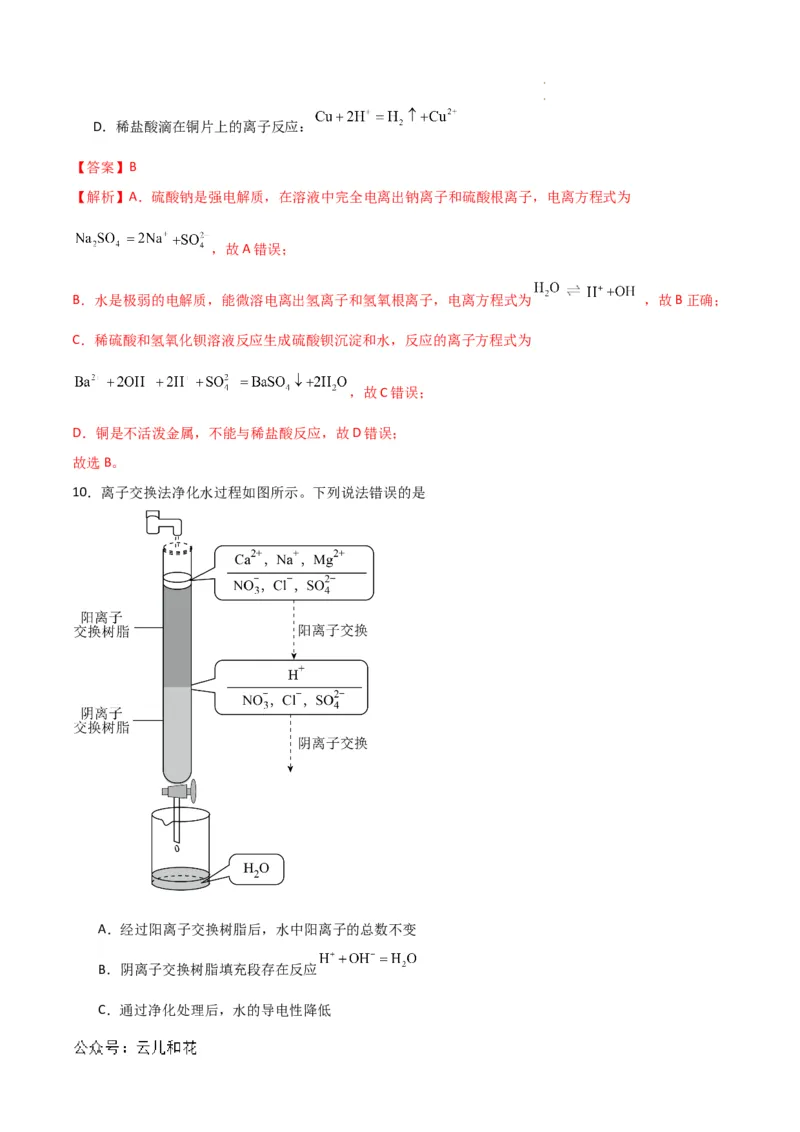
10.离子交换法净化水过程如图所示。下列说法错误的是
A.经过阳离子交换树脂后,水中阳离子的总数不变
B.阴离子交换树脂填充段存在反应
C.通过净化处理后,水的导电性降低
学科网(北京)股份有限公司 学科网(北京)股份有限公司D.水中 、 、 通过阴离子交换树脂后被除去
【答案】A
【解析】A. 、 、 等阳离子被 代替,根据电荷守恒可知,经过阳离子交换树脂后,水中
阳离子总数增加,A项错误;
B.溶液中阳离子被 代替、阴离子被 代替,阴离子树脂填充段存在反应: ,B项正
确;
C.通过净化处理后,溶液中离子的浓度降低,水的导电性降低,C项正确;
D.由题中图示可知,经阴离子交换膜后, 、 、 被除去,D项正确;
故选A。
11.下列关于氧化还原反应的叙述正确的是
A.失电子越多,还原性越强,得电子越多,氧化性越强
B.置换反应都是氧化还原反应,所以 既是置换反应又是氧化还原反应
C.具有该元素最高价态的元素,对应物质在氧化还原反应中一定表现氧化性
D.在同一个氧化还原反应中,氧化剂和还原剂可以为同一种物质
【答案】D
【解析】A.物质的氧化性或还原性,与得电子能力或失电子能力有关,其得失电子的数目无关,A错误;
B. 反应中,无单质参加,所以不属于置换反应,B错误;
C.具有该元素最高价态的元素,对应物质中的其它元素在氧化还原反应中化合价可以升高,可能表现还
原性,C错误;
D.在同一个氧化还原反应中,氧化剂和还原剂可以为同一种物质,如过氧化氢分解反应等,D正确;
故选D。
12.对于反应 ,以下叙述正确的是
A. 是氧化剂, 是还原剂
学科网(北京)股份有限公司 学科网(北京)股份有限公司B.被氧化的 原子和被还原的 原子的个数比为
C. 既做氧化剂又做还原剂
D.氧化剂得电子数与还原剂失电子数之比为
【答案】C
【解析】A.该反应中只有Cl元素的化合价变化,氯气既是氧化剂又是还原剂,故A错误;
B.由Cl元素守恒及元素的化合价变化可知,该反应中1个Cl原子失去电子时5个Cl原子得到电子,则被
氧化的Cl原子和被还原的Cl原子的个数比为1:5,故B错误;
C.该反应中只有Cl元素的化合价变化,氯气既是氧化剂又是还原剂,故C正确;
D.由电子守恒可知,氧化剂得电子总数与还原剂失电子总数之比为1:1,故D错误;
故答案选C。
13.已知:① ;② 。则下列判断正确的是
A.在反应②中 只表现出还原性
B.氧化性强弱:
C. 只有氧化性, 只有还原性
D.用双线桥法表示反应②电子得失情况:
【答案】B
【解析】A.反应 中有5个HCl的Cl由-1价升高为0价,作还原
剂,表现还原性,有1个HCl的Cl化合价不变,表现酸性,A错误;
B.氧化剂的氧化性大于氧化产物,反应 中Cl 作氧化剂,Fe3+作氧化产物,则氧化性
2
Cl > FeCl ,反应 中KClO 作氧化剂,Cl 作氧化产物,则氧化性
2 3 3 2
KClO >Cl ,综上氧化性强弱: ,B正确;
3 2
学科网(北京)股份有限公司 学科网(北京)股份有限公司C. 是Fe元素的最高价态,只有氧化性, 是Fe元素的中间价态,既有氧化性又有还原性,C错误;
D.氧化还原反应中同种元素遵循只靠拢不交叉的原则,根据得失电子守恒,该反应用双线桥法表示电子
得失情况为 ,D错误;
答案选B。
14.在一定条件下,RO n-和F 可发生如下反应:RO n-+F +2OH-=RO -+2F-+H O,从而可知在RO n-中 ,元
3 2 3 2 4 2 3
素R的化合价、n的值分别是
A.+4价 2 B.+5价 1 C.+6价 0 D.+3价 3
【答案】B
【解析】根据电荷守恒得n+1×2=1+1×2,则n=1,所以 为 ,该离子中O元素化合价为-2价,R、
O元素化合价的代数和为-1,所以该离子中R元素化合价=-1-(-2)×3=+5;故答案选B。
15.硫化氢的转化是资源利用和环境保护的重要研究课题。将 和空气的混合气体通入 、 和
的混合溶液中回收 ,其转化如下图所示(CuS不溶于水)。下列说法中,不正确的是
A.过程①中,生成 的反应为
学科网(北京)股份有限公司 学科网(北京)股份有限公司B.过程②中, 作氧化剂
C.过程③中,各元素化合价均未改变
D.回收 的总反应为
【答案】C
【解析】A.过程①中,发生复分解反应,生成CuS的反应为, ,A正确;
B.过程②中,S元素化合价升高,具有还原性,则Fe3+为氧化剂,B正确;
C.过程③中,氧气是氧化剂,Fe2+是还原剂,O元素和Fe元素化合价发生变化,C错误;
D.根据转化关系图可判断回收S的总反应为 ,D正确;
故选:C。
二、填空题(本题共4大题,共40分。)
16.(10分)某课外活动小组甲、乙、丙、丁四名同学进行氢氧化铁胶体的制备实验及其性质探究如下。
Ⅰ. 胶体的制备
甲:向40mL沸腾的蒸馏水中逐滴加入6滴氯化铁饱和溶液(浓度约为30%);
乙:向40mL沸腾的自来水中逐滴加入6滴氯化铁饱和溶液(浓度约为30%);
丙:直接加热饱和的氯化铁溶液;
丁:向40mL蒸馏水中滴入6滴10% 溶液,然后滴入1滴10%NaOH溶液,边滴边搅拌。
(1)检验以上四名同学胶体制备是否成功,可利用胶体的 ,经检验发现只有乙同学没有成功,
试分析不成功的原因 。
(2)甲、丙、丁三位同学胶体制备成功,但所用时间长短是丙>甲>丁
①丁与甲对比,除了胶体制备所用时间较短,丁的优点还有 (写出2条即可)。
②综合上述实验:制备 胶体时,提供 的物质可以是 ,只要控制反应条件即可制
得。
Ⅱ. 胶体的性质
学科网(北京)股份有限公司 学科网(北京)股份有限公司(3)甲同学向 胶体中逐滴滴加稀 至过量,观察到的现象是 。
(4)丙、丁同学想探究 ,胶体能稳定存在的主要原因,通过以下___________(填序号)操作可以实现。
A.渗析 B.电泳 C.聚沉 D.丁达尔效应
【答案】(10分)(1) 丁达尔效应 (1分) 自来水中含电解质,易使制备的胶体发生聚沉(2
分)
(2) 不需要加热,节约能源,所需氯化铁浓度少 (2分) 或 (1分)
(3)先出现红褐色沉淀,后沉淀溶解,溶液变成棕黄色(2分)
(4)B(2分)
【解析】(1)胶体的检验方法是利用胶体的特性丁达尔效应,故检验四名同学胶体制备是否成功,利用
丁达尔效应;在胶体中加入电解质溶液可以使胶体发生聚沉,乙同学实验中用的是自来水,自来水中含电
解质,易使制备的胶体发生聚沉,所以乙同学没有成功制备胶体,答案为自来水中含电解质,易使制备的
胶体发生聚沉;
(2)丁同学用的 溶液浓度小,滴加NaOH溶液,常温下就可以反应生成 ,不需要加热,节
约能源,故答案为不需要加热,节约能源,所需 溶液浓度小;甲同学和丙同学制备 胶体的
原理是 ,丁同学制备 胶体的原理是
,故制备 胶体时,提供 的物质可以是 或 ;
(3) 胶体粒子吸附分散系中的阳离子带正电荷,相互排斥而稳定, 溶液为电解质溶液,
含有 阴离子中和胶体粒子的正电荷,使胶粒聚沉,溶液中的 可以与 发生反应
,使沉淀溶解,故现象为:先出现红褐色沉淀,后沉淀溶解,溶液变成棕黄色;
(4)胶体能稳定存在是胶粒具有吸附性,吸附带电微粒使胶粒带同种电荷,胶粒之间相互排斥而稳定存
学科网(北京)股份有限公司 学科网(北京)股份有限公司在, 胶体粒子带正电荷,带电微粒可以在电场中定向移动,移向阴极使阴极附近红褐色颜色加深,
这个操作是电泳实验,通过该实验判断胶粒带电荷,证明胶体稳定存在的原因,故答案为B。
17.(10分)天宫课堂第二课中,王亚平老师用醋酸钠(化学式:CH COONa)的过饱和溶液做了一个“太空
3
冰雪”的趣味实验,在微重力环境下,使一颗“水球”瞬间变成了一颗“冰球”,因此同学们想对醋酸和
醋酸钠的性质进行深入学习。回答下列问题:
任务一:认识醋酸和醋酸钠
(1)从物质的分类上看,醋酸钠属于 (填字母,下同),醋酸溶液属于 。
A.酸 B.碱 C.盐 D.电解质 E.混合物
任务二:性质探究
已知:醋酸是一种弱酸,属于弱电解质,在水中不能完全电离,因此其在水中的电离方程式为
。
(2)同学们将醋酸钠溶液接入如图所示的电路中,闭合开关,电流表的示数为0.10A,继续往溶液中添加适
量醋酸钠固体,并用玻璃棒不断搅拌,电流表示数不断增大,最终示数为0.24A。据此推测,在水溶液中
存在着能导电的微粒是 (填微粒符号、不考虑H+、OH-)。
(3)醋酸钠在水中完全电离的电离方程式为 ;水是一种弱电解质,可以电离出极少量的H+和
OH-,根据已知信息推断其电离方程式为 ,因此水在书写离子方程式时,不能拆写为H+和
OH-。
(4)①往盛有NaOH溶液的烧杯中逐滴滴加等浓度的醋酸溶液,直至过量。请写出醋酸溶液与NaOH溶液反
应的离子方程式: 。
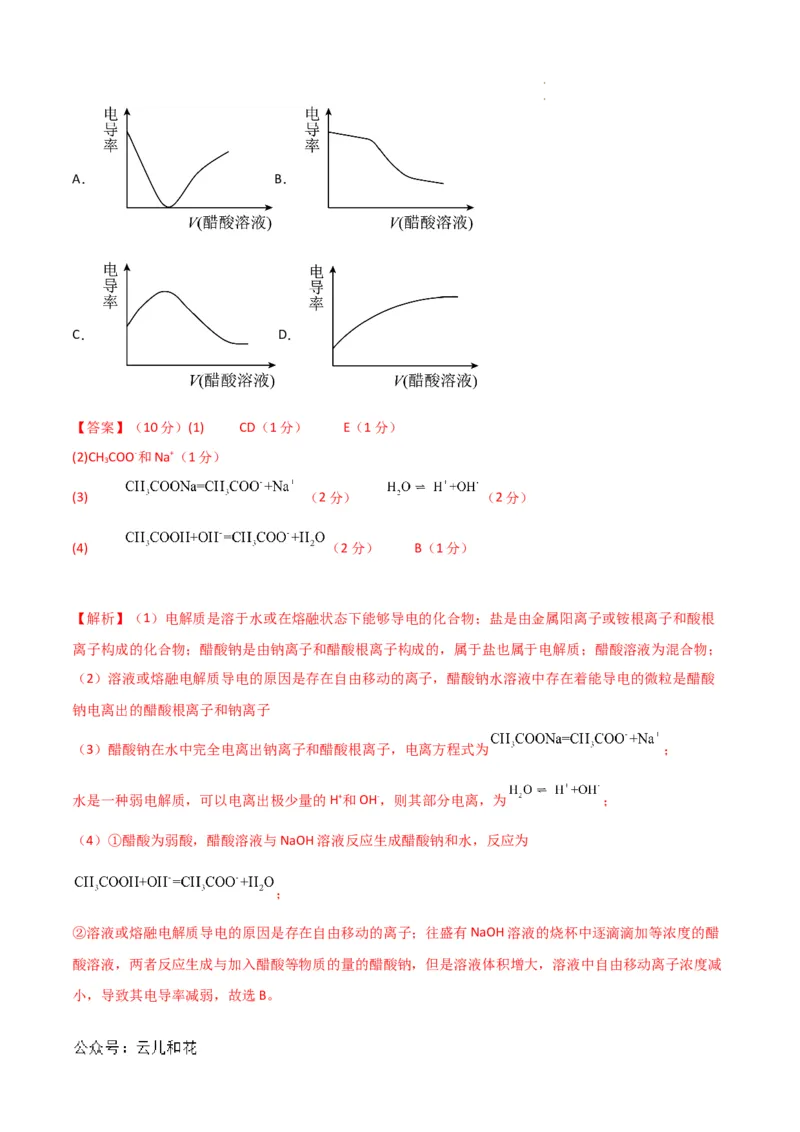
②随着醋酸的滴入,烧杯中溶液的电导率随滴入醋酸溶液的体积变化趋势与下图一致的是 。
(填字母)
学科网(北京)股份有限公司 学科网(北京)股份有限公司A. B.
C. D.
【答案】(10分)(1) CD(1分) E(1分)
(2)CH COO-和Na+(1分)
3
(3) (2分) (2分)
(4) (2分) B(1分)
【解析】(1)电解质是溶于水或在熔融状态下能够导电的化合物;盐是由金属阳离子或铵根离子和酸根
离子构成的化合物;醋酸钠是由钠离子和醋酸根离子构成的,属于盐也属于电解质;醋酸溶液为混合物;
(2)溶液或熔融电解质导电的原因是存在自由移动的离子,醋酸钠水溶液中存在着能导电的微粒是醋酸
钠电离出的醋酸根离子和钠离子
(3)醋酸钠在水中完全电离出钠离子和醋酸根离子,电离方程式为 ;
水是一种弱电解质,可以电离出极少量的H+和OH-,则其部分电离,为 ;
(4)①醋酸为弱酸,醋酸溶液与NaOH溶液反应生成醋酸钠和水,反应为
;
②溶液或熔融电解质导电的原因是存在自由移动的离子;往盛有NaOH溶液的烧杯中逐滴滴加等浓度的醋
酸溶液,两者反应生成与加入醋酸等物质的量的醋酸钠,但是溶液体积增大,溶液中自由移动离子浓度减
小,导致其电导率减弱,故选B。
学科网(北京)股份有限公司 学科网(北京)股份有限公司18.(8分)硫有多种化合物,如 、 等,它们对环境均有一定的影响,含硫化合物的综合利用既可
以消除污染,又可以带来一定的经济效益。
(1)有学者提出利用 、 等离子的作用。在常温下将 氧化成 而实现 的回收利用,写出
将 氧化成 反应的离子方程式 。
(2)含有 、 的硫酸盐混合溶液可用于吸收 回收硫单质,其转化关系如图所示。该图示中总反应
的化学方程式为 ,其中催化剂是 。
(3)某企业利用下列流程综合处理工厂排放的含 的烟气,以减少其对环境造成的污染。“ 吸收塔”
中发生反应的化学方程式为 ,该流程中可循环利用的物质为 (填化学式)。
【答案】(8分)(1)SO +2Fe3++2H O=2Fe2++SO +4H+(2分)
2 2
(2) 2H S+O 2S+2H O (1分) Fe3+(1分)
2 2 2
(3) SO +(NH ) SO +H O=2NH HSO4 (2分) (NH ) SO 、NH HSO (2分)
2 4 2 3 2 4 4 2 3 4 3
【解析】(1)硫元素的化合价由+4价升高为+6价, 的化合价应降低,被还原成 ,离子方程式为
SO +2Fe3++2H O=2Fe2++SO +4H+;
2 2
(2)根据转化关系,Fe3+作催化剂,使H S与氧气发生氧化还原反应,得到S和水,其总反应方程式
2
学科网(北京)股份有限公司 学科网(北京)股份有限公司2H S+O 2S+2H O;
2 2 2
(3)根据转化关系,吸收塔内通入物质是SO 、(NH ) SO ,生成物质为NH HSO ,发生反应有SO +
2 4 2 3 4 3 2
(NH ) SO +H O=2NH HSO ;循环使用物质是 (NH ) SO 、NH HSO ;
4 2 3 2 4 3 4 2 3 4 3
19.(12分)填空。
(1)有下列四个反应:
①SO +H O=H SO
3 2 2 4
②Cl +H O=HCl+HClO
2 2
③2F +2H O=4HF+O
2 2 2
④SO +2NaOH=Na SO +H O
2 2 3 2
上述反应中不属于氧化还原反应的是 (填序号,下同);H O只作还原剂的是 ;属于
2
氧化还原反应,但其中的H O既不被氧化,又不被还原的是 。
2
(2)工业盐的主要成分是NaNO ,以前有许多起因误食NaNO 而中毒的事件,其原因是NaNO 把人体内的
2 2 2
Fe2+转化为Fe3+而失去与O 结合的能力,这说明NaNO 具有 性。下列不能实现这种转化的物质
2 2
是 (填字母)。
a.酸性KMnO 溶液 b.FeCl c.O d.浓硫酸
4 3 2
(3)已知氧化性Fe3+>Cu2+>Fe2+,在溶有Fe (SO ) 和CuSO 的溶液中加入一定量的铁粉,下列说法正确的是
2 4 3 4
___________。(填字母)
A.若铁粉无剩余,且溶液中有Cu2+,则溶液中可能有Fe3+
B.若铁粉无剩余,溶液中一定有Fe2+,一定无Cu2+
C.若铁粉有剩余,则不溶物一定有铜
D.若铁粉有剩余,则溶液中一定有Fe2+和Cu2+
(4)我国古代炼丹术中用的铅丹与硝酸反应方程式是:X(铅丹)+4HNO =PbO +2Pb(NO ) +2H O,则铅丹的化学
3 2 3 2 2
式为 ,其中+2价的Pb和+4价的Pb含量之比为: 。
(5)治理汽车尾气方法之一是在汽车的排气管上安装“催化转化器”,CO和NO可以转化为两种无毒的气体,
写出化学方程式,用单线桥标出电子转移的方向和数目: 。
【答案(12分)】(1) ①④ (1分) ③(1分) ②(1分)
(2) 氧化 (1分) c(1分)
(3)AC(2分)
(4) Pb O (2分) 2:1(1分)
3 4
学科网(北京)股份有限公司 学科网(北京)股份有限公司(5) (2分)
【解析】(1)①④中没有元素化合价的变化,是非氧化还原反应;②③中有元素化合价发生变化,属于
氧化还原反应;反应②中水既不是氧化剂,也不是还原剂;反应③中,水中氧元素的化合价从-2价升高到
0价,失去电子,水作还原剂,被氧化;反应②是氧化还原反应,反应中只有Cl元素的化合价发生变化,
水既不被氧化,又不被还原,故答案为:①④;③;②;
(2)NaNO 能将Fe2+转化为Fe3+,Fe2+被氧化成Fe3+,则NaNO 做氧化剂,具有氧化性;选项中4中物质都
2 2
有氧化性,但Fe3+不能将Fe2+转化为Fe3+,故不能实现转化的是FeCl ;
3
(3)三价铁离子氧化性强于铜离子,加入铁粉,铁粉先与三价铁离子反应生成二价铁离子,剩余铁粉再
与铜离子反应生成二价铁离子;
A.若铁粉无剩余,且溶液中有Cu2+,则可能有三种情况,一种为铜离子只反应一部分,则三价铁离子完全
反应,一种为铜离子未反应,则三价铁离子恰好反应,一种为铜离子未反应,三价铁离子只反应一部分,
溶液中含有三价铁离子,故A正确;
B.若铁粉无剩余,结合A项分析,溶液中一定含有Fe2+,可能有Cu2+,故B错误;
C.若有铁粉剩余,则三价铁离子、铜离子完全反应,不溶物中一定含有铜,故C正确;
D.若有铁粉剩余,则三价铁离子、铜离子完全反应,则溶液中的金属阳离子只有Fe2+,故D错误;
答案选AC;
(4)氧化还原反应遵循原子个数守恒,依据方程式:X(铅丹)+4HNO ═PbO +2Pb(NO ) +2H O可知,X含有3
3 2 3 2 2
个Pb和4个O,化学式为:Pb O ;根据Pb的常见价态为+2、+4价,所以根据化合价代数和为0,则Pb O
3 4 3 4
中Pb2+与Pb4+的物质的量之比为2:1;
(5)CO和NO在催化剂作用下生成无毒、无害气体CO 和氮气,氧化剂是NO,还原剂是CO,电子转移如
2
图所示, 。
学科网(北京)股份有限公司 学科网(北京)股份有限公司