文档内容
江苏省苏州市中考化学试题
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Mg-24 Cl-35.5
一、单项选择题(包括20小题、每题2分,共40分。每题只有一个选项符合题意。)
1.“垃圾分类工作就是新时尚”。废旧报纸应投入的垃圾箱是
A. B. C. D.
2.下列物质属于氧化物的是
A. O B. SO C. NaOH D. KSO
3 3 2 4
3.下列变化属于化学变化的是
A. 干冰升华
B. 衣服晾干
C. 冰雪融化
D. 食物腐败
4.下列物质由离子构成的是( )
A. 铜
B. 水
C. 氯化钠
D. 氖气
的
5.四氯化钛(TiCl )可用于冶炼金属钛。四氯化钛中钛元素 化合价为
4
A. +4 B. -4 C. 0 D. -1
6.下列实验操作图示正确的是
A. 加热液体 B. 测定pHC. 滴加液体 D. 检查气密性
7.下列常见材料中,属于合成材料的是
A. 陶瓷
B. 焊锡
C. 塑料
D. 钢筋混凝土
8.下列有关化学用语表示正确的是
A. 五氧化二磷:PO
2 5
B. 银元素:AG
C. 2个镁离子:2Mg+2
D. 8个硫原子:S
8
9.工业用反应 来制备纯碱,该反应属于
A. 分解反应
B. 化合反应
C. 置换反应
D. 复分解反应
10.下列有关氧气的说法中,不正确的是
A. 氧气可供给呼吸
B. 鱼类能在水中生存,说明氧气易溶于水
C. 植物的光合作用是空气中氧气的主要来源
D. 焊接或切割金属时使用纯氧代替空气以获得更高的温度
11.某净水装置如图所示。下列说法正确的是A. 该装置能对水进行杀菌消毒
B. 该装置能除去水中的颜色和异味
C. 硬水经过该装置后可转化为软水
.
D 自来水经过该装置后可得蒸馏水
12.下列指定反应的化学方程式正确的是( )
A. 镁条燃烧:
B. 铜绿分解:
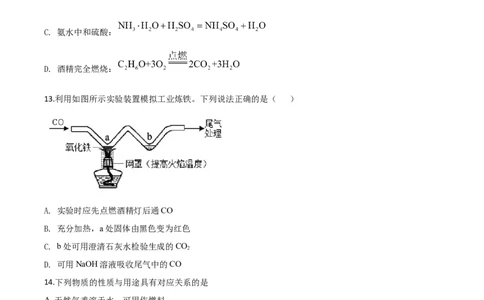
C. 氨水中和硫酸:
D. 酒精完全燃烧:
13.利用如图所示实验装置模拟工业炼铁。下列说法正确的是( )
A. 实验时应先点燃酒精灯后通CO
B. 充分加热,a处固体由黑色变为红色
C. b处可用澄清石灰水检验生成的CO
2
D. 可用NaOH溶液吸收尾气中的CO
14.下列物质的性质与用途具有对应关系的是
A. 天然气难溶于水,可用作燃料
B. 碳酸氢铵受热易分解,可用作化肥
C. 石墨有导电性,可用于生产铅笔芯
D. 小苏打能与盐酸反应,可用于治疗胃酸过多
15.下列关于溶液的说法正确的是( )
A. 溶液一定是无色透明的液体
B. 饱和溶液降温后都有溶质结晶析出
C. 碘酒溶液中,碘是溶质,酒精是溶剂D. 水加入蔗糖后形成溶液,导电性明显增强
16.下列各组离子在溶液中能大量共存的是( )
A. NH 、SO 、NO
B. H+、Ba2+、OH-
C. Fe2+、Na+、OH-
D. Ca2+、Cl-、CO
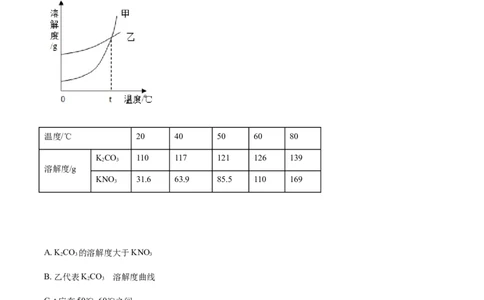
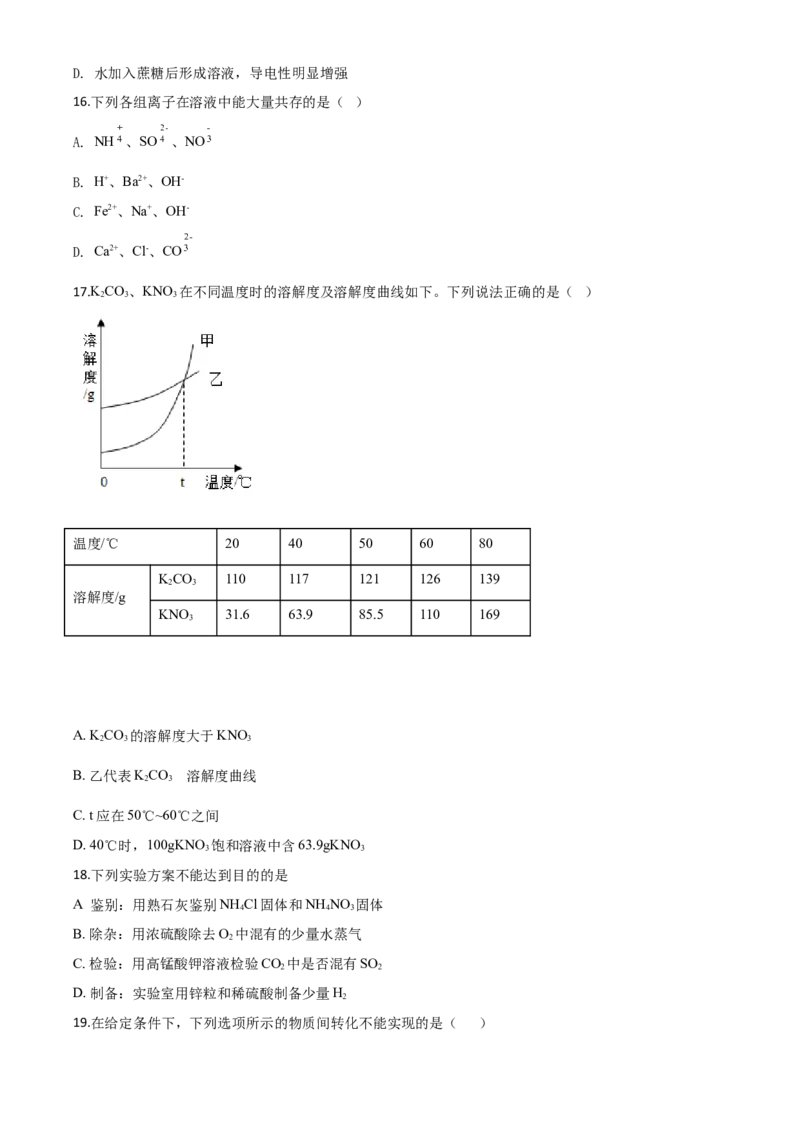
17.KCO、KNO 在不同温度时的溶解度及溶解度曲线如下。下列说法正确的是( )
2 3 3
温度/℃ 20 40 50 60 80
KCO 110 117 121 126 139
2 3
溶解度/g
KNO 31.6 63.9 85.5 110 169
3
A. K CO 的溶解度大于KNO
2 3 3
的
B. 乙代表KCO 溶解度曲线
2 3
C. t应在50℃~60℃之间
D. 40℃时,100gKNO 饱和溶液中含63.9gKNO
3 3
18.下列实验方案不能达到目的的是
.
A 鉴别:用熟石灰鉴别NH Cl固体和NH NO 固体
4 4 3
B. 除杂:用浓硫酸除去O 中混有的少量水蒸气
2
C. 检验:用高锰酸钾溶液检验CO 中是否混有SO
2 2
D. 制备:实验室用锌粒和稀硫酸制备少量H
2
19.在给定条件下,下列选项所示的物质间转化不能实现的是( )A.
B.
C.
D.
20.用如图所示装置探究CO 能否与HO反应。滴加盐酸,待试管乙中液体变红后,将其加热至沸腾,红色
2 2
不褪去。下列说法正确的是
A. 甲中逸出的气体只含CO
2
B. 乙中液体变红,证明CO 能与水反应
2
C. 加热后红色不褪去,说明碳酸受热不分解
D. 欲达到实验目的,可将盐酸改为稀硫酸
二、非选择题(共60分)
21.化学与人类生活息息相关。请回答下列问题。
(1)化石燃料燃烧产生大量CO,加剧了大气层的______________效应。
2
(2)油锅起火可盖上锅盖使火熄灭,其灭火原理是_______________。
(3)大米中含有的糖类物质主要是_____________(填名称)。
(4)儿童患佝偻病、骨骼疏松是因为缺少_____________元素。
(5)用铁制作炊具是利用其良好的延展性和___________性。
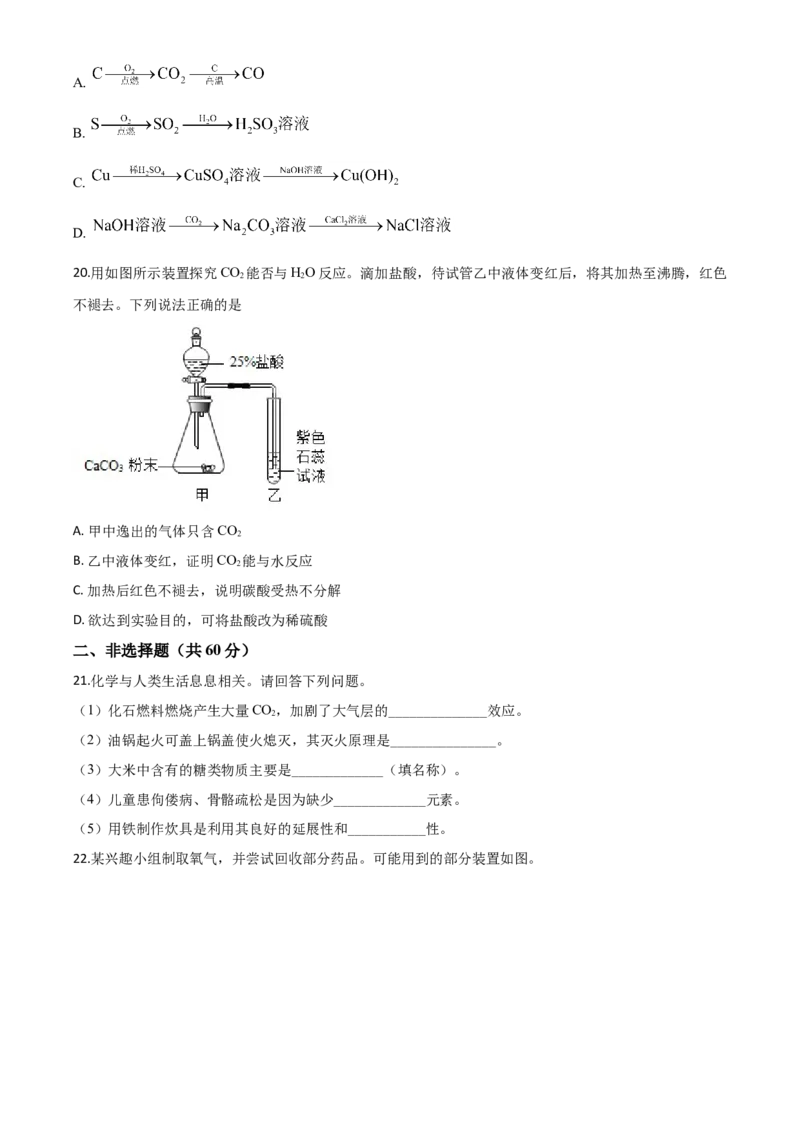
22.某兴趣小组制取氧气,并尝试回收部分药品。可能用到的部分装置如图。(1)上图中仪器a的名称是_______________。
(2)用双氧水和MnO 制氧气。发生反应的化学方程式为_____,收集氧气的装置可选用_____(填字母)。
2
(3)加热KClO 固体制氧气(1.5gMnO 作催化剂),并对KClO 完全分解后的残留固体进行分离。(已
3 2 3
知反应原理为: )
①发生装置应选用____________(填字母)。
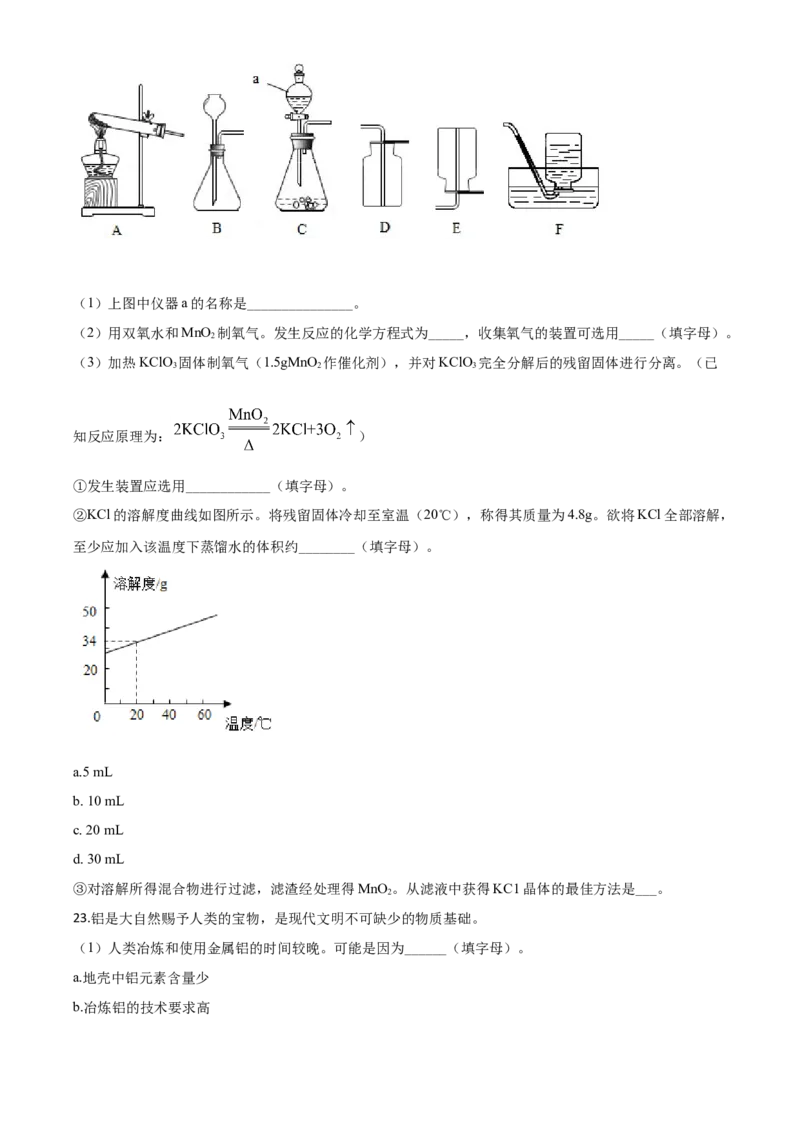
②KCl的溶解度曲线如图所示。将残留固体冷却至室温(20℃),称得其质量为4.8g。欲将KCl全部溶解,
至少应加入该温度下蒸馏水的体积约________(填字母)。
a.5 mL
b. 10 mL
c. 20 mL
d. 30 mL
③对溶解所得混合物进行过滤,滤渣经处理得MnO 。从滤液中获得KC1晶体的最佳方法是___。
2
23.铝是大自然赐予人类的宝物,是现代文明不可缺少的物质基础。
(1)人类冶炼和使用金属铝的时间较晚。可能是因为______(填字母)。
a.地壳中铝元素含量少
b.冶炼铝的技术要求高(2)用铝锂合金制造“神舟号”航天飞船的一些部件,主要是利用其强度高、耐腐蚀和____(写一条)等性
质。高温下,铝与LiO反应可置换出金属锂,写出该反应的化学方程式:_____。
2
(3)用砂纸去除铝片表面的氧化膜,将其浸人硫酸铜溶液中,一段时间后,观察到铝片表面有红色物质
析出,并有气泡产生,经检验气体为氢气。
①写出生成红色物质的化学方程式:_________。
②硫酸铜溶液中 的阳离子有_________(填离子符号)。
(4)原子簇是若干个原子的聚集体,有望开发成新材料。某铝原子簇由13个铝原子构成,其最外层电子
数的总和为40时相对稳定。写出该稳定铝原子簇的微粒符号:________。【铝原子的结构示意图为
】
24.阅读下面的科普短文,回答相关问题
氨是一种重要的化学物质,可用于制造硝酸和氮肥。氨主要来自于人工合成。1909年,弗里茨·哈伯成功
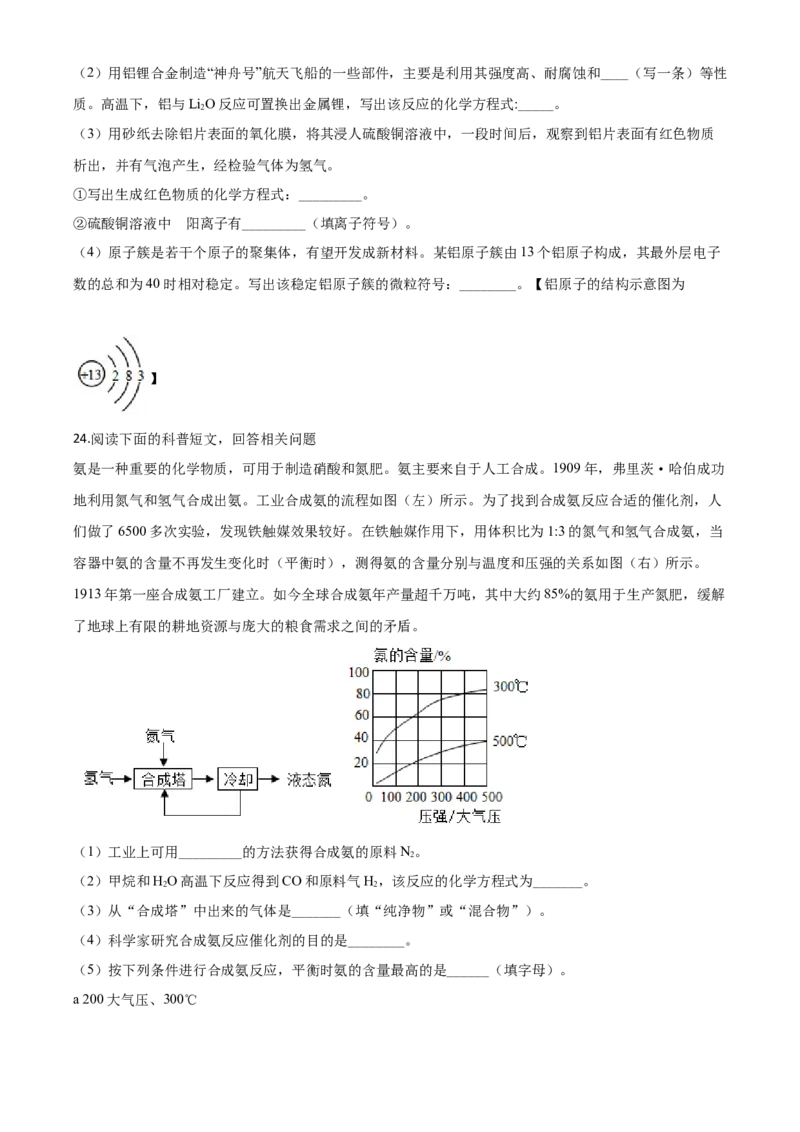
地利用氮气和氢气合成出氨。工业合成氨的流程如图(左)所示。为了找到合成氨反应合适的催化剂,人
们做了6500多次实验,发现铁触媒效果较好。在铁触媒作用下,用体积比为1:3的氮气和氢气合成氨,当
容器中氨的含量不再发生变化时(平衡时),测得氨的含量分别与温度和压强的关系如图(右)所示。
1913年第一座合成氨工厂建立。如今全球合成氨年产量超千万吨,其中大约85%的氨用于生产氮肥,缓解
了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。
(1)工业上可用_________的方法获得合成氨的原料N。
2
(2)甲烷和HO高温下反应得到CO和原料气H,该反应的化学方程式为_______。
2 2
(3)从“合成塔”中出来的气体是_______(填“纯净物”或“混合物”)。
(4)科学家研究合成氨反应催化剂的目的是________。
(5)按下列条件进行合成氨反应,平衡时氨的含量最高的是______(填字母)。
a 200大气压、300℃b 200大气压、500℃
c 400大气压、300℃
d 400大气压、500℃
25.氢气被看作是理想的能源。氢气的制取和储存是氢能源利用领域的研究热点
Ⅰ.氢气的制取
(1)科学家正致力于研究在催化剂和光照条件下分解水制氢气。写出该反应的化学方程式:_____,该反
应_______(填“放出”或“吸收”)能量。
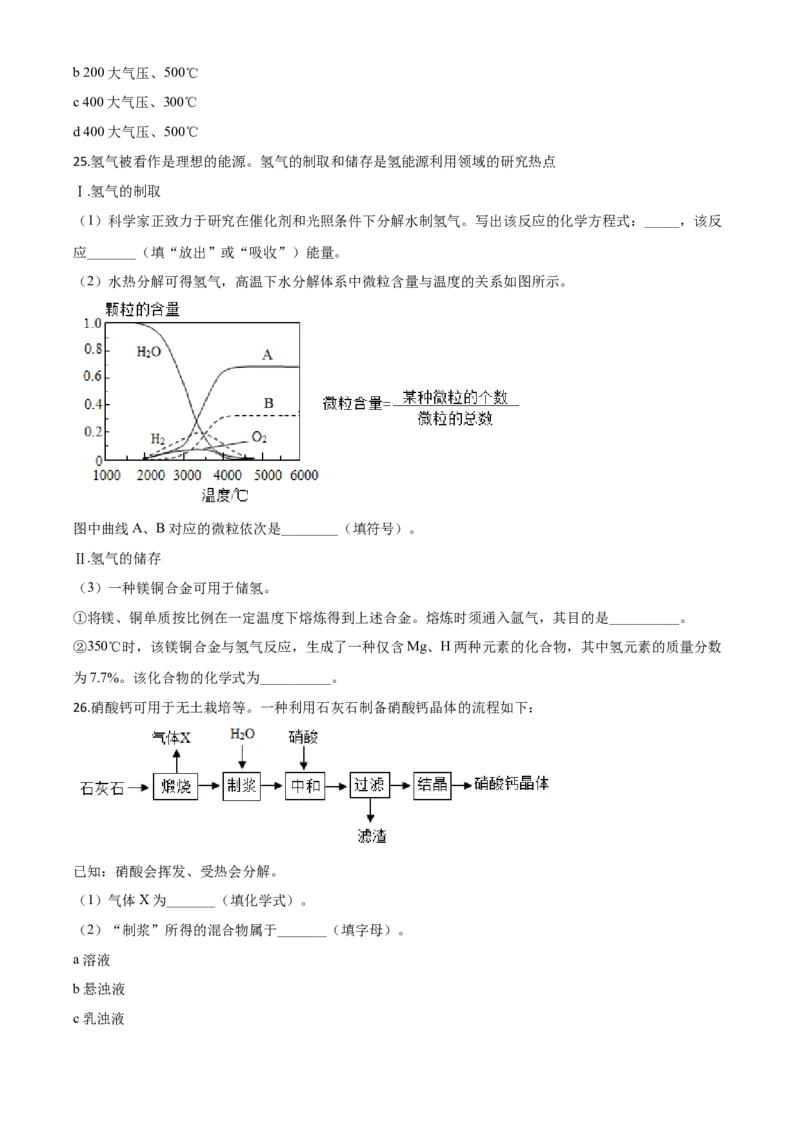
(2)水热分解可得氢气,高温下水分解体系中微粒含量与温度的关系如图所示。
图中曲线A、B对应的微粒依次是________(填符号)。
Ⅱ.氢气的储存
(3)一种镁铜合金可用于储氢。
①将镁、铜单质按比例在一定温度下熔炼得到上述合金。熔炼时须通入氩气,其目的是__________。
②350℃时,该镁铜合金与氢气反应,生成了一种仅含Mg、H两种元素的化合物,其中氢元素的质量分数
为7.7%。该化合物的化学式为__________。
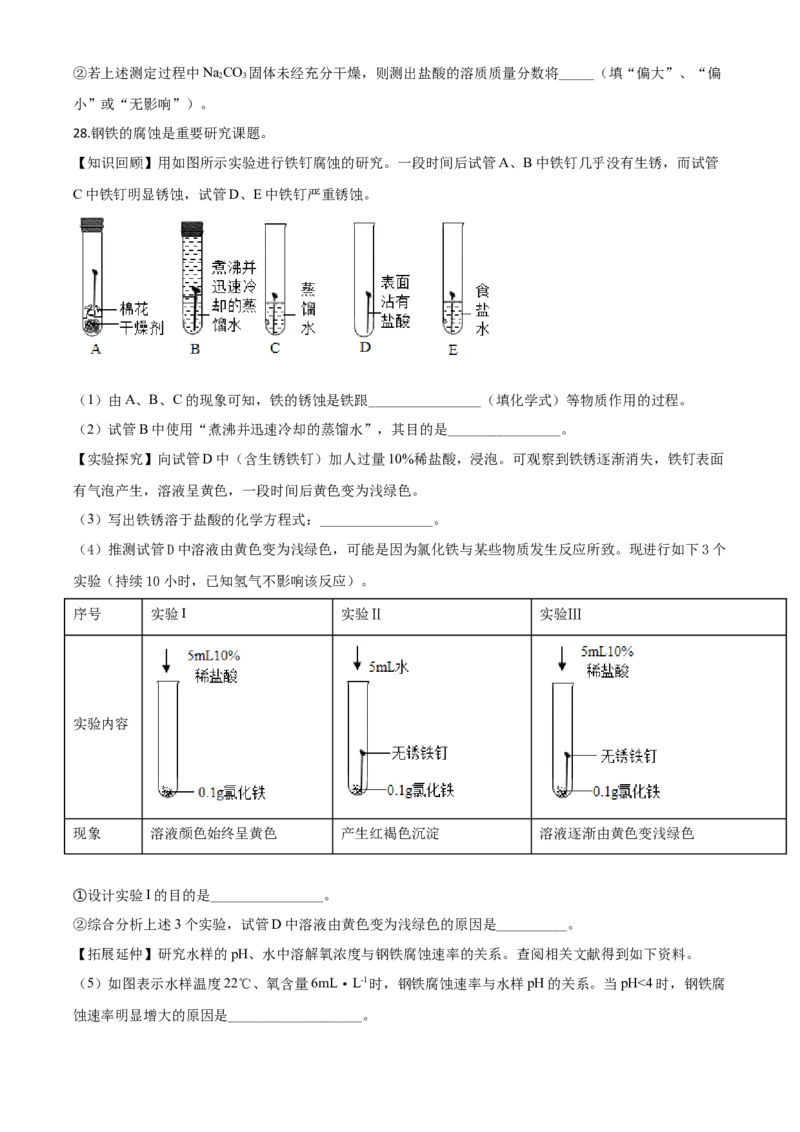
26.硝酸钙可用于无土栽培等。一种利用石灰石制备硝酸钙晶体的流程如下:
已知:硝酸会挥发、受热会分解。
(1)气体X为_______(填化学式)。
(2)“制浆”所得的混合物属于_______(填字母)。
a 溶液
b 悬浊液
c 乳浊液(3)写出“中和”步骤主要反应的化学方程式:________。
(4)工业生产根据以下两项指标判断“中和”反应完全发生:容器内混合物基本变澄清和_____。
(5)“制浆”时须控制好加入水的量。加入水量太少会导致制浆困难;加入水量太多会导致_。
(6)若省去“制浆”步骤也可制得硝酸钙。但硝酸利用率会降低、同时会产生污染气体NO 。产生NO
x x
的原因是______。
27.碳酸钠俗称纯碱或苏打,在生活、生产和实验硏究中均有广泛应用。
【配制溶液】配制溶质质量分数分別为1%、2%和4%的NaCO 溶液
2 3
(1)若配制50g溶质质量分数为4%的NaCO 溶液,下列操作正确的是______(填字母)。
2 3
a.用托盘天平称取2gNaCO 固体
2 3
b.选用50mL量筒量取所需体积的水
c.选用带玻璃塞的广口试剂瓶,将配好的溶液装瓶并贴标签
(2)分别测定25℃时,上述3种溶液的pH,记录数据如下:
实验编号 Ⅰ Ⅱ Ⅲ
溶质质量分数 1% 2% 4%
溶液pH 11.62 11.76 11.90
分析I、Ⅱ、Ⅲ三组数据可得出的结论是________。
【制备物质】用NaCO 溶液和FeSO 溶液发生复分解反应制备FeCO
2 3 4 3
【已知溶液pH大于8.8时,Fe2+完全生成Fe(OH) 沉淀】
2
(3)在烧杯中制备FeCO 沉淀时,应选用的加料方式是______(填字母)。
3
a.将FeSO 溶液与NaCO 溶液同时加入到烧杯中
4 2 3
b.将NaCO 溶液缓慢加入到盛有FeSO 溶液的烧杯中
2 3 4
c.将FeSO 溶液缓慢加入到盛有NaCO 溶液的烧杯中
4 2 3
(4)潮湿的FeCO 固体置于空气中易变质,反应如下: ,则X的化
3
学式为___________。
【标定浓度】标定待测盐酸的溶质质量分数
(5)将NaCO 固体在270℃干燥至恒重,准确称取0.212g无水NaCO 于锥形瓶中,加入50mL蒸馏水溶
2 3 2 3
解,滴入待测盐酸,当两者恰好完全反应时,消耗盐酸的体积为20.00mL(该盐酸的密度近似等于
1g·mL-1,反应中NaCO 所含的碳元素全部转化为CO)。
2 3 2
①列式计算待测盐酸的溶质质量分数_____(结果用百分数表示,保留两位小数)。②若上述测定过程中NaCO 固体未经充分干燥,则测出盐酸的溶质质量分数将_____(填“偏大”、“偏
2 3
小”或“无影响”)。
28.钢铁的腐蚀是重要研究课题。
【知识回顾】用如图所示实验进行铁钉腐蚀的研究。一段时间后试管A、B中铁钉几乎没有生锈,而试管
C中铁钉明显锈蚀,试管D、E中铁钉严重锈蚀。
(1)由A、B、C的现象可知,铁的锈蚀是铁跟________________(填化学式)等物质作用的过程。
(2)试管B中使用“煮沸并迅速冷却的蒸馏水”,其目的是________________。
【实验探究】向试管D中(含生锈铁钉)加人过量10%稀盐酸,浸泡。可观察到铁锈逐渐消失,铁钉表面
有气泡产生,溶液呈黄色,一段时间后黄色变为浅绿色。
(3)写出铁锈溶于盐酸的化学方程式:________________。
(4)推测试管D中溶液由黄色变为浅绿色,可能是因为氯化铁与某些物质发生反应所致。现进行如下3个
实验(持续10小时,已知氢气不影响该反应)。
序号 实验I 实验Ⅱ 实验Ⅲ
实验内容
现象 溶液颜色始终呈黄色 产生红褐色沉淀 溶液逐渐由黄色变浅绿色
①设计实验I的目的是________________。
②综合分析上述3个实验,试管D中溶液由黄色变为浅绿色的原因是__________。
【拓展延仲】研究水样的pH、水中溶解氧浓度与钢铁腐蚀速率的关系。查阅相关文献得到如下资料。
(5)如图表示水样温度22℃、氧含量6mL·L-1时,钢铁腐蚀速率与水样pH的关系。当pH<4时,钢铁腐
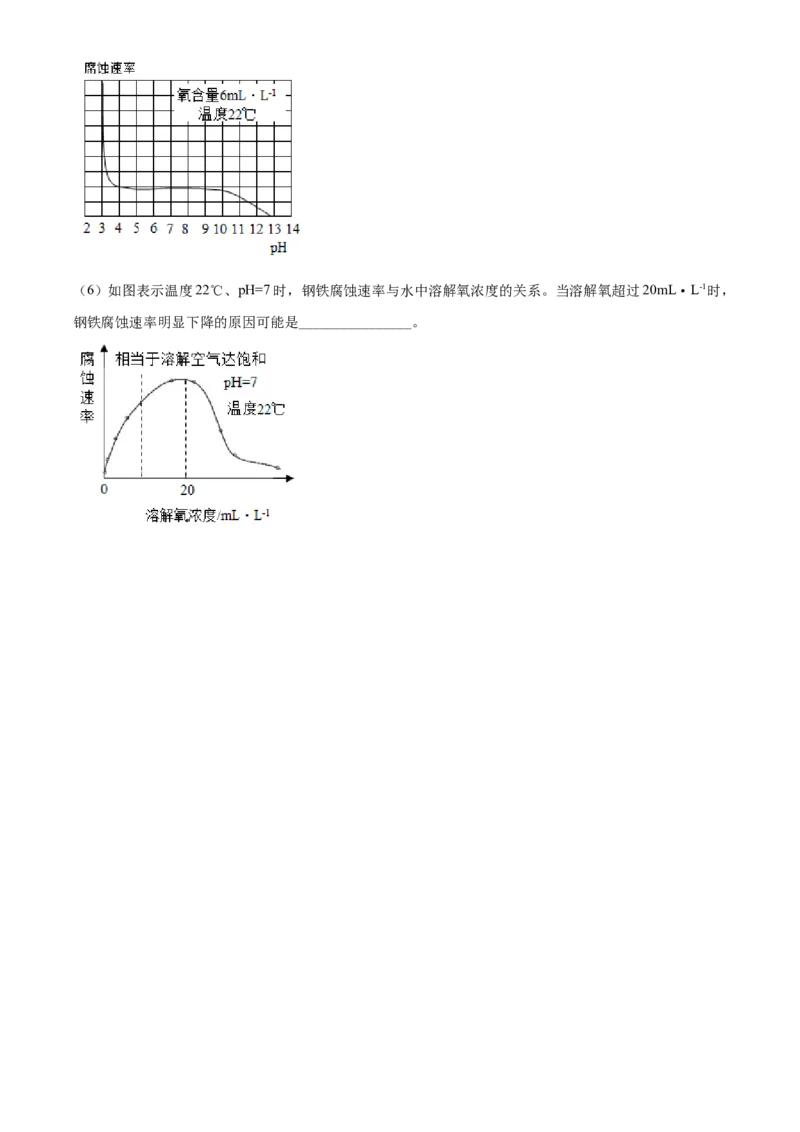
蚀速率明显增大的原因是___________________。(6)如图表示温度22℃、pH=7时,钢铁腐蚀速率与水中溶解氧浓度的关系。当溶解氧超过20mL·L-1时,
钢铁腐蚀速率明显下降的原因可能是________________。本试卷的题干、答案和解析均由组卷网(http://zujuan.xkw.com)专业教师团队编校出品。
登录组卷网可对本试卷进行单题组卷、细目表分析、布置作业、举一反三等操作。
试卷地址:在组卷网浏览本卷
组卷网是学科网旗下的在线题库平台,覆盖小初高全学段全学科、超过900万精品解析试题。
关注组卷网服务号,可使用移动教学助手功能(布置作业、线上考试、加入错题本、错题训练)。
学科网长期征集全国最新统考试卷、名校试卷、原创题,赢取丰厚稿酬,欢迎合作。
钱老师 QQ:537008204 曹老师 QQ:713000635