文档内容
2025-2026学年第一学期高三期初学情调研测试
化学试题
(考试时间:75分钟满分:100分)
可能用到的相对原子质量:H-l C-12 N-14 0-16 Na-23 V-51 Sr-88
1 .我国科学家在月壤中发现一种新矿物一一嫦娥石[Ca8YFe(PO4)7]。下列元素不属于主族元素的是
A.P B.Ca C.Fe D.O
2 .反应2NH3+NaCK>=NaCl+N,H4+H2O可用于制备股(NH)。下列说法正确的是
B.NaClO既含有离子键又含有共价键
H H
c.c「的结构示意图为逊,
D.N2H4的结构式为 I I
H—N=N—H
3. 实验室利用氨气和氯气反应制备氯化镂, 下列实验装置和操作不能达到实验目的的是
NH4H 和 浓盐酸
Ca(0H)2 固体
MnO2
A.制备NH3 B.制备Cl2 C.净化并干燥C12 D.制备NH4C1
4 .CO(NH2)2是常用氮肥。下列说法不正确的是
A.原子半径:r(C)>r(N)>r(O) B.稳定性:CH4>NH3>H2O
C.第一电离能:/i(N)>/i(O)>7i(C) D.电负性:x(O)>x(N)>x(C)
阅读下列资料,完成5〜7题:
周期表中IVA族元素及其化合物应用广泛,甲烷具有较大的燃烧热(890.3kJ・mo厂1),Si、Ge
是重要的半导体材料,硅晶体表面SiCh能与氢氟酸(HF,弱酸)反应生成H2SiF6(H2SiF6在水中完全电
离为H+和SiF「);1885年德国化学家将硫化楮(GeS?)与H?共热制得了门捷列夫预言的类硅一卷的4
是一种高强度耐高温材料,可由SiCh、C、2高温反应制得,同时生成CO。Pb, PbCh是铅蓄电池
的电极材料。
5 .下列说法正确的是
A.CH4空间构型为平面正方形 B.Si3N4为分子晶体
C.Ge基态核外价层电子排布式:[Ar]4s24P2 D.HF能形成分子间氢键
6 .下列化学反应表示不亚确的是
A.制备氮化硅:3SiO2+6C+2N2=S^= Si3N4+6CO
B.铅蓄电池放电时负极反应:Pb-2e- + SOF=PbSO4
C.电解水制氢的阳极反应:2H2O—2e. = H2 + 2OH-
D.甲烷的燃烧:CH4(g)+201(g)=CO2(g)+2H2O(1) A£T=-890.3kJ • mol"17 .下列物质结构与性质或物质性质与用途具有对应关系的是
A.甲烷具有还原性,可用作燃料 B.石墨能导电、可用作润滑剂
C.含铅化合物颜色丰富,可用作电极材料 D.SiCh为酸性氧化物,可用作光导纤维
催化齐
8 .对于反应 4NH3(g) + 5O2(g)、 4N0(g) + 6H2O(g); A//<0o 下列说法正确的是
4
A.该反应的ASV0
B.该反应的平衡常数长=―打西一
c4(NHJ c (O2)
C.催化剂能降低该反应的焰变
D.该反应中每消耗lmolNH3,转移电子数约为5 X 6.02X 1023
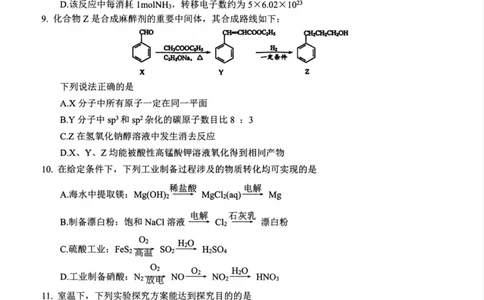
9 .化合物Z是合成麻醉剂的重要中间体,其合成路线如下:
CHO
ch3copc1.
CiHjONa, △
X Y Z
下列说法正确的是
A.X分子中所有原子一定在同一平面
B.Y分子中sp3和sp2杂化的碳原子数目比8 : 3
C.Z在氢氧化钠醇溶液中发生消去反应
D.X、Y、Z均能被酸性高镒酸钾溶液氧化得到相同产物
10.在给定条件下,下列工业制备过程涉及的物质转化均可实现的是
A.海水中提取镁:Mg(OH)2触般MgCL(aq)型鳗 Mg
B.制备漂白粉:饱和NaCl溶液电鳗Cb亘次到 漂白粉
C,硫酸工业:FeSz 高温 SC)2 H2SO4
D.工业制备硝酸:N2放电 NO °?» NO2-HNO3
11.室温下,下列实验探究方案能达到探究目的的是
选项 探究方案 探究目的
A 向盛有淀粉KI溶液的试管中滴加几滴澳水,震荡,观察溶液颜色的变化 B。的氧化性比12强
B 将SCh气体通入少量酸性KMnO4溶液中,观察溶液是否褪色 SO2具有漂白性
用pH试纸分别测定浓度均为(Mmol,Lr的NaClO溶液和NaNOz溶液的 比较HC1O和HNCh
C
pH,比较读数大小 的酸性强弱
向盛有2 mL 0.1 mol •L-1AgNO3溶液的试管中滴加2滴0.1 mol • L-1NaCl 探究&p(AgCl)和
D
溶液,振荡试管,然后向其中滴加4滴0.1 mol ・L「KI溶液,观察现象 Ksp(Agl)的大小12 .室温下,通过下列实验探究NaHCCh、Na2cO3溶液的性质。
实验1:用pH试纸测量0.1mol・L/NaHCO3溶液的pH,测得pH约为8
实验2:将0.1mol・L」NaHCO3溶液与O.lmokL-iCaCb溶液等体积混合,产生白色沉淀
实验3:向饱和Na2c03溶液中通入CO2,溶液pH从12下降到约为9
下列说法正确的是
A.NaHCCh 溶液中:c(CO ; ) + c(H*) = c(H2CO3) + c(Oir)
B.由实验 1 可得出:c(CO 3") > c(H2CO3)
C.实验2中两溶液混合时有:c(Ca2+) - c(C0:) = Ksp(CaC03)
D.实验3中发生反应的化学方程式为:2Na+ + COi~ + H20 + C02= 2NaHCO3 I
13 .二氧化碳加氢制甲烷过程中的主要反应为
反应 I CO2(g) + 4H2® = CH4(g) + 2H20(g) Mil
反应 II CO2(g) + H2(g) = CO(g) + H2O(g) Aft
在密闭容器中,L01X105pa、〃起始(CO?):"起始(见)=1:4时,C02平衡转化率、在催化剂作用下反应
*翳°0%。
相同时间测得C02实际转化率随温度的变化如题图所示。CH4的选择性可表示为
下列说法正确的是
、、、? CO2平衡
A.估算机需要4种化学键的键能数据 转化率
CO]实际:--
B.提高〃起始(CO?):麓起始(凡)=1 : 4的值,能增大CO2平衡转化率
转化率 .
C.CO的平衡选择性随着温度的升高而减小
D.使用合适的催化剂催化,二氧化碳的转化率可达到X
14. (14分)碎广泛应用F•冶金工业,以郁铜废料(主要含CgTe)为原料回收璐单质的一种工艺流
程如下:
硫酸、氏。2溶液 Na2c2O4溶液 Na2sO3溶液
铜蹄渣已 知: ①Kal (H2c2。4)=5.0x10-2、 心(H2c2O4) =L 5*ICT*、 ,^(CuCzO^.OxIO-8 ;
@Cu2+ +2C20r ^[Cu(C2O4)2]2"②=L8x!0%
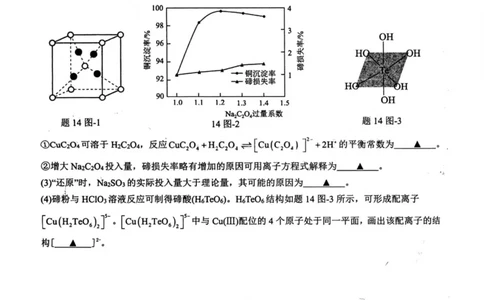
。)“氧化酸浸”的浸出液中降主要以HzTeCh形式存在(晶胞结构如题14图・1所示),滤渣可用于提炼
贵金属银。
①CuzTe晶胞中Te的配位数为 ▲ 。
②酸浸时温度控制在80c左右,目的是 ▲ ,
③写出CiuTe发生反应的离子方程式: A
(2)“沉铜”时测得铜沉淀率随Na2c2。4投入量的变化关系如题14图.2所示。
100 4
①CUC2O4可溶于 H2c2。4,反应C11C2O4 +H2c2。,u [Cu(C2OJ ] -»-2H4 的平衡常数为 ▲ 。
②增大Na2c2。4投入量,础损失率略有增加的原因可用离子方程式解释为 ▲。
(3)“还原”时,Na2s03的实际投入量大于理论量,其可能的原因为 ▲ 。
(4)璃新与HC103溶液反应可制得磺酸(H6TeO6)。HeTeC%结构如题14图・3所示,可形成配离子
[Cu(H2TeO6)2]5\ [Cu(H2TeO6)2丁中与Cu®)配位的4个原子处于同一平面,画出该配离子的结
构[▲ 广。
15,(16分)氯化锂在医疗领域有重要作用。工业上利用某含锢(Sr)废渣(主要含有SrS04、SiCh、
CaC03. SrCCh 和 MgCCh 等)制备 SrCL。
已知 25℃时,^(SrSO^lO-646, Ksp(BaSO4)=10'9.97
(1)酸浸。向某含锂废渣中加入足量稀盐酸充分反应后过滤。
①勰位于元素周期表第五周期第na族,其基态原子外围电子排布式为 ▲。
②,,浸出液”中主要的金属离子有Ca2\ ▲(填离子符号)。
(2)盐浸。向酸浸后所得滤渣中加入BaCL溶液,充分反应。
①“盐浸”中SrSCh转化反应的离子方程式为▲。
②25c时,向0.01molSrS04粉末中力口入100ml0.11mol・L-iBaCL溶液,充分反应后,理论上溶液中
c(Sr2+) c(SO^j=^o (仅填数值;忽略溶液体积的变化)
4(3)酸浸和盐浸后的溶液合并,将窝穴体a(结构如右图)与K+形成的超分子
加入合并后的溶液中,能实现SF+与其它离子的有效分离。从结构的角度分析,
窝穴体a能提取溶液中se的原因是 ▲。
(4)产品纯度检测:
①称取1.000g产品加水溶解,向其中加入0.01 mol的AgNCh溶液,待C厂完全沉淀后,滴入卜2滴
含Fe3+的溶液作指示剂,用0.2000 mol-L「的NH4SCN标准溶液滴定剩余的AgNCh,平均消耗
NH4SCN溶液20.00mL (已知:SCN-♦ Ag-AgSCNpo计算产品中SrCLFIfcO的百分含量一4_。
(写出计算过程)。
②制备SrCho由SrCl2-6H2O制备尢水SrCl2的最优方法是 ▲。(填序号)。
a.直接加热脱水 b.在HC1气流中加热脱水
16. (15分)纳米铜用途广泛,以黄铜矿(主要成分为CuFeSz,含有杂质SiCh)为原料制备纳米铜的过
程如下:
FeClj溶液H2s04溶液、Ch 氨水 N2H[溶液
黄铜矿 I~~H *泡 |----H |------H|~IN 纳米铜 I
S、Si()2等 Fe(OH)3
已知:铁氟化钾(K3[Fe(CN)6])溶液能与Fe2+形成蓝色沉淀
(1)①浸泡时,加料完成后,以一定速率搅拌反应“提高浸出率的方法还有▲。
②写出“浸泡”时CuFeSz发生反应的离子方程式_」。
(2)判断“氧化”反应已完成的实验操作及现象为 ▲ 。
(3) “除铁”步骤,除用氨水调节pH外,还可用的氧化物为-4^ (填化学式)。
(4)制备纳米铜。调节[Cu(NH3)4]2+溶液的pH=ll,加入3moi・L—iN2H4溶液,75 ℃水浴加热,充分反
应得到纳米铜。
①获得纳米铜时,N2H4被氧化成N2,反应的离子方程式为一
②N2H4还原过程中可能生成难溶的CuCl(白色)和CU2O(红色),为判断纳米铜样品中是否含有上述
两种杂质,补充完整实验方案:将制得的样品先后用蒸储水、无水乙醇洗涤干净。取少量样品,上。
(已知:Cu2O+2H+=Cu2++Cu+H2O;必须使用的试剂和设备:2 moiI। H2sO4溶液、6mol1一】HNO3
溶液、2% AgNCh溶液,通风设备)
17. (16分)氢气是•种理想的清洁能源,将成为未来的主要能源。金属材料在制氢、储氢和用氢
方面发挥了重要作用
⑴制氢。用氧缺位铁酸铜(CuFezOQ)作催化剂,利用太阳能热化学循环分解HzO可制Hz。
①氧缺位铁酸铜通过两步反应分解水制氢。已知第二步反应为:2CuFe2O4=2CuFe2O4*O2T,则第
一步反应的化学方程式为 ▲ 。
②CuFezO’可用电化学方法得到,其原理如题17图-1所示,则阳极的电极反应式为. ▲一
中
间
体
X
熔融口。
2
题17图-1
(2)储氢。部分Hz和Mg一定条件下化合生成Mg%以储氢;部分H?和N2在催化剂表面合成氨以储
氢,其反应机理的部分过程如题17图・2所示
①请画出中间体X的结构 ▲。
②研究发现,使用Ru系催化剂时,4在催化剂表面的吸附活化是整个反应过程的控速步骤,实际
工业生产时,将〃(H2)/"(N2)控制在1.8〜2.2之间,比理论值3小,其原因是一 ▲ °
(3)释氢。储氢材料MgH2能与水反应放氢,但与纯水反应产生H?很少。MgCL、NiCL、CuCL等盐
溶液能提升MgH2的放氢性能。Imol -L1的几种盐溶液与MgH2制备H2时MgH2转化率如题17图.3
所示。
已知:Ksp[Mg(OH)2] = 5.6xl(r】2; Ksp[Ni(OH)2] = 5.5xlO-q ^SP[Cu(OH)2] = 2.2x1 O-20;
i .氧化性:
ii . MgH2在MCb(M代表Mg、Ni、Cu)溶液中水解的示意图如题17图必所示。
题17图-4
①MgHz受热分解能放氢,采用与水反应放氢的优点是 ▲ °
②使用NiCL溶液制备H2的反应速率大于MgCl2溶液,可能的原因是 ▲ 。
③40min后,CuCb溶液制备H2时MgHz转化率小于MgCb溶液,可能的原因是 ▲ 0
(4)储氢物质的运用。NH3常用于烟气(主要成分NO、NO2)脱硝。以N2为载气,将含一定量NO、NH3
及02的模拟烟气以一定流速通过装有催化剂CeO2的反应管。
实验证明,烟气中含S02会导致催化剂不可逆的中毒(Ce,,氧化S02生成SO「覆盖在生成的Ce3+
表面,阻止了 02氧化而添加CuO后抗硫能力显著增强。请结合图示机理,说明抗硫能力增
强的原因 ▲ 」
题17图・52025-2026学年第一学期高三期初学情调研测试
化学试题答案
一、单项选择题(每题3分,共计39分)
CBCBD CADDB ADA
14 . (14 分)
(1) 4 温度较低时反应速率较慢,但温度过高会加速H2O2分解
Cu2Te + 4H+ + 4H2O2 = H2TeO3 + 2Cu2+ + 5H2O
(2) 2.7x10" H2TeO3 + 2C2O^ + 4H+ = Te J +4CO2 T +3H2O
⑶提高H2T6O3的还原率;Na2sO3会与“沉铜”后所得滤液中的酸反应生成SO?,SO从溶液中逸出
OH OH
(除标注外每空2分)
OH OH
15 . (16 分)
(l)5s2 (2)Sr2\ Mg2+
(2)®SrSO4(s)+Ba2+ (做)□ BaSO4(s)+Sr2+ (四) ② 10一& 97
⑶窝穴体a的空腔与“2+更匹配,可通过分子间相互作用形成超分子,且S*+具有更多的空轨道,能
够与更多的N、O形成配位键,形成超分子后,结构更稳定
⑷①80.1 %
H(NH4SCN)=0.2000mol^x0.02L=4.0xl0-3mol, n(Ag+)=4.0xW3mol, (1 分)
与 C「反应的 Ag+的物质的量为:n(Ag+)=lxl0-2mol-4.0xl0_3mol=6.0xl0-3mol, (1 分)
n(SrC12*6H2O)= xn(Ag+)=3x 10-3mol, m(SrC12*6H2O)=3x 10_3molx267 g/mol=0.801g, (1 分)产品纯度为:粤比xl00%=80.1% (1分)
1g
②a (除标注外每空2分)
16 . (15 分)
⑴①延长反应时间、适当升高温度。②CuFeS2+4Fe3+=5Fe2++Ci?++2S
⑵取少量氧化后的溶液于试管中,滴加K^FeUNkl溶液,无蓝色沉淀产生
⑶CuO
75
⑷① 2[Cu(NHa)4]2"+N,H +4OH =^=2Cu+N2 T +8NH3 T +4H2O
②加入过量2moi17 H2sO4溶液中(1分),边加边搅拌,若固体部分溶解,溶液呈现蓝色,则含有C%。
(1分);在通风设备里(1分),另取少量样品加入过量6moi-lThN03溶液中(1分),边加边搅拌,
使固体充分溶解,向其中滴加几滴2%AgNO3溶液,若有白色沉淀产生,则含有CuCl (1分)
(除标注外每空2分)
17 . (16 分)
⑴ CuFe2O4-x+xH2O=CuFe2O4 +汨2T
Cu+2Fe+4O2--8e" = CuFe2()4
(2) 提高N2在合成气中比例,增大N2在催化剂表面的吸附活化总量,加快反应速
率;利于提高H2的转化率,同时提高储氢率
⑶①不需要加热,能耗低;相同量的MgH2与水反应释放氢气更多 ②
Ksp[Ni(OH)2]