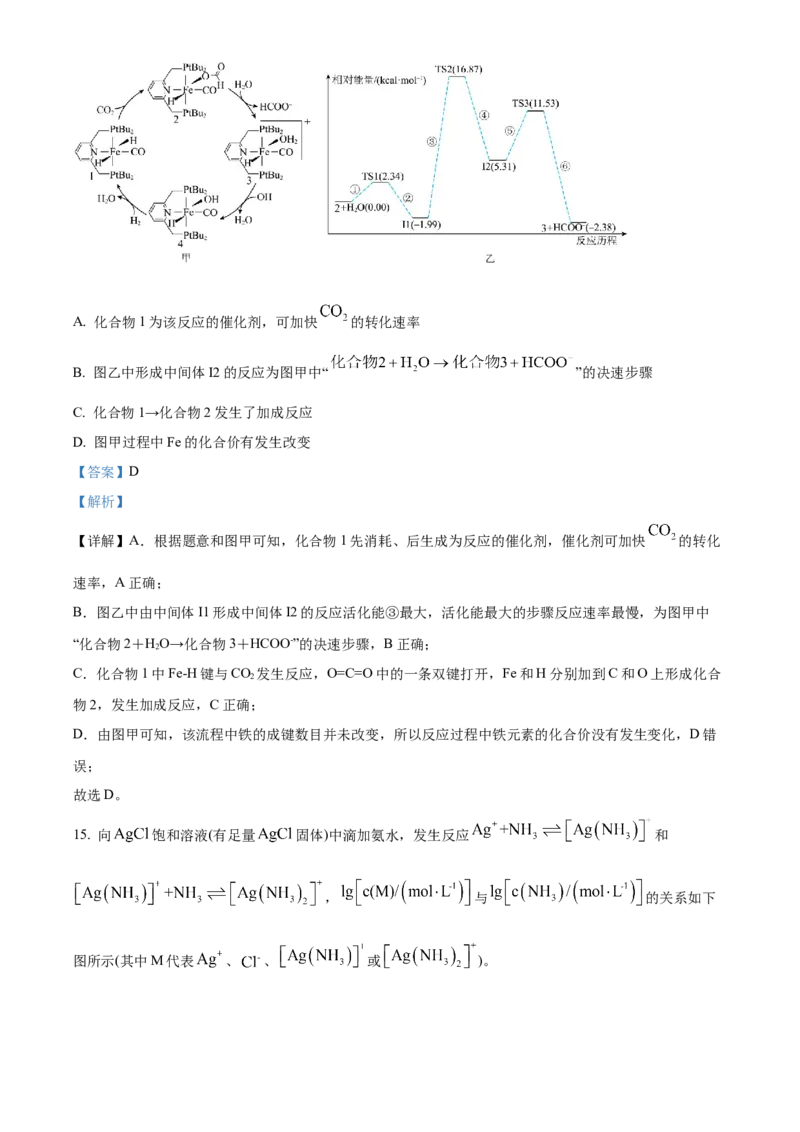
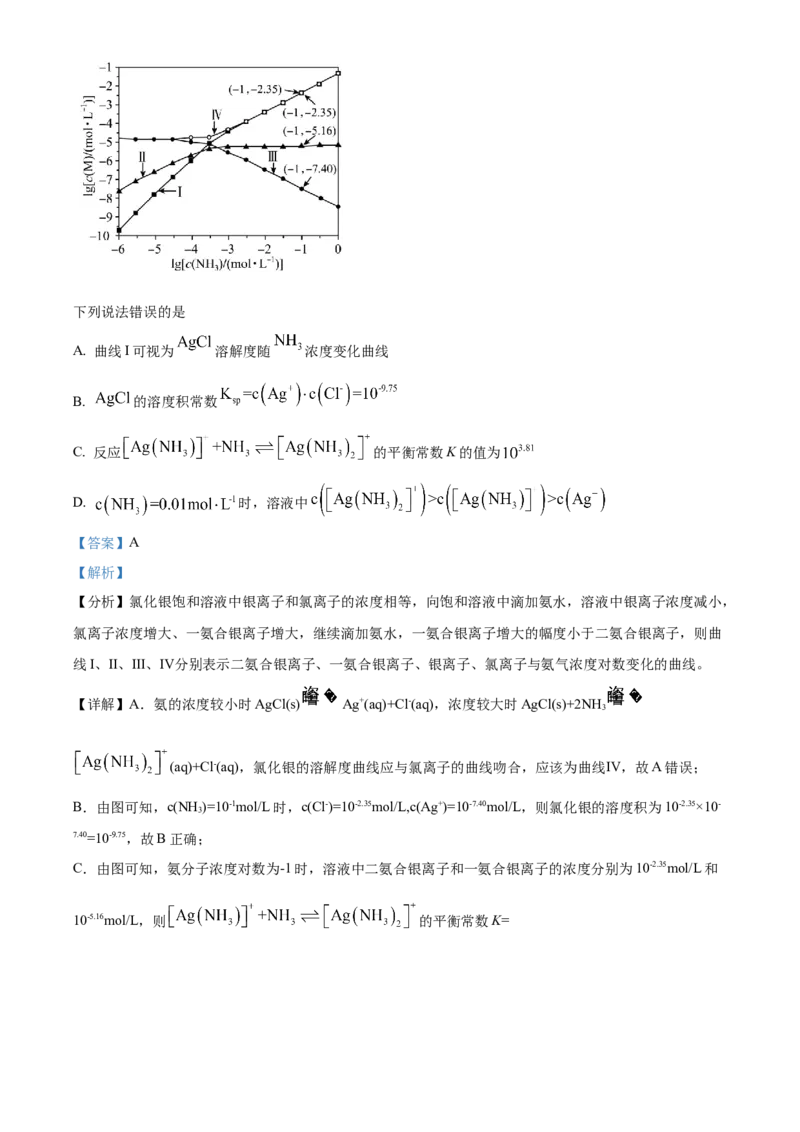
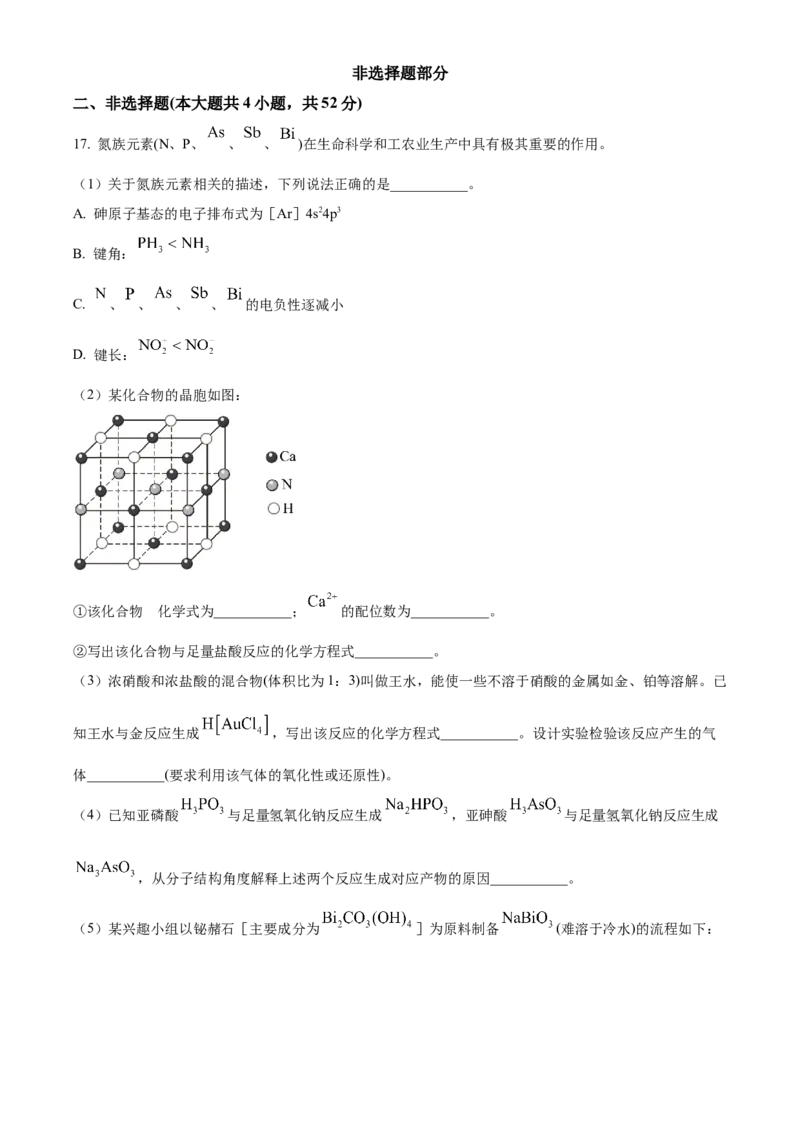
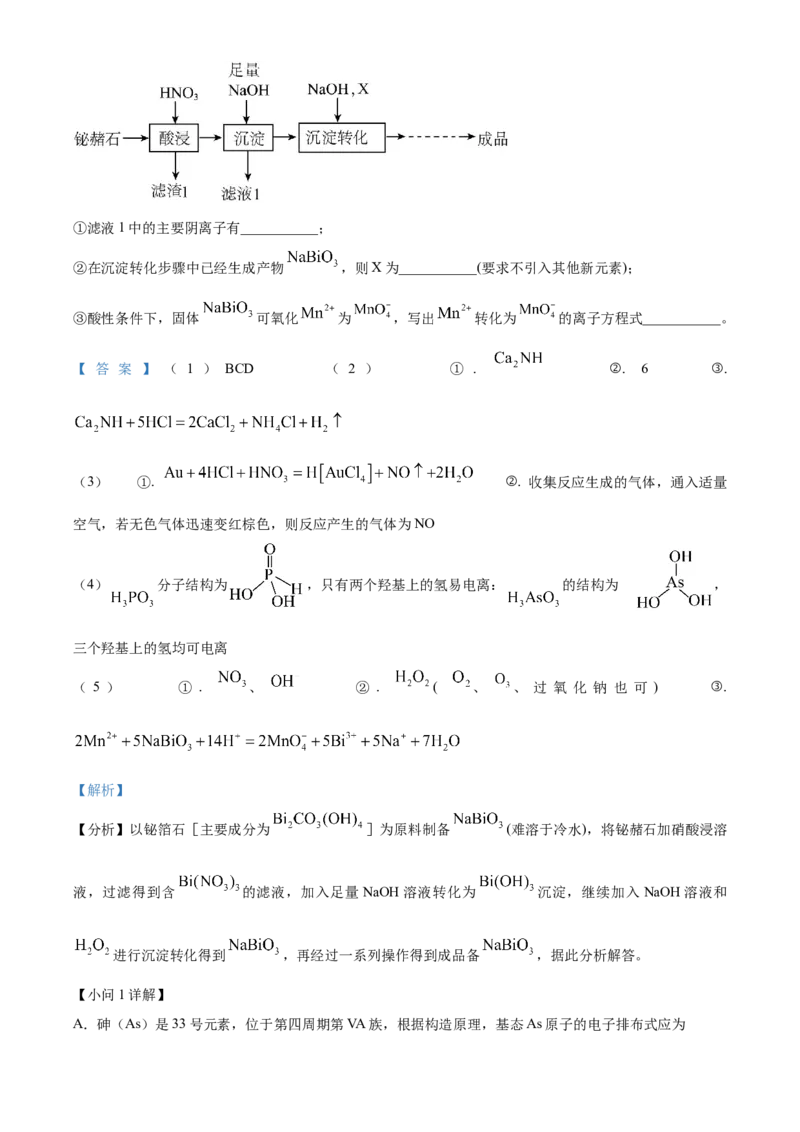
文档内容
杭州二中 2025 学年第一学期高三年级十月月考
化学试题
可能用到的相对原子质量:H1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Si 28 P 31
S32 Cl 35.5 K 39 Ca40 Fe56 Cu 64 Zn 65 Br 80 Ag 108
选择题部分
一、选择题(本大题共16小题,每小题3分,共48分。每小题列出的四个备选项中只有一个
是符合题目要求的,不选、多选、错选均不得分)
1. 下列物质中含有非极性共价键的是
A. NaCl B. C. NaOH D. HCOOH
【答案】B
【解析】
【详解】A.NaCl中只有离子键,不含非极性共价键,A错误;
B. 中 内的O-O键为同种原子间的非极性共价键,B正确;
C.NaOH中OH-含O-H极性键,不含非极性键,C错误;
D.HCOOH中所有共价键均为不同原子间的极性键,D错误;
故答案选B。
2. 下列化学用语或图示表示正确的是
A. 基态S原子的价电子轨道表示式:
B. 反-2-丁烯的结构简式:
C. p-p 键形成的轨道重叠示意图:
D. 的VSEPR模型:
【答案】D
【解析】【详解】A.基态S原子价电子为3s23p4,3p轨道有3个轨道,根据洪特规则,4个电子应先分占3个轨道
(自旋平行),再成对,轨道表示式: ,A错误;
B.反-2-丁烯中两个甲基应在双键异侧,即正确结构简式为 ,题目结构简式中两个甲基在
同侧,为顺式结构,B错误;
C.p-p 键为肩并肩重叠,图示为头碰头重叠(形成σ键),C错误;
D.NH 中心N原子价层电子对数= ,有1对孤对电子,VSEPR模型为正四面体形,图示
3
符合,D正确;
故答案选D。
3. 根据元素周期律,下列说法不正确的是
A. 第一电离能:Cl>P>S B. 热稳定性:
C. 碱性: D. 非金属性:Si0,若升高温度,反应正向移动,可以增大H 的转化率;该反应反应前后气体的总物质的
2
量不变,改变压强,平衡不移动;催化剂只能改变反应速率,不能改变平衡转化率;投料比[n(CO ):n(H)]
2 2
不同,H 的转化率不同,综上所述,能改变H 的平衡转化率的有AD两个选项。
2 2
【小问2详解】
①由图可知,240℃时,甲醇的产率为30%,由起始二氧化碳的物质的量为1mol,反应管出口处检测到二
氧化碳的物质的量为0.68mol可知,甲醇的选择性为 =93.75%;
②由图可知,在催化剂表面修饰羟基可以降低生成HCOO *的活化能,加快反应速率。
【小问3详解】
①由反应机理图中反应物和生成物的结构可推知,中间体X的结构简式为 ;
②由反应机理可知,若用 代替环氧乙烷,相同条件下,生成 的产率远大于
,因为是 右侧两个甲基的体积大于氢原子,空间位阻大,Nu-易进攻左侧碳原
子或难进攻右侧碳原子。
【小问4详解】
①HCOO−的中心原子C的价层电子对数为 ,C的孤电子对数为0,则其空间
构型为平面三角形;
②CO(碳元素为+4价)在左侧电极转化为HCOO−(碳元素为+2价),则CO 被还原,左侧电极为阴极,根
2 2据电荷守恒和原子守恒,阴极反应式可写2CO+2e−+H O=HCOO−+HCO 。
2 2
19. 为探究工业品硫的性质并测定其纯度设计了如下实验(忽略杂质的反应)。
Ⅰ.性质探究:
实验一向试管加入工业品硫、KOH水溶液,持续振荡,淡黄色固体完全溶解;继续滴加 溶液产生
白色沉淀,加足量盐酸沉淀完全溶解。
实验二
向试管加入工业品硫、KOH水溶液、双氧水,持续振荡,淡黄色固体完全溶解;继续滴加 溶液产
生白色沉淀,加足量盐酸沉淀不溶解。
Ⅱ.纯度测定:
①取少量工业品硫研成粉末,准确称取 置于圆底烧瓶中,准确加入 的乙醇溶液(过量),加
入蒸馏水,搅拌,85℃回流至样品完全溶解后,蒸馏除去乙醇。
②冷却后,向圆底烧瓶中加入适量蒸馏水,搅拌下缓慢滴加足量 ,加热至100℃,保持20min,
冷却至室温。
③将圆底烧瓶中溶液全部转移至锥形瓶中,加入2滴甲基橙,用 标准溶液滴定至终点,平行
实验多次,记录实验数据。
④不加工业品硫,重复步骤①②③做空白实验,平行实验多次,记录实验数据。
已知:25℃时, 的 、 ; 的 、 。
回答下列问题:
(1)“实验一”中0.3molS与0.8molKOH充分反应,若向反应后溶液中加入含0.3molHCl的盐酸,得到
100mL溶液,在25℃时,则该溶液的pH最接近___________。
A. 14 B. 13 C. 12 D. 11
(2)若“实验一”中S过量,则反应时会生成 。 的阴离子能与 形成配合物离子
,画出 的结构并圈出与 形成配位键的S原子___________。
(3)“实验二”中淡黄色固体溶解的化学反应方程式为___________。乙醇的作用是___________,样品
完全溶解后,必须蒸馏除去乙醇的原因是___________。
(4)实验数据如下:加入工业品硫实验数据
序号 1 2 3 4 5
滴定前读数/mL 0.00 23.98 0.00 0.00 0.00
滴定后读数/mL 23.98 48 24 24.22 24.02
进行空白实验,平均消耗 标准溶液40.00mL。应舍弃的数据为___________(填序号),测得工
业品硫的纯度为___________(写出计算式)。
【答案】(1)B (2) 或
(3) ①. ②. 增大硫在水中的溶解度 ③. 乙醇可能会
被 氧化成乙酸,与KOH反应,干扰后续测定
(4) ①. 2、4 ②.
【解析】
【分析】实验一中,向试管中加入工业品硫和KOH水溶液,持续振荡,淡黄色固体(硫)完全溶解,发
生的反应为: ,继续滴加BaCl 溶液产生白色沉淀,是因为KSO 与
2 2 3
BaCl 反应生成了BaSO 白色沉淀,反应方程式为: ,加足量盐酸后沉淀完
2 3
全溶解,是因为BaSO 能与盐酸反应,生成氯化钡、二氧化硫和水,反应方程式为:
3
。
实验二中,向试管中加入工业品硫、KOH水溶液和双氧水,持续振荡,淡黄色固体(硫)完全溶解,首先,
硫与KOH发生反应,同时双氧水作为强氧化剂,会将硫与KOH反应的产物进一步氧化,反应生成了含硫
酸根( )的化合物,反应方程式为: ,继续滴加BaCl 溶液,
2
产生白色沉淀,是因为溶液中的 与Ba2+结合生成了BaSO 白色沉淀,反应方程式为:
4,加足量盐酸后沉淀不溶解,是因为BaSO 不溶于盐酸,这也证明了沉
4
淀是BaSO,进一步说明反应过程中生成了硫酸根离子。
4
纯度测定时,取少量工业品硫研成粉末,准确称取m g置于圆底烧瓶中,准确加入V mL KOH的乙醇溶
1
液(过量),加入蒸馏水,搅拌,发生的反应为: ,85℃回流至样品完全
溶解后,蒸馏除去乙醇,冷却后,向圆底烧瓶中加入适量蒸馏水,搅拌下缓慢滴加足量30% H O,加热至
2 2
100℃,发生的反应为: 、 ,将溶液转移至锥形
瓶,加入甲基橙作指示剂,用 标准溶液滴定,此时是用盐酸滴定溶液中剩余的KOH,最后
做空白实验,是为了消除实验中KOH乙醇溶液、HO 等试剂以及实验操作本身带来的误差,通过空白实
2 2
验数据与样品实验数据对比,能更准确计算出与工业硫反应的KOH的量,进而确定工业硫的相关含量等。
【小问1详解】
“实验一”中硫和KOH发生反应 ,则0.3molS与0.6molKOH反应生成
0.2mol ,还剩余0.2molKOH,若向反应后溶液中加入含0.3molHCl的盐酸,发生中和反应
,剩余0.1molHCl,0.1mol HCl与0.2mol 发生反应 ,
则得到的100mL溶液中 ,此时以 的第一步水解为主,
, ,
,则 ,因此在25℃时,pH最接近13,故选
B。
【小问2详解】可看作是 中的一个O原子被S原子取代,取代O原子的那个S原子与 形成配位键,结构
如图 或 。
【小问3详解】
“实验二”中淡黄色固体溶解生成了含硫酸根( )的化合物,化学反应方程式为
;硫难溶于水,因此加入乙醇,可增大硫在水中的溶解度;样品完
全溶解后,必须蒸馏除去乙醇,原因是:乙醇可能会被 氧化成乙酸,与KOH反应,干扰后续测定。
【小问4详解】
加入工业品硫实验数据中,第2组滴定后读数为48 mL,与第1组23.98 mL、第3组24.00 mL、第5组
24.02 mL偏差较大,应舍弃,差值计算中,第4组数据差值为24.22 mL,与其他组数据(第1组23.98
mL、第3组24.00 mL、第5组24.02 mL)偏差较大,应舍弃,所以应舍弃的是2、4;加入工业品硫实验
的有效数据为第1、3、5组, ,根据反应 ,
与硫反应的KOH的物质的量等于空白实验中HCl的物质的量减去样品实验中HCl的物质的量,即
,由
可知, ,则工业品硫的纯度为:
(32为硫的摩尔质量)。
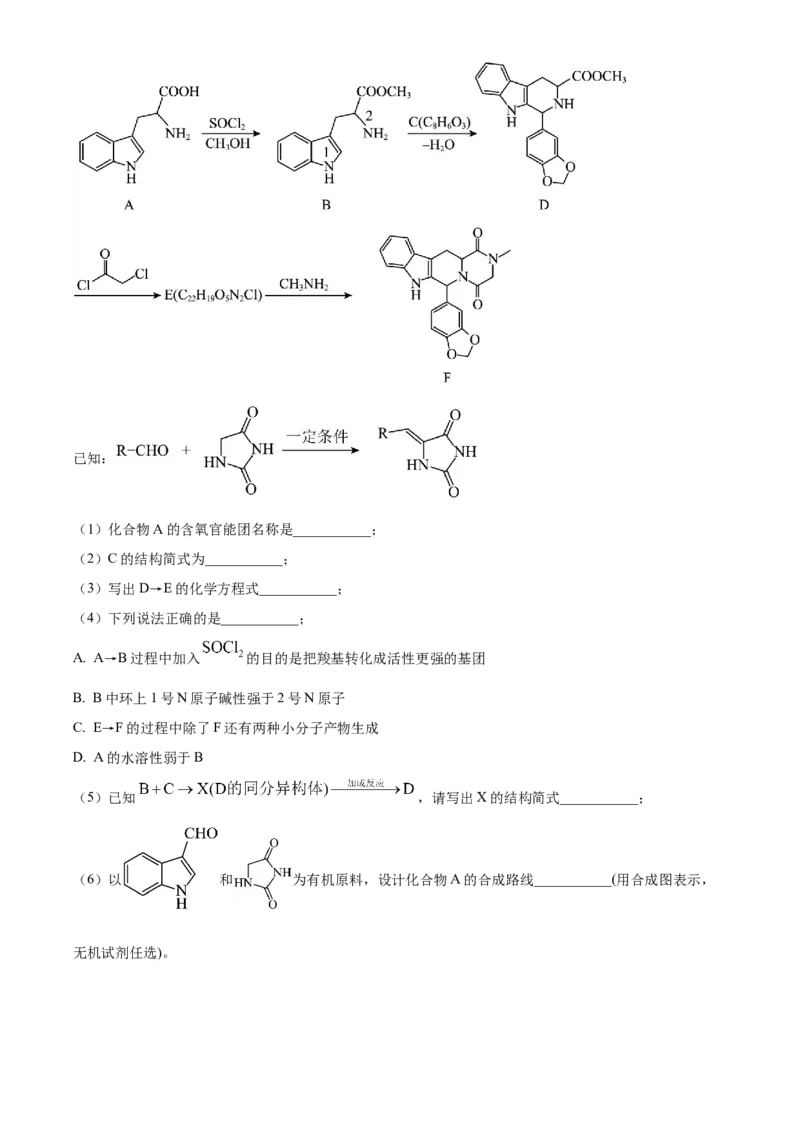
20. 他达拉非是一种已经上市的PDE5抑制剂,其常见的合成路线如下:已知:
(1)化合物A的含氧官能团名称是___________;
(2)C的结构简式为___________;
(3)写出D→E的化学方程式___________;
(4)下列说法正确的是___________;
A. A→B过程中加入 的目的是把羧基转化成活性更强的基团
B. B中环上1号N原子碱性强于2号N原子
C. E→F的过程中除了F还有两种小分子产物生成
D. A的水溶性弱于B
(5)已知 ,请写出X的结构简式___________;
(6)以 和 为有机原料,设计化合物A的合成路线___________(用合成图表示,
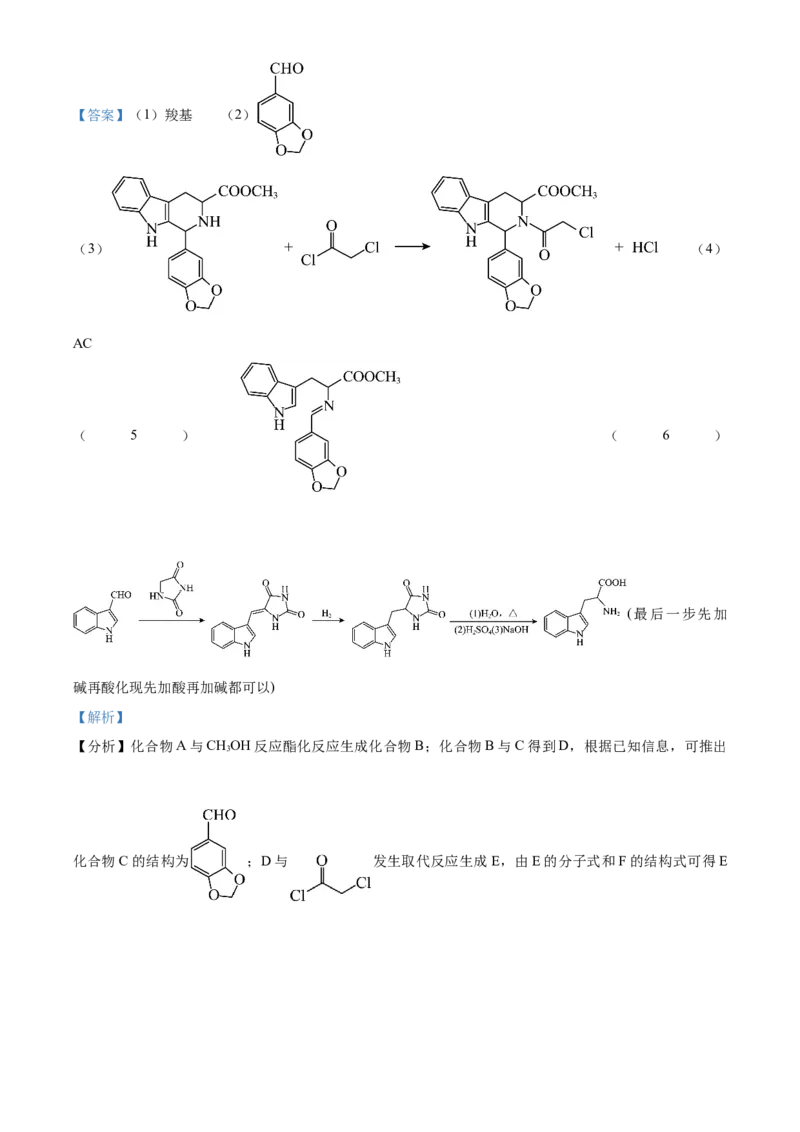
无机试剂任选)。【答案】(1)羧基 (2)
(3) (4)
AC
( 5 ) ( 6 )
(最后一步先加
碱再酸化现先加酸再加碱都可以)
【解析】
【分析】化合物A与CHOH反应酯化反应生成化合物B;化合物B与C得到D,根据已知信息,可推出
3
化合物C的结构为 ;D与 发生取代反应生成E,由E的分子式和F的结构式可得E为 ; 与CHNH 发生取代反应生成F,据此回答问题。
3 2
【小问1详解】
由化合物A的结构简式可知,其含氧官能团名称是羧基;
【小问2详解】
由分析可得,C的结构简式为 ;
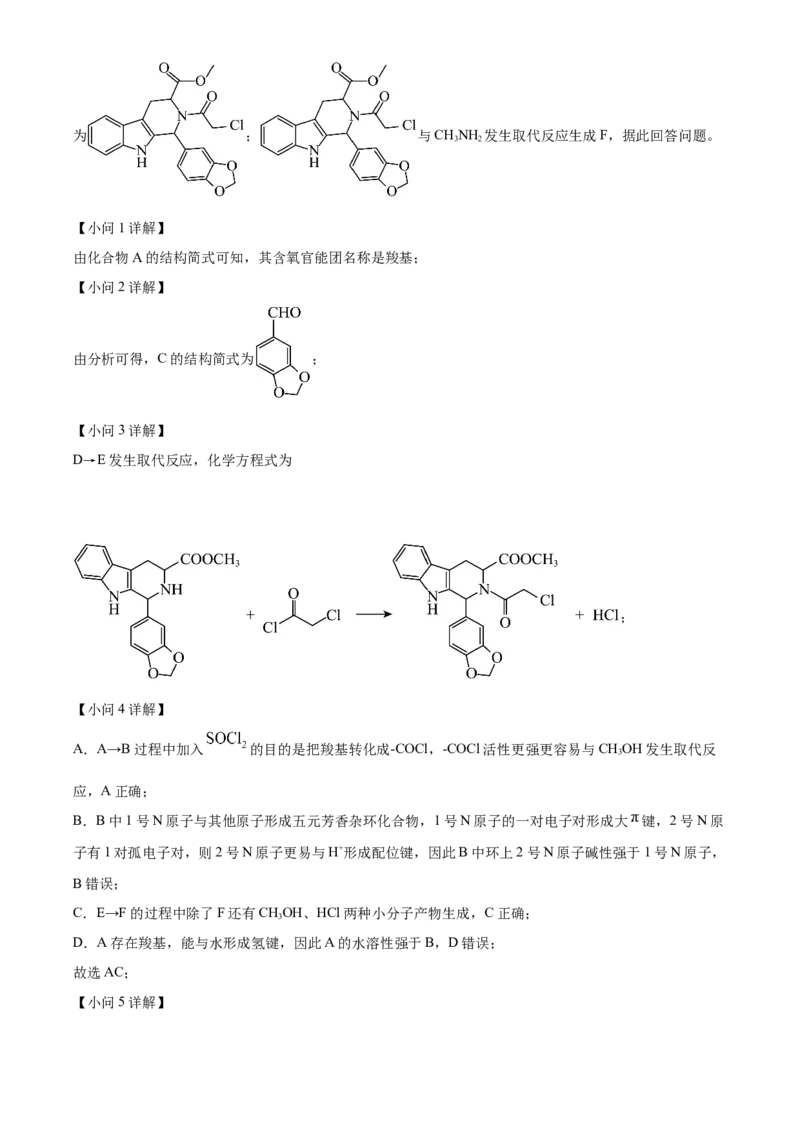
【小问3详解】
D→E发生取代反应,化学方程式为
;
【小问4详解】
A.A→B过程中加入 的目的是把羧基转化成-COCl,-COCl活性更强更容易与CHOH发生取代反
3
应,A正确;
B.B中1号N原子与其他原子形成五元芳香杂环化合物,1号N原子的一对电子对形成大 键,2号N原
子有1对孤电子对,则2号N原子更易与H+形成配位键,因此B中环上2号N原子碱性强于1号N原子,
B错误;
C.E→F的过程中除了F还有CHOH、HCl两种小分子产物生成,C正确;
3
D.A存在羧基,能与水形成氢键,因此A的水溶性强于B,D错误;
故选AC;
【小问5详解】B与 反应生成 , 成环生成
,则X的结构简式为 ;
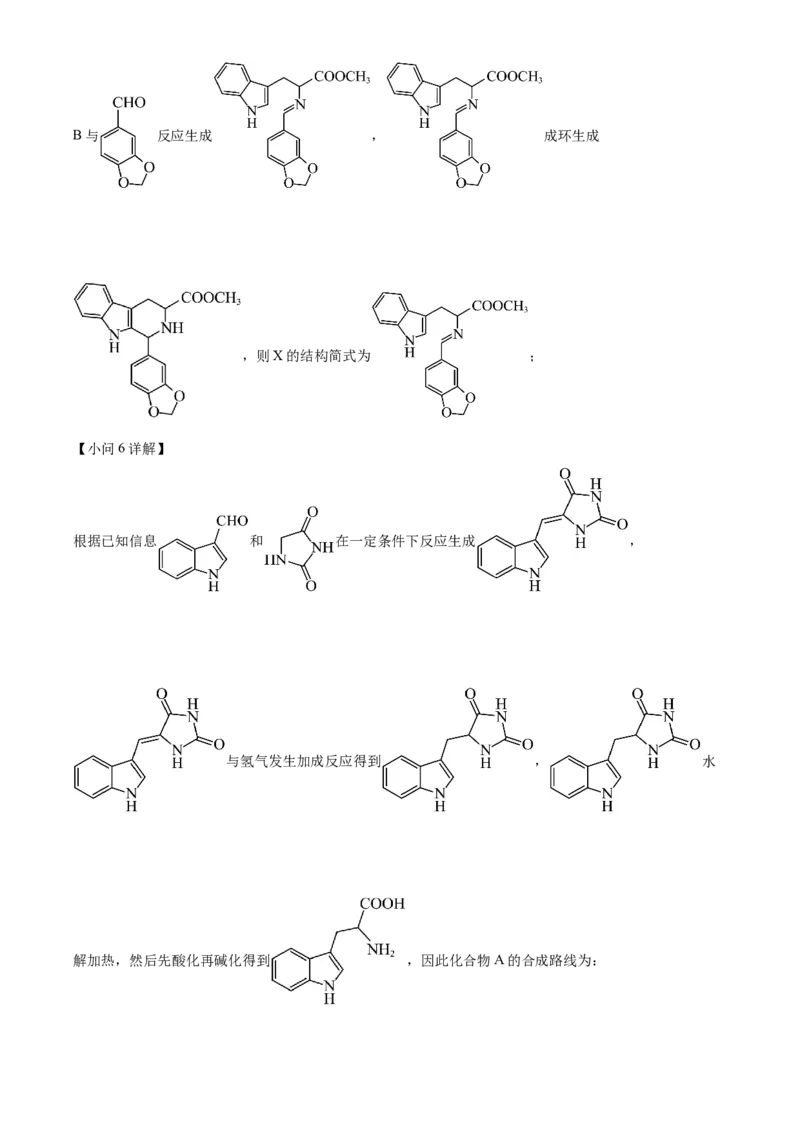
【小问6详解】
根据已知信息 和 在一定条件下反应生成 ,
与氢气发生加成反应得到 , 水
解加热,然后先酸化再碱化得到 ,因此化合物A的合成路线为: