文档内容
绝密★启用前
长沙大学附属中学高三 10 月月考化学
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑;如
需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题
卡上,写在试卷上无效。
3.考试结束后,本试卷和答题卡一并交回。
一、单选题:本大题共14小题,共42分。
1.下列各组中属于同位素的是
A. ❑ 40K与❑ 40Ca B. ❑ 35Cl 和❑ 37Cl
2 2
C. D与T D. O 和O
3 2
2.下列表示物质结构的化学用语正确的是
A. 镁离子的电子式:M g2+
B. HF的电子式:H:F
C. Cl−离子的结构示意图:
D. N H Cl的电子式:
4
3.下列说法正确的是( )
A. 铝具有较强抗腐蚀性能主要是因为铝耐酸碱腐蚀
B. 铝制容器可盛放冷的浓硝酸因为两者间不发生化学反应,发生钝化
C. 二氧化硅可用作太阳能电池的芯片
D. 复合材料由基体和增强体构成
4.关于硅及其化合物的叙述中,正确的是( )
A. 硅是良好的半导体材料,且是制造光缆的主要材料
B. SiO 不溶于水,也不溶于任何酸
2
高温
C. 可以用焦炭还原二氧化硅生产硅:SiO +C = Si+CO ↑
2 2
D. SiO 是酸性氧化物,在一定条件下能和氧化钙反应
2
5.取50mL稀硫酸与一定质量的镁、铝合金反应,合金全部溶解,向所得溶液中滴加
5mol⋅L−1NaOH溶液到过量,生成沉淀质量与加入NaOH溶液体积关系如图,则…
…
…
…
○
…
…
…
…
线
…
…
…
…
○
…
…
…
…
订
…
…
…
…
○
…
…
…
…
装
…
…
…
…
○
…
…
…
…
内
…
…
…
…
○
…
…
…
…
※※题※※答※※内※※线※※订※※装※※在※※要※※不※※请※※
…
…
…
…
○
…
…
…
…
线
…
…
…
…
○
…
…
…
…
订
…
…
…
…
○
…
…
…
…
装
…
…
…
…
○
…
…
…
…
外
…
…
…
…
○
…
…
…
…
( )
A. 原合金中铝质量为7.8g
B. 原合金的质量为19.4g
C. 原合金中镁的质量为4.8g
D. 硫酸的物质的量浓度为5mol⋅L−1
6.科技强国、科技强军,化学在现代化建设中起到了非常重要的作用。下列说法不正
确的是( )
A. “北斗三号”导航卫星搭载计时铷原子钟,铷是第ⅠA族元素
B. 量子通信材料螺旋碳纳米管与石墨烯互为同素异形体
C. 可控核聚变运行纪录的“人造太阳”,其原料中的❑ 2H与❑ 3H互为同位素
D. “雪龙2号”破冰船极地科考,破冰过程中水发生了化学变化
7.下列说法正确的是( )
A. 随着元素原子序数的递增,原子半径从小到大(稀有气体除外)发生周期性变化
B. 从Li→F、Na→Cl,元素的最高化合价均呈现从+1价→+7价的变化
C. 第三周期非金属元素含氧酸的酸性从左到右依次增强
D. 在二、三周期中,第ⅠA族元素金属性最强,第ⅦA族元素的非金属性最强
8.四种短周期元素X、Y、Z、W,已知X、Y的阳离子❑ Xn+ 、❑ Y(n+1)+ 电子层结
a b
构与Z、W的阴离子❑ Zm− 、❑ W(m+1)− 电子层结构相同。下列叙述正确的是( ) c d
A. 最高价氧化物对应水化物的碱性:X>Y
B. 离子半径和原子半径由大到小的顺序均为X>Y>Z>W
C. 最简单氢化物的稳定性是ZW(m+1)−,氧化性Xn+>Y(n+1)+
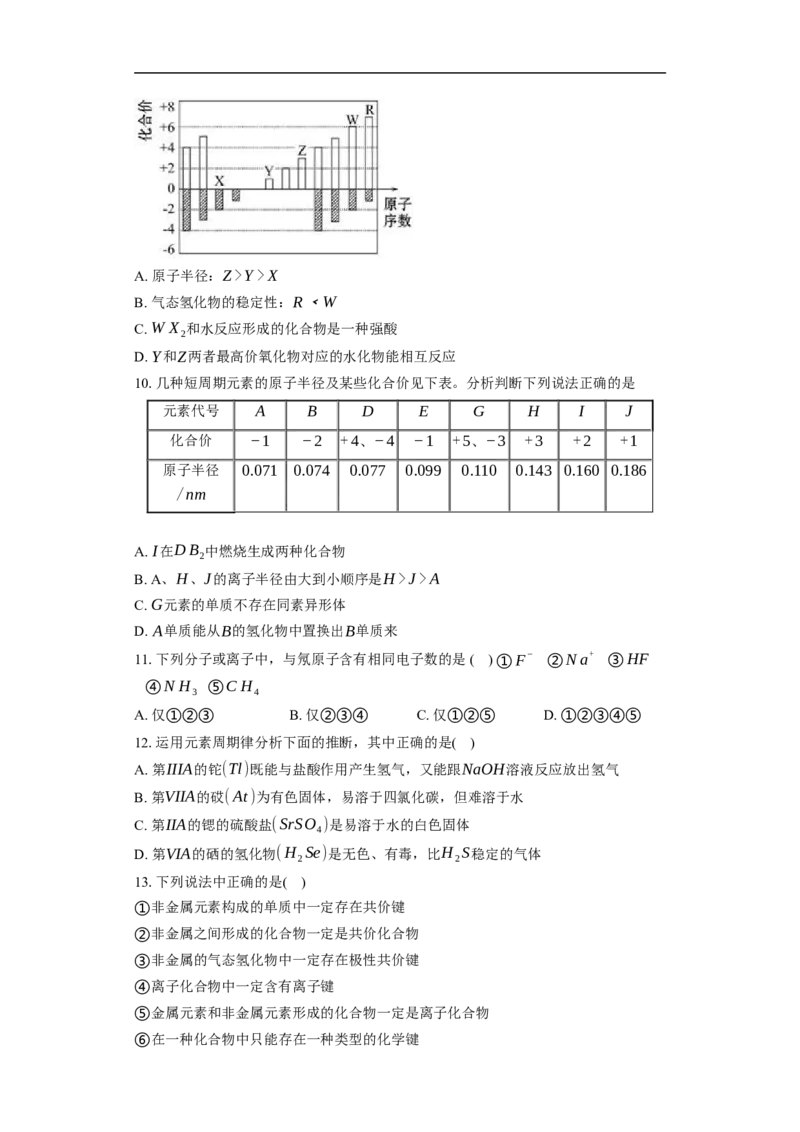
9.如图所示是部分短周期元素化合价与原子序数的关系图,下列说法正确的是 ( )
第 页,共 页
2 2…
…
…
…
○
…
…
…
…
线
…
…
…
…
○
…
…
…
…
订
…
…
…
…
○
…
…
…
…
装
…
…
…
…
○
…
…
…
…
内
…
…
…
…
○
…
…
…
…
※※题※※答※※内※※线※※订※※装※※在※※要※※不※※请※※
…
…
…
…
○
…
…
…
…
线
…
…
…
…
○
…
…
…
…
订
…
…
…
…
○
…
…
…
…
装
…
…
…
…
○
…
…
…
…
外
…
…
…
…
○
…
…
…
…
A. 原子半径:Z>Y>X
B. 气态氢化物的稳定性:R﹤W
C. W X 和水反应形成的化合物是一种强酸
2
D. Y和Z两者最高价氧化物对应的水化物能相互反应
10.几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是
元素代号 A B D E G H I J
化合价 −1 −2 +4、−4 −1 +5、−3 +3 +2 +1
原子半径 0.071 0.074 0.077 0.099 0.110 0.143 0.160 0.186
/nm
A. I在DB 中燃烧生成两种化合物
2
B. A、H、J的离子半径由大到小顺序是H>J>A
C. G元素的单质不存在同素异形体
D. A单质能从B的氢化物中置换出B单质来
11.下列分子或离子中,与氖原子含有相同电子数的是 ( ) ①F− ②Na+ ③HF
④N H ⑤CH
3 4
A. 仅①②③ B. 仅②③④ C. 仅①②⑤ D. ①②③④⑤
12.运用元素周期律分析下面的推断,其中正确的是( )
A. 第IIIA的铊(Tl)既能与盐酸作用产生氢气,又能跟NaOH溶液反应放出氢气
B. 第VIIA的砹(At)为有色固体,易溶于四氯化碳,但难溶于水
C. 第IIA的锶的硫酸盐(SrSO )是易溶于水的白色固体
4
D. 第VIA的硒的氢化物(H Se)是无色、有毒,比H S稳定的气体
2 2
13.下列说法中正确的是( )
①非金属元素构成的单质中一定存在共价键
②非金属之间形成的化合物一定是共价化合物
③非金属的气态氢化物中一定存在极性共价键
④离子化合物中一定含有离子键
⑤金属元素和非金属元素形成的化合物一定是离子化合物
⑥在一种化合物中只能存在一种类型的化学键…
…
…
…
○
…
…
…
…
线
…
…
…
…
○
…
…
…
…
订
…
…
…
…
○
…
…
…
…
装
…
…
…
…
○
…
…
…
…
内
…
…
…
…
○
…
…
…
…
※※题※※答※※内※※线※※订※※装※※在※※要※※不※※请※※
…
…
…
…
○
…
…
…
…
线
…
…
…
…
○
…
…
…
…
订
…
…
…
…
○
…
…
…
…
装
…
…
…
…
○
…
…
…
…
外
…
…
…
…
○
…
…
…
…
⑦含有共价键的化合物不一定是共价化合物
⑧含离子键的化合物一定是离子化合物
⑨氯化钠和HCl溶于水都发生电离,克服粒子间作用力的类型相同
A. ③④⑦⑧ B. ①③④⑦⑧ C. ②⑤⑥⑧⑨ D. ①④⑦⑨
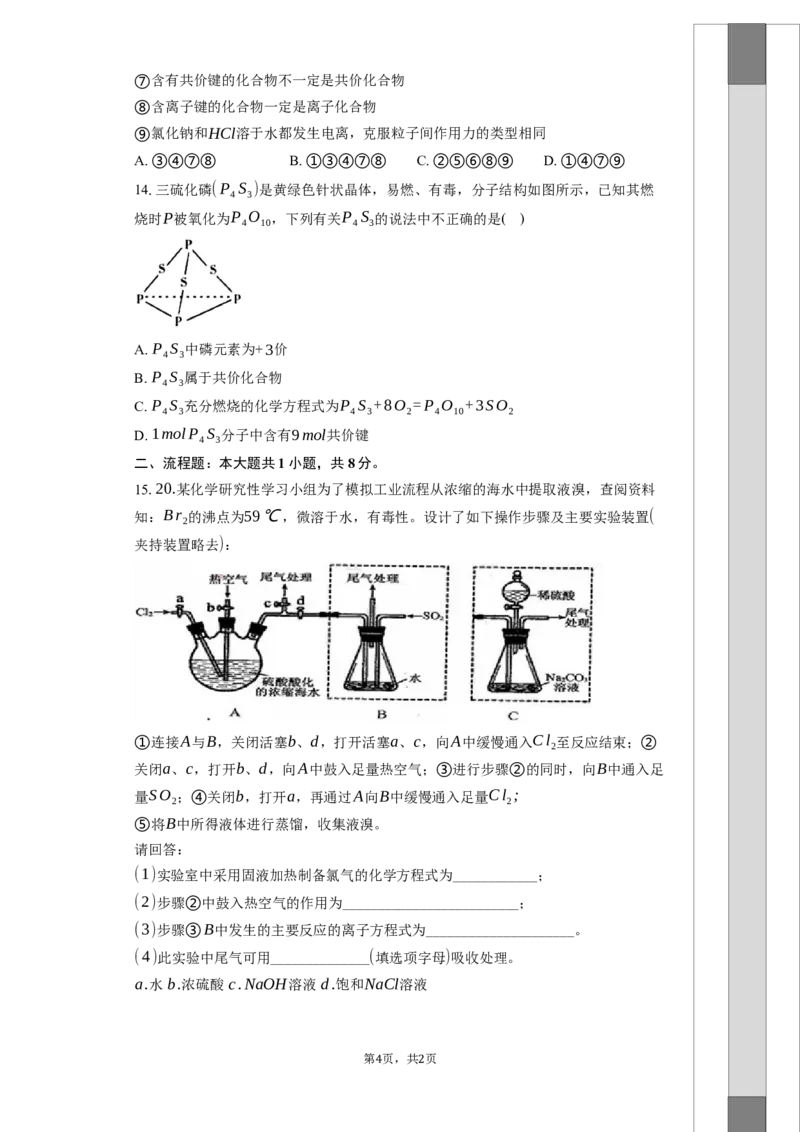
14.三硫化磷(P S )是黄绿色针状晶体,易燃、有毒,分子结构如图所示,已知其燃
4 3
烧时P被氧化为P O ,下列有关P S 的说法中不正确的是( )
4 10 4 3
A. P S 中磷元素为+3价
4 3
B. P S 属于共价化合物
4 3
C. P S 充分燃烧的化学方程式为P S +8O =P O +3SO
4 3 4 3 2 4 10 2
D. 1molP S 分子中含有9mol共价键
4 3
二、流程题:本大题共1小题,共8分。
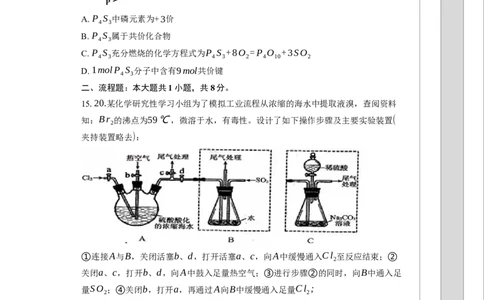
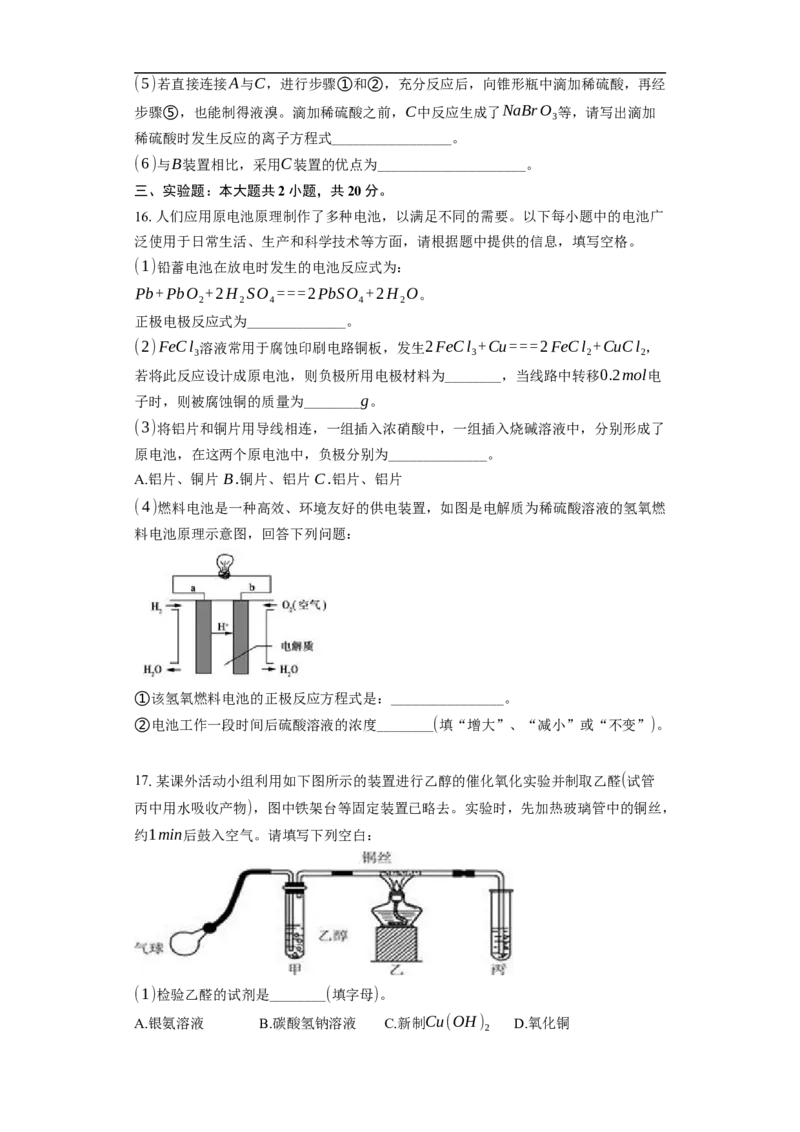
15.20.某化学研究性学习小组为了模拟工业流程从浓缩的海水中提取液溴,查阅资料
知:Br 的沸点为59℃,微溶于水,有毒性。设计了如下操作步骤及主要实验装置(
2
夹持装置略去):
①连接A与B,关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl 至反应结束;②
2
关闭a、c,打开b、d,向A中鼓入足量热空气;③进行步骤②的同时,向B中通入足
量SO ;④关闭b,打开a,再通过A向B中缓慢通入足量Cl ;
2 2
⑤将B中所得液体进行蒸馏,收集液溴。
请回答:
(1)实验室中采用固液加热制备氯气的化学方程式为____________;
(2)步骤②中鼓入热空气的作用为_________________________;
(3)步骤③B中发生的主要反应的离子方程式为_____________________。
(4)此实验中尾气可用______________(填选项字母)吸收处理。
a.水 b.浓硫酸 c.NaOH溶液 d.饱和NaCl溶液
第 页,共 页
4 2…
…
…
…
○
…
…
…
…
线
…
…
…
…
○
…
…
…
…
订
…
…
…
…
○
…
…
…
…
装
…
…
…
…
○
…
…
…
…
内
…
…
…
…
○
…
…
…
…
※※题※※答※※内※※线※※订※※装※※在※※要※※不※※请※※
…
…
…
…
○
…
…
…
…
线
…
…
…
…
○
…
…
…
…
订
…
…
…
…
○
…
…
…
…
装
…
…
…
…
○
…
…
…
…
外
…
…
…
…
○
…
…
…
…
(5)若直接连接A与C,进行步骤①和②,充分反应后,向锥形瓶中滴加稀硫酸,再经
步骤⑤,也能制得液溴。滴加稀硫酸之前,C中反应生成了NaBrO 等,请写出滴加
3
稀硫酸时发生反应的离子方程式_________________。
(6)与B装置相比,采用C装置的优点为_____________________。
三、实验题:本大题共2小题,共20分。
16.人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广
泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为:
Pb+PbO +2H SO ===2PbSO +2H O。
2 2 4 4 2
正极电极反应式为______________。
(2)FeCl 溶液常用于腐蚀印刷电路铜板,发生2FeCl +Cu===2FeCl +CuCl ,
3 3 2 2
若将此反应设计成原电池,则负极所用电极材料为________,当线路中转移0.2mol电
子时,则被腐蚀铜的质量为________g。
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了
原电池,在这两个原电池中,负极分别为______________。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃
料电池原理示意图,回答下列问题:
①该氢氧燃料电池的正极反应方程式是:________________。
②电池工作一段时间后硫酸溶液的浓度________(填“增大”、“减小”或“不变”)。
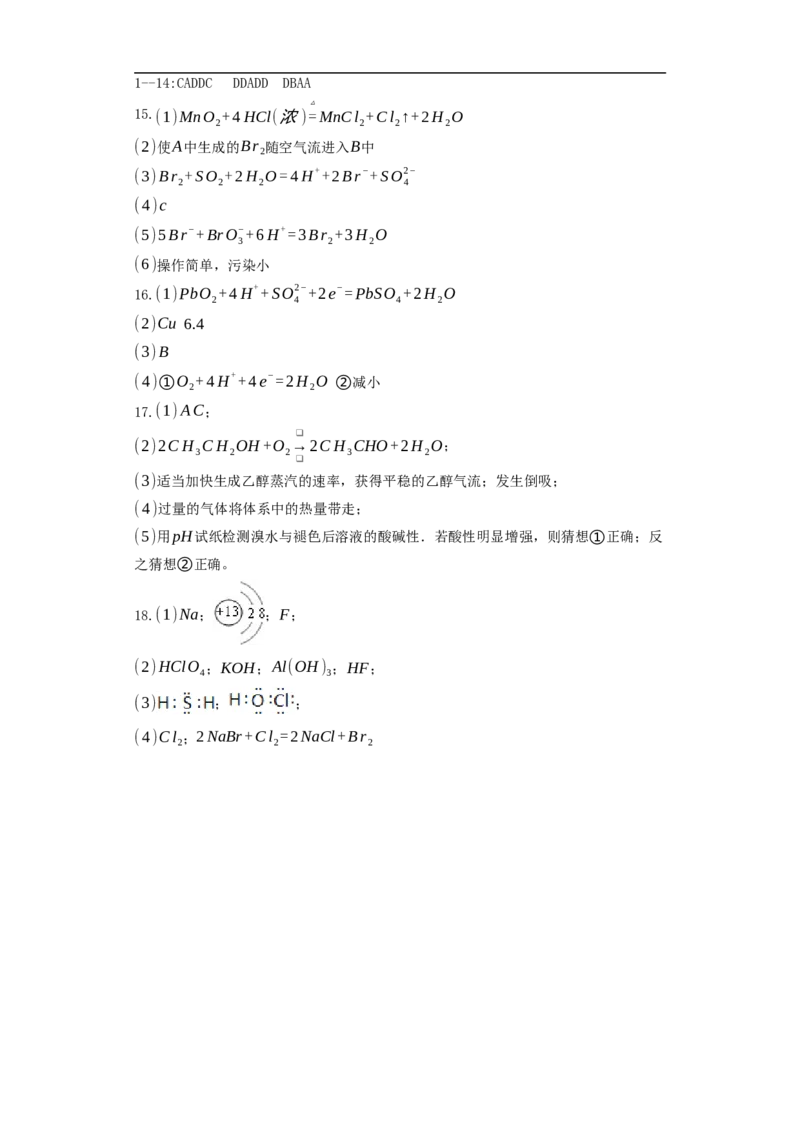
17.某课外活动小组利用如下图所示的装置进行乙醇的催化氧化实验并制取乙醛(试管
丙中用水吸收产物),图中铁架台等固定装置已略去。实验时,先加热玻璃管中的铜丝,
约1min后鼓入空气。请填写下列空白:
(1)检验乙醛的试剂是________(填字母)。
A.银氨溶液 B.碳酸氢钠溶液 C.新制Cu(OH) D.氧化铜
2…
…
…
…
○
…
…
…
…
线
…
…
…
…
○
…
…
…
…
订
…
…
…
…
○
…
…
…
…
装
…
…
…
…
○
…
…
…
…
内
…
…
…
…
○
…
…
…
…
※※题※※答※※内※※线※※订※※装※※在※※要※※不※※请※※
…
…
…
…
○
…
…
…
…
线
…
…
…
…
○
…
…
…
…
订
…
…
…
…
○
…
…
…
…
装
…
…
…
…
○
…
…
…
…
外
…
…
…
…
○
…
…
…
…
(2)乙醇发生催化氧化反应的化学方程式为:____________________________。
(3)实验时,常常将甲装置浸在70~80℃的水浴中,目的是
_______________________,由于装置设计上的缺陷,实验进行时可能会
_____________________。
(4)反应发生后,移去酒精灯,利用反应自身放出的热量可维持反 应继续进行。试解
释鼓气速度过快,反应体系温度反而下降的原因________________。
(5)该课外活动小组偶然发现向溴水中加入乙醛溶液,溴水褪色。该同学为解释上述现
象,提出两种猜想:①溴水将乙醛氧化为乙酸;②溴水与乙醛发生加成反应。请你设
计一个简单的实验,探究哪一种猜想正确?_______________________________。
四、简答题:本大题共1小题,共8分。
18.如表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式等
化学用语填空回答以下问题:
主族
IA IIA IIIA IVA VA VIA VIIA 0
周期
二 ① ②
三 ③ ④ ⑤ ⑥ ⑦ ⑧
四 ⑨ ⑩
(1) 在③~⑦中元素,原子半径最大的是 ______ ,⑤其离子的结构示意图为
______ ,非金属性最强的是 ______ .
(2)①~⑩中元素的最高价氧化物对应的水化物中酸性最强的是 ______ ,碱性最强
的是 ______ ,呈两性的氢氧化物是 ______ ;氢化物最稳定的是 ______ .
(3)按要求写出下列两种物质的电子式:⑥的氢化物 ______ ;含有化合价为+1价的
⑦的具有漂白性的一种含氧酸 ______ ;
(4)在⑦与⑩对应的两种单质中,化学性质较活泼的是 ______ ,可用什么化学反应证
明明该事实(写出反应的化学方程式): ______ .
参考答案:
第 页,共 页
6 2…
…
…
…
○
…
…
…
…
线
…
…
…
…
○
…
…
…
…
订
…
…
…
…
○
…
…
…
…
装
…
…
…
…
○
…
…
…
…
内
…
…
…
…
○
…
…
…
…
※※题※※答※※内※※线※※订※※装※※在※※要※※不※※请※※
…
…
…
…
○
…
…
…
…
线
…
…
…
…
○
…
…
…
…
订
…
…
…
…
○
…
…
…
…
装
…
…
…
…
○
…
…
…
…
外
…
…
…
…
○
…
…
…
…
1--14:CADDC DDADD DBAA
△
15. (1)MnO +4HCl(浓)=MnCl +Cl ↑+2H O
2 2 2 2
(2)使A中生成的Br 随空气流进入B中
2
(3)Br +SO +2H O=4H++2Br−+SO2−
2 2 2 4
(4)c
(5)5Br−+BrO−+6H+=3Br +3H O
3 2 2
(6)操作简单,污染小
16.(1)PbO +4H++SO2−+2e−=PbSO +2H O
2 4 4 2
(2)Cu 6.4
(3)B
(4)①O +4H++4e−=2H O ②减小
2 2
17.(1)AC;
❑
(2)2CH CH OH+O →2CH CHO+2H O;
3 2 2 3 2
❑
(3)适当加快生成乙醇蒸汽的速率,获得平稳的乙醇气流;发生倒吸;
(4)过量的气体将体系中的热量带走;
(5)用pH试纸检测溴水与褪色后溶液的酸碱性.若酸性明显增强,则猜想①正确;反
之猜想②正确。
18.(1)Na; ;F;
(2)HClO ;KOH;Al(OH) ;HF;
4 3
(3) ; ;
(4)Cl ;2NaBr+Cl =2NaCl+Br
2 2 2