文档内容
专题43 热化学反应方程式书写
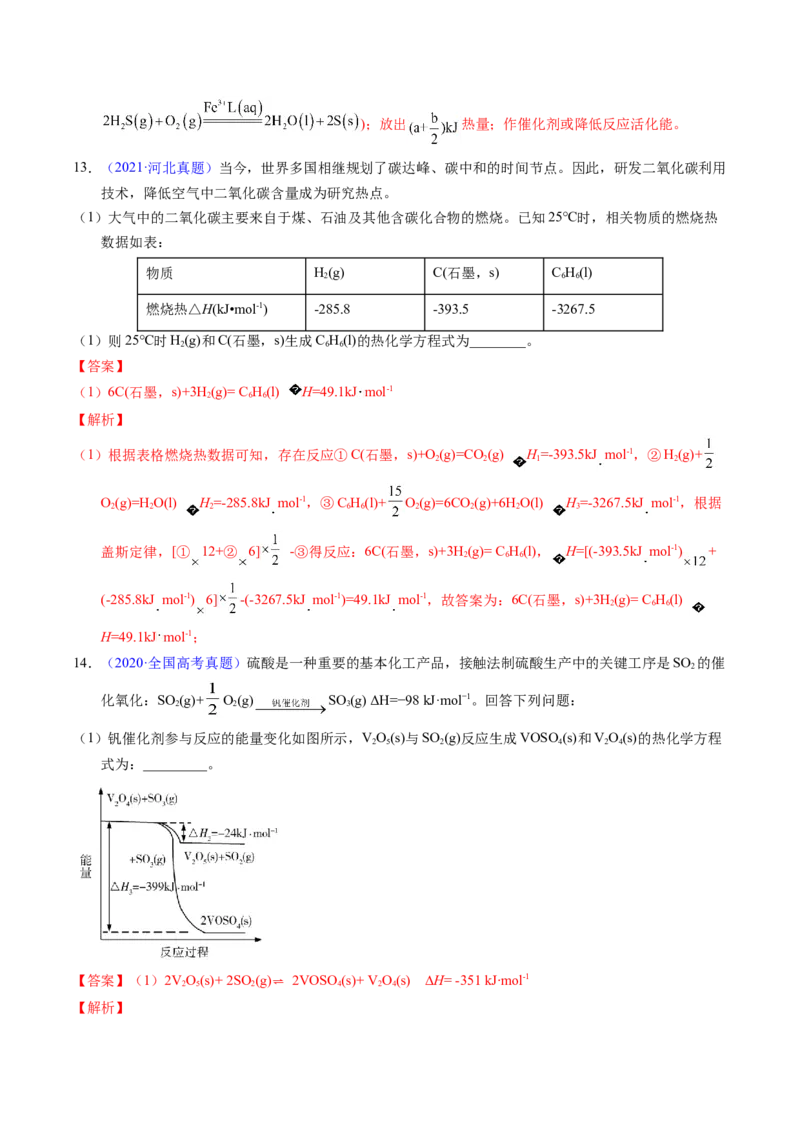
1.(2017·浙江高考真题)根据能量变化示意图,下列热化学方程式正确的是( )
A.N(g)+3H(g)=2NH (g) ΔH=-(b-a)kJ/mol
2 2 3
B.N(g)+3H(g)=2NH (g) ΔH=-(a-b)kJ/mol
2 2 3
C.2NH (l)=N (g)+3H(g) ΔH=2(b+c-a)kJ/mol
3 2 2
D.2NH (l)=N (g)+3H(g) ΔH=2(a+b-c)kJ/mol
3 2 2
【答案】C
【解析】焓变等于反应物断裂化学键吸收的能量减去形成化学键释放的能量,由图可知, N(g)+
2
H(g)=NH (g) △H=(a-b)kJ•mol-1, N(g)+ H(g)=NH (l) △H=(a-b-c)kJ•mol-1,据此分析判断。A.
2 3 2 2 3
N(g)+ H(g)=NH (g) △H=(a-b)kJ•mol-1,则N(g)+3H(g)=2NH (g) △H=-2(b-a)kJ•mol-1,错误;
2 2 3 2 2 3
B. N(g)+ H(g)=NH (g) △H=(a-b)kJ•mol-1,则N(g)+3H(g)=2NH (g)△H═-2(b-a)kJ•mol-1,错误;
2 2 3 2 2 3
C. N(g)+ H(g)=NH (l) △H=(a-b-c)kJ•mol-1,则N(g)+3H(g)=2NH (l) △H=2(a-b-c)kJ•mol-1,则
2 2 3 2 2 3
2NH (1)=N (g)+3H(g)△H=2(b+c-a)kJ•mol-1,正确;D. N(g)+ H(g)=NH (l) △H=(a-b-
3 2 2 2 2 3
c)kJ•mol-1,则N(g)+3H(g)=2NH (l) △H=2(a-b-c)kJ•mol-1,则2NH (1)=N (g)+3H(g)△H=2(b+c-
2 2 3 3 2 2
a)kJ•mol-1,错误;故选C。
2.(2014·海南高考真题)标准状态下,气态分子断开1 mol化学键的焓变称为键焓。已知H—H、H—O
和O=O键的键焓ΔH分别为436 kJ·mol-1、463 kJ·mol-1和495 kJ·mol-1。下列热化学方程式正确的是
A.HO(g)==H +1/2O (g)ΔH=-485 kJ·mol-1
2 2 2B.HO(g)==H (g)+1/2O (g) ΔH=+485 kJ·mol-1
2 2 2
C.2H(g)+O(g)==2H O(g) ΔH=+485 kJ·mol-1
2 2 2
D.2H(g)+O(g)==2H O(g) ΔH=-485 kJ·mol-1
2 2 2
【答案】D
【解析】化学反应的实质是旧化学键的断裂和新化学键的形成过程,断裂化学键需要吸收能量,形成化学
键需要释放能量,根据HO(g)=H (g)+1/2O (g),该反应的能量变化为2×463kJ/mol-436kJ/mol-
2 2 2
=+242.5kJ/mol,化学反应逆向进行,反应热数值不变,符号相反,化学方程式系数加倍,
反应热加倍,则2H(g)+O(g)=2HO(g) △H =-485kJ/mol,答案选D。
2 2 2
3.(2016·浙江高考真题)已知1 mol CH 气体完全燃烧生成气态CO 和液态HO,放出890.3 kJ热量,则
4 2 2
表示该反应的热化学方程式正确的是
A.CH(g)+2O(g)=CO(g)+2HO(g) ΔH=+890.3 kJ·molˉ1
4 2 2 2
B.CH(g)+2O(g)=CO(g)+2HO(l) ΔH=-890.3 kJ·molˉ1
4 2 2 2
C.CH(g)+2O(g)=CO(g)+2HO(l) ΔH=+890.3 kJ·molˉ1
4 2 2 2
D.CH(g)+2O(g)=CO(g)+2HO(g) ΔH=-890.3 kJ·molˉ1
4 2 2 2
【答案】B
【解析】1 mol CH 气体完全燃烧生成气态CO 和液态HO,放出890.3 kJ热量,表示该反应的热化学方程
4 2 2
式为CH(g)+2O(g)=CO(g)+2HO(l) ΔH=-890.3 kJ·mol-1,答案选B。
4 2 2 2
4.(2009·重庆高考真题)下列热化学方程式正确的是(注:△H的绝对值均正确)
A.C HOH(l)+3O (g)=2CO (g)+3HO(g);△H=-1367.0kJ/mol(燃烧热)
2 5 2 2 2
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H O(l);△H=-57.3kJ(中和热)
2
C.S(s)+O (g)=SO(g);△H=-269.8kJ/mol(反应热)
2 2
D.2NO =O +2NO;△H=+116.2kJ/mol(反应热)
2 2
【答案】C
【解析】A.燃烧热是25℃、101kPa时,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,此时的
水应为液体,因此反应热不是燃烧热,错误;B.△H的单位是kJ·mol-1,错误;C.符合书写热化学
反应方程式的要求,正确;D.没有写上状态,错误;答案:C。
5.(2009·四川高考真题)25 ℃,101 k Pa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3
kJ/mol,辛烷的燃烧热为5518 kJ/mol。下列热化学方程式书写正确的是( )
A.2H+(aq) + (aq)+Ba2+ (aq)+2OH (aq)=BaSO (s)+2HO(l);ΔH=-57.3 kJ/mol
4 2
B.KOH(aq)+ HSO (aq)= KSO (aq)+H O(l);ΔH=-57.3kJ/mol
2 4 2 4 2
C.C H (l)+ O(g)=8CO (g)+ 9H O(g);ΔH=-5518 kJ/mol
8 18 2 2 2
D.2C H (g)+25O(g)=16CO (g)+18HO(l);ΔH=-5518 kJ/mol
8 18 2 2 2
【答案】B【解析】中和热是强酸与强碱的稀溶液发生中和反应生成1mol水时放出的热量;燃烧热是1mol可燃物完
全反应生成稳定氧化物时放出的热量。A.反应热化学方程式中生成的是2mol水,不符合中和热的定
义,A错误;B.符合中和热的定义,B正确;C.反应热化学方程式中生成的水是气体,不是稳定氧
化物,不符合燃烧热的定义,C错误;D.热化学方程式中不是1mol可燃物的燃烧,不符合燃烧热的
定义,D错误;故合理选项为B。
6.(2008·重庆高考真题)N 和H 合成NH 的能量变化如图所示,该反应的热化学方程式是( )
2 2 3
A.N(g)+3H(g)=2NH (l) △H=2(a-b-c)kJ/mol
2 2 3
B.N(g)+3H(g)=2NH (g) △H=2(b-a)kJ/mol
2 2 3
C.1/2 N (g)+3/2H (g)=NH (l) △H=(b+c-a)kJ/mol
2 2 3
D.1/2 N (g)+3/2H (g)=NH (g) △H=(a+b)kJ/mol
2 2 3
【答案】A
【解析】根据图像, molN (g)+ molH (g)的能量比1molNH (g)的能量大(b-a)kJ,因此 N(g)+
2 2 3 2
H(g)=NH (g) △H=(a-b)kJ/mol,而1mol的NH (g)转化为1mol的NH (l)放出的热量为ckJ,所以有:
2 3 3 3
N(g)+ H(g)=NH (l) △H=(a-b-c)kJ/mol,即:N(g)+3H(g)=2NH (1) △H=2(a-b-c)kJ•mol-1,故
2 2 3 2 2 3
选A。
7.(2007·全国高考真题)已知:①1 mol H 分子中化学键断裂时需要吸收436kJ的能量
2
②1 mol Cl 分子中化学键断裂时需要吸收243kJ的能量
2
③由H原子和Cl原子形成1 mol HCl分子时释放431kJ的能量
下列叙述正确的是
A.氢气和氯气反应生成氯化氢气体的热化学方程式是H(g)+Cl(g)=2HCl(g)
2 2
B.氢气和氯气反应生成2 mol氯化氢气体,反应的△H=183kJ/mol
C.氢气和氯气反应生成2 mol氯化氢气体,反应的△H=-183kJ/mol
D.氢气和氯气反应生成1 mol氯化氢气体,反应的△H=-183kJ/mol
【答案】C
【解析】反应热就是断键吸收的能量和形成化学键所放出的能量的差值,因此生成2mol氯化氢的反应热
是436 kJ/mol+243 kJ/mol-2×431 kJ/mol=-183 kJ/mol,所以选项C正确,其余都是错误的,答案选
C。
8.(2017·江苏高考真题)通过以下反应可获得新型能源二甲醚(CHOCH )。下列说法不正确的是
3 3
①C(s) + H O(g)==CO(g) + H (g) ΔH = akJ·mol−1
2 2 1②CO(g) + H O(g)==CO (g) + H (g) ΔH = bkJ·mol−1
2 2 2 2
③CO (g) + 3H (g)==CH OH(g) + H O(g) ΔH = ckJ·mol−1
2 2 3 2 3
④2CHOH(g)==CHOCH (g) + H O(g) ΔH = dkJ·mol−1
3 3 3 2 4
A.反应①、②为反应③提供原料气
B.反应③也是CO 资源化利用的方法之一
2
1 1 d
C.反应CHOH(g)== CHOCH (g) + HO(l)的ΔH = kJ·mol−1
3 2 3 3 2 2 2
D.反应2CO(g) + 4H (g)==CH OCH (g) + H O(g)的ΔH = ( 2b + 2c + d ) kJ·mol−1
2 3 3 2
【答案】C
【解析】A.反应①、②的生成物CO 和H 是反应③的反应物,A正确;B.反应③可将二氧化碳转化为
2 2
甲醇,变废为宝,B正确;C.4个反应中,水全是气态,没有给出水由气态变为液态的焓变,C错误;
D.根据盖斯定律可知把反应②③④三个反应按(②+③)×2+④可得该反应对应的焓变,D正确,答案
选C。
9.(2016·江苏高考真题)通过以下反应均可获取H。下列有关说法正确的是( )
2
①太阳光催化分解水制氢:2HO(l)=2H (g)+ O(g) ΔH=+571.6 kJ·mol-1
2 2 2 1
②焦炭与水反应制氢:C(s)+ HO(g)=CO(g)+ H(g) ΔH=+131.3 kJ·mol-1
2 2 2
③甲烷与水反应制氢:CH(g)+ HO(g)=CO(g)+3H(g) ΔH=+206.1 kJ·mol-1
4 2 2 3
A.反应①中电能转化为化学能
B.反应②为放热反应
C.反应③使用催化剂,ΔH 减小
3
D.反应CH(g)=C(s)+2H(g)的ΔH=+74.8 kJ·mol-1
4 2
【答案】D
【解析】A.反应①中,太阳光催化分解水制氢,由光能转化为化学能,A不正确;B.反应②中,
ΔH>0,为吸热反应,B不正确;C.反应③中,使用催化剂,对ΔH 不产生影响,C不正确;D.应
2 3
用盖斯定律,将反应③-反应②得,反应CH(g)=C(s)+2H(g)的ΔH=+74.8 kJ·mol-1,D正确;答案
4 2
选D。
10.【2022年河北卷】氢能是极具发展潜力的清洁能源,以氢燃料为代表的燃料电池有良好的应用前景。
(1) 时, 燃烧生成 )放热 , 蒸发吸热 ,表示 燃烧热的热化学方
程式为_______。
【答案】(1)H(g)+ O (g)=HO(1) △H= -286 kJ•mol-1
2 2 2
【解析】
(1)298K时,1gH 燃烧生成HO(g)放热121 kJ,1 mol H O(1)蒸发吸热44kJ,则1mol H 燃烧生成1
2 2 2 2
mol HO(1) 放热286kJ,表示H 燃烧热的热化学方程式为:H(g)+ O (g)=HO(1) △H= -286
2 2 2 2 2
kJ•mol-1;
11.【2022年福建卷】异丙醇 可由生物质转化得到,催化异丙醇脱水制取高值化学品丙烯的工业化技术已引起人们的关注,其主要反应如下:
Ⅰ.
Ⅱ.
回答下列问题:
(1)已知 ,则 燃烧生成 和
的热化学方程式为_______。
【答案】(1)
【解析】(1)设Ⅲ ,根据盖斯定律Ⅲ-2×Ⅰ
得 。
12.【2022年天津卷】天津地处环渤海湾,海水资源丰富。科研人员把铁的配合物 (L为配体)溶于弱
碱性的海水中,制成吸收液,将气体 转化为单质硫,改进了湿法脱硫工艺。该工艺包含两个阶段:
① 的吸收氧化;② 的再生。反应原理如下:
①
②
回答下列问题:
(1)该工艺的总反应方程式为___________。1mol 发生该反应的热量变化为___________,
在总反应中的作用是___________。
【答案】(1) (或 ) 放
出 热量 作催化剂或降低反应活化能
【解析】(1)将第一个方程式2倍加上第二个方程式得到该工艺的总反应方程式为
(或 ),该反应的热化学方程式
,因此1mol 发生该反应的热
量变化为放出 热量, 参与了化学反应,但反应前后量没有改变,因此 在总反应中
的作用是作催化剂或降低反应活化能;故答案为: (或);放出 热量;作催化剂或降低反应活化能。
13.(2021·河北真题)当今,世界多国相继规划了碳达峰、碳中和的时间节点。因此,研发二氧化碳利用
技术,降低空气中二氧化碳含量成为研究热点。
(1)大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧。已知25℃时,相关物质的燃烧热
数据如表:
物质 H(g) C(石墨,s) C H(l)
2 6 6
燃烧热△H(kJ•mol-1) -285.8 -393.5 -3267.5
(1)则25℃时H(g)和C(石墨,s)生成C H(l)的热化学方程式为________。
2 6 6
【答案】
(1)6C(石墨,s)+3H(g)= C H(l) H=49.1kJ mol-1
2 6 6
【解析】
(1)根据表格燃烧热数据可知,存在反应①C(石墨,s)+O(g)=CO (g) H=-393.5kJ mol-1,②H(g)+
2 2 1 2
O(g)=HO(l) H=-285.8kJ mol-1,③C H(l)+ O(g)=6CO (g)+6HO(l) H=-3267.5kJ mol-1,根据
2 2 2 6 6 2 2 2 3
盖斯定律,[① 12+② 6] -③得反应:6C(石墨,s)+3H(g)= C H(l), H=[(-393.5kJ mol-1) +
2 6 6
(-285.8kJ mol-1) 6] -(-3267.5kJ mol-1)=49.1kJ mol-1,故答案为:6C(石墨,s)+3H(g)= C H(l)
2 6 6
H=49.1kJ mol-1;
14.(2020·全国高考真题)硫酸是一种重要的基本化工产品,接触法制硫酸生产中的关键工序是SO 的催
2
化氧化:SO (g)+ O(g) SO (g) ΔH=−98 kJ·mol−1。回答下列问题:
2 2 3
(1)钒催化剂参与反应的能量变化如图所示,VO(s)与SO (g)反应生成VOSO(s)和VO(s)的热化学方程
2 5 2 4 2 4
式为:_________。
【答案】(1)2V
2
O
5
(s)+ 2SO
2
(g)⇌ 2VOSO
4
(s)+ V
2
O
4
(s) ∆H= -351 kJ∙mol-1
【解析】(1)由题中信息可知:
①SO
2
(g)+ O
2
(g)⇌SO
3
(g) ∆H= -98kJ∙mol-1
②V
2
O
4
(s)+ SO
3
(g)⇌V
2
O
5
(s)+ SO
2
(g) ∆H
2
= -24kJ∙mol-1
③V
2
O
4
(s)+ 2SO
3
(g)⇌2VOSO
4
(s) ∆H
1
= -399kJ∙mol-1
根据盖斯定律可知,③-②2得2V
2
O
5
(s)+ 2SO
2
(g)⇌ 2VOSO
4
(s)+ V
2
O
4
(s),则∆H= ∆H
1
-
2∆H=( -399kJ∙mol-1)-( -24kJ∙mol-1)2= -351kJ∙mol-1,所以该反应的热化学方程式为:2VO(s)+
2 2 5
2SO
2
(g)⇌ 2VOSO
4
(s)+ V
2
O
4
(s) ∆H= -351 kJ∙mol-1;
15.(2016·四川高考真题)资源的高效利用对保护环境、促进经济持续健康发展具有重要作用。磷尾矿主
要含Ca (PO )F和CaCO ·MgCO 。某研究小组提出了磷尾矿综合利用的研究方案,制备具有重要工业
5 4 3 3 3
用途的CaCO 、Mg(OH) 、P 和H,其简化流程如下:
3 2 4 2
已知:①Ca (PO )F在950℃不分解;
5 4 3
②4Ca (PO )F+18SiO +30C 2CaF +30CO+18CaSiO +3P
5 4 3 2 2 3 4
请回答下列问题:
(5)工业上常用磷精矿[Ca (PO )F]和硫酸反应制备磷酸。已知25℃,101kPa时:
5 4 3
CaO(s)+H SO (l)=CaSO (s)+HO(l) ΔH=-271kJ/mol
2 4 4 2
5 CaO(s)+3H PO (l)+HF(g)= Ca (PO )F (s)+5HO(l) ΔH=-937kJ/mol
3 4 5 4 3 2
则Ca (PO )F和硫酸反应生成磷酸的热化学方程式是_________________。
5 4 3
【答案】
(5)Ca (PO )F (s)+ 5H SO (l)=5CaSO (s) +H PO (l)+HF(g) ΔH =-418kJ/mol
5 4 3 2 4 4 3 4
【解析】
(5)已知25℃,101kPa时:
①CaO(s)+H SO (l)=CaSO4(s)+H O(l) ΔH =-271kJ/mol
2 4 2
②5 CaO(s)+3H PO (l)+HF(g)= Ca (PO )F (s)+5HO(l) ΔH =-937kJ/mol
3 4 5 4 3 2
根据盖斯定律:①×5-②得Ca (PO )F和硫酸反应生成磷酸的热化学方程式是Ca (PO )F (s)+
5 4 3 5 4 3
5HSO (l)=5CaSO (s) +H PO (l)+HF(g) ΔH =-418kJ/mol 。
2 4 4 3 4
16.(2017·全国高考真题)[2017·新课标I]近期发现,HS是继NO、CO之后的第三个生命体系气体信号
2
分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。通过计算,可知系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式分别为______________、______________,
制得等量H 所需能量较少的是_____________。
2
【答案】(2) HO(l)=H(g)+ O(g) ΔH=+286 kJ/mol H S(g)=H(g)+S(s) ΔH=+20 kJ/mol
2 2 2 2 2
【解析】
(1)根据盖斯定律,把系统(Ⅰ)的三个热化学方程式相加可得:HO(l)=H(g)+ O(g) ΔH=286 kJ•mol-1;
2 2 2
把系统(Ⅱ)的三个热化学方程式相加可得:HS(g)=H(g)+S(s) ΔH=20 kJ•mol-1;由上述两个热化学方
2 2
程式可得,制得1mol H,系统(Ⅰ)需要吸收286kJ能量,系统(Ⅱ) 需要吸收20kJ能量,所以制得等量
2
H 所需能量较少的是系统(Ⅱ)。
2
17.(2008·全国高考真题)红磷P(s)和Cl(g)发生反应生成PCl (g)和PCl (g)。反应过程和能量关系如图所
2 3 5
示(图中的△H表示生成1mol产物的数据)。
根据上图回答下列问题:
(1)P和Cl 反应生成PCl 的热化学方程式_________________________________。
2 3
(2)PCl 分解成PCl 和Cl 的热化学方程式_________________________________,上述分解反应是一个
5 3 2
可逆反应,温度T 时,在密闭容器中加入0.80molPCl ,反应达到平衡时PCl 还剩0.60mol,其分解率
1 5 5
α 等于_________;若反应温度由T 升高到T,平衡时PCl 的分解率为α ,α _______α (填“大于”、
1 1 2 5 2 2 1
“小于”或“等于”)。【答案】(1)P(s)+Cl(g)=PCl (g) △H=-306kJ·mol-1 (2)PCl (g)=PCl (g)+Cl(g) △H=
2 3 5 3 2
+93kJ·mol-1 25% 大于
【解析】
(1)由图可以看出,1molP在Cl 中完全燃烧生成PCl 放出的热量为306kJ·mol-1,所以P与Cl 反应生成
2 3 2
PCl 的热化学反应方程式为P(s)+Cl(g)===PCl (g) △H=-306kJ·mol-1。
3 2 3
(2)中间产物PCl 和未完全反应的Cl 的总能量高于最终产物PCl 的能量,其△H=-93kJ·mol-1,所以
3 2 5
PCl (g)===PCl (g)+Cl(g) △H=+93kJ·mol-1;分解率α = ×100%=25%,由热化
5 3 2 1
学反应方程式可知,此反应的正反应为吸热反应,所以升高温度,平衡向正反应方向移动,PCl 的分
5
解率增大,即α 大于α 。
2 1
18.(2018·北京高考真题)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过
程如下:
(1)反应Ⅰ:2HSO (l)=2SO (g)+2HO(g)+O (g) ΔH=+551 kJ·mol-1
2 4 2 2 2 1
反应Ⅲ:S(s)+O (g)=SO(g) ΔH=-297 kJ·mol-1
2 2 3
反应Ⅱ的热化学方程式:_________________________________________。
【答案】(1)3SO (g)+2HO (g)=2H SO (l)+S(s) ΔH=−254 kJ·mol−1
2 2 2 4 2
【解析】
(1)根据过程,反应II为SO 催化歧化生成HSO 和S,反应为3SO +2H O=2HSO +S。应用盖斯定律,
2 2 4 2 2 2 4
反应I+反应III得,2HSO (l)+S(s)=3SO(g)+2H O(g)ΔH=ΔH+ΔH =(+551kJ/mol)+
2 4 2 2 1 3
(-297kJ/mol)=+254kJ/mol,反应II的热化学方程式为3SO (g)+2H O(g)=2H SO (l)+S(s)
2 2 2 4
ΔH=-254kJ/mol。
19.(2009·江苏高考真题)废旧印刷电路板的回收利用可实现资源再生,并减少污染。废旧印刷电路板经
粉碎分离,能得到非金属粉末和金属粉末。
(2)用HO 和HSO 的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
2 2 2 4
Cu(s)+2H+(aq)=Cu2+(aq)+H(g) △H=64.39kJ·mol-1
2
2HO(l)=2HO(l)+O(g) △H=-196.46kJ·mol-1
2 2 2 2
H(g)+1/2O (g)=HO(l) △H=-285.84kJ·mol-1
2 2 2
在HSO 溶液中Cu 与HO 反应生成Cu2+和HO的热化学方程式为:__________。
2 4 2 2 2
【答案】(2) Cu(s)+HO(l)+2H+(aq)=Cu2+(aq)+2HO(l) △H=-319.68kJ·mol-1
2 2 2
【解析】
(2)根据盖斯定律,将三个方程式加合得:
Cu(s)+HO(l)+2H+(aq)=Cu2+(aq)+2HO(l) △H=-319.68kJ·mol-1
2 2 220.(2019·天津高考真题)多晶硅是制作光伏电池的关键材料。以下是由粗硅制备多晶硅的简易过程。
回答下列问题:
Ⅰ.硅粉与 在300℃时反应生成 气体和 ,放出 热量,该反应的热化学方程式
为________________________。 的电子式为__________________。
【答案】
【解析】
I.参加反应的物质是固态的Si、气态的HCl,生成的是气态的SiHCl 和氢气,反应条件是300℃,配平后发
3
现SiHCl 的化学计量数恰好是1,由此可顺利写出该条件下的热化学方程式:Si(s)+3HCl(g)
3
SiHCl (g)+H(g) ∆H=-225kJ·mol-1;SiHCl 中硅与1个H、3个Cl分别形成共价单键,由此可写出其电
3 2 3
子式为: ,注意别漏标3个氯原子的孤电子对;
21.(2014·全国高考真题)化合物AX 和单质X 在一定条件下反应可生成化合物AX 。回答下列问题:
3 2 5
(1)已知AX 的熔点和沸点分别为-93.6 ℃和76 ℃,AX 的熔点为167 ℃。室温时AX 与气体X 反应
3 5 3 2
生成1 mol AX ,放出热量123.8 kJ。该反应的热化学方程式为_____________________________。
5
【答案】.(1)AX (l)+X(g)===AX (s) ΔH=-123.8 kJ/mol
3 2 5
【解析】
⑴据题意,先写出反应方程式并标出各物质的状态AX (l)+X(g) = AX (s),然后确定其反应热ΔH=-
3 2 5
123.8KJ·mol-1,综上便可写出完整的热化学方程式。
22.(2013·四川高考真题)明矾石经处理后得到明矾( KAl(SO )·12H O)。从明矾制备Al、KSO 和
4 2 2 2 4
HSO 的工艺过程如下所示:
2 4
焙烧明矾的化学方程式为:4KAl(SO )·12H O+3S=2KSO +2AlO+9SO+48H O
4 2 2 2 4 2 3 2 2请回答下列问题:
(5)焙烧产生的SO 可用于制硫酸。已知25℃、101 kPa时:
2
2SO (g) +O (g) 2SO (g) △H= 一197 kJ/mol;
2 2 3 1
2HO (g)=2HO(1) △H=一44 kJ/mol;
2 2 2
2SO (g)+O(g)+2HO(g)=2HSO (l) △H=一545 kJ/mol。
2 2 2 2 4 3
则SO (g)与HO(l)反应的热化学方程式是__________________________。
3 2
焙烧948t明矾(M=474 g/mol ),若SO 的利用率为96%,可生产质量分数为98%的硫酸________t。
2
【答案】(5) SO (g)+HO(l)=HSO (l)△H=-152kJ·mol-1 432
3 2 2 4
【解析】
(5)2SO
2
(g)+O
2
(g)⇌2SO
3
(g)△H
1
=-197kJ/mol; ①
2HO(g)=2H O(1)△H=-44kJ/mol; ②
2 2 2
2SO (g)+O (g)+2H O(g)=2H SO (l)△H=-545kJ/mol. ③
2 2 2 2 4 3
依据盖斯定律③-①-②得到:2SO (g)+2H O(l)=2H SO (l)△H=-304KJ/mol,
3 2 2 4
即反应的热化学方程式为:SO (g)+H O(l)=H SO (l)△H=-152KJ/mol;
3 2 2 4
948 t明矾生成SO 物质的量为4500mol 故生成硫酸的质量m=4500×0.96×98÷0.98=432000Kg=432t.
2
故答案为SO (g)+H O(l)=H SO (l)△H=-152 kJ/mol;432.
3 2 2 4