文档内容
微信公众号:【高中精品资料君】
2024 届明日之星高考化学精英模拟卷 【重庆版】
可能用到的相对原子质量:H-1、C-12、N-14、O-16、Na-23、S-32、K-39、Cu-64、Fe-56
一、 单项选择题:本题共 14 小题,每小题 3 分,共 42 分。在每小题给出的四个选项中,只
有一项是符合题目要求的。
1.2023年4月24日是第八个“中国航天日”,今年的主题是“格物致知,叩问苍穹”。下列有关
材料的叙述正确的是( )
A.铝合金广泛应用于航天飞船建造,铝合金比纯铝的硬度大、熔点低
B.返回舱表层材料中的碳纤维复合材料属于新型有机高分子材料
C.“天和”核心舱的霍尔发动机燃料氙气性质非常稳定,不与任何物质发生反应
D.宇航服使用了多种合成纤维,其中涤纶(聚对苯二甲酸乙二酯)是纯净物
2.下列生产过程中发生反应的离子方程式或电极反应式正确的是( )
A.胆矾溶液和石灰乳配制波尔多液:CuSO Ca(OH) Cu(OH) CaSO
4 2 2 4
B.氢氟酸和硅酸钠溶液反应产生气体:6HFSiO2 2F SiF 3H O
3 4 2
C.酸性高锰酸钾溶液测废气中SO 含量:3SO MnO 2H O 3SO2 Mn2 4H
2 2 4 2 4
D.对酸性废水中的NO进行电解脱氮:NO 10H 8e NH 3H O
3 3 4 2
3.下列有关物质性质说法正确的是( )
A.绚丽多彩的烟花主要利用了Na、K、Fe、Cu等金属元素的焰色
B.Li、Na、K是同族元素,化学性质相似,它们的单质和O 反应均可生成相应的氧化物和过
2
氧化物
C.苯酚具有一定的毒性,可用作外科消毒剂
D.可用蘸有浓氨水的玻璃棒检验氯气是否泄漏,该过程不涉及氧化还原反应
4.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.1molL1 FeCl 溶液中Fe3的数目小于N
3 A
B.足量锌和100mL18.4molL1硫酸充分反应,生成的气体分子数为0.92N
A
C.标准状况下,1.12LH 和1.12LF 完全反应,生成的气体体积为2.24 L
2 2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
D.7.8g Na S和Na O 混合物中含有的阴离子数目为0.1N
2 2 2 A
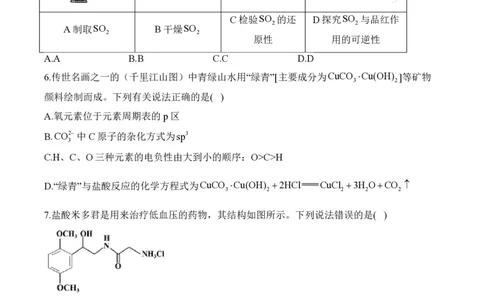
5.实验室制取SO 时,下列装置不能达到相应实验目的的是( )
2
C检验SO 的还 D探究SO 与品红作
2 2
A制取SO B干燥SO
2 2
原性 用的可逆性
A.A B.B C.C D.D
6.传世名画之一的(千里江山图)中青绿山水用“绿青”[主要成分为CuCO Cu(OH) ]等矿物
3 2
颜料绘制而成。下列有关说法正确的是( )
A.氧元素位于元素周期表的p区
B.CO2中C原子的杂化方式为sp3
3
C.H、C、O三种元素的电负性由大到小的顺序:O>C>H
D.“绿青”与盐酸反应的化学方程式为CuCO Cu(OH) 2HCl CuCl 3H OCO
3 2 2 2 2
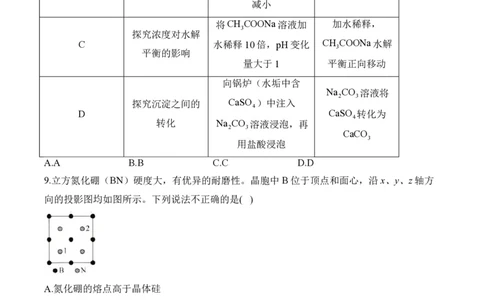
7.盐酸米多君是用来治疗低血压的药物,其结构如图所示。下列说法错误的是( )
A.该物质分子式为C H N O Cl
12 20 2 4
B.其水解产物之一可以发生缩聚反应
C.1mol该物质最多可以消耗2molNaOH
D.该物质可以发生加成、取代、氧化、还原反应
8.根据实验目的,下列实验现象及结论均正确的是( )
选项 实验目的 实验及现象 结论
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
在
2NO (g)‡ˆ ˆˆ†ˆ N O (g)
探究压强对化学 2 2 4
A 的平衡体系中,压缩容 平衡逆向移动
平衡的影响
积,混合气体的颜色变
深
向HR溶液中加入NaR
证明HR为弱电
B 固体,测得溶液的pH HR是弱电解质
解质
减小
将CH COONa溶液加 加水稀释,
3
探究浓度对水解
C 水稀释 10倍,pH变化 CH COONa水解
3
平衡的影响
量大于1 平衡正向移动
向锅炉(水垢中含
Na CO 溶液将
2 3
探究沉淀之间的 CaSO )中注入
4
D CaSO 转化为
4
转化 Na CO 溶液浸泡,再
2 3
CaCO
3
用盐酸浸泡
A.A B.B C.C D.D
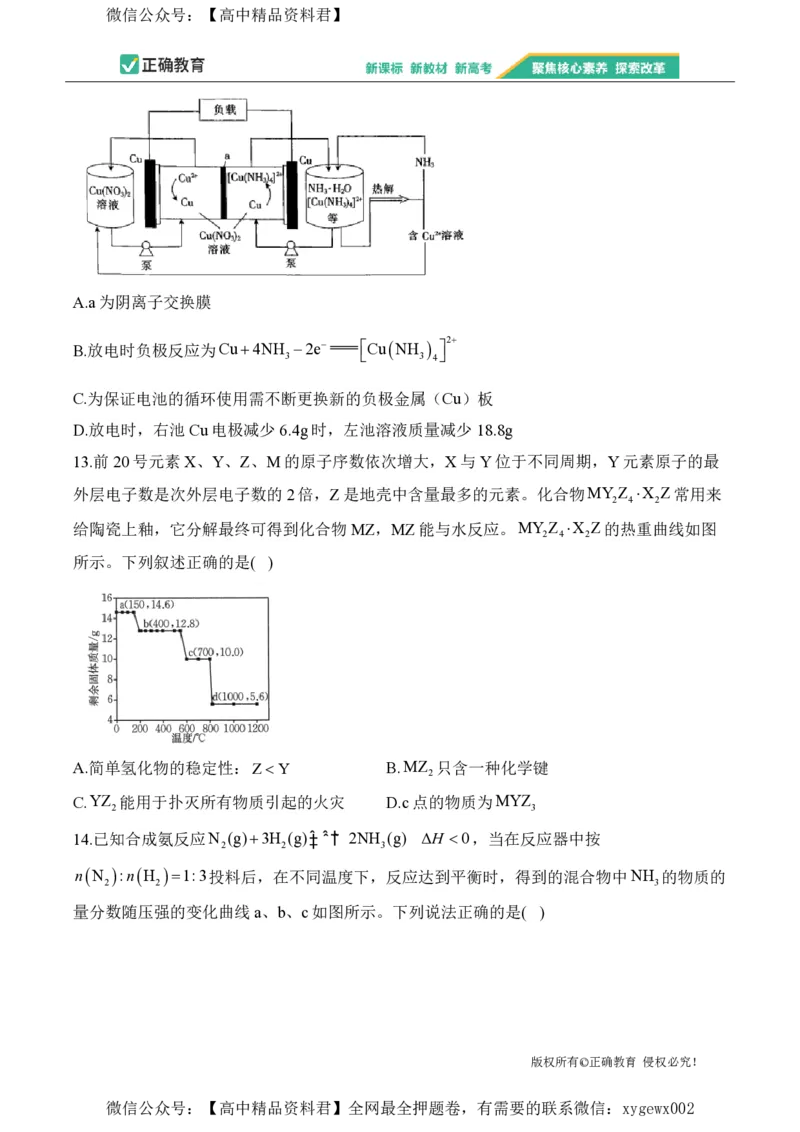
9.立方氮化硼(BN)硬度大,有优异的耐磨性。晶胞中 B位于顶点和面心,沿x、y、z轴方
向的投影图均如图所示。下列说法不正确的是( )
A.氮化硼的熔点高于晶体硅
3
B.若晶胞参数为apm,则 N与B之间的最近距离为 a pm
4
C.晶胞中 N填充在B构成的正四面体空隙中
1 1 1 3 3 1
D.若标号1的N原子分数坐标为 , , ,则标号2的N原子分数坐标一定为 , ,
4 4 4 4 4 4
10.三卤化硼(BX )因能接受电子对而被称为路易斯酸,可用作有机合成催化剂,水解时生
3
成硼酸(H BO )和相应的卤化氢(HX)。硼酸具有片层状结构,如图所示。下列说法错误
3 3
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
的是( )
A.稳定性:BF BCl BBr BI
3 3 3 3
B.H BO 分子间存在氢键,1 mol H BO 分子中有3 mol氢键
3 3 3 3
C.随着卤素原子半径的增大,卤素原子的p轨道与硼原子的p轨道重叠的程度降低,难形成
大T键,因此BF 表现出更强的路易斯酸性
3
D.H BO 溶于水,形成B(OH) ,其结构为正四面体形
3 3 4
11.常温下,用0.1000molL1的NaOH溶液滴定10.00mL等浓度的HCl溶液和用0.1000molL1
的CH COOH溶液滴定10.00mL等浓度的NaOH溶液,滴定过程中溶液的导电能力如图所
3
示。下列说法不正确的是( )
A.a点的K 等于 b点的K
w w
B.等浓度等体积的HCl溶液与NaOH溶液的导电能力不相同
C.c点溶液中阴离子总浓度大于d点溶液中阴离子总浓度
D.e点溶液中:c H cCH COOH2c OH c CH COO
3 3
12.一种热再生氨基液流电池的工作原理如图所示,下列有关说法错误的是( )
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
A.a为阴离子交换膜
B.放电时负极反应为Cu4NH 2e CuNH 2
3 3 4
C.为保证电池的循环使用需不断更换新的负极金属(Cu)板
D.放电时,右池Cu电极减少6.4g时,左池溶液质量减少 18.8g
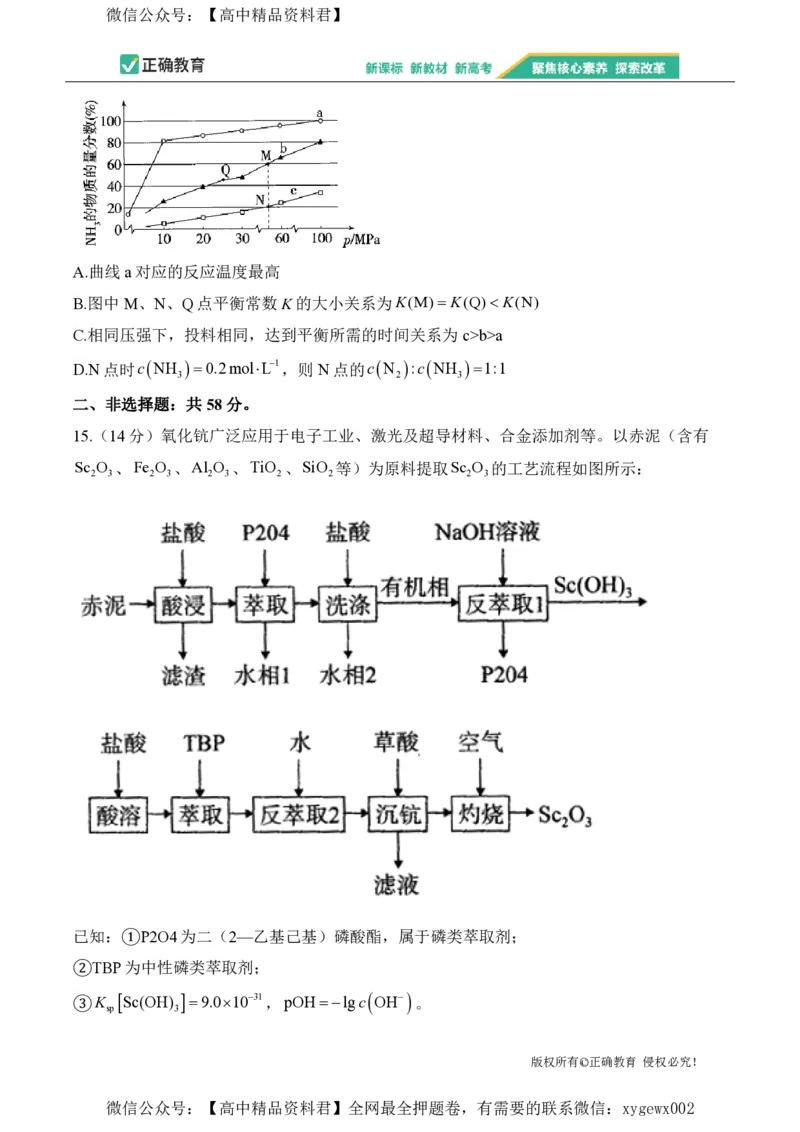
13.前20号元素X、Y、Z、M的原子序数依次增大,X与Y位于不同周期,Y元素原子的最
外层电子数是次外层电子数的2倍,Z是地壳中含量最多的元素。化合物MY Z X Z常用来
2 4 2
给陶瓷上釉,它分解最终可得到化合物MZ,MZ能与水反应。MY Z X Z的热重曲线如图
2 4 2
所示。下列叙述正确的是( )
A.简单氢化物的稳定性:ZY B.MZ 只含一种化学键
2
C.YZ 能用于扑灭所有物质引起的火灾 D.c点的物质为MYZ
2 3
14.已知合成氨反应N (g)3H (g)‡ˆ ˆˆ†ˆ 2NH (g) ΔH 0,当在反应器中按
2 2 3
nN :nH 1:3投料后,在不同温度下,反应达到平衡时,得到的混合物中NH 的物质的
2 2 3
量分数随压强的变化曲线a、b、c如图所示。下列说法正确的是( )
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
A.曲线a对应的反应温度最高
B.图中 M、N、Q点平衡常数K的大小关系为K(M) K(Q) K(N)
C.相同压强下,投料相同,达到平衡所需的时间关系为c>b>a
D.N点时cNH 0.2 molL1,则N点的cN :cNH 1:1
3 2 3
二、非选择题:共 58 分。
15.(14分)氧化钪广泛应用于电子工业、激光及超导材料、合金添加剂等。以赤泥(含有
Sc O 、Fe O 、Al O 、TiO 、SiO 等)为原料提取Sc O 的工艺流程如图所示:
2 3 2 3 2 3 2 2 2 3
已知:①P2O4为二(2—乙基己基)磷酸酯,属于磷类萃取剂;
②TBP为中性磷类萃取剂;
③K Sc(OH) 9.01031,pOHlgc OH 。
sp 3
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
回答下列问题:
(1)基态Sc原子的价层电子排布式为__________。
(2)为提高“酸浸”效率,可采取的措施有_______________________(任写两条)。
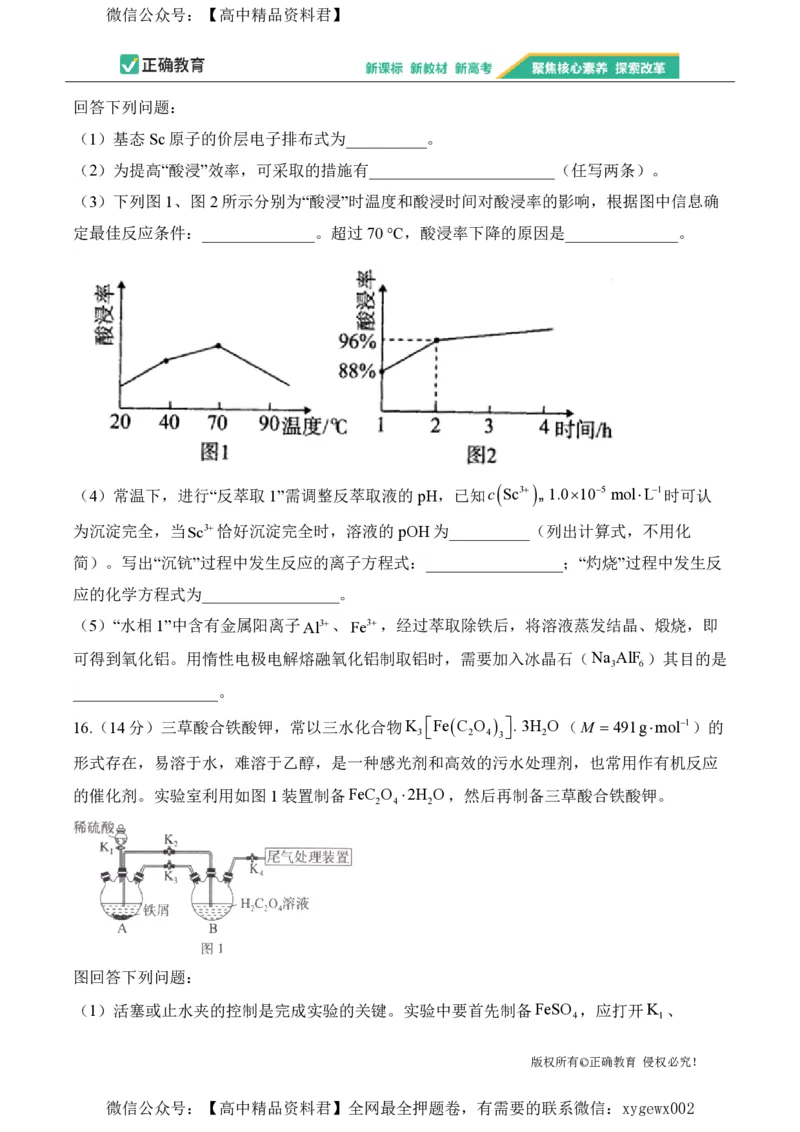
(3)下列图1、图2所示分别为“酸浸”时温度和酸浸时间对酸浸率的影响,根据图中信息确
定最佳反应条件:______________。超过70 ℃,酸浸率下降的原因是______________。
(4)常温下,进行“反萃取 1”需调整反萃取液的 pH,已知c Sc3 „ 1.0105 molL1时可认
为沉淀完全,当Sc3恰好沉淀完全时,溶液的pOH为__________(列出计算式,不用化
简)。写出“沉钪”过程中发生反应的离子方程式:_________________;“灼烧”过程中发生反
应的化学方程式为_________________。
(5)“水相1”中含有金属阳离子Al3、Fe3,经过萃取除铁后,将溶液蒸发结晶、煅烧,即
可得到氧化铝。用惰性电极电解熔融氧化铝制取铝时,需要加入冰晶石(Na AlF )其目的是
3 6
__________________。
16.(14分)三草酸合铁酸钾,常以三水化合物K FeC O . 3H O(M 491gmol1)的
3 2 4 3 2
形式存在,易溶于水,难溶于乙醇,是一种感光剂和高效的污水处理剂,也常用作有机反应
的催化剂。实验室利用如图1装置制备FeC O 2H O,然后再制备三草酸合铁酸钾。
2 4 2
图回答下列问题:
(1)活塞或止水夹的控制是完成实验的关键。实验中要首先制备FeSO ,应打开K 、
4 1
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
________,关闭_______________(根据需要选择合适的止水夹)。
(2)向制得的FeC O (难溶于水)中加入过量的K C O 溶液和H C O 溶液,在水浴40 ℃
2 4 2 2 4 2 2 4
下加热,缓慢滴加H O 溶液,制得K FeC O ,该反应的离子方程式为
2 2 3 2 4 3
___________________;缓慢滴加H O 溶液,水浴控温在40 ℃的原因是
2 2
______________________(用化学方程式表示)。
(3)将上述混合物煮沸,加入饱和H C O 溶液,充分反应后加入乙醇,经过一系列操作,
2 2 4
得到 K FeC O 3H O。
3 2 4 3 2
ⅰ.加入乙醇的作用是________________________。
ⅱ.三草酸合铁酸钾的溶解度曲线如图2所示。“经过一系列操作”得到K FeC O 3H O的
3 2 4 3 2
操作方法为____________________________。
(4)K FeC O 3H O晶体具有光敏性,在强光下分解生成草酸亚铁
3 2 4 3 2
(FeC O )且产物中只有一种气体,该反应的化学方程式为
2 4
__________________________________。
(5)制得的K FeC O 3H O中含少量的FeC O . 2H O,为测定其纯度,进行如下实
3 2 4 3 2 2 4 2
验:
步骤Ⅰ:称取 5.000 g三草酸合铁酸钾晶体,配制成1.000 L溶液,固体完全溶解。
步骤Ⅱ:取20.00 mL溶液,用0.1000molL1酸性KMnO 溶液滴定至终点,消耗2.46 mL酸
4
性KMnO 溶液。
4
步骤Ⅲ:另取 20.00 mL溶液,加入过量铜粉,过滤,洗涤,将滤液和洗涤液合并。
步骤Ⅴ:用0.1000molL1酸性KMnO 溶液滴定合并后的溶液至终点,消耗2.86 mL酸性
4
KMnO 溶液。
4
已知C O2、Fe2与MnO的反应如下:
2 4 4
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
5C O2 2MnO 16H 10CO 2Mn2 8H O
2 4 4 2 2
5Fe2 MnO 8H 5Fe3 Mn2 4H O
4 2
则制得的K FeC O 3H O纯度为____________。
3 2 4 3 2
17.(15分)以CO 和NH 为原料合成尿素和氨基甲酸铵有利于实现“碳达峰、碳中和”,体系
2 3
中同时存在反应:
Ⅰ.2NH (g)CO (g)‡ˆ ˆˆ†ˆ NH COONH (s) H 159kJmol1
3 2 2 4 1
Ⅱ.2NH (g)CO (g)‡ˆ ˆˆ†ˆ CONH (s)H O(g) H
3 2 2 2 2 2
Ⅲ.NH COONH (s)‡ˆ ˆˆ†ˆ CONH (s)H O(g) H 72kJmol1
2 4 2 2 2 3
(1)反应Ⅱ的H ______kJmol1,S________0(填“>”“<”或“=”),二氧化碳为(填
2
“极性”或“非极性”)分子。
(2)一定温度下,向密闭容器中以物质的量之比为2:1充入NH 和CO ,发生反应Ⅰ,达到
3 2
平衡后,CO 的平衡浓度为c molL1,其他条件不变,缩小容器容积,重新达到平衡后,
2 1
CO 的平衡浓度为c molL1,则c _____c (填“>”“<”或“=”)。
2 2 1 2
(3)用太阳能电池电解水得到的H 与CO 反应生成液态甲醇有利于实现“碳达峰、碳中
2 2
和”,这是目前推动“碳达峰、碳中和”的新路径。主要发生以下反应:
ⅰ.CO (g)3H (g)‡ˆ ˆˆ†ˆ CH OH(g)H O(g) H 49.4kJmol1
2 2 3 2 1
ⅱ.CO (g)H (g)‡ˆ ˆˆ†ˆ CO(g)H O(g) H 41.1kJmol1
2 2 2 2
在某催化剂作用下,一定条件下的密闭容器中发生反应ⅰ、ⅱ,已知H 、CO 按照物质的量分
2 2
别为300 mol、100 mol投料,在2 MPa和5 MPa下,二氧化碳的平衡转化率和甲醇的选择性
nCH OH
[已知甲醇的选择性 3 100 %]随温度的变化如图1所示:
nCO nCO
2 起始 2 平衡
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
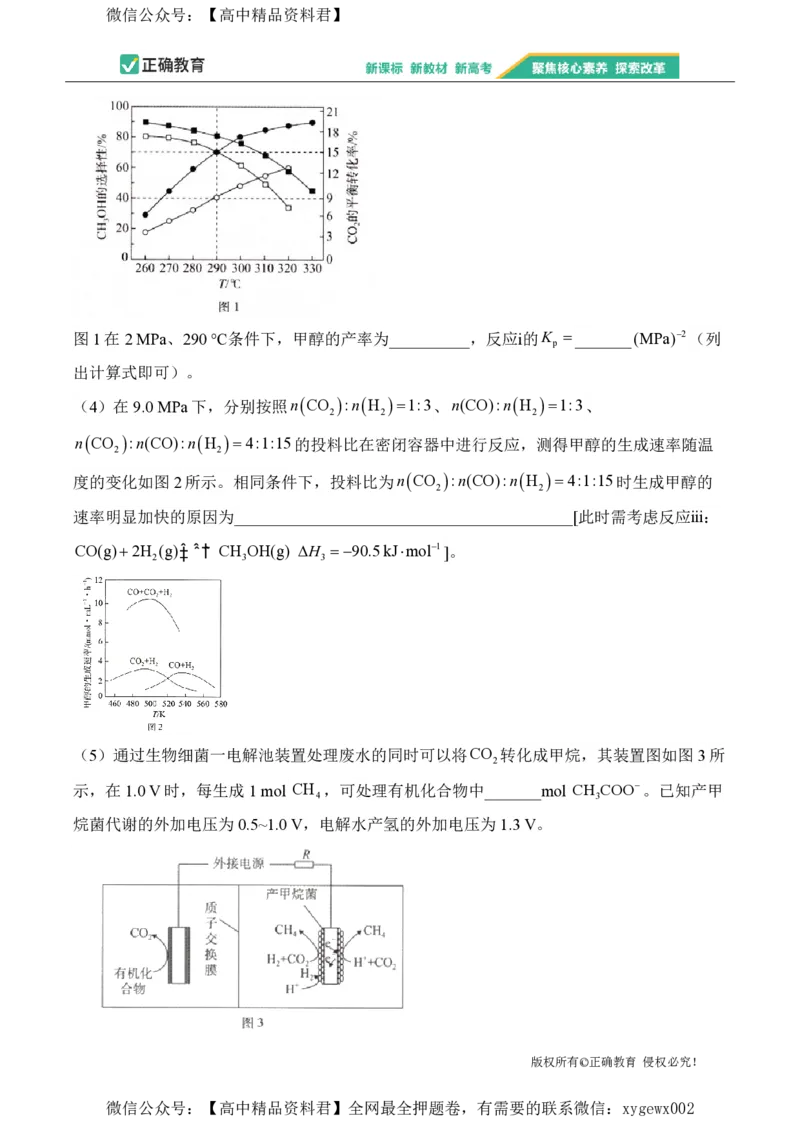
图1在2 MPa、290 ℃条件下,甲醇的产率为__________,反应ⅰ的K _______(MPa)2(列
p
出计算式即可)。
(4)在9.0 MPa下,分别按照nCO :nH 1:3、n(CO):nH 1:3、
2 2 2
nCO :n(CO):nH 4:1:15的投料比在密闭容器中进行反应,测得甲醇的生成速率随温
2 2
度的变化如图2所示。相同条件下,投料比为nCO :n(CO):nH 4:1:15时生成甲醇的
2 2
速率明显加快的原因为__________________________________________[此时需考虑反应ⅲ:
CO(g)2H (g)‡ˆ ˆˆ†ˆ CH OH(g) H 90.5kJmol1]。
2 3 3
(5)通过生物细菌一电解池装置处理废水的同时可以将CO 转化成甲烷,其装置图如图3所
2
示,在1.0 V时,每生成1 mol CH ,可处理有机化合物中_______mol CH COO。已知产甲
4 3
烷菌代谢的外加电压为0.5~1.0 V,电解水产氢的外加电压为1.3 V。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
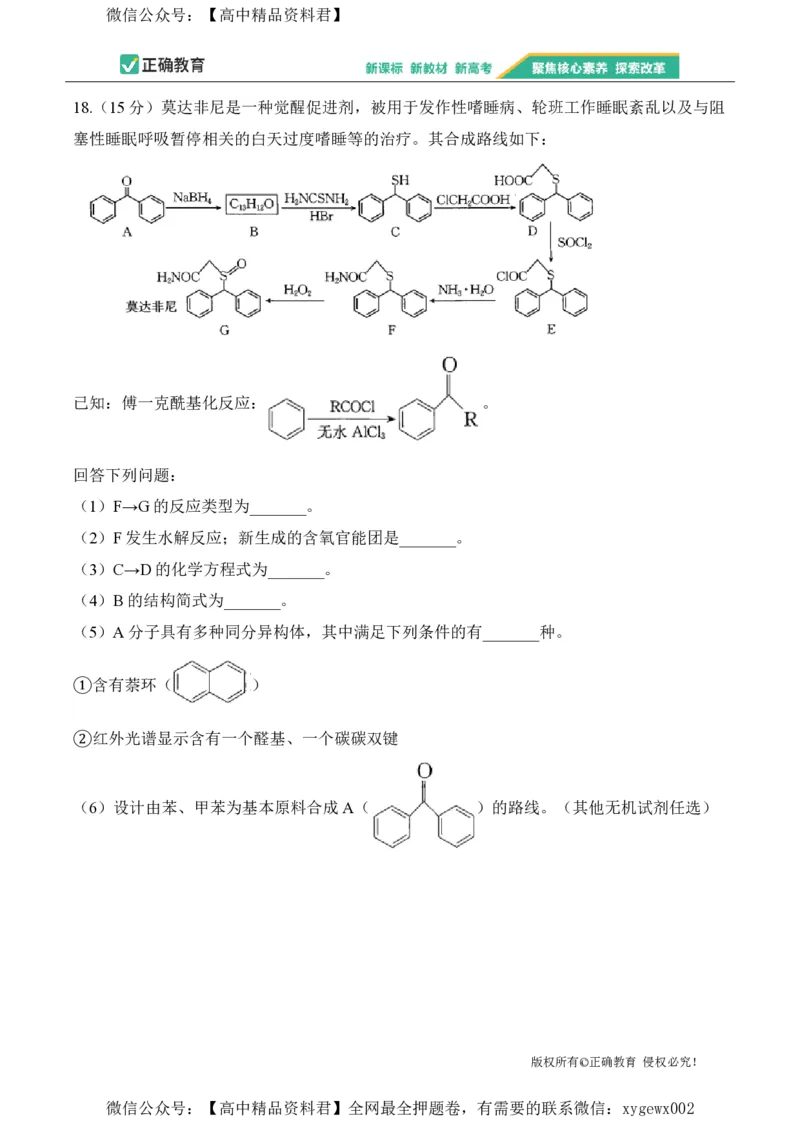
18.(15分)莫达非尼是一种觉醒促进剂,被用于发作性嗜睡病、轮班工作睡眠紊乱以及与阻
塞性睡眠呼吸暂停相关的白天过度嗜睡等的治疗。其合成路线如下:
已知:傅一克酰基化反应: 。
回答下列问题:
(1)F→G的反应类型为_______。
(2)F发生水解反应;新生成的含氧官能团是_______。
(3)C→D的化学方程式为_______。
(4)B的结构简式为_______。
(5)A分子具有多种同分异构体,其中满足下列条件的有_______种。
①含有萘环( )
②红外光谱显示含有一个醛基、一个碳碳双键
(6)设计由苯、甲苯为基本原料合成A( )的路线。(其他无机试剂任选)
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
答案以及解析
1.答案:A
解析:合金一般比其它成分金属的硬度大、熔点低,A正确;碳纤维复合材料主要由碳网点
原子构成,属于新型无机非金属材料,不属于有机高分子材料,B错误,氙气在一定条件下
可以与F 化合生成XeF 、XeF 等氟化物,C错误;涤纶属于高分子材料,绝大多数高分子材
2 2 4
料是许多相对分子质量不同的分子组成的混合物,D错误。
2.答案:B
解析:CuSO 是易溶于水的强电解质,应拆成离子形式,Ca(OH) 以石灰乳的形式出现应不
4 2
拆,其正确的离子方程式为Cu2 SO2 Ca(OH) Cu(OH) CaSO ,A错误;氢氟酸是
4 2 2 4
弱酸,HF不拆,生成的气体为SiF ,离子方程式无误,B正确;该离子方程式的得失电子、
4
电荷不守恒,正确的离子方程式为5SO 2MnO 2H O 5SO2 2Mn2 4H,C错误;
2 4 2 4
生成的NH仍存在于废水中,没有达到脱氨的目的,应生成无害气体脱离体系,正确的电极
4
反应式应为2NO 10e 12H N 6H O,D错误。
3 2 2
3.答案:C
解析:F元素的焰色为无色,不能使烟花绚丽多彩,A错误;Li与O 反应只能生成Li O,K
2 2
与O 反应可生成K O、K O 、KO ,B错误;苯酚具有杀菌功能,C正确;用蘸有浓氨水
2 2 2 2 2
的玻璃棒检验氯气是否泄漏,原理为8NH 3Cl N 6NH Cl,涉及氧化还原反应,D
3 2 2 4
错误。
4.答案:D
解析:FeCl 溶液体积未知,无法求出溶液中Fe3的数目,A错误;开始时,Zn与浓硫酸发
3
生反应2H SO (浓) ZnSO SO 2H O,随着反应进行,硫酸浓度变低,Zn与稀硫
2 4 4 2 2
酸发生反应ZnH SO H ZnSO ,100mL18.4molL1的硫酸含1.84molH SO ,和
2 4 2 4 2 4
足量锌充分反应,生成气体的物质的量大于0.92 mol,B错误;标准状况下,1.12LH 和
2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
1.12LF 完全反应生成0.1 mol HF,HF在标准状况下是液体,C错误;Na S和Na O 的摩尔
2 2 2 2
质量均为78gmol1,阴、阳离子数目比均为1:2,故7.8g Na S和Na O 混合物总物质的量
2 2 2
为0.1 mol,含有的阴离子数目为0.1N ,D正确。
A
5.答案:B
解析:铜与浓硫酸在加热的条件下可以产生二氧化硫,A项不符合题意;二氧化硫会与碱石
灰反应,不能达到相应的实验目的,B项符合题意;二氧化硫可以与酸性KMnO 溶液发生氧
4
化还原反应,酸性KMnO 溶液褪色,可以用来检验二氧化硫的还原性,C项不符合题意;二
4
氧化硫可以使品红溶液褪色,加热后品红溶液恢复至原色,可以用来探究二氧化硫与品红作
用的可逆性,D项不符合题意。
6.答案:C
解析:H、C、O三种元素的电负性由大到小的顺序:O>C>H,C正确。
7.答案:A
解析:A.该物质分子式为C H N O Cl,A错误;B.该物质水解可生成氨基酸,在一定条件
12 19 2 4
下可以发生缩聚反应,B正确;C.1mol该物质中酰胺基水解消耗1molNaOH,—NH Cl消耗
3
1molNaOH,共消耗2molNaOH,C正确;D.苯环可发生加成,取代反应,羟基可以被氧化,
与氢气加成也属于还原反应,D正确。
8.答案:D
解析:在2NO (g)‡ˆ ˆˆ†ˆ N O (g)的平衡体系中,压缩容积,各物质浓度增大,混合气体的颜
2 2 4
色变深,平衡向气体分子数减少的方向进行,即正向移动,混合气体的颜色稍变浅,故压缩
容积,混合气体的颜色变深,A错误;HR溶液为酸性溶液,HR为弱电解质时,NaR显碱
性,HR为强电解质时,NaR显中性,向酸性溶液中加入碱性或中性溶液,溶液的 H均增
大,B错误;加水稀释,CH COONa水解平衡正向移动,将CH COONa溶液加水稀释10
3 3
倍,pH变化量小于1,C错误;K CaSO K CaCO ,故Na CO 溶液可将CaSO 转化
sp 4 sp 3 2 3 4
为CaCO ,再用盐酸除去CaCO 沉淀,D正确。
3 3
9.答案:D
解析:氮化硼和晶体硅都是共价晶体,N、B的原子半径均小于 Si的原子半径,故N—B键
的键长更短,键能更大,则氮化硼的熔点高于晶体硅,A说法正确;晶胞参数为apm,N原
1 3
子均位于体对角线的 处,故B原子和N原子之间的最短距离为 a pm,B说法正确:根
4 4
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
据解题突破可知,晶胞中N原子填充在由B原子构成的正四面体空隙中,C说法正确;因为
x、y、z轴方向的投影图均为题图所示,若为沿y轴的投影,则标号2的N原子的分数坐标为
3 1 3 1 3 3
, , ,若为沿x轴的投影,标号2的N原子的分数坐标为 , , ,若为沿z轴的投
4 4 4 4 4 4
3 3 1
影,标号2的N原子的分数坐标为 , , ,D说法误。
4 4 4
10.答案:C
解析:BX 的稳定性与其所含化学键(共价键)的强弱有关,随着X原子半径的增大,共价
3
键逐渐减弱,稳定性逐渐变差,故稳定性:BF BCl BBr BI ,A说法正确;由题图可
3 3 3 3
知,H BO 分子间存在氢键,1个B原子与3个OH基团结合成平面三角形结构的B(OH) 单
3 3 3
元,各个B(OH) 单元之间通过氢键形成层状结构,1个B(OH) 单元对应6个氢键,1个氢键
3 3
为2个B(OH) 单元共用,因此1 mol H BO 分子中有3 mol氢键,B说法正确;随着卤素原
3 3 3
子半径的增大,卤素原子的p轨道与硼原子的P轨道重叠的程度降低,难形成大 π键,但更
容易接受电子对,因此BI 表现出更强的路易斯酸性,C说法错误;BI 中B还有一个没有参
3 3
与杂化的空的p轨道,当BI 溶于水时,水解离出的OH中的孤电子对进入该空的p轨道
3
中,形成以B为中心的配位单元B(OH) ,结构为正四面体形,D说法正确。
4
11.答案:D
解析:A.a、b两点的温度相同,两点的K 相等;B.由图可知,等浓度等体积的HCl溶液与
w
NaOH溶液的导电能力不相同;C.c、d两点的溶质分别为NaCl、CH COONa,c点有:
3
c
Na
c
H
c
Cl
c
OH
,d点有:c
Na
c
H
c
CH
COO
c
OH
,由于
3
CH COONa溶液呈碱性,c
OH
c
H
,故NaCl溶液中的c
H
大于CH COONa溶液中
3 3
的c
H
,两种溶液中c
Na
一样大,c点溶液中阴离子总浓度大于d点溶液中阴离子总浓
度;D.e点是等物质的量的CH COONa和CH COOH的混合溶液,由电荷守恒得
3 3
c
Na
c
H
c
CH
COO
c
OH
,由物料守恒得,
3
2c Na c CH COO cCH COOH,联合得:
3 3
2c H cCH COOH2c OH c CH COO 。
3 3
12.答案:C
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
解析:由图可知,该原电池溶液中阴离子移向负极,a为阴离子交换膜,A项正确;放电时负
极反应为Cu4NH 2e CuNH 2 ,B项正确;只需将正、负两极的电极板交换就
3 3 4
可实现电池的循环使用,C项错误;放电时,右池Cu电极减少6.4g时,Cu2e Cu2,
转移0.2mol电子,左池溶液中析出0.1mol铜离子,有0.2mol硝酸根离子移向右池,故左池
溶液质量减少0.2mol62gmol10.1mol64gmol1 18.8g,D项正确。
13.答案:D
解析:A.非金属性越强,其简单氢化物稳定性越强,简单氢化物的稳定性:CO,A错误;
B.MZ 为CaO 是钙离子和过氧根离子构成的,过氧根离子中含有氧氧共价键,故含2种化学
2 2
键,B错误;
C.CO 能和镁单质反应,不能用于扑灭镁等物质引起的火灾,C错误。
2
14.答案:D
解析:该反应的正反应是放热反应,升高温度,平衡逆向移动,氨气的物质的量分数减小,
而压强相同时,曲线a对应的反应中氨气的物质的量分数最大,所以曲线a对应的反应温度
最低,A错误;K只与温度有关,温度不变平衡常数不变,所以K(M) K(Q),该反应的正
反应为放热反应,升高温度平衡逆向移动,平衡常数减小,Q点的温度低于N,所以
K(Q) K(N),B错误;相同压强下,投料相同,温度越高反应速率越快,达到平衡所需的
时间越短,曲线c、b、a对应的反应温度依次降低,所以达到平衡所需的时间关系为a>b>c,
故C错误;N点时氨气的物质的量分数为20%,设N 的平衡转化率是b,N 的起始浓度为
2 2
a molL1,则
N (g)3H (g)‡ˆ ˆˆ†ˆ 2NH (g)
2 2 3
起始 molL1
a 3a 0
转化 molL1
ab 3ab 2ab
平衡 molL1
aab 3a3ab 2ab
2ab 1
根据题意, 20%,2ab0.2,解得a0.3,b ,则N点的
aab3a3ab2ab 3
1
cN :cNH (0.30.3 ) molL1:0.2 molL1 1:1,故D正确。
2 3 3
15.(14分)答案:(1)3d14s2(1分)
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(2)适当加热、搅拌(2分)
(3)70 ℃、2 h盐酸受热易挥发(2分)
9.01031
(4)lg3 (3分);2Sc3 3H C O Sc C O 6H(2分);
1.0105 2 2 4 2 2 4 3
灼烧
2Sc C O 3O 2Sc O 12CO (2分)
2 2 4 3 2 2 3 2
(5)做助熔剂,降低氧化铝的熔点(2分)
解析:(1)Sc为21号元素,基态Sc原子的电子排布式为1s22s22p63s23p63d14s2,则价层电
子排布式为3d14s2。
(2)提高“酸浸”效率可从反应的充分性、反应速率、物质溶解性等方面入手。提高“酸浸”温
度、进行搅拌、增加酸的浓度、粉碎矿物以增加接触面积等均可提高“酸浸”效率。
(3)由题图1可知,温度为70 ℃时,酸浸率最高;由题图2可知,酸浸时间为2 h后,酸
浸率变化很小,所以最佳反应条件为70 ℃、2 h。盐酸易挥发,温度超过70 ℃加快挥发,酸
浸液酸性减弱,酸浸率降低。
(4)Sc3恰好沉淀完全,说明c Sc3 1.0105 molL1,
c OH 3 K sp c S S c c (O 3 H ) 3 3 9 1 . . 0 0 1 1 0 0 3 5 1 molL1,pOHlgc OH lg3 9 1 . . 0 0 1 1 0 0 3 5 1 。“沉
钪”过程是Sc3与草酸(H C O )生成Sc C O 沉淀的过程,发生反应的离子方程式为
2 2 4 2 2 4 3
2Sc3 3H C O Sc C O 6H;“灼烧”过程中,Sc C O 变为Sc O ,Sc化合价
2 2 4 2 2 4 3 2 2 4 3 2 3
不变,只有碳与氧的化合价发生变化,反应的化学方程式为
灼烧
2Sc C O 3O 2Sc O 12CO 。
2 2 4 3 2 2 3 2
(5)冰晶石(Na AlF )做助熔剂,可降低氧化铝的熔点。
3 6
16.(14分)答案:(1)K 、K (1分);K (1分)
3 4 2
(2)2FeC O H O 3C O2 H C O 2FeC O 3 2H O(2分);
2 4 2 2 2 4 2 2 4 2 4 3 2
△
2H O 2H OO (2分)
2 2 2 2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(3)ⅰ.降低三草酸合铁酸钾的溶解度,使其更容易析出(2分)
ⅱ.蒸发浓缩、降温结晶、过滤、乙醇洗涤强光(2分)
强光
(4)2K FeC O 3H O 2FeC O 2CO 3K C O 6H O(2分)
3 2 4 3 2 2 4 2 2 2 4 2
(5)98.2%(2分)
解析:(1)制取FeSO 的同时,利用生成的H 排尽装置内的空气,防止Fe2被氧化;再利
4 2
用生成的H 将A装置内的FeSO 压入B装置内,所以制备 FeSO,时应先打开K 、K 、
2 4 1 3
K ,关闭K 。
4 2
(2)向制得的FeC O (s)中加入过量的K C O 溶液和H C O 溶液,在水浴40 ℃下加热,缓
2 4 2 2 4 2 2 4
慢滴加H
2
O
2
溶液,将Fe2氧化为Fe3,同时制得K
3
FeC
2
O
4
3
,该反应的化学方程式为
2FeC O H O 3K C O H C O 2K FeC O 2H O,离子方程式为
2 4 2 2 2 2 4 2 2 4 3 2 4 3 2
2FeC O H O 3C O2 H C O 2FeC O 3 2H O。由于H 0 热稳定性差,加热
2 4 2 2 2 4 2 2 4 2 4 3 2 2 2
时需控制温度,所以缓慢滴加H O 溶液,水浴控温在40 ℃的原因是为了防止H O 分解,即
2 2 2 2
△
2H O 2H OO 。
2 2 2 2
(3)ⅰ.三草酸合铁酸钾难溶于乙醇,加入乙醇的目的是降低三草酸合铁酸钾的溶解度,使其
更容易析出。
ⅱ.K FeC O 3H O易溶于水,难溶于乙醇,且溶解度随温度的降低而降低,故“经过一
3 2 4 3 2
系列操作”得到K FeC O 3H O的操作方法为蒸发浓缩、降温结晶、过滤、乙醇洗涤、
3 2 4 3 2
干燥。
(4)K FeC O 3H O在强光下分解生成草酸亚铁(FeC O ),Fe元素化合价降低,
3 2 4 3 2 2 4
则C元素化合价升高,且产物中只有一种气体,则该气体是CO ,故该反应的化学方程式为
2
强光
2K FeC O 3H O 2FeC O 2CO 3K C O 6H O。
3 2 4 3 2 2 4 2 2 2 4 2
(5)铜将Fe3还原为Fe2,两份溶液相比,第二份溶液中多消耗的2.86 mL—2.46 mL=0.4
mL酸性高锰酸钾溶液与铜转化生成的亚铁离子发生反应,根据反应比例可知,20 mL溶液中
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
n K FeC O 3H O n Fe3 0.4103 L0.1000molL152104 mol,故纯度为
3 2 4 3 2
1000mL
2104 mol491gmol1
20.00mL 。
100%98.2%
5.000g
17.(15分)答案:(1)—87(1分)<(1分);非极性(1分)
(2)=(2分)
6.3 9
2 2
387.4 387.4
(3)6.3%(2分); (3分)
3
91 278.4
2 2
378.4 387.4
(4)将少量CO加入CO 和H 的混合气体中时,CO与H O反应生成CO 和H ,一方面消
2 2 2 2 2
耗了反应ⅰ生成的H O,使平衡正向移动,另一方面又增大了CO 和H 的浓度,进一步提高
2 2 2
了反应i的反应速率(3分)
(5)1(2分)
解析:(1)由盖斯定律可得H H H
2 1 3
159kJmol1 72kJmol1 87kJmol1,反应Ⅱ正向气体分子数减少,混乱程度减
小,则S 0。二氧化碳分子的正电中心和负电中心重合,为非极性分子。
(2)一定温度下,向密闭容器中充入NH 和CO 的物质的量之比为2:1,与反应Ⅰ中两种气
3 2
体的化学计量数之比相同,即两种气体参加反应的物质的量之比和平衡时物质的量之比均为
1
2:1,反应Ⅰ的平衡常数K ,只与温度有关,故其他条件不变,缩小容器
c2NH cCO
3 2
容积,重新达到平衡后,两种气体的平衡浓度均不变,则c c 。
1 2
(3)反应ⅰ为放热反应,反应ⅱ为吸热反应,温度升高,反应逆向移动,甲醇的选择性降低,
所以曲线随温度升高而下降的为甲醇的选择性随温度的变化,随温度升高而上升的为二氧化
碳的转化率随温度的变化,随着温度升高反应逆向移动,二氧化碳的转化率应降低,但二氧
化碳的转化率升高,说明随着温度升高反应ⅱ正向移动程度更大。反应的正反应为气体分子数
减少的反应,压强越大,甲醇的选择性越大,二氧化碳的转化率越高,题图1中曲线趋势下
降且同一温度下甲醇的选择性较低的为2 MPa条件下的曲线,曲线趋势上升且同一温度下二
氧化碳的转化率较低的为2 MPa条件下的曲线。从题图 1中可以看出在2MP a、290 ℃条件
下,二氧化碳的平衡转化率为9%,甲醇的选择性为70%,则甲醇的产率为70%×9%=6.3%。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
投料时nH 300mol、nCO 100mol,二氧化碳的平衡转化率为9%,所以平衡
2 2
nCO 100mol(19%)91mol,生成nnCH OH6.3mol,n(CO)2.7mol,
2 3
nH O9mol,平衡时nH (30036.32.7)mol278.4mol,则平衡时气体总物质的
2 2
量为387.4 mol,又因为在2 MPa条件下反应,所以反应ⅰ的
6.3 9
2 2
387.4 387.4
K (MPa)2。
p 3
91 278.4
2 2
378.4 387.4
(4)由题图2可知,在9.0 MPa下,低温时反应ⅰ比反应ⅲ速率快,生成甲醇的主反应为反应
ⅰ,反应ⅰ和ⅱ为竞争反应,将少量CO加入CO 和H 的混合气体中时,CO与H O反应生成
2 2 2
CO 和H ,一方面消耗了反应ⅰ生成的H O,另一方面又增大了CO 和H 的浓度,进一步提
2 2 2 2 2
高了反应的反应速率和甲醇的选择性。
(5)由题意可知,当外加电压为1.0 V时,没有H 生成:根据题图3可知,电解液显酸性,
2
则左侧电极上发生反应CH COO 8e 2H O 2CO 7H,右侧电极上发生反应
3 2 2
8H CO 8e CH 2H O,故每生成1 mol CH ,可处理有机化合物中1 mol
2 4 2 4
CH COO。
3
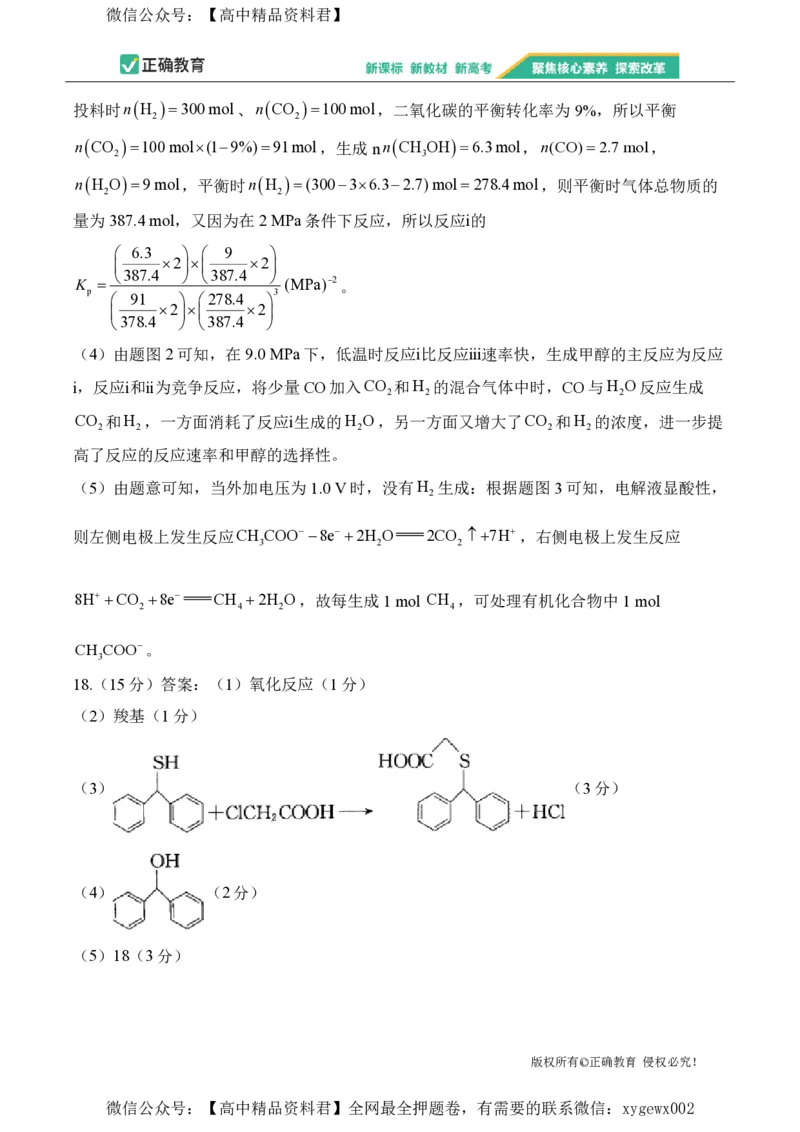
18.(15分)答案:(1)氧化反应(1分)
(2)羧基(1分)
(3) (3分)
(4) (2分)
(5)18(3分)
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(6) (5
分)
解析:(2)F中酰胺基发生水解反应生成羧基,故新生成的含氧官能团是羧基,
(4)A→B是还原反应,再比较二者的分子式,发现 B比A多2个H,说明B的结构简式应
为 。
(5)当萘环上连有1个侧链时,有4种同分异构体: ;当萘
环上有2个侧链时,有14种同分异构体: ,故共有18
种。
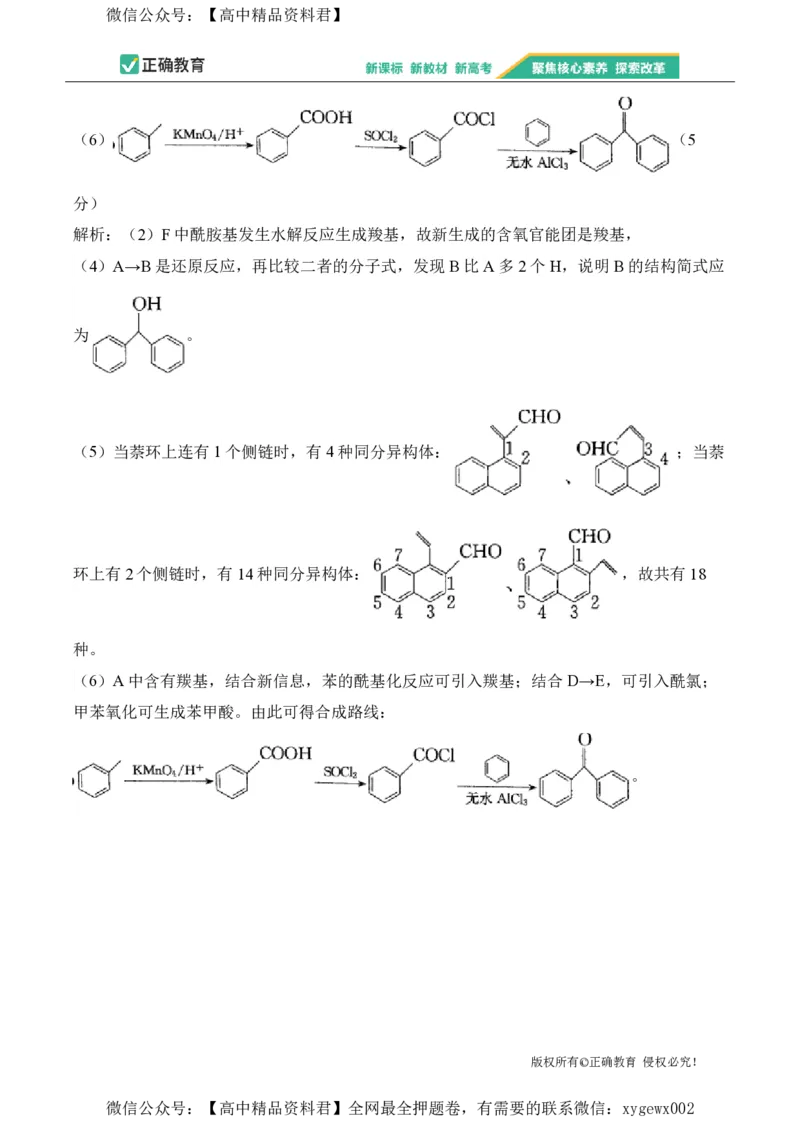
(6)A中含有羰基,结合新信息,苯的酰基化反应可引入羰基;结合 D→E,可引入酰氯;
甲苯氧化可生成苯甲酸。由此可得合成路线:
。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002