文档内容
2024年湖南高考化学试题
一、单选题
1.近年来,我国新能源产业得到了蓬勃发展,下列说法错误的是
A.理想的新能源应具有资源丰富、可再生、对环境无污染等特点
B.氢氧燃料电池具有能量转化率高、清洁等优点
C.锂离子电池放电时锂离子从负极脱嵌,充电时锂离子从正极脱嵌
D.太阳能电池是一种将化学能转化为电能的装置
2.下列化学用语表述错误的是
NaOH
A. 的电子式:
B.异丙基的结构简式:
C.NaCl溶液中的水合离子:
Cl σ
2
D. 分子中 键的形成:
3.下列实验事故的处理方法不合理的是
实验事故 处理方法
A 被水蒸气轻微烫伤 先用冷水处理,再涂上烫伤药膏
B 稀释浓硫酸时,酸溅到皮肤上 用3-5%的NaHCO 溶液冲洗
3
C 苯酚不慎沾到手上 先用乙醇冲洗,再用水冲洗
D 不慎将酒精灯打翻着火 用湿抹布盖灭
A.A B.B C.C D.D
4.下列有关化学概念或性质的判断错误的是
A.CH 分子是正四面体结构,则CH Cl 没有同分异构体
4 2 2
B.环己烷与苯分子中C-H键的键能相等
C.甲苯的质谱图中,质荷比为92的峰归属于
D.由 与 组成的离子液体常温下呈液态,与其离子的体积较大有关
R N+ PF-
4 6
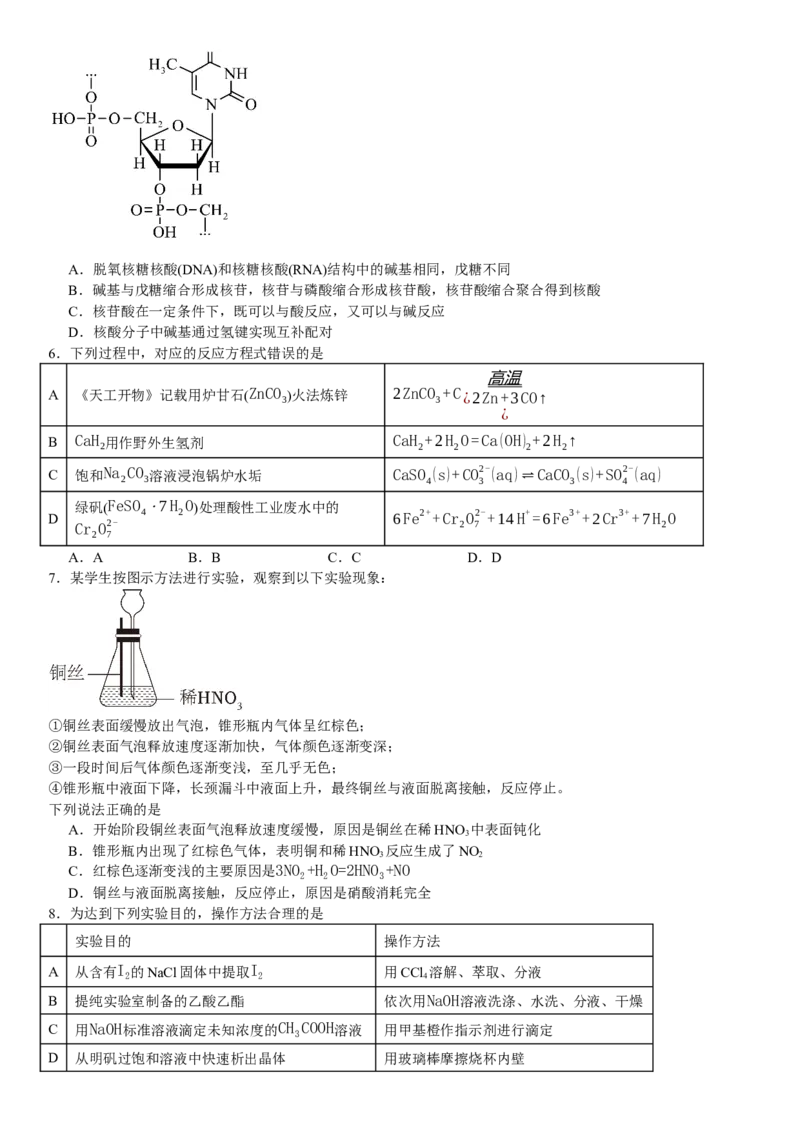
5.组成核酸的基本单元是核苷酸,下图是核酸的某一结构片段,下列说法错误的是A.脱氧核糖核酸(DNA)和核糖核酸(RNA)结构中的碱基相同,戊糖不同
B.碱基与戊糖缩合形成核苷,核苷与磷酸缩合形成核苷酸,核苷酸缩合聚合得到核酸
C.核苷酸在一定条件下,既可以与酸反应,又可以与碱反应
D.核酸分子中碱基通过氢键实现互补配对
6.下列过程中,对应的反应方程式错误的是
高温
A 《天工开物》记载用炉甘石( ZnCO
3
)火法炼锌 2ZnCO
3
+C ¿2Zn+3CO↑
¿
B CaH 用作野外生氢剂 CaH +2H O=Ca(OH) +2H ↑
2 2 2 2 2
C 饱和Na
2
CO
3
溶液浸泡锅炉水垢 CaSO
4
(s)+CO
3
2- (aq)⇌ CaCO
3
(s)+SO2
4
- (aq)
绿矾( FeSO ⋅7H O )处理酸性工业废水中的
D 4 2 6Fe2++Cr O2-+14H+=6Fe3++2Cr3++7H O
Cr O2- 2 7 2
2 7
A.A B.B C.C D.D
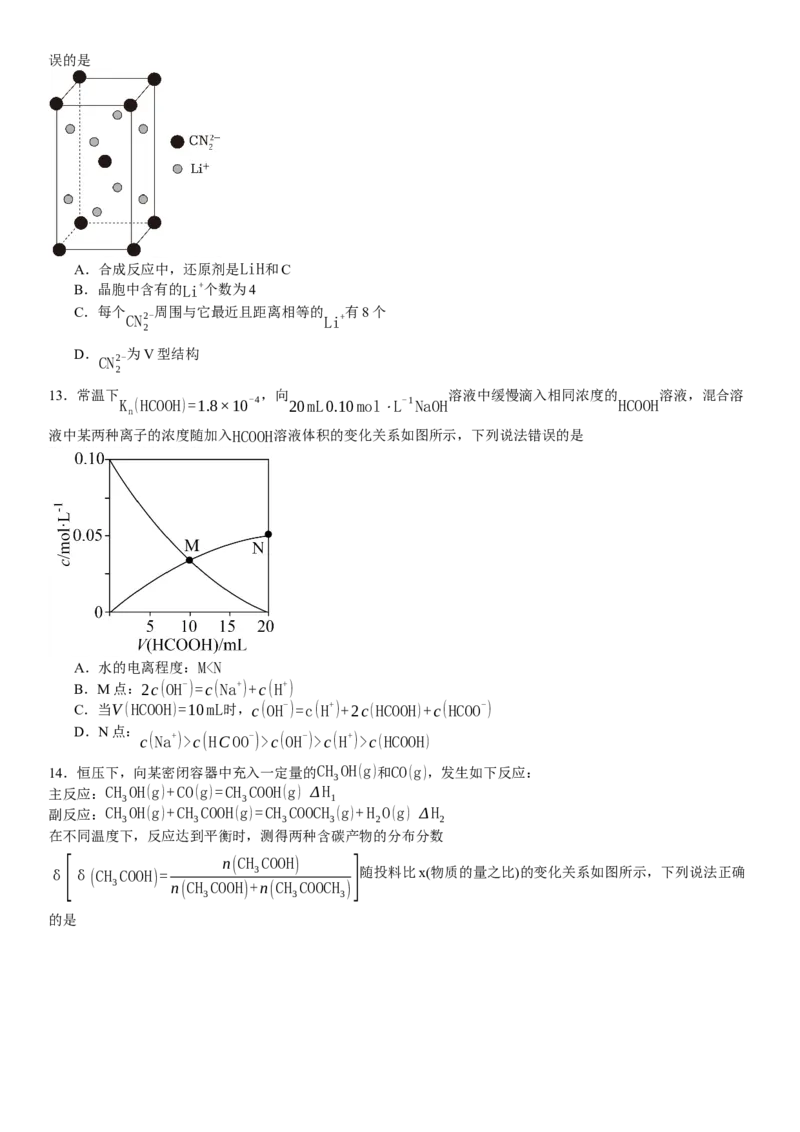
7.某学生按图示方法进行实验,观察到以下实验现象:
①铜丝表面缓慢放出气泡,锥形瓶内气体呈红棕色;
②铜丝表面气泡释放速度逐渐加快,气体颜色逐渐变深;
③一段时间后气体颜色逐渐变浅,至几乎无色;
④锥形瓶中液面下降,长颈漏斗中液面上升,最终铜丝与液面脱离接触,反应停止。
下列说法正确的是
A.开始阶段铜丝表面气泡释放速度缓慢,原因是铜丝在稀HNO 中表面钝化
3
B.锥形瓶内出现了红棕色气体,表明铜和稀HNO 反应生成了NO
3 2
C.红棕色逐渐变浅的主要原因是3NO +H O=2HNO +NO
2 2 3
D.铜丝与液面脱离接触,反应停止,原因是硝酸消耗完全
8.为达到下列实验目的,操作方法合理的是
实验目的 操作方法
A 从含有I 的NaCl固体中提取I 用CCl 溶解、萃取、分液
2 2 4
B 提纯实验室制备的乙酸乙酯 依次用NaOH溶液洗涤、水洗、分液、干燥
C 用NaOH标准溶液滴定未知浓度的CH COOH溶液 用甲基橙作指示剂进行滴定
3
D 从明矾过饱和溶液中快速析出晶体 用玻璃棒摩擦烧杯内壁A.A B.B C.C D.D
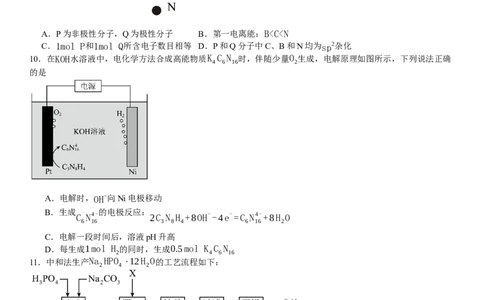
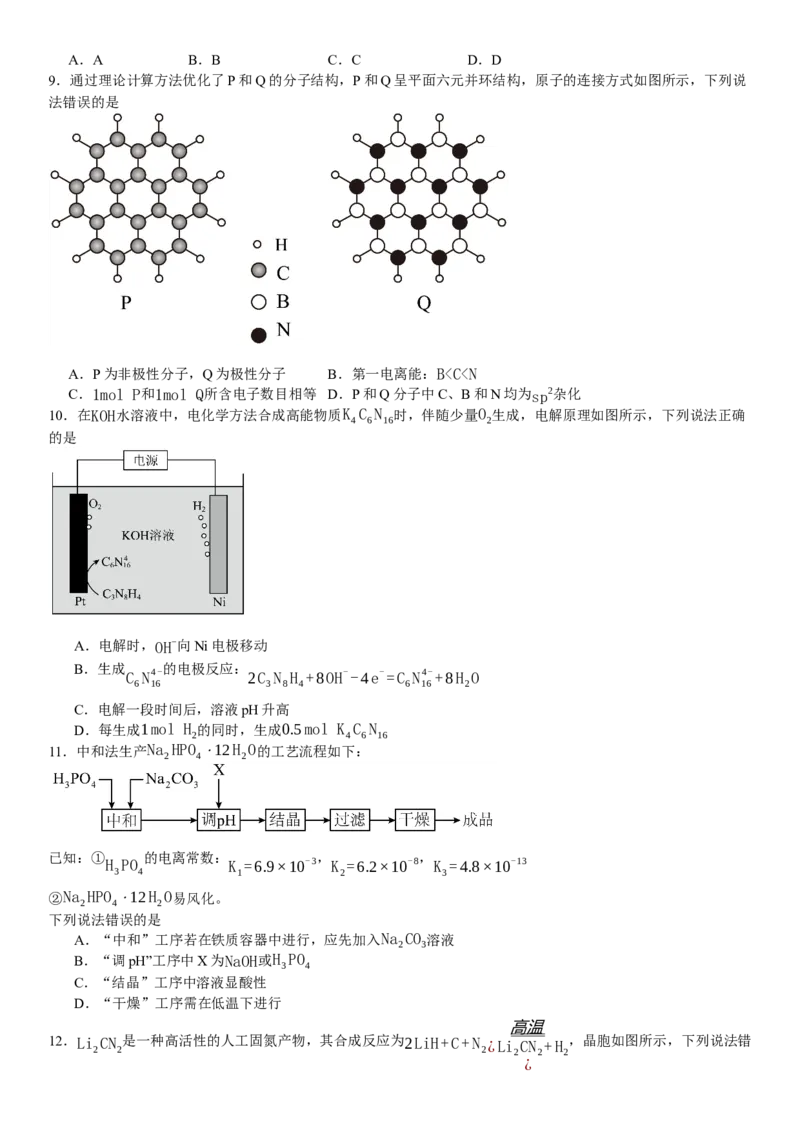
9.通过理论计算方法优化了P和Q的分子结构,P和Q呈平面六元并环结构,原子的连接方式如图所示,下列说
法错误的是
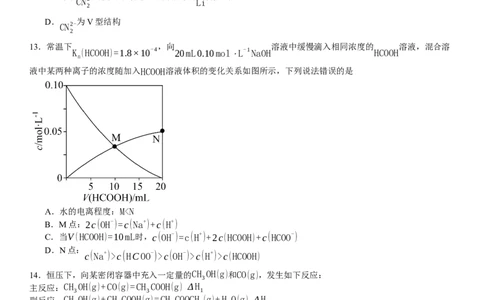
A.P为非极性分子,Q为极性分子 B.第一电离能:Bc(HCOO-)>c(OH-)>c(H+)>c(HCOOH)
14.恒压下,向某密闭容器中充入一定量的CH OH(g)和CO(g),发生如下反应:
3
主反应:CH OH(g)+CO(g)=CH COOH(g) ΔH
3 3 1
副反应:CH OH(g)+CH COOH(g)=CH COOCH (g)+H O(g) ΔH
3 3 3 3 2 2
在不同温度下,反应达到平衡时,测得两种含碳产物的分布分数
[ n(CH COOH) ]
δ δ(CH COOH)= 3 随投料比x(物质的量之比)的变化关系如图所示,下列说法正确
3 n(CH COOH)+n(CH COOCH )
3 3 3
的是A.投料比x代表n(CH OH)
3
n(CO)
B.曲线c代表乙酸的分布分数
C.ΔH <0,ΔH >0
1 2
D.L、M、N三点的平衡常数:K(L)=K(M)>K(N)
二、解答题
15.亚铜配合物广泛用作催化剂。实验室制备 的反应原理如下:
[Cu(CH CN) ]ClO
3 4 4
Cu(ClO ) ⋅6H O+Cu+8CH CN=2[Cu(CH CN) ]ClO +6H O
4 2 2 3 3 4 4 2
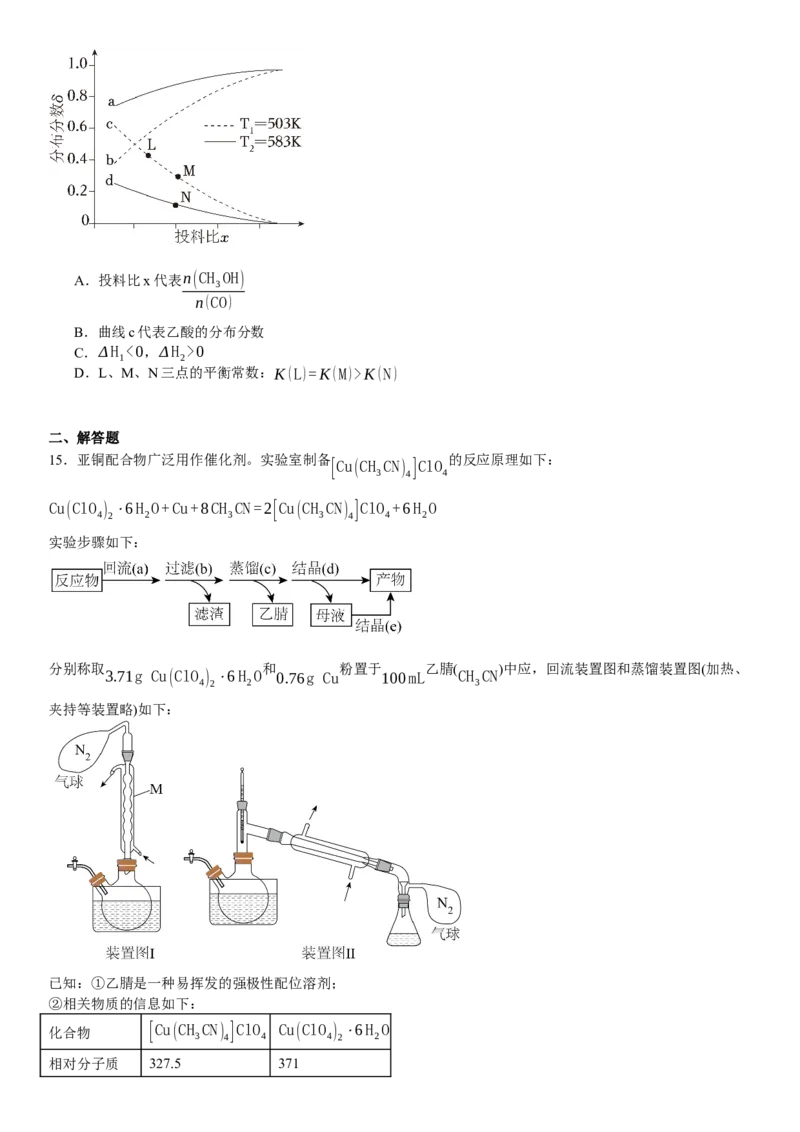
实验步骤如下:
分别称取 和 粉置于 乙腈( )中应,回流装置图和蒸馏装置图(加热、
3.71g Cu(ClO ) ⋅6H O 0.76g Cu 100mL CH CN
4 2 2 3
夹持等装置略)如下:
已知:①乙腈是一种易挥发的强极性配位溶剂;
②相关物质的信息如下:
化合物 [Cu(CH CN) ]ClO Cu(ClO ) ⋅6H O
3 4 4 4 2 2
相对分子质 327.5 371量
在乙腈中颜
无色 蓝色
色
回答下列问题:
(1)下列与实验有关的图标表示排风的是 (填标号);
A. B. C. D. E.
(2)装置Ⅰ中仪器M的名称为 ;
(3)装置Ⅰ中反应完全的现象是 ;
(4)装置Ⅰ和Ⅱ中N 气球的作用是 ;
2
(5) 不能由步骤c直接获得,而是先蒸馏至接近饱和,再经步骤d冷却结晶获得。这样处理的目
[Cu(CH CN) ]ClO
3 4 4
的是
(6)为了使母液中的 结晶,步骤e中向母液中加入的最佳溶剂是 (填标号);
[Cu(CH CN) ]ClO
3 4 4
A.水 B.乙醇 C.乙醚
(7)合并步骤d和e所得的产物,总质量为5.32g,则总收率为 (用百分数表示,保留一位小数)。
16.铜阳极泥(含有Au、Ag Se、Cu Se、PbSO 等)是一种含贵金属的可再生资源,回收贵金属的化工流程如下:
2 2 4
已知:①当某离子的浓度低于1.0×10-5mol⋅L-1时,可忽略该离子的存在;
② AgCl(s)+Cl- (aq)⇌ ❑ [AgCl ] - (aq) K=2.0×10-5;
2
③Na SO 易从溶液中结晶析出;
2 3
④不同温度下Na SO 的溶解度如下:
2 3
温度/℃ 0 20 40 60 80
溶解度/g 14.4 26.1 37.4 33.2 29.0
回答下列问题:
(1)Cu属于 区元素,其基态原子的价电子排布式为 ;
(2)“滤液1”中含有Cu2+和H SeO ,“氧化酸浸”时Cu Se反应的离子方程式为 ;
2 3 2
(3)“氧化酸浸”和“除金”工序抣需加入一定量的NaCl:
①在“氧化酸浸”工序中,加入适量NaCl的原因是 。
②在“除金”工序溶液中,Cl-浓度不能超过 mol⋅L-1。
(4)在“银转化”体系中,
[Ag(SO ) ]
3-和
[Ag(SO ) ]
5-浓度之和为
0.075mol⋅L-1
,两种离子分布分数
3 2 3 3
[ n([Ag(SO ) ] 3-) ]
δ δ([Ag(SO ) ] 3-)= 3 2 随 SO2-浓度的变化关系如图所示,若 SO2-浓度为
3 2 n([Ag(SO ) ] 3-)+n([Ag(SO ) ] 5-) 3 3
3 2 3 3
1.0mol⋅L-1 ,则 [Ag(SO ) ] 5-的浓度为 mol⋅L-1 。
3 3(5)滤液4中溶质主要成分为 (填化学式);在连续生产的模式下,“银转化”和“银还原”工序需在40℃左
右进行,若反应温度过高,将难以实现连续生产,原因是 。
17.化合物H是一种具有生物活性的苯并呋喃衍生物,合成路线如下(部分条件忽略,溶剂未写出):
回答下列问题:
(1)化合物A在核磁共振氢谱上有 组吸收峰;
(2)化合物D中含氧官能团的名称为 、 ;
(3)反应③和④的顺序不能对换的原因是 ;
(4)在同一条件下,下列化合物水解反应速率由大到小的顺序为 (填标号);
① ② ③
(5)化合物G→H的合成过程中,经历了取代、加成和消去三步反应,其中加成反应的化学方程式为 ;
Cl CHOCH
2 3
(6)依据以上流程信息,结合所学知识,设计以 和 为原料合成 的路线
(HCN等无机试剂任选)。
18.丙烯腈(CH =CHCN)是一种重要的化工原料。工业上以N 为载气,用TiO 作催化剂生产CH =CHCN的流程如下:
2 2 2 2
已知:①进料混合气进入两釜的流量恒定,两釜中反应温度恒定:
②反应釜Ⅰ中发生的反应:
ⅰ:HOCH CH COOC H (g)→CH =CHCOOC H (g)+H O(g) ΔH
2 2 2 5 2 2 5 2 1
③反应釜Ⅱ中发生的反应:
ⅱ:CH =CHCOOC H (g)+NH (g)→CH =CHCONH (g)+C H OH(g) ΔH
2 2 5 3 2 2 2 5 2ⅲ:CH =CHCONH (g)→CH =CHCN(g)+H O(g) ΔH
2 2 2 2 3
④在此生产条件下,酯类物质可能发生水解。
回答下列问题:
(1)总反应HOCH CH COOC H (g)+NH (g)→CH =CHCN(g)+C H OH(g)+2H O(g) ΔH= (用含ΔH 、ΔH 、
2 2 2 5 3 2 2 5 2 1 2
和ΔH 的代数式表示);
3
(2)进料混合气中 ,出料中四种物质( 、 、
n(HOCH CH COOC H ):n(C H OH)=1:2 CH =CHCOOC H CH =CHCN
2 2 2 5 2 5 2 2 5 2
C H OH、H O )的流量,(单位时间内出料口流出的物质的量)随时间变化关系如图:
2 5 2
①表示CH =CHCN的曲线是 (填“a”“b”或“c”);
2
②反应釜Ⅰ中加入C H OH的作用是 。
2 5
③出料中没有检测到CH =CHCONH 的原因是 。
2 2
④反应11h后,a、b、c曲线对应物质的流量逐渐降低的原因是 。
(3)催化剂TiO 再生时会释放CO ,可用氨水吸收获得NH HCO 。现将一定量的NH HCO 固体(含0.72g水)置于密闭
2 2 4 3 4 3
真空容器中,充入CO 和NH ,其中CO 的分压为100kPa,在27℃下进行干燥。为保证NH HCO 不分解,NH 的分
2 3 2 4 3 3
压应不低于 (已知 分解的平衡常数 );
kPa p(H O)=2.5×102kPa⋅mol-1×n(H O) NH HCO Kp=4×104 (kPa) 3
2 2 4 3
(4)以 为原料,稀硫酸为电解液,Sn作阴极,用电解的方法可制得 ,其阴极反应式
CH =CHCN Sn(CH CH CN)
2 2 2 4
。