文档内容
【赢在高考·黄金 8 卷】备战 2024 年高考化学模拟卷(浙江专用)
黄金卷 07
((考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Si 28 P 31 S 32 Cl 35.5 K
39 Ca 40 Ti 48 Cr 52 Mn 55 Fe 56 Cu 64 Zn 65 Br 80 Ag 108 Ba 137
第Ⅰ卷
一、单项选择题:共16题,每题3分,共48分。每题只有一个选项最符合题意。
1.下列物质属于离子晶体且含有非极性共价键的是( )
A.NaOH B.H O C.NaCl D.Na C O
2 2 2 2 4
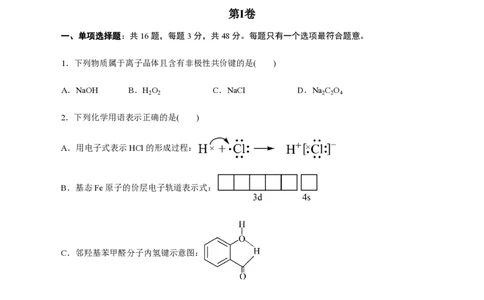
2.下列化学用语表示正确的是( )
A.用电子式表示HCl的形成过程:
B.基态Fe原子的价层电子轨道表示式:
C.邻羟基苯甲醛分子内氢键示意图:
D.NH 的VSEPR模型:
3
3.硫化氢是一种气体信号分子,人体中微量的 H S能有效预防心脏病。下列有关说法不正确的是
2
( )
A.H S 属于弱电解质
2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002B.H S可以使稀酸性高锰酸钾溶液褪色
2
C.H S 通入CuSO 溶液中无明显现象
2 4
D.人体内H S可由含硫蛋白质通过复杂反应产生
2
4.下列说法不正确的是( )
A.溴单质、氯气等虽然有毒,但可用于合成药物
B.NO 环境污染太大,工业生产中没有利用价值
x
C.纯碱溶液虽呈碱性,但在玻璃、造纸等工业中有着重要的应用
D.氯化铁、硫酸铜等溶液虽呈弱酸性,但常可用作消毒剂
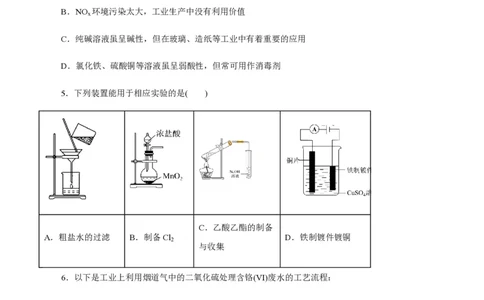
5.下列装置能用于相应实验的是( )
C.乙酸乙酯的制备
A.粗盐水的过滤 B.制备Cl D.铁制镀件镀铜
2
与收集
6.以下是工业上利用烟道气中的二氧化硫处理含铬(Ⅵ)废水的工艺流程:
设N 为阿伏加德罗常数的值,下列说法不正确的是( )
A
A.2CrO 2-+2H+ Cr O 2-+H O转化过程中,溶液颜色由黄色变为橙色
4 2 7 2
B.过程Ⅱ中SO 是还原剂,Cr3+为还原产物
2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002C.处理废水中的1mol CrO 2-(不考虑其它氧化剂存在),转移电子数为3N
4 A
D.烟道气可以用Na SO 或 Fe (SO ) 代替
2 3 2 4 3
7.N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.1mol苯甲醛分子中含键的数目为7N
A
B.1mol XeF 中氙的价层电子对数为4N
4 A
C.标准状况下,22.4L CH 和44.8L Cl 在光照下充分反应后的分子数为3N
4 2 A
D.25℃时,pH=2的醋酸溶液1L,溶液中含H的数目小于0.01N
A
8.下列说法不正确的是( )
A.煤在一定条件下可与H 直接作用,生成液体燃料
2
B.氢化植物油可用于生产人造奶油、起酥油等食品工业原料
C.乙醇和二甲醚互为同分异构体,两者的质谱图不完全相同
D.分子式为C H 且能被酸性KMnO 氧化成苯甲酸的有机物共有8种
11 16 4
9.下列方程式与所给事实不相符的是( )
A.硫酸亚铁溶液出现棕黄色沉淀:6FeSO +O +2H O=2Fe (SO ) +2Fe(OH) ↓
4 2 2 2 4 3 2
B.向银氨溶液中滴加乙醛溶液并水浴加热:CH CHO+2[Ag(NH ) ]++2OH-
3 3 2
CH COO-+2Ag↓+3NH +H O
3 3 2
C.乙炔制丙烯腈:CH≡CH+HCN CH =CHCN
2
D.用硫化亚铁除去废水中的汞离子:FeS(s)+Hg2+-(aq) HgS(s)+ Fe2+(aq)
10.甘草素是从甘草中提炼制成的甜味剂,其结构如图所示,下列说法正确的是( )
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002A.甘草素分子中无手性碳原子
B.甘草素分子中至少有5个碳原子共直线
C.甘草素可与HCN反应
D.1mol甘草素最多可消耗3molNaOH
11.前四周期元素V、W、X、Y、Z原子序数依次增大,V的基态原子有2个未成对电子,X的族序
数为周期数的3倍,X、Y、Z均不在同一周期,三者的最外层电子数之和为10,Z的价电子数是Y的3倍。
下列说法不正确的是( )
A.第一电离能:WX
B.Y与V形成的化合物中可能含非极性共价键
C.氢化物的稳定性:XWV
D.Y和Z两者对应的最高价氧化物的水化物可能会发生反应
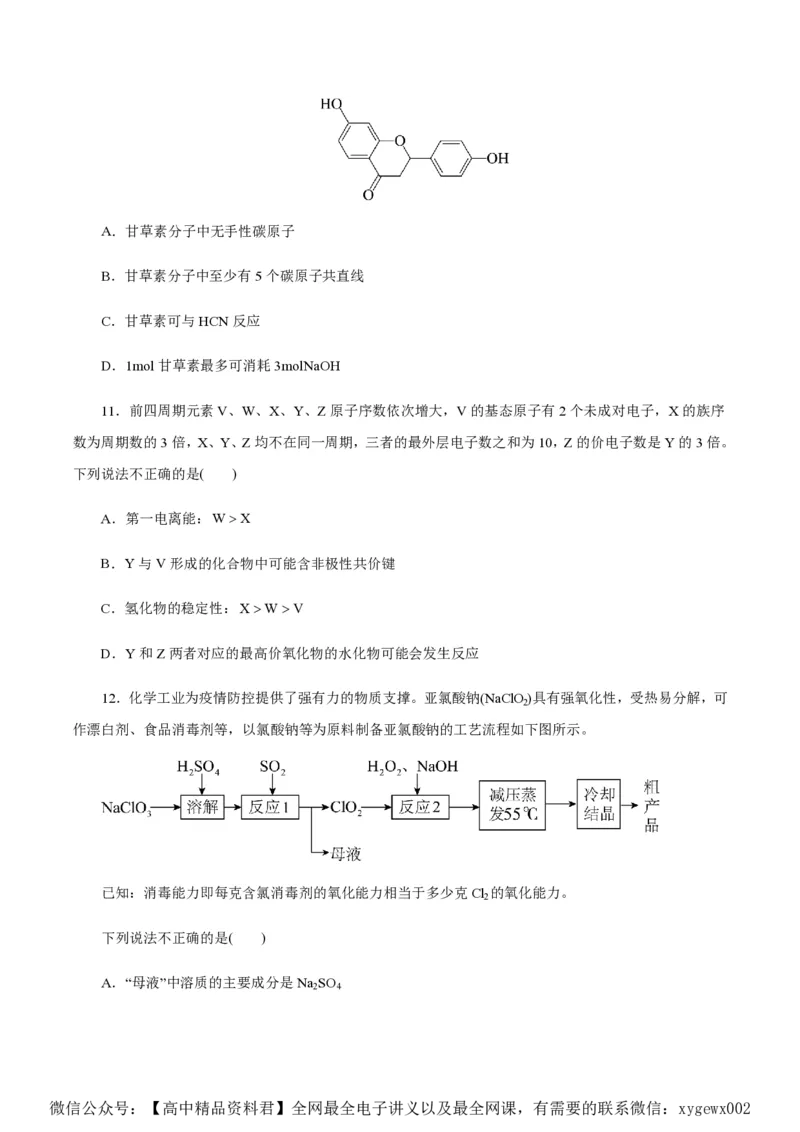
12.化学工业为疫情防控提供了强有力的物质支撑。亚氯酸钠(NaClO)具有强氧化性,受热易分解,可
2
作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如下图所示。
已知:消毒能力即每克含氯消毒剂的氧化能力相当于多少克Cl 的氧化能力。
2
下列说法不正确的是( )
A.“母液”中溶质的主要成分是Na SO
2 4
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002B.相同质量ClO 的消毒能力是Cl 的2.5倍
2 2
C.“反应2”中氧化剂与还原剂的物质的量之比为2∶1
D.“减压蒸发”可以降低蒸发时的温度,提高产品产率
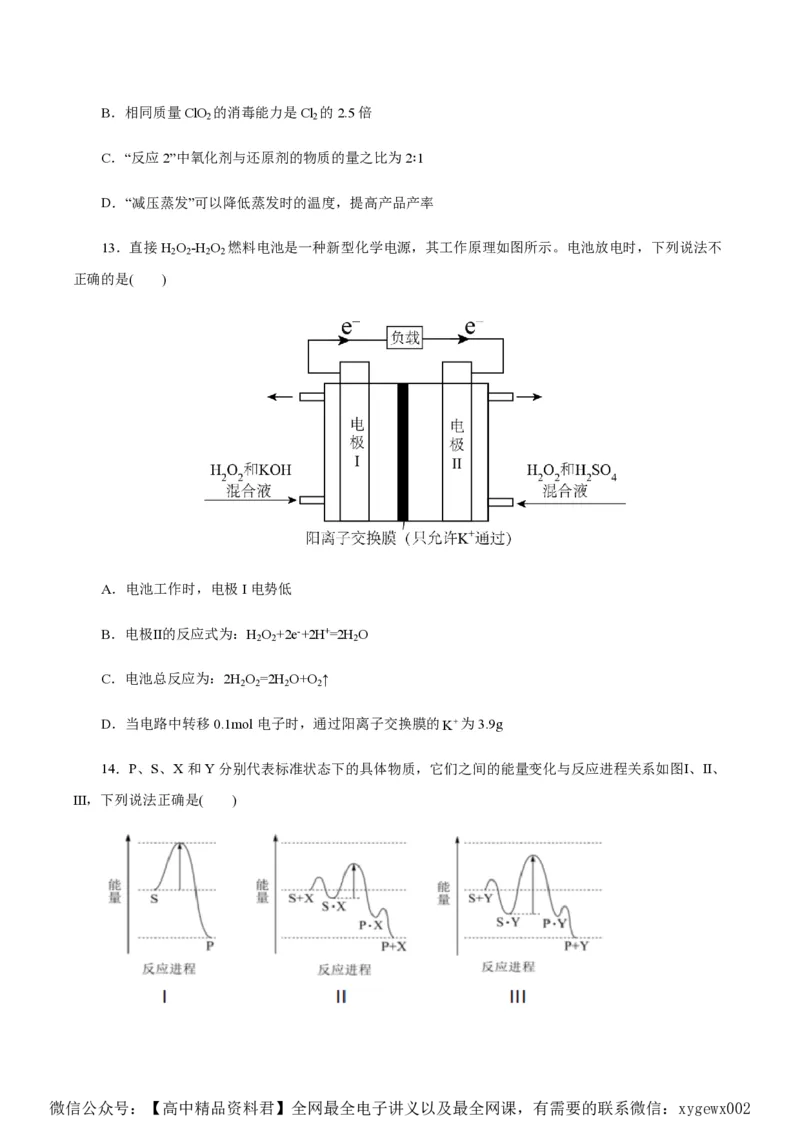
13.直接H O -H O 燃料电池是一种新型化学电源,其工作原理如图所示。电池放电时,下列说法不
2 2 2 2
正确的是( )
A.电池工作时,电极I电势低
B.电极Ⅱ的反应式为:H O +2e- +2H+=2H O
2 2 2
C.电池总反应为:2H O =2H O+O ↑
2 2 2 2
D.当电路中转移0.1mol电子时,通过阳离子交换膜的K为3.9g
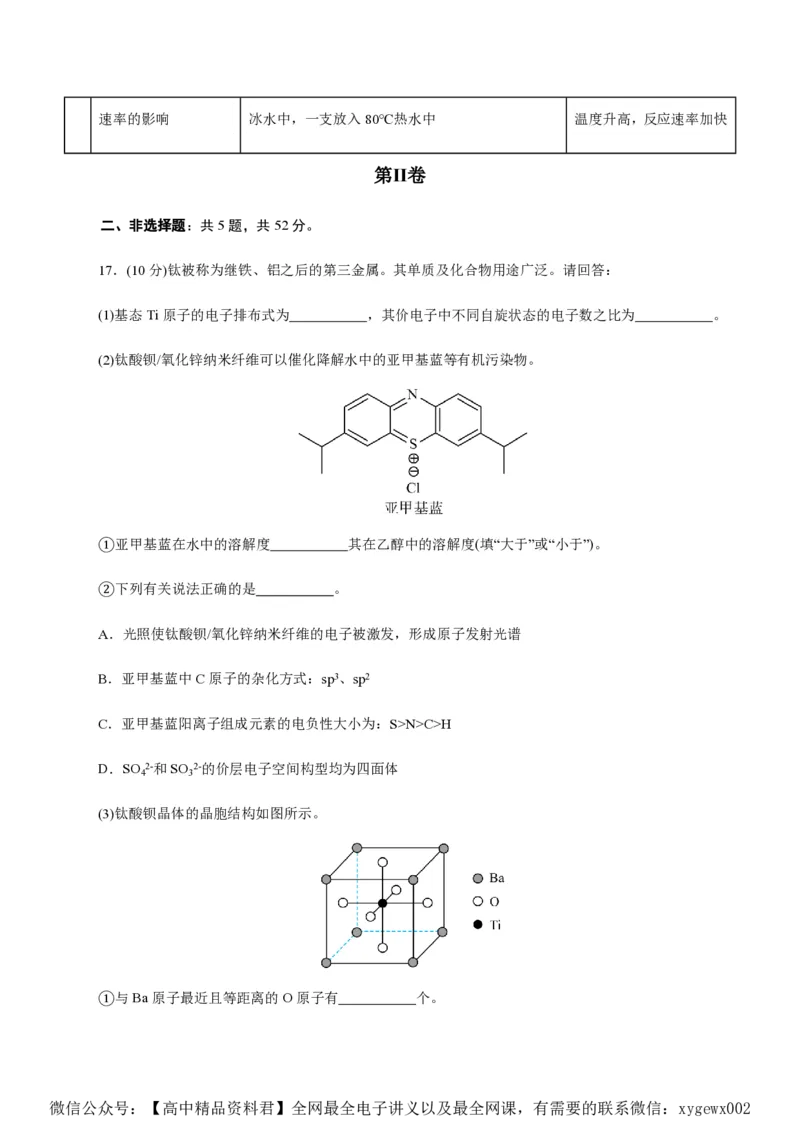
14.P、S、X和Y分别代表标准状态下的具体物质,它们之间的能量变化与反应进程关系如图Ⅰ、Ⅱ、
Ⅲ,下列说法正确是( )
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002A.在标准状态时,物质的ΔH: S<P
B.X和Y为催化剂,进程Ⅰ、Ⅱ、Ⅲ中:ΔH <ΔH <ΔH <0
1 2 3
C.反应S
P达平衡所需时间:进程Ⅰ<Ⅱ<Ⅲ
D.反应S
P平衡时P的产率:进程Ⅰ=Ⅱ=Ⅲ
15.氢氧化镁是常见难溶物,将过量氢氧化镁粉末置于水中达到溶解平衡:Mg(OH) (s) Mg2+
2
(aq)+ 2OH-(aq)。已知K [Mg(OH) ]=1.8×10-11,K (MgCO )=3.5×10-8;通常,溶液中某离子的浓度小于
sp 2 sp 3
1.0×10-5mol·L-1时,可以认为该离子已沉淀完全。下列有关说法不正确的是( )
A.滴入几滴稀硫酸,溶液的pH先下降后上升,最后保持一个稳定值
B.MgCO 的饱和溶液中c(Mg2+)>c(CO 2-)
3 3
C.NaOH溶液可使MgCO 较彻底地转化为Mg(OH)
3 2
D.氢氧化镁可处理印染厂的酸性废水,处理后c(Mg2+)=1.8×10-3mol·L-1,此时溶液呈碱性
16.下列实验方案设计、现象和结论均正确的是
目的 方案设计 现象和结论
检验乙醇是否发生消 将乙醇和浓H SO 共热产生的气体依次通入足量的 KMnO 溶液褪色,证明
2 4 4
A
去反应 KOH溶液、稀酸性KMnO 溶液 发生了消去反应
4
检验Fe2+与I-的还原 向含0.1mol FeI 的溶液中通入0.1mol Cl ,再滴加 溶液变蓝色,说明还原性
2 2
B
性强弱 淀粉溶液,观察现象 I->Fe2+
鉴别同为白色粉末状 分别取少量晶体于试管中,加入足量浓NaOH溶液 若试纸不变蓝色,说明该
C 晶体的尿素[CO(NH ) ] 加热,在试管口放置湿润的红色石蕊试纸,观察试 晶体为尿素,若试纸变蓝
2 2
和氯化铵 纸是否变色 色,说明该晶体为氯化铵
向两支试管各加入2mL0.1mol·L-1酸性KMnO 溶
D 4
探究温度对化学反应 80℃热水中褪色快,说明
液和2mL0.01mol·L-1H C O 溶液,将其中一支放入
2 2 4
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002速率的影响 冰水中,一支放入80℃热水中 温度升高,反应速率加快
第Ⅱ卷
二、非选择题:共5题,共52分。
17.(10分)钛被称为继铁、铝之后的第三金属。其单质及化合物用途广泛。请回答:
(1)基态Ti原子的电子排布式为 ,其价电子中不同自旋状态的电子数之比为 。
(2)钛酸钡/氧化锌纳米纤维可以催化降解水中的亚甲基蓝等有机污染物。
①亚甲基蓝在水中的溶解度 其在乙醇中的溶解度(填“大于”或“小于”)。
②下列有关说法正确的是 。
A.光照使钛酸钡/氧化锌纳米纤维的电子被激发,形成原子发射光谱
B.亚甲基蓝中C原子的杂化方式:sp3、sp2
C.亚甲基蓝阳离子组成元素的电负性大小为:S>N>C>H
D.SO 2-和SO 2-的价层电子空间构型均为四面体
4 3
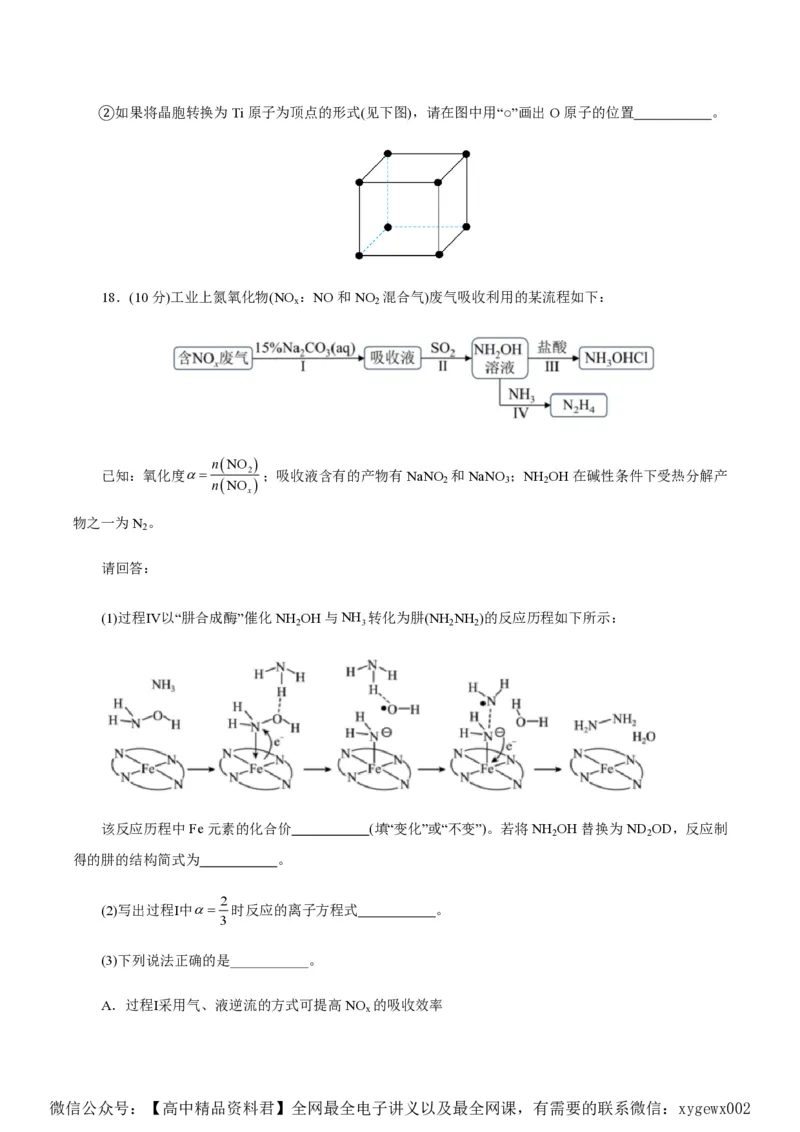
(3)钛酸钡晶体的晶胞结构如图所示。
①与Ba原子最近且等距离的O原子有 个。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002②如果将晶胞转换为Ti原子为顶点的形式(见下图),请在图中用“○”画出O原子的位置 。
18.(10分)工业上氮氧化物(NO :NO和NO 混合气)废气吸收利用的某流程如下:
x 2
nNO
已知:氧化度 2 ;吸收液含有的产物有NaNO 和NaNO ;NH OH在碱性条件下受热分解产
nNO 2 3 2
x
物之一为N 。
2
请回答:
(1)过程Ⅳ以“肼合成酶”催化NH OH与NH 转化为肼(NH NH )的反应历程如下所示:
2 3 2 2
该反应历程中Fe元素的化合价 (填“变化”或“不变”)。若将NH OH替换为ND OD,反应制
2 2
得的肼的结构简式为 。
2
(2)写出过程Ⅰ中 时反应的离子方程式 。
3
(3)下列说法正确的是___________。
A.过程Ⅰ采用气、液逆流的方式可提高NO 的吸收效率
x
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002B.SO 的键角小于
2
C.NH OH可作为配体,与Zn2+等金属离子形成配合物
2
D.NH OH的水溶液显弱碱性,且K NH OHK NH H O
2 b 2 b 3 2
(4) NH OHCl是一种理想还原剂,氧化产物对环境友好,写出NH OHCl还原FeCl 的化学方程
3 3 3
式 。
(5)设计实验证明NH OH中存在N元素 。
2
19.(10分)在“碳达峰、碳中和”的明确目标下,利用CO、CO 的甲烷化制备人造天然气既可以避免碳
2
排放造成的资源浪费和环境污染,又可以缩短碳循环获得清洁能源。甲烷化工艺中主要涉及到如下反应:
甲烷化反应i.CO(g)+3H (g) CH (g)+H O(g) ΔH =-206.3kJ·mol−1
2 4 2 1
甲烷化反应ii.CO (g)+4H (g) CH (g)+2H O(g) ΔH =-164.9kJ·mol−1
2 2 4 2 2
副反应iii.CO (g)+H (g) CO(g)+H O(g) ΔH
2 2 2 3
副反应 iv.CH (g) C(s)+2H (g) ΔH =+74.8kJ·mol−1
4 2 4
(1)计算ΔH = kJ∙mol−1
3
(2)为了研究Ni/TiO 在光热和热催化过程中CO 转化率和 CH 选择性随温度的变化,将 CO合成气(含
2 4
23%CO、69%H₂和8%N₂)通入反应器,在恒压及一定时间内进行反应,测得以下数据:[α表示转化率,S(CH )
4
表示得到甲烷物质的量与消耗CO 的物质的量之比]
光热催化 热催化
α(CO) S(CH ) α(CO) S(CH )
4 4
250 90% 85% 0% 0%
300 92% 82% 88% 78%
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002350 96% 84% 89% 79%
400 95% 83% 92% 78%
450 92% 82% 91% 79%
①光热催化时CO甲烷化的活化能E 热催化 CO 甲烷化的活化能E (填“大于”或者“小于”)。
a a
②当温度高于400℃时,热催化下CO转化率降低的原因是 。
(3)某温度下,恒容容器中充入1mol∙L−1CO 和4mol∙L−1 H ,若只发生反应ii、iii,平衡时测得α(CO )
2 2 2
为50%、S(CH )为90%,反应iii的平衡常数为 。[S(CH )表示得到甲烷物质的量与消耗 CO
4 4 2
的物质的量之比]。
(4)为了进一步研究CO 的甲烷化反应,科学家研究催化剂M/TiO (M 表示 Ni 或Ru)在300℃光照的
2 2
条件下进行反应,催化反应的核心过程表示如下:
①关于核心反应过程,下列说法正确的是 。
A.步骤I中生成了非极性键
B.步骤Ⅲ发生的反应为COOHCO+OH(X代表吸附态中间体)
C.步骤Ⅳ中碳元素发生还原反应
D.整个反应过程中只有金属M起到催化作用
②研究发现,光诱导电子从TiO 转移到M,富电子的M表面可以促进H 的解离和CO 的活化,从而
2 2 2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002提高反应效率。已知Ni 和Ru 的电负性分别为1.91和2.20,使用Ru/TiO 催化剂的反应效率 (填“高
2
于”或“低于”)使用 Ni/TiO 作催化剂的反应效率。
2
20.(10分)某兴趣小组设计如图实验装置制备次磷酸钠(NaH PO )。
2 2
已知:①白磷(P )在空气中可自燃,与过量烧碱溶液混合,80~90℃时反应生成NaH PO 和PH 。
4 2 2 3
②PH 是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成NaH PO 。
3 2 2
请回答:
(1)①仪器a的名称是 。
②仪器b组成的装置的作用是 。
(2)检查装置气密性后,应先打开K通入N 一段时间,目的是 。
2
(3)仪器c中充分反应后生成NaH PO 和NaCl,经过一系列操作可获得固体NaH PO 。相关物质的溶解
2 2 2 2
度(S)如下:
S(25℃) S(100℃)
NaCl 37 39
NaH PO
2
100 667
2
从下列选项中选择合理的仪器和操作,补全如下步骤。[“___________”上填写一件最关键仪器,
“( )”内填写一种操作,均用字母表示]。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002取仪器c中溶液,用蒸发皿( )→用 (趁热过滤)→用烧杯(冷却结晶)→用漏斗(过
滤得到NaH PO )→洗涤→干燥→NaH PO 粗产品。
2 2 2 2
仪器:d.普通三角漏斗;e.铜制保温漏斗;
操作:f.蒸发浓缩至有大量晶体析出;g.蒸发浓缩至溶液表面出现晶膜。
(4)下列有关说法不正确的是___________。
A.次磷酸(H PO )是三元酸
3 2
B.为加快反应速率,投料前应先在通风橱内将白磷碾成薄片状
C.反应结束后应继续通入N 一段时间,可提高NaH PO 产率
2 2 2
D.d中所盛硫酸铜溶液可用酸性高锰酸钾溶液代替
(5)产品纯度测定:取产品x g配成100 mL溶液,取10 mL于锥形瓶中,酸化后加入50 mL0.1000
mol/L的NH Fe(SO ) 溶液,以邻二氮菲做指示剂,再用0.1000 mol/L的硫酸铈滴定至终点,平均消耗V
4 4 2
mL。相关反应的离子方程式为:H O+H PO -+2Fe3+=H PO -+2Fe2++2H+、Ce4++Fe2+=Ce3++Fe3+,产品纯度表
2 2 2 2 3
达式为 (用含x、V的式子表示)。
21.(12分)抗肿瘤药物他莫昔芬的一种合成路线如下图所示:
已知: HBr
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002H+/H2O
(1)化合物B官能团名称 。
(2)下列说法正确的是___________。
A.反应C→D可能得到副产物
B.由化合物A和B生成C的反应属于加成反应
C.化合物F具有碱性,能和盐酸反应生成盐和水
D.他莫昔芬存在顺反异构现象
(3)化合物G的结构简式是 。
(4)写出E→F的化学方程式 。
(5)参照以上合成路线,设计用 和CH I为原料制备 的合成路线(无机试剂
3
任选,限四步): 。
(6)写出同时符合下列条件的化合物C的3种同分异构体的结构简式 。
①IR谱检测表明分子中含有1个-COOH和1个-CH ;
3
②分子中含有2个苯环,且苯环上共有4种不同化学环境的氢原子。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002