文档内容
注意事项:
1本试卷分第I卷(选择题)和第ll卷(非选择题)两部分。答卷前,考生务必将自己的姓名、
准考证号填写在答题卡上。
2回答第I卷时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如
需改动,用橡皮擦干净后,再选涂其它答案标号。写在本试卷上无效。
3回答第II卷时,将答案写在答题卡上。写在本试卷上无效。
4考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H1 C 12 N14 O16 Na 23 C1 35.5 Zn 65
第 I 卷
4.下列实验操作正确的是
A.可用氨水除去试管内壁上的银镜
B.硅酸钠溶液应保存在带玻璃塞的试剂瓶中
C.将三氯化铁溶液蒸干,可制得无水三氯化铁
D.锌与稀硫酸反应时,要加大反应速率可滴加少量硫酸铜
5.分子式为C H 的单取代芳烃,其可能的结构有
10 14
A.2种 B.3种 C.4种 D.5种
6.将0.195g锌粉加入到20.0mL的0.100 mol·L-1MO +溶液中,恰好完全反应,则还原产物
2
可能是
A.M B.M2+ C.M3+ D.MO2+
二、选择题:本题共6小题。每小题4分,共24分。每小题有一个或两个选项符合题意,
若正确答案只包括一个选项,多选得0分;若正确答案包括两个选项,只选一个且正确得2
分,选两个且都正确得4分,但只要选错一个就得0分。
7.N 为阿伏加德罗常数的数值,下列说法中正确的是
A
A.在密闭容器中加入l.5mol H 和0.5molN ,充分反应后可得到NH 分子数为N
2 2 3 A
B.一定条件下,2.3g的Na完全与O 反应生成3.6g产物时失去的电子数为0.1N
2 A
C.1.0L的0.1 mol·L-1Na S溶液中含有的S2-离子数为0.1N
2 A
第1页 | 共6页D.标准状况下,22.4L的CCl 中含有的CCl 分子数为N
4 4 A
11.25℃时,a mol·L-1一元酸HA与b mol·L-1NaOH等体积混合后,pH为7,则下列关系一
定正确的是
A.a=b B.a>b C.c (A-)= c(Na+) D.c (A-)< c(Na+)
12.能正确表示下列反应的离子方程式为
A.碳酸氢钠溶液中滴入氢氧化钙溶液:HCO -+OH–= CO 2-+ H O
3 3 2
B.二氧化硫通入次氯酸钠溶液:SO + ClO- + 2OH–= SO 2-+Cl-+ H O
2 4 2
C.硫化钡加入稀硫酸:BaS+ 2H+ = H S↑+ Ba2+
2
D.新制的氧化铝可溶于氢氧化钠溶液:Al O +2OH–=2AlO –+H O
2 3 2 2
第 II 卷
本卷包括必考题和选考题两部分。第l3题~第17题为必考题,每个试题考生都必需做答。
第l8题~第20题为选考题,考生根据要求做答。
14.(9分)
在FeCl 溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:
3
I:向废液中投入过量铁屑,充分反应后分离出固体和滤液;
II:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
己知:Ksp[Fe(OH) ]= 4.0×10-38
3
回答下列问题:
[来源:学科网]
(1)FeCl 蚀刻铜箔反应的离子方程式为 :
3
(2)过程I 加入铁屑的主要作用是 ,分离得到固体的主要成分是 ,从固
第2页 | 共6页体中分离出铜需采用的方法是 ;
(3)过程II中发生反应的化学方程式为 ;
(4)过程II中调节溶液的pH为5,金属离子浓度为 。(列式计算)
16.(9分)
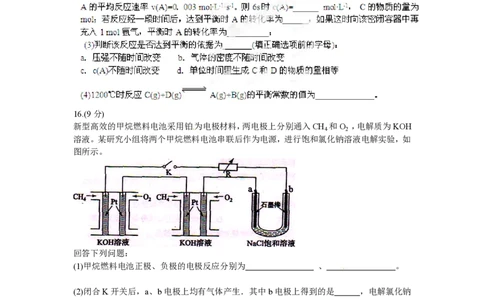
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH 和O ,电解质为KOH
4 2
溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如
图所示。
回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为 、 。
[来源:学|
科|网Z|X|X|K]
(2)闭合K开关后,a、b电极上均有气体产生.其中b电极上得到的是 ,电解氯化钠
溶液的总反应方程式为 ;
(3)若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上通过电解池的电量为
(法拉第常数F=9.65×l04C.mol-1,列式计算),最多能产生的氯气体积为 L(标准
状况)。
17.(9分)
实验室制备1,2-二溴乙烷的反应原理如下:
第3页 | 共6页可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。
用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:
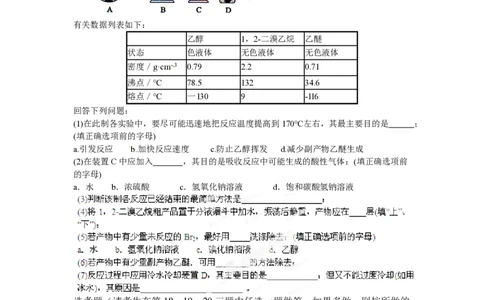
有关数据列表如下:
乙醇 1,2-二溴乙烷 乙醚
状态 色液体 无色液体 无色液体
密度/g·cm-3 0.79 2.2 0.71
沸点/℃ 78.5 132 34.6
熔点/℃ 一l30 9 -1l6
回答下列问题:
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是 ;
(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入 ,其目的是吸收反应中可能生成的酸性气体:(填正确选项前
的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
选考题(请考生在第18、19、20三题中任选一题做答,如果多做,则按所做的
第一题计分。做答时用2B铅笔在答题卡上把所选题目的题号涂黑。)
第18、19、20三题的第I题为选择题,在给出的四个选项中,有两项是符合题
目要求的,请将符合题目要求的选项标号填在答题卡相应位置;第II题为非选
择题,请在答题卡相应位置做答并写明小题号。
18.[选修5——有机化学基础] (20分)
18-I(6分)下列化合物在核磁共振氢谱中能出现两组峰.且其峰面积之比为3:1的有
A.乙酸异丙酯 B.乙酸叔丁酯
C.对二甲苯 D.均三甲苯
18一II(14分)
化合物A是合成天然橡胶的单体,分子式为C H 。A的一系列反应如下(部分反应条件略
5 8
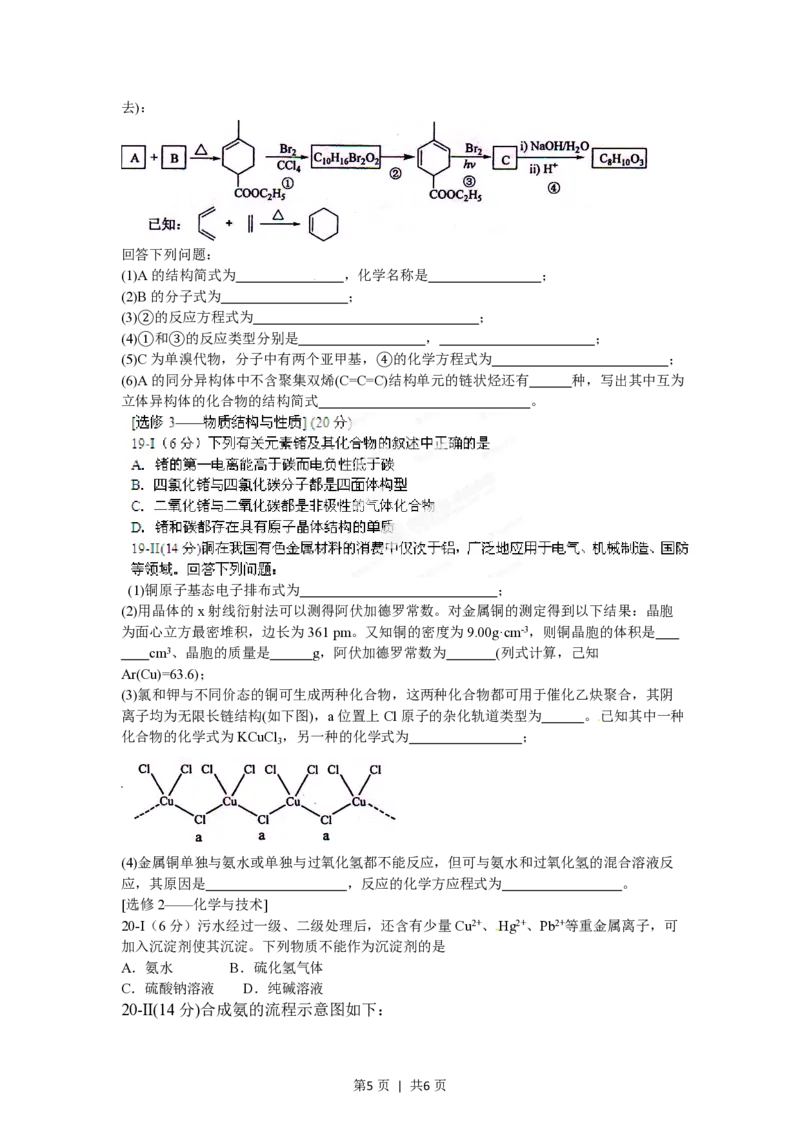
第4页 | 共6页去):
回答下列问题:
(1)A的结构简式为 ,化学名称是 ;
[来源:学+科+网Z+X+X+K]
(2)B的分子式为 ;
(3)②的反应方程式为 ;
(4)①和③的反应类型分别是 , ;
(5)C为单溴代物,分子中有两个亚甲基,④的化学方程式为 ;
(6)A的同分异构体中不含聚集双烯(C=C=C)结构单元的链状烃还有 种,写出其中互为
立体异构体的化合物的结构简式 。
[来源:学,科,网]
(1)铜原子基态电子排布式为 ;
(2)用晶体的x射线衍射法可以测得阿伏加德罗常数。对金属铜的测定得到以下结果:晶胞
为面心立方最密堆积,边长为361 pm。又知铜的密度为9.00g·cm-3,则铜晶胞的体积是
cm3、晶胞的质量是 g,阿伏加德罗常数为 (列式计算,己知
Ar(Cu)=63.6);
(3)氯和钾与不同价态的铜可生成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴
离子均为无限长链结构(如下图),a位置上Cl原子的杂化轨道类型为 。已知其中一种
化合物的化学式为KCuCl ,另一种的化学式为 ;
3
(4)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反
应,其原因是 ,反应的化学方应程式为 。
[选修2——化学与技术]
20-I(6分)污水经过一级、二级处理后,还含有少量Cu2+、Hg2+、Pb2+等重金属离子,可
加入沉淀剂使其沉淀。下列物质不能作为沉淀剂的是
A.氨水 B.硫化氢气体
C.硫酸钠溶液 D.纯碱溶液
20-II(14分)合成氨的流程示意图如下:
第5页 | 共6页回答下列问题:
第6页 | 共6页