文档内容
专题97 工艺流程——非金属元素载体
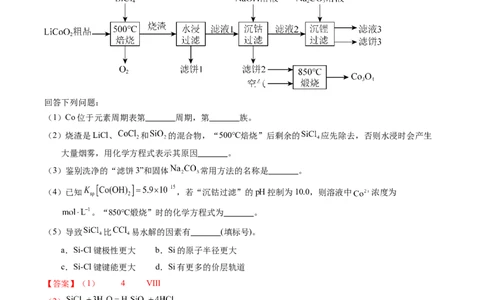
1.【2023年湖北卷】 是生产多晶硅的副产物。利用 对废弃的锂电池正极材料 进行氯化
处理以回收Li、Co等金属,工艺路线如下:
回答下列问题:
(1)Co位于元素周期表第 周期,第 族。
(2)烧渣是LiCl、 和 的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会产生
大量烟雾,用化学方程式表示其原因 。
(3)鉴别洗净的“滤饼3”和固体 常用方法的名称是 。
(4)已知 ,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为
。“850℃煅烧”时的化学方程式为 。
(5)导致 比 易水解的因素有 (填标号)。
a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
【答案】(1) 4 Ⅷ
(2)
(3)焰色反应
(4)
(5)abd
【解析】由流程和题中信息可知, 粗品与 在500℃焙烧时生成氧气和烧渣,烧渣是LiCl、
和 的混合物;烧渣经水浸、过滤后得滤液1和滤饼1,滤饼1的主要成分是 和 ;
滤液1用氢氧化钠溶液沉钴,过滤后得滤饼2(主要成分为 )和滤液2(主要溶质为LiCl);滤饼2置于空气中在850℃煅烧得到 ;滤液2经碳酸钠溶液沉锂,得到滤液3和滤饼3,滤饼3
为 。
(1)Co是27号元素,其原子有4个电子层,其价电子排布为 ,元素周期表第8、9、10三个纵行
合称第Ⅷ族,因此,其位于元素周期表第4周期、第Ⅷ族。
(2)“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大量烟雾,由此可知,四氯化硅与可水
反应且能生成氯化氢和硅酸,故其原因是: 遇水剧烈水解,生成硅酸和氯化氢,该反应的化学
方程式为 。
(3)洗净的“滤饼3”的主要成分为 ,常用焰色反应鉴别 和 , 的焰色反应为
紫红色,而 的焰色反应为黄色。故鉴别“滤饼3”和固体 常用方法的名称是焰色反应。
(4)已知 ,若“沉钴过滤”的pH控制为10.0,则溶液中
, 浓度为 。“850℃煅烧”时,
与 反应生成 和 ,该反应的化学方程式为 。
(5)a.Si-Cl键极性更大,则 Si-Cl键更易断裂,因此, 比 易水解,a有关;
b.Si的原子半径更大,因此, 中的共用电子对更加偏向于 ,从而导致Si-Cl键极性更大,且Si原
子更易受到水电离的 的进攻,因此, 比 易水解,b有关;
c.通常键能越大化学键越稳定且不易断裂,因此,Si-Cl键键能更大不能说明Si-Cl更易断裂,故不能说明
比 易水解,c无关;
d.Si有更多的价层轨道,因此更易与水电离的 形成化学键,从而导致 比 易水解,d有关;
综上所述,导致 比 易水解的因素有abd。
2.【2023年湖北卷】超纯 是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开
发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯 方面取得了显著成果,工
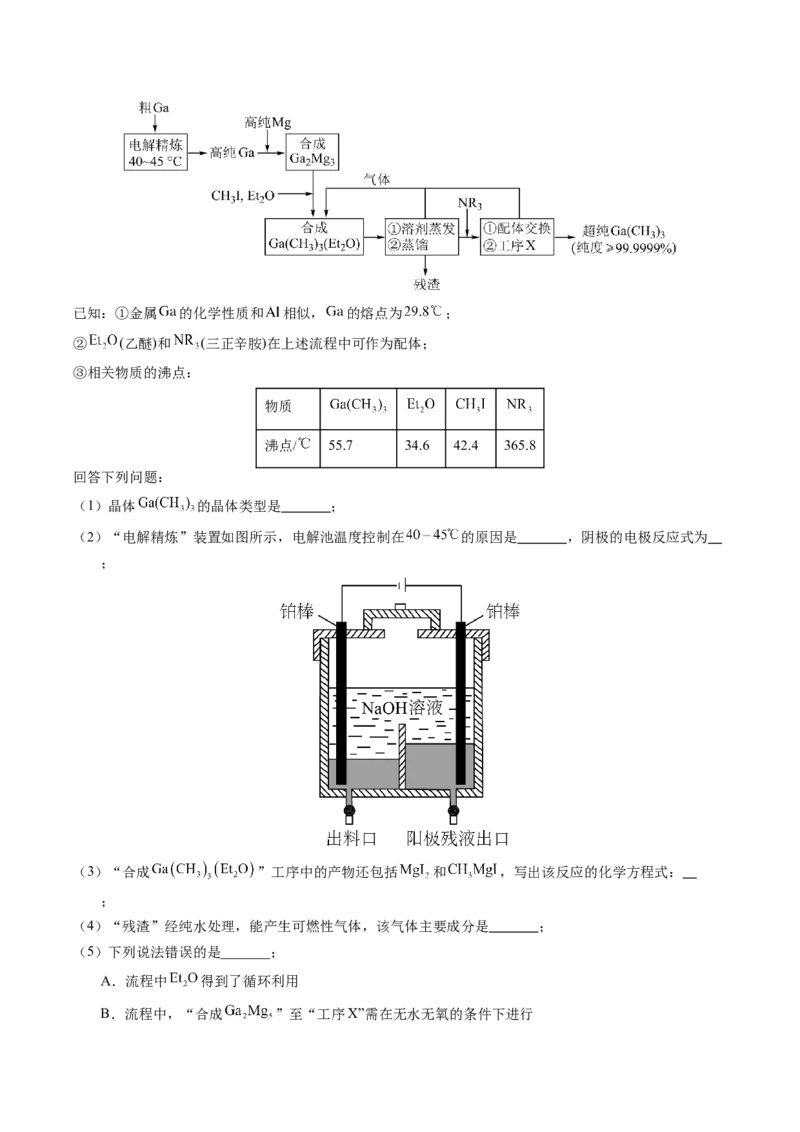
业上以粗镓为原料,制备超纯 的工艺流程如下:已知:①金属 的化学性质和 相似, 的熔点为 ;
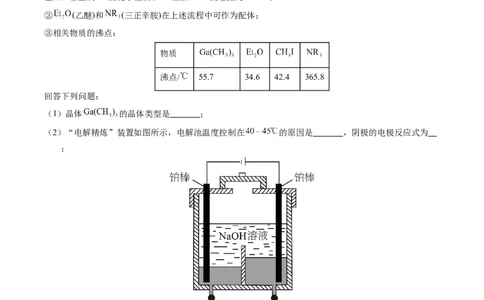
② (乙醚)和 (三正辛胺)在上述流程中可作为配体;
③相关物质的沸点:
物质
沸点/ 55.7 34.6 42.4 365.8
回答下列问题:
(1)晶体 的晶体类型是 ;
(2)“电解精炼”装置如图所示,电解池温度控制在 的原因是 ,阴极的电极反应式为
;
(3)“合成 ”工序中的产物还包括 和 ,写出该反应的化学方程式:
;
(4)“残渣”经纯水处理,能产生可燃性气体,该气体主要成分是 ;
(5)下列说法错误的是_______;
A.流程中 得到了循环利用
B.流程中,“合成 ”至“工序X”需在无水无氧的条件下进行C.“工序X”的作用是解配 ,并蒸出
D.用核磁共振氢谱不能区分 和
(6)直接分解 不能制备超纯 ,而本流程采用“配体交换”工艺制备超纯
的理由是 ;
(7)比较分子中的 键角大小: (填“>”“<”或“=”),其原因
是 。
【答案】(1)分子晶体
(2) 保证Ga为液体,便于纯Ga流出 Ga3++3eˉ=Ga
(3)8CHI+2EtO+Ga Mg=2 +3 +2 ;
3 2 2 5
(4)CH
4
(5)D
(6)NR 沸点较高,易与Ga(CH ) 分离,EtO的沸点低于Ga(CH ),一起气化,难以得到超纯Ga(CH )
3 3 3 2 3 3 3 3
(7) > Ga(CH) 中Ga为sp2杂化,所以为平面结构,而Ga(CH )(Et O)中Ga为sp3杂化,所以
3 3 3 3 2
为四面体结构,故夹角较小
【解析】以粗镓为原料,制备超纯 ,粗Ga经过电解精炼得到纯Ga,Ga和Mg反应生产
GaMg,GaMg 和CHI、EtO反应生成 、MgI 和CHMgI,然后经过蒸发溶剂、蒸
2 5 2 5 3 2 2 3
馏,除去残渣MgI 、CHMgI,加入NR 进行配体交换、进一步蒸出得到超纯 ,EtO重复利
2 3 3 2
用,据此解答。
(1)晶体 的沸点较低,晶体类型是分子晶体;
(2)电解池温度控制在 可以保证Ga为液体,便于纯Ga流出;粗Ga在阳极失去电子,阴极得到
Ga,电极反应式为Ga3++3eˉ=Ga;
(3)“合成 ”工序中的产物还包括 和 ,该反应的化学方程式
8CHI+2EtO+Ga Mg=2 +3 +2 ;
3 2 2 5
(4)“残渣”含 ,经纯水处理,能产生可燃性气体CH;
4
(5)A.根据分析,流程中 得到了循环利用,A正确;
B. 容易和水反应,容易被氧化,则流程中,“合成 ”至“工序X”需在无水无氧
的条件下进行,B正确;
C. “配体交换”得到 ,“工序X”先解构 后蒸出 ,C正确;
D.二者甲基的环境不同,核磁共振氢谱化学位移不同,用核磁共振氢谱能区分 和 ,D错误;
故选D;(6)直接分解 时由于EtO的沸点较低,与Ga(CH ) 一起蒸出,不能制备超纯 ,
2 3 3
而本流程采用“配体交换”工艺制备超纯 的理由是,根据题给相关物质沸点可知,NR 沸点
3
远高于Ga(CH ),与Ga(CH ) 易分离;
3 3 3 3
(7)分子中的 键角 > ,其原因是Ga(CH ) 中Ga为sp2杂化,所以为
3 3
平面结构,而Ga(CH )(Et O)中Ga为sp3杂化,所以为四面体结构,故夹角较小。
3 3 2
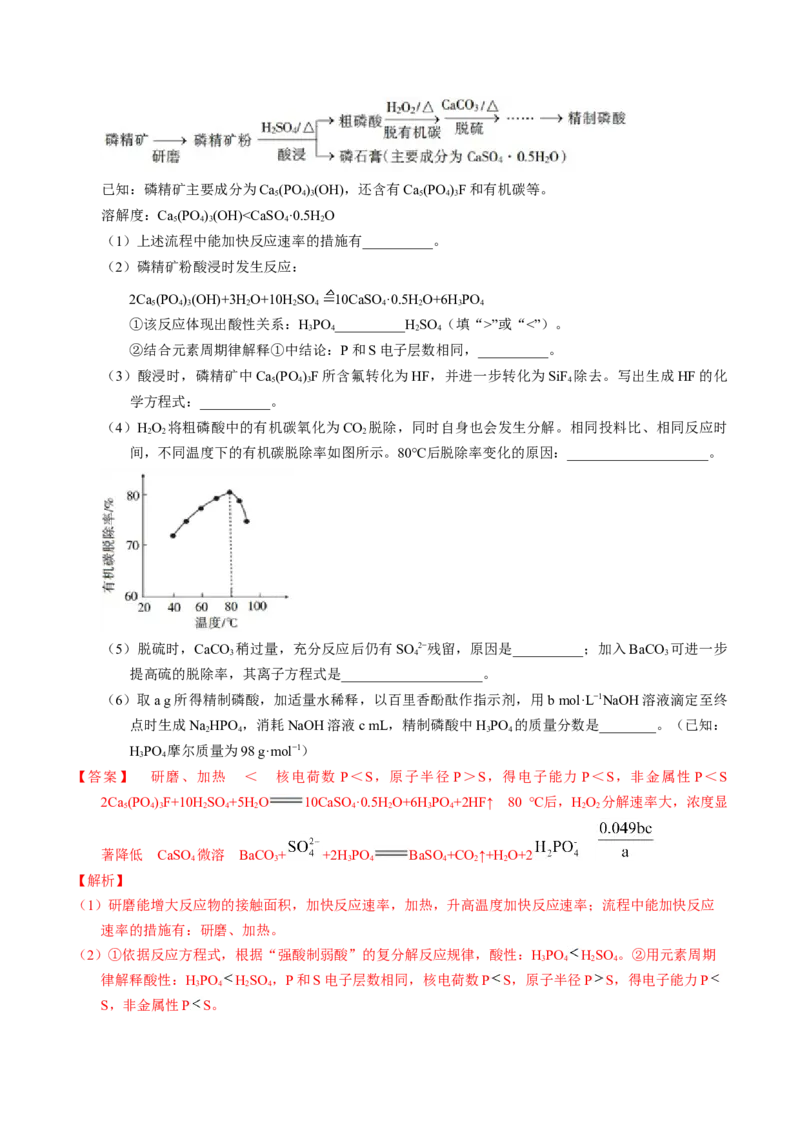
3.【2023年6月浙江卷】工业上煅烧含硫矿物产生的 可以按如下流程脱除或利用。
已知:
请回答:
(1)富氧煅烧燃煤产生的低浓度的 可以在炉内添加 通过途径Ⅰ脱除,写出反应方程式
。
(2)煅烧含硫量高的矿物得到高浓度的 ,通过途径Ⅱ最终转化为化合物A。
①下列说法正确的是 。
A.燃煤中的有机硫主要呈正价 B.化合物A具有酸性
C.化合物A是一种无机酸酯 D.工业上途径Ⅱ产生的 也可用浓 吸收
②一定压强下,化合物A的沸点低于硫酸的原因是 。
(3)设计实验验证化合物A中含有S元素 ;写出实验过程中涉及的反应方程式 。
【答案】(1)
(2) BCD 硫酸分子能形成更多的分子间氢键
(3) 取化合物A加入足量氢氧化钠,反应完全后加入盐酸酸化,无明显现象,再加入氯化钡生成白
色沉淀,说明A中含有S元素 +2NaOH=CHOH+Na SO +H O、
3 2 4 2
NaSO +BaCl =BaSO ↓+2NaCl
2 4 2 4
【解析】含硫矿物燃烧生成二氧化硫,二氧化硫和氧气、碳酸钙生成硫酸钙和二氧化碳,二氧化硫被氧气
氧化为三氧化硫,三氧化硫和等物质量的甲醇发生已知反应生成A: ;(1)氧气具有氧化性,能被四价硫氧化为六价硫,二氧化硫、空气中氧气、碳酸钙高温生成硫酸钙和二
氧化碳,反应为 ;
(2)①A.硫的电负性大于碳、氢等,故燃煤中的有机硫主要呈负价,A错误;
B.根据分析可知,化合物A分子中与硫直接相连的基团中有-OH,故能电离出氢离子,具有酸性,B正
确;
C.化合物A含有 基团,类似酯基-COO-结构,为硫酸和醇生成的酯,是一种无机酸酯,C正确;
D.工业上途径Ⅱ产生的 也可用浓 吸收用于生产发烟硫酸,D正确;
故选BCD;
②一定压强下,化合物A分子只有1个-OH能形成氢键,而硫酸分子中有2个-OH形成氢键,故导致A的
沸点低于硫酸;
(3)由分析可知,A为 ,A碱性水解可以生成硫酸钠、甲醇,硫酸根离子能和氯化钡生
成不溶于酸的硫酸钡沉淀,故实验设计为:取化合物A加入足量氢氧化钠,反应完全后加入盐酸酸化,
无明显现象,再加入氯化钡生成白色沉淀,说明A中含有S元素;涉及反应为:
+2NaOH=CHOH+Na SO +H O、NaSO +BaCl =BaSO ↓+2NaCl。
3 2 4 2 2 4 2 4
4.(2021·全国甲卷真题)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答下列
问题:
(1) 的一种制备方法如下图所示:
①加入 粉进行转化反应的离子方程式为_______,生成的沉淀与硝酸反应,生成_______后可循环使
用。
②通入 的过程中,若氧化产物只有一种,反应的化学方程式为_______;若反应物用量比
时,氧化产物为_______;当 ,单质碘的收率会降低,原
因是_______。(2)以 为原料制备 的方法是:先向 溶液中加入计量的 ,生成碘化物;再向混合溶
液中加入 溶液,反应得到 ,上述制备 的总反应的离子方程式为_______。
(3) 溶液和 溶液混合可生成 沉淀和 ,若生成 ,消耗的 至少为_______ 。
在 溶液中可发生反应 。实验室中使用过量的 与 溶液反应后,过滤,滤液经水
蒸气蒸馏可制得高纯碘。反应中加入过量 的原因是_______。
【答案】
(1)①2AgI+Fe=2Ag+ Fe2++2I- AgNO ②FeI+Cl= I +FeCl I、FeCl I 被过量的 进一
3 2 2 2 2 2 3 2
步氧化
(2)
(3)4 防止单质碘析出
【解析】
(1) ①由流程图可知悬浊液中含AgI ,AgI可与Fe反应生成FeI 和Ag,FeI 易溶于水,在离子方程式
2 2
中能拆,故加入 粉进行转化反应的离子方程式为2AgI+Fe=2Ag+ Fe2++2I-,生成的银能与硝酸反应生
成硝酸银参与循环中,故答案为:2AgI+Fe=2Ag+ Fe2++2I-;AgNO;
3
②通入 的过程中,因I-还原性强于Fe2+, 先氧化还原性强的I-,若氧化产物只有一种,则该氧化产物
只能是I,故反应的化学方程式为FeI+Cl= I +FeCl ,若反应物用量比 时即 过
2 2 2 2 2
量,先氧化完全部I-再氧化Fe2+,恰好将全部I-和Fe2+氧化,故氧化产物为I、FeCl ,当
2 3
即 过量特别多,多余的氯气会与生成的单质碘以及水继续发生氧化还原反应,
单质碘的收率会降低,故答案为:FeI+Cl= I +FeCl ;I、FeCl ;I 被过量的 进一步氧化;
2 2 2 2 2 3 2
(2)先向 溶液中加入计量的 ,生成碘化物即含I-的物质;再向混合溶液中(含I-)加入
溶液,反应得到 ,上述制备 的两个反应中I-为中间产物,总反应为 与 发生氧化还
原反应,生成 和 ,根据得失电子守恒、电荷守恒]及元素守恒配平离子方程式即可得:
,故答案为: ;
(3) 溶液和 溶液混合可生成 沉淀和 ,化学方程式为4KI+2CuSO =2CuI +I +2K SO ,
4 2 2 4
若生成 ,则消耗的 至少为4mol;反应中加入过量 ,I-浓度增大,可逆反应 平衡
右移,增大 溶解度,防止 升华,有利于蒸馏时防止单质碘析出,故答案为:4;防止单质碘析出。
5.【2018新课标1卷】焦亚硫酸钠(NaSO )在医药、橡胶、印染、食品等方面应用广泛。回答下列问
2 2 5
题:
(1)生产 NaSO ,通常是由 NaHSO 过饱和溶液经结晶脱水制得。写出该过程的化学方程式
2 2 5 3
__________。
(2)利用烟道气中的SO 生产NaSO 的工艺为:
2 2 2 5①pH=4.1时,Ⅰ中为__________溶液(写化学式)。
②工艺中加入NaCO 固体、并再次充入SO 的目的是__________。
2 3 2
(3)制备NaSO 也可采用三室膜电解技术,装置如图所示,其中 SO 碱吸收液中含有NaHSO 和
2 2 5 2 3
NaSO 。阳极的电极反应式为_____________。电解后,__________室的NaHSO 浓度增加。将该
2 3 3
室溶液进行结晶脱水,可得到NaSO。
2 2 5
(4)NaSO 可用作食品的抗氧化剂。在测定某葡萄酒中NaSO 残留量时,取50.00 mL葡萄酒样品,
2 2 5 2 2 5
用 0.01000 mol·L−1 的碘标准液滴定至终点,消耗 10.00 mL。滴定反应的离子方程式为
_____________,该样品中NaSO 的残留量为____________g·L−1(以SO 计)。
2 2 5 2
【答案】 2NaHSO =NaSO+H O NaHSO 得到NaHSO 过饱和溶液 2HO-4e-=4H++O ↑ a
3 2 2 5 2 3 3 2 2
SO2-+2I +3H O=2SO 2-+4I-+6H+ 0.128
2 5 2 2 4
【解析】
(1)亚硫酸氢钠过饱和溶液脱水生成焦亚硫酸钠,根据原子守恒可知反应的方程式为 2NaHSO =
3
NaSO+H O;
2 2 5 2
(2)①碳酸钠饱和溶液吸收SO 后的溶液显酸性,说明生成物是酸式盐,即Ⅰ中为NaHSO;
2 3
②要制备焦亚硫酸钠,需要制备亚硫酸氢钠过饱和溶液,因此工艺中加入碳酸钠固体、并再次充入二
氧化硫的目的是得到NaHSO 过饱和溶液;
3
(3)阳极发生失去电子的氧化反应,阳极区是稀硫酸,氢氧根放电,则电极反应式为 2HO-4e-=
2
4H++O ↑。阳极区氢离子增大,通过阳离子交换膜进入a室与亚硫酸钠结合生成亚硫酸钠。阴极
2
是氢离子放电,氢氧根浓度增大,与亚硫酸氢钠反应生成亚硫酸钠,所以电解后 a室中亚硫酸氢
钠的浓度增大。
(4)单质碘具有氧化性,能把焦亚硫酸钠氧化为硫酸钠,反应的方程式为SO2-+2I +3H O=2SO 2-
2 5 2 2 4
+4I-+6H+;消耗碘的物质的量是 0.0001mol,所以焦亚硫酸钠的残留量(以 SO 计)是
2
。
6.【2018北京卷】磷精矿湿法制备磷酸的一种工艺流程如下:已知:磷精矿主要成分为Ca (PO )(OH),还含有Ca (PO )F和有机碳等。
5 4 3 5 4 3
溶解度:Ca (PO )(OH)”或“<”)。
3 4 2 4
②结合元素周期律解释①中结论:P和S电子层数相同,__________。
(3)酸浸时,磷精矿中Ca (PO )F所含氟转化为HF,并进一步转化为SiF 除去。写出生成HF的化
5 4 3 4
学方程式:__________。
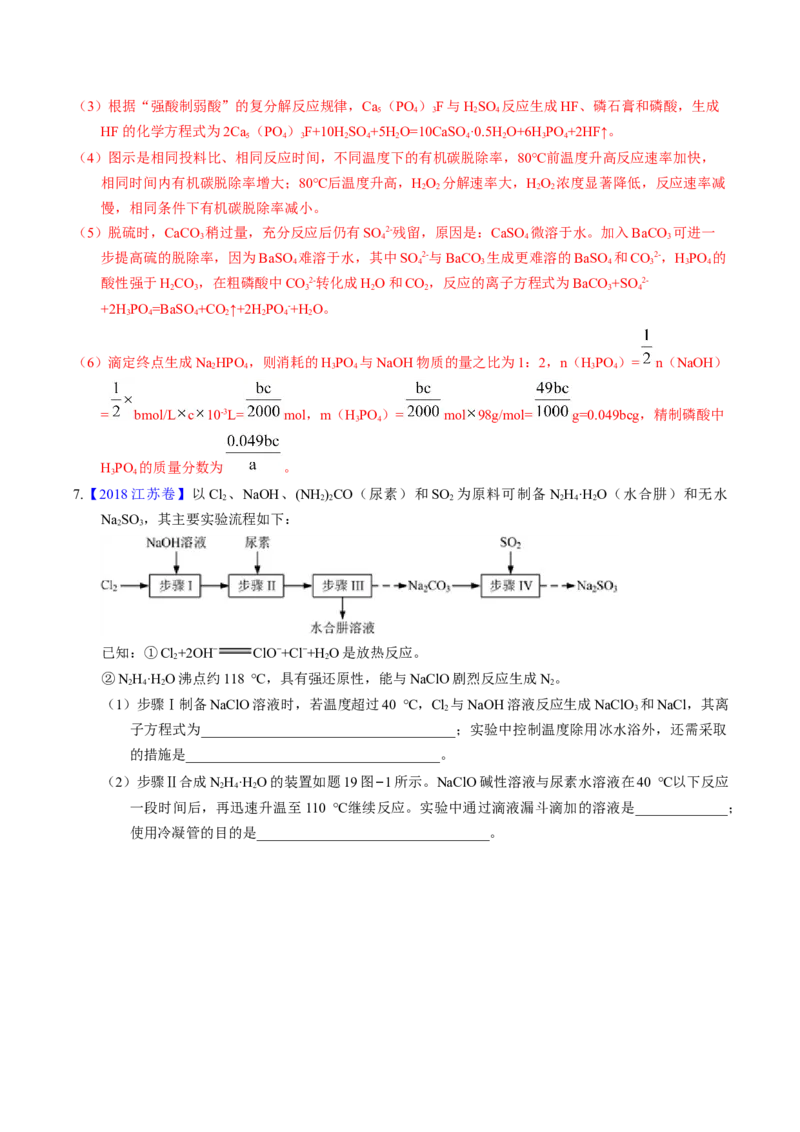
(4)HO 将粗磷酸中的有机碳氧化为CO 脱除,同时自身也会发生分解。相同投料比、相同反应时
2 2 2
间,不同温度下的有机碳脱除率如图所示。80℃后脱除率变化的原因:____________________。
(5)脱硫时,CaCO 稍过量,充分反应后仍有SO 2−残留,原因是__________;加入BaCO 可进一步
3 4 3
提高硫的脱除率,其离子方程式是____________________。
(6)取a g所得精制磷酸,加适量水稀释,以百里香酚酞作指示剂,用b mol·L−1NaOH溶液滴定至终
点时生成NaHPO ,消耗NaOH溶液c mL,精制磷酸中HPO 的质量分数是________。(已知:
2 4 3 4
HPO 摩尔质量为98 g·mol−1)
3 4
【答案】 研磨、加热 < 核电荷数 P<S,原子半径 P>S,得电子能力 P<S,非金属性 P<S
2Ca (PO )F+10HSO +5H O 10CaSO·0.5H O+6HPO +2HF↑ 80 ℃后,HO 分解速率大,浓度显
5 4 3 2 4 2 4 2 3 4 2 2
著降低 CaSO 微溶 BaCO + +2H PO BaSO+CO ↑+H O+2
4 3 3 4 4 2 2
【解析】
(1)研磨能增大反应物的接触面积,加快反应速率,加热,升高温度加快反应速率;流程中能加快反应
速率的措施有:研磨、加热。
(2)①依据反应方程式,根据“强酸制弱酸”的复分解反应规律,酸性:HPO HSO 。②用元素周期
3 4 2 4
律解释酸性:HPO HSO ,P和S电子层数相同,核电荷数P S,原子半径P S,得电子能力P
3 4 2 4
S,非金属性P S。(3)根据“强酸制弱酸”的复分解反应规律,Ca (PO )F与HSO 反应生成HF、磷石膏和磷酸,生成
5 4 3 2 4
HF的化学方程式为2Ca (PO )F+10HSO +5H O=10CaSO·0.5H O+6HPO +2HF↑。
5 4 3 2 4 2 4 2 3 4
(4)图示是相同投料比、相同反应时间,不同温度下的有机碳脱除率,80℃前温度升高反应速率加快,
相同时间内有机碳脱除率增大;80℃后温度升高,HO 分解速率大,HO 浓度显著降低,反应速率减
2 2 2 2
慢,相同条件下有机碳脱除率减小。
(5)脱硫时,CaCO 稍过量,充分反应后仍有SO 2-残留,原因是:CaSO 微溶于水。加入BaCO 可进一
3 4 4 3
步提高硫的脱除率,因为BaSO 难溶于水,其中SO 2-与BaCO 生成更难溶的BaSO 和CO2-,HPO 的
4 4 3 4 3 3 4
酸性强于HCO,在粗磷酸中CO2-转化成HO和CO,反应的离子方程式为BaCO +SO2-
2 3 3 2 2 3 4
+2H PO =BaSO +CO ↑+2H PO -+H O。
3 4 4 2 2 4 2
(6)滴定终点生成NaHPO ,则消耗的HPO 与NaOH物质的量之比为1:2,n(HPO )= n(NaOH)
2 4 3 4 3 4
= bmol/L c 10-3L= mol,m(HPO )= mol 98g/mol= g=0.049bcg,精制磷酸中
3 4
HPO 的质量分数为 。
3 4
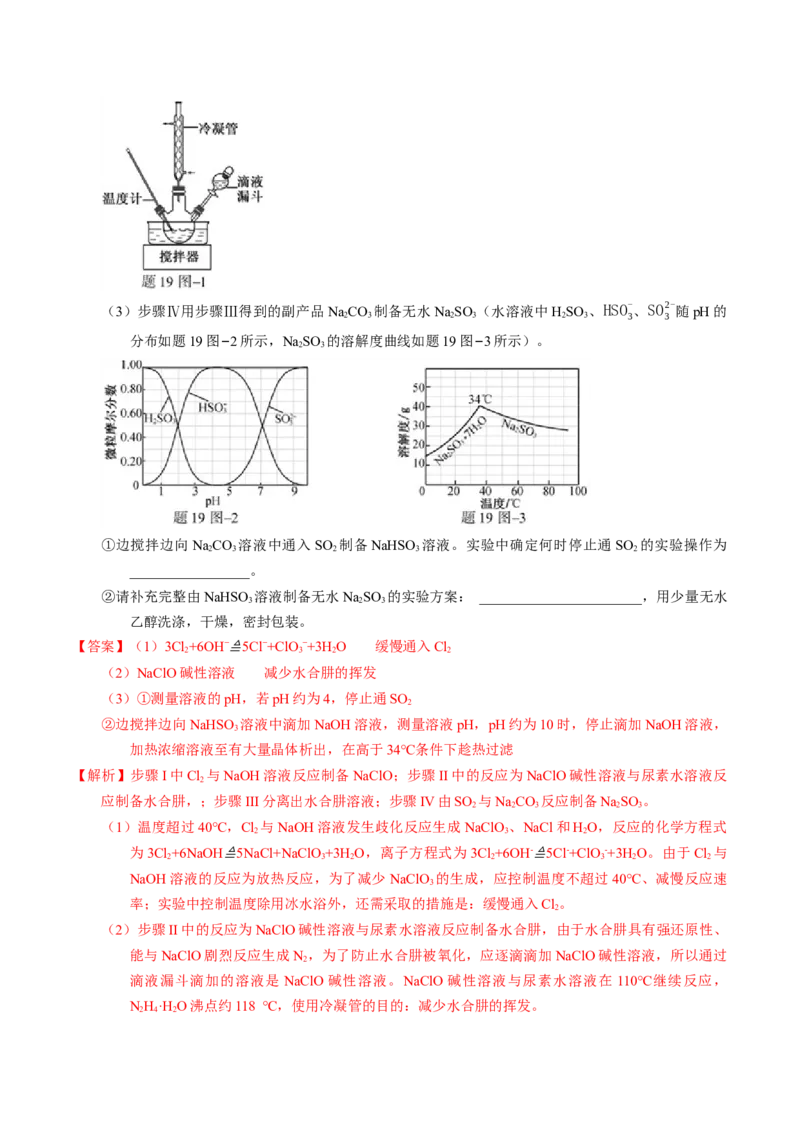
7.【2018江苏卷】以Cl 、NaOH、(NH )CO(尿素)和SO 为原料可制备NH·H O(水合肼)和无水
2 2 2 2 2 4 2
NaSO ,其主要实验流程如下:
2 3
已知:①Cl+2OH− ClO−+Cl−+H O是放热反应。
2 2
②NH·H O沸点约118 ℃,具有强还原性,能与NaClO剧烈反应生成N。
2 4 2 2
(1)步骤Ⅰ制备NaClO溶液时,若温度超过40 ℃,Cl 与NaOH溶液反应生成NaClO 和NaCl,其离
2 3
子方程式为____________________________________;实验中控制温度除用冰水浴外,还需采取
的措施是____________________________________。
(2)步骤Ⅱ合成NH·H O的装置如题19图−1所示。NaClO碱性溶液与尿素水溶液在40 ℃以下反应
2 4 2
一段时间后,再迅速升温至110 ℃继续反应。实验中通过滴液漏斗滴加的溶液是_____________;
使用冷凝管的目的是_________________________________。(3)步骤Ⅳ用步骤Ⅲ得到的副产品NaCO 制备无水NaSO (水溶液中HSO
、HSO- 、SO2-
随pH的
2 3 2 3 2 3 3 3
分布如题19图−2所示,NaSO 的溶解度曲线如题19图−3所示)。
2 3
①边搅拌边向NaCO 溶液中通入SO 制备NaHSO 溶液。实验中确定何时停止通SO 的实验操作为
2 3 2 3 2
_________________。
②请补充完整由NaHSO 溶液制备无水NaSO 的实验方案: _______________________,用少量无水
3 2 3
乙醇洗涤,干燥,密封包装。
【答案】(1)3Cl
2
+6OH−≜5Cl−+ClO
3
−+3H
2
O 缓慢通入Cl
2
(2)NaClO碱性溶液 减少水合肼的挥发
(3)①测量溶液的pH,若pH约为4,停止通SO
2
②边搅拌边向NaHSO 溶液中滴加NaOH溶液,测量溶液pH,pH约为10时,停止滴加NaOH溶液,
3
加热浓缩溶液至有大量晶体析出,在高于34℃条件下趁热过滤
【解析】步骤I中Cl 与NaOH溶液反应制备NaClO;步骤II中的反应为NaClO碱性溶液与尿素水溶液反
2
应制备水合肼,;步骤III分离出水合肼溶液;步骤IV由SO 与NaCO 反应制备NaSO 。
2 2 3 2 3
(1)温度超过40℃,Cl 与NaOH溶液发生歧化反应生成NaClO 、NaCl和HO,反应的化学方程式
2 3 2
为3Cl
2
+6NaOH≜5NaCl+NaClO
3
+3H
2
O,离子方程式为3Cl
2
+6OH-≜5Cl-+ClO
3
-+3H
2
O。由于Cl
2
与
NaOH溶液的反应为放热反应,为了减少NaClO 的生成,应控制温度不超过40℃、减慢反应速
3
率;实验中控制温度除用冰水浴外,还需采取的措施是:缓慢通入Cl。
2
(2)步骤II中的反应为NaClO碱性溶液与尿素水溶液反应制备水合肼,由于水合肼具有强还原性、
能与NaClO剧烈反应生成N ,为了防止水合肼被氧化,应逐滴滴加NaClO碱性溶液,所以通过
2
滴液漏斗滴加的溶液是 NaClO碱性溶液。NaClO碱性溶液与尿素水溶液在 110℃继续反应,
NH·H O沸点约118 ℃,使用冷凝管的目的:减少水合肼的挥发。
2 4 2(3)①向NaCO 溶液中通入SO 制备NaHSO 溶液,根据图示溶液pH约为4时,HSO -的摩尔分数
2 3 2 3 3
最大,则溶液的pH约为4时停止通入SO ;实验中确定何时停止通入SO 的实验操作为:测量溶
2 2
液的pH,若pH约为4,停止通SO 。
2
②由NaHSO 溶液制备无水NaSO ,首先要加入NaOH将NaHSO 转化为NaSO ,根据含硫微粒与pH
3 2 3 3 2 3
的关系,加入NaOH应调节溶液的pH约为10;根据NaSO 的溶解度曲线,温度高于34℃析出
2 3
NaSO ,低于34℃析出NaSO ·7H O,所以从NaSO 溶液中获得无水NaSO 应控制温度高于
2 3 2 3 2 2 3 2 3
34℃。由NaHSO 溶液制备无水NaSO 的实验方案为:边搅拌边向NaHSO 溶液中滴加NaOH溶
3 2 3 3
液,测量溶液pH,pH约为10时,停止滴加NaOH溶液,加热浓缩溶液至有大量晶体析出,在高
于34℃条件下趁热过滤,用少量无水乙醇洗涤,干燥,密封包装。
8.【2016新课标1卷】NaClO 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
2
回答下列问题:
(1)NaClO 中Cl的化合价为_______。
2
(2)写出“反应”步骤中生成ClO 的化学方程式_______。
2
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去 Mg2+和Ca2+,要加入的试剂分别为
________、________。“电解”中阴极反应的主要产物是______。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO 。此吸收反应中,氧化剂与还原剂的物质的
2
量之比为________,该反应中氧化产物是_________。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相
当于多少克Cl 的氧化能力。NaClO 的有效氯含量为____。(计算结果保留两位小数)
2 2
【答案】(1)+3;(2)2NaClO+SO+H SO =2ClO +2NaHSO ;
3 2 2 4 2 4
(3)NaOH溶液 ;NaCO 溶液 ;ClO −(或NaClO);(4)2:1; O; (5)1.57。
2 3 2 2 2
【解析】
(1)在NaClO 中Na为+1价,O为-2价,根据正负化合价的代数和为0,可得Cl的化合价为+3。
2
(2)NaClO 和SO 在HSO 酸化条件下生成ClO ,其中NaClO 是氧化剂,还原产物为NaCl,根据得失电
3 2 2 4 2 2
子守恒和原子守恒,此反应的化学方程式为2NaClO+SO+H SO =2ClO +2NaHSO 。
3 2 2 4 2 4
(3)食盐溶液中混有Mg2+和Ca2+,可利用过量NaOH溶液除去Mg2+,利用过量NaCO 溶液除去Ca2+;向
2 3
NaCl溶液中加入ClO ,进行电解,阳极发生反应2Cl--2e-=Cl↑,反应产生Cl , 阴极发生反应产生
2 2 2
NaClO,可见“电解”中阴极反应的主要产物是NaClO;
2 2
(4)根据图示可知:利用含有过氧化氢的NaOH溶液吸收ClO 气体,产物为NaClO ,则此吸收反应中,
2 2
氧化剂为ClO,还原产物为NaClO,还原剂是HO,氧化产物是O,每1 mol的HO 转移2 mol电子
2 2 2 2 2 2 2
反应方程式是:2NaOH+2ClO +H O=2NaClO +O +2H O,可知氧化剂和还原剂的物质的量之比为
2 2 2 2 2 2
2:1,该反应中氧化产物为O。
21 1
(5)每克NaClO 的物质的量n(NaClO)=1g÷90.5 g/mol= 90.5 mol,其获得电子的物质的量是n(e−)= 90.5
2 2
mol×4=4/90.5 mol,1 mol Cl 获得电子的物质的量是2 mol,根据电子转移数目相等,可知其相对于氯
2
1 2 2
气的物质的量为n= 90.5 mol×4÷2= 90.5 mol,则氯气的质量为90.5 mol×71 g/mol=1.57 g。
9.[2019新课标Ⅰ]硼酸(HBO )是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以
3 3
硼镁矿(含MgB O·H O、SiO 及少量Fe O、Al O)为原料生产硼酸及轻质氧化镁的工艺流程如下:
2 2 5 2 2 2 3 2 3
回答下列问题:
(1)在95 ℃“溶浸”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式为_________。
(2)“滤渣1”的主要成分有_________。为检验“过滤1”后的滤液中是否含有Fe3+离子,可选用的化
学试剂是_________。
(3)根据HBO 的解离反应:HBO+H O H++B(OH)− ,K=5.81×10−10,可判断HBO 是______
3 3 3 3 2 4 a 3 3
酸;在“过滤2”前,将溶液pH调节至3.5,目的是_______________。
(4)在“沉镁”中生成 Mg(OH) ·MgCO 沉淀的离子方程式为__________,母液经加热后可返回
2 3
___________工序循环使用。由碱式碳酸镁制备轻质氧化镁的方法是_________。
【答案】(1)NH HCO +NH (NH )CO
4 3 3 4 2 3
(2)SiO、Fe O、Al O KSCN
2 2 3 2 3
(3)一元弱 转化为HBO,促进析出
3 3
(4)2Mg2++3 +2H O Mg(OH) ·MgCO ↓+2
2 2 3
(或2Mg2++2 +H O Mg(OH) ·MgCO ↓+CO ↑) 溶浸 高温焙烧
2 2 3 2
【解析】(1)根据流程图知硼镁矿粉中加入硫酸铵溶液产生的气体为氨气,用碳酸氢铵溶液吸收,反应
方程式为:NH +NHHCO (NH )CO。
3 4 3 4 2 3
(2)滤渣I为不与硫酸铵溶液反应的Fe O、Al O、SiO;检验Fe3+,可选用的化学试剂为KSCN,
2 3 2 3 2
(3)由硼酸的离解方程式知,硼酸在水溶液中是通过与水分子的配位作用产生氢离子,而三价硼原子最
多只能再形成一个配位键,且硼酸不能完全解离,所以硼酸为一元弱酸;在“过滤2”前,将溶液pH
调节至3.5,目的是将B(OH)− 转化为HBO,并促进HBO 析出,
4 3 3 3 3
(4)沉镁过程中用碳酸铵溶液与Mg2+反应生成Mg(OH) ∙MgCO,沉镁过程的离子反应为:2Mg2+
2 3
+2H O+3CO2- Mg(OH) ∙MgCO↓+2HCO-;母液加热分解后生成硫酸铵溶液,可以返回“溶浸”
2 3 2 3 3工序循环使用;碱式碳酸镁不稳定,高温下可以分解,故由碱式碳酸镁制备轻质氧化镁的方法是高温
焙烧。
10.【2018新课标3卷】KIO 是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
3
(1)KIO 的化学名称是_______。
3
(2)利用“KClO 氧化法”制备KIO 工艺流程如下图所示:
3 3
“酸化反应”所得产物有KH(IO) 、Cl 和KCl。“逐Cl”采用的方法是________。“滤液”中的溶质
3 2 2 2
主要是_______。“调pH”中发生反应的化学方程式为__________。
(3)KIO 也可采用“电解法”制备,装置如图所示。
3
①写出电解时阴极的电极反应式______。
②电解过程中通过阳离子交换膜的离子主要为_________,其迁移方向是_____________。
③与“电解法”相比,“KClO 氧化法”的主要不足之处有______________(写出一点)。
3
【答案】 碘酸钾 加热 KCl KH(IO )+KOH 2KIO +H O 或(HIO +KOH KIO +H O)
3 2 3 2 3 3 2
2HO+2e- 2OH-+H ↑ K+ a到b 产生Cl 易污染环境等
2 2 2
【解析】
(1)根据氯酸钾(KClO)可以推测KIO 为碘酸钾。
3 3
(2)将溶解在溶液中的气体排出的一般方法是将溶液加热,原因是气体的溶解度是随温度上升而下
减小。第一步反应得到的产品中氯气在“逐Cl”时除去,根据图示,碘酸钾在最后得到,所以过
2
滤时KH(IO) 应该在滤渣中,所以滤液中主要为KCl。“调pH”的主要目的是将KH(IO) 转化为
3 2 3 2
KIO ,所以方程式为:KH(IO)+KOH=2KIO +H O。
3 3 2 3 2
(3)①由图示,阴极为氢氧化钾溶液,所以反应为水电离的氢离子得电子,反应为 2HO + 2e- =
2
2OH- + H ↑。
2
②电解时,溶液中的阳离子应该向阴极迁移,明显是溶液中大量存在的钾离子迁移,方向为由左向右,
即由a到b。
③KClO 氧化法的最大不足之处在于,生产中会产生污染环境的氯气。
3
11.【2016江苏卷】以电石渣[主要成分为Ca(OH) 和CaCO ]为原料制备KClO 的流程如下:
2 3 3(1)氯化过程控制电石渣过量,在75℃左右进行。氯化时存在Cl 与Ca(OH) 作用生成Ca(ClO) 的反
2 2 2
应,Ca(ClO) 进一步转化为Ca(ClO ),少量Ca(ClO) 分解为CaCl 和O。
2 3 2 2 2 2
①生成Ca(ClO) 的化学方程式为 。
2
②提高Cl 转化为Ca(ClO ) 的转化率的可行措施有 (填序号)。
2 3 2
A.适当减缓通入Cl 速率
2
B.充分搅拌浆料
C.加水使Ca(OH) 完全溶解
2
(2)氯化过程中Cl 转化为Ca(ClO ) 的总反应方程式为
2 3 2
6Ca(OH) +6Cl=Ca(ClO )+5CaCl +6H O
2 2 3 2 2 2
氯化完成后过滤。
①滤渣的主要成分为 (填化学式)。
②滤液中Ca(ClO ) 与CaCl 的物质的量之比n[Ca(ClO )]∶n[CaCl ] 1∶5(填“>”、“<”
3 2 2 3 2 2
或“=”)。
(3)向滤液中加入稍过量KCl固体可将Ca(ClO ) 转化为KClO,若溶液中KClO 的含量为100g▪L-1,
3 2 3 3
从该溶液中尽可能多地析出KClO 固体的方法是 。
3
【答案】(1)①2Cl+2Ca(OH) =Ca(ClO) +CaCl +2H O ②AB (2)①CaCO 、Ca(OH) ②<
2 2 2 2 2 3 2
(3)蒸发浓缩、冷却结晶
【解析】
(1)①氯气与氢氧化钙反应生成次氯酸钙、氯化钙和水,则生成 Ca(ClO) 的化学方程式为
2
2Cl+2Ca(OH) =Ca(ClO) +CaCl +2H O。
2 2 2 2 2
②A.适当减缓通入Cl 速率可以使氯气被氢氧化钙充分吸收而反应,可以提高氯气的转化率,A正确;
2
B.充分搅拌浆料可以增大反应物的接触面积,使氯气被氢氧化钙充分吸收而反应,可以提高氯气的转化率,B正确;C.加水使Ca(OH) 完全溶解氢氧化钙浓度降低,不利于氯气的吸收,C错
2
误,答案选AB。
(2)①碳酸钙不溶于水,与氯气不反应,氢氧化钙微溶,因此滤渣的主要成分为CaCO 、Ca(OH) 。
3 2
②由于氯气还能与氢氧化钙反应生成次氯酸钙、氯化钙和水,因此滤液中Ca(ClO ) 与CaCl 的物质的
3 2 2
量之比n[Ca(ClO )]∶n[CaCl ]<1∶5。
3 2 2
(3)根据图像可知氯酸钾的溶解度受温度影响最大,因此从该溶液中尽可能多地析出 KClO 固体的
3
方法是蒸发浓缩、冷却结晶。
12.[2019新课标Ⅱ]立德粉ZnS·BaSO(也称锌钡白),是一种常用白色颜料。回答下列问题:
4
(1)利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧立德粉样品
时,钡的焰色为__________(填标号)。
A.黄色 B.红色 C.紫色 D.绿色
(2)以重晶石(BaSO)为原料,可按如下工艺生产立德粉:
4
①在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为
______________________。回转炉尾气中含有有毒气体,生产上可通过水蒸气变换反应将其
转化为CO 和一种清洁能源气体,该反应的化学方程式为______________________。
2
②在潮湿空气中长期放置的“还原料”,会逸出臭鸡蛋气味的气体,且水溶性变差。其原因是
“还原料”表面生成了难溶于水的___________(填化学式)。
③沉淀器中反应的离子方程式为______________________。
(3)成品中S2−的含量可以用“碘量法”测得。称取m g样品,置于碘量瓶中,移取25.00 mL 0.1000
mol·L−1的I−KI溶液于其中,并加入乙酸溶液,密闭,置暗处反应5 min,有单质硫析出。以淀粉
2
为指示剂,过量的I 用0.1000 mol·L−1NaSO 溶液滴定,反应式为I+2 2I−+ 。测定
2 2 2 3 2
时消耗 NaSO 溶液体积 V mL。终点颜色变化为_________________,样品中 S2−的含量为
2 2 3
______________(写出表达式)。
【答案】(1)D
(2)①BaSO+4C BaS+4CO↑ CO+HO CO+H
4 2 2 2
②BaCO
3
③S2−+Ba2++Zn2++ BaSO·ZnS↓
4
(3)浅蓝色至无色
【解析】
(1)焰色反应不是化学变化,常用来检验金属元素存在,常见金属元素焰色:A.钠的焰色为黄色,故A错误;B.钙的焰色为红色,故B错误;C.钾的焰色为紫色,故C错误;D.钡的焰色为绿色,故D
正确;故选D。
(2)①注意焦炭过量生成CO,反应物为硫酸钡与焦炭,产物为BaS与CO,写出方程式BaSO+4C
4
BaS+4CO↑;CO与水蒸气反应生成CO 与H,写出方程式:CO+HO CO+H 。
2 2 2 2 2
②根据信息臭鸡蛋气味气体为硫化氢气体,由强酸制弱酸原理,还原料硫化钡与空气中水,二氧化碳反应
生成了碳酸钡与硫化氢气体。
③硫化钡与硫酸锌为可溶性强电解质,写成离子形式,产物硫酸钡与硫化锌为沉淀,不可电离,写出离子
方程式:S2−+Ba2++Zn2++ BaSO·ZnS↓。
4
(3)碘单质与硫离子的反应:S2-+I S+2I-;碘单质与淀粉混合为蓝色,用硫代硫酸钠滴定过量的I,
2 2
故终点颜色变化为浅蓝色至无色;根据氧化还原反应得失电子数相等,利用关系式法解题;根据化合
价升降相等列关系式,设硫离子物质的量为n mol:
S2- ~ I 2SO2- ~ I
2 2 3 2
1 mol 1 mol 2 mol 1 mol
n mol n mol 0.1V×10-3mol 0.1V×10-3mol
n+ 0.1V×10-3mol=25 0.1V×10-3mol,得n=(25- V)0.1×10-3mol
则样品中硫离子含量为: ×100%= ×100%。