文档内容
2024~2025 学年第二学期高三开学质量检测卷
化学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用 2B铅笔把答题卡上
对应题目的答案标号涂黑;非选择题请用直径 0.5毫米黑色墨水签字笔在答题卡上各题的答
题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:高考范围。
5.可能用到的相对原子质量:H1 C12 O16 Mg24 K39 Fe56 I127
一、选择题(本题共 14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的)
1.生活中蕴含着丰富的化学知识。下列变化涉及氧化还原反应的是( )
A.柠檬酸去除水垢 B.污水中加入混凝剂聚合氯化铝
C.做豆腐用石膏作凝固剂 D.黑火药爆炸
2.下列化学用语表达正确的是( )
A.含有10个中子的氧核素:
B.空间填充模型 既可以表示甲烷分子,也可以表示四氯化碳分子
C. 电子云示意图:
D.用电子式表示HCl的形成过程:
3.盐泥是氯碱工业的废渣,主要成分为 、 (含少量的FeO、 、 及
)。实验室中利用盐泥制备无水 的流程如下:
上述制备过程中,下列不需要使用的实验装置是
学科网(北京)股份有限公司A. B. C. D.
4.下列关于非金属及其化合物的性质或转化错误的是( )
B.铵盐受热易分解,但是产物不一定含有氨气
C. 既能使酸性高锰酸钾溶液褪色又能使溴水褪色
D.磷酸中少量的水极难除去的原因是磷酸与水形成分子间氢键
5 . 高 铜 酸 钠 ( ) 是 黑 色 难 溶 于 水 的 固 体 。 一 种 制 备 高 铜 酸 钠 的 原 理 为
。设 表示阿伏加德罗常数的值,下列说法正
确的是( )
A.1mol基态Cu原子中未成对电子数为
B. 的NaOH溶液中含 的数目为
C.1mol 参加反应转移电子数为
D.1mol 分子中含氢键数目为
6.下列过程中的化学反应,相应的离子方程式正确的是( )
A. 通入 溶液中:
B.向 溶液中通入 :
C.少量铁粉加入稀 溶液中:
D.向 溶液中通入 :
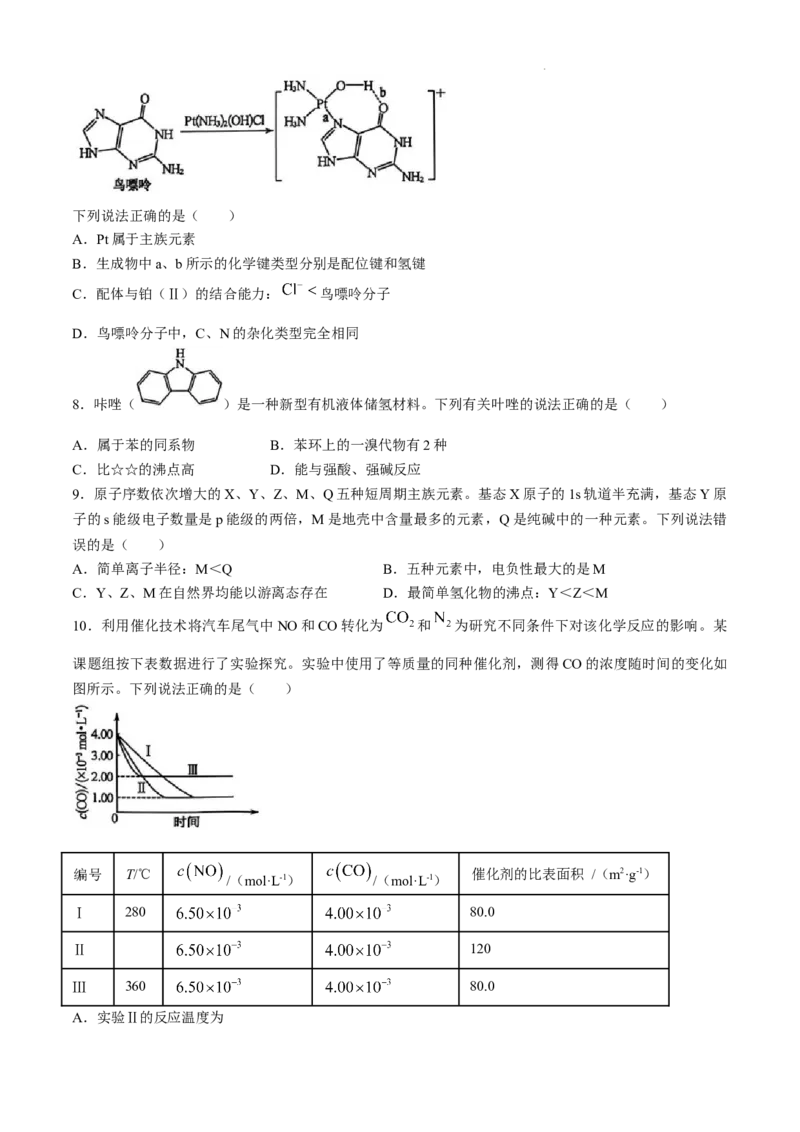
7.配合物顺铂 是临床使用的第一代铂类抗癌药物。顺铂的抗癌机理:在铜转运蛋白的作
用下,顺铂进入人体细胞发生水解,生成的 与DNA结合,破坏DNA的结构,阻止癌
细胞增殖。
学科网(北京)股份有限公司下列说法正确的是( )
A.Pt属于主族元素
B.生成物中a、b所示的化学键类型分别是配位键和氢键
C.配体与铂(Ⅱ)的结合能力: 鸟嘌呤分子
D.鸟嘌呤分子中,C、N的杂化类型完全相同
8.咔唑( )是一种新型有机液体储氢材料。下列有关叶唑的说法正确的是( )
A.属于苯的同系物 B.苯环上的一溴代物有2种
C.比☆☆的沸点高 D.能与强酸、强碱反应
9.原子序数依次增大的X、Y、Z、M、Q五种短周期主族元素。基态X原子的1s轨道半充满,基态Y原
子的s能级电子数量是p能级的两倍,M是地壳中含量最多的元素,Q是纯碱中的一种元素。下列说法错
误的是( )
A.简单离子半径:M<Q B.五种元素中,电负性最大的是M
C.Y、Z、M在自然界均能以游离态存在 D.最简单氢化物的沸点:Y<Z<M
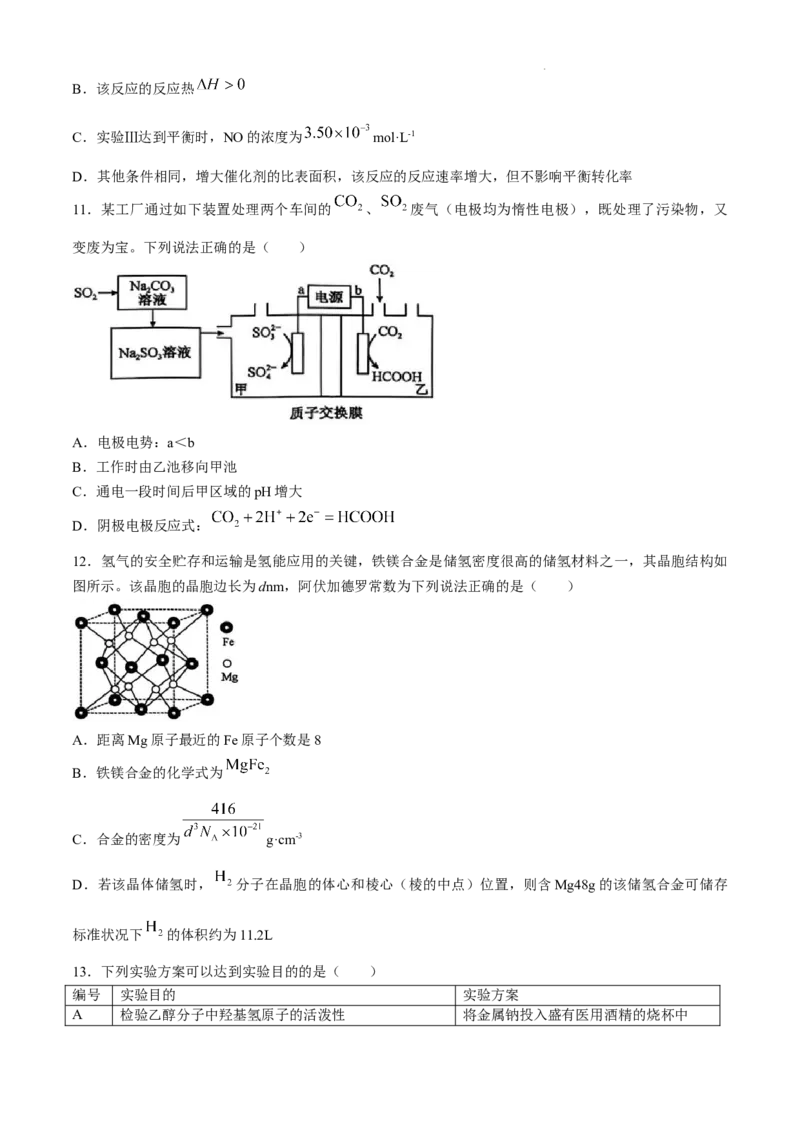
10.利用催化技术将汽车尾气中NO和CO转化为 和 为研究不同条件下对该化学反应的影响。某
课题组按下表数据进行了实验探究。实验中使用了等质量的同种催化剂,测得CO的浓度随时间的变化如
图所示。下列说法正确的是( )
编号 T/℃ 催化剂的比表面积 /(m2·g-1)
/(mol·L-1) /(mol·L-1)
Ⅰ 280 80.0
Ⅱ 120
Ⅲ 360 80.0
A.实验Ⅱ的反应温度为
学科网(北京)股份有限公司B.该反应的反应热
C.实验Ⅲ达到平衡时,NO的浓度为 mol·L-1
D.其他条件相同,增大催化剂的比表面积,该反应的反应速率增大,但不影响平衡转化率
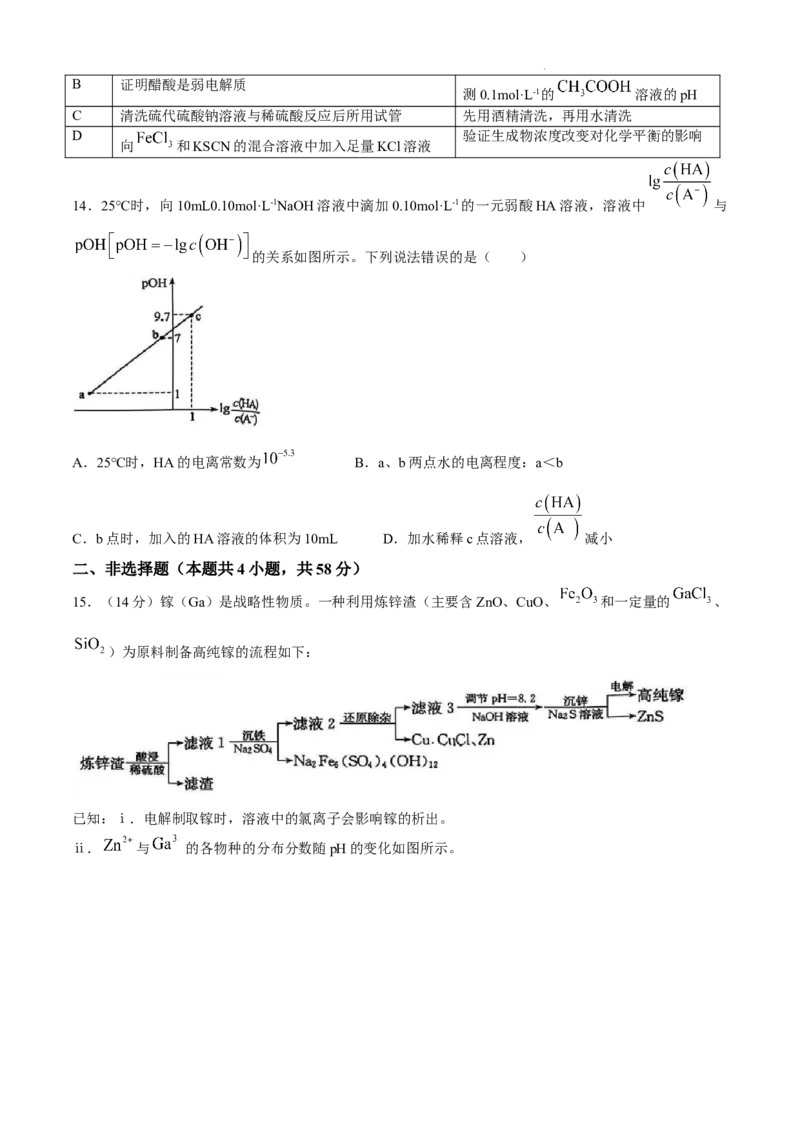
11.某工厂通过如下装置处理两个车间的 、 废气(电极均为惰性电极),既处理了污染物,又
变废为宝。下列说法正确的是( )
A.电极电势:a<b
B.工作时由乙池移向甲池
C.通电一段时间后甲区域的pH增大
D.阴极电极反应式:
12.氢气的安全贮存和运输是氢能应用的关键,铁镁合金是储氢密度很高的储氢材料之一,其晶胞结构如
图所示。该晶胞的晶胞边长为dnm,阿伏加德罗常数为下列说法正确的是( )
A.距离Mg原子最近的Fe原子个数是8
B.铁镁合金的化学式为
C.合金的密度为 g·cm-3
D.若该晶体储氢时, 分子在晶胞的体心和棱心(棱的中点)位置,则含Mg48g的该储氢合金可储存
标准状况下 的体积约为11.2L
13.下列实验方案可以达到实验目的的是( )
编号 实验目的 实验方案
A 检验乙醇分子中羟基氢原子的活泼性 将金属钠投入盛有医用酒精的烧杯中
学科网(北京)股份有限公司B 证明醋酸是弱电解质
测0.1mol·L-1的 溶液的pH
C 清洗硫代硫酸钠溶液与稀硫酸反应后所用试管 先用酒精清洗,再用水清洗
D 验证生成物浓度改变对化学平衡的影响
向 和KSCN的混合溶液中加入足量KCl溶液
14.25℃时,向10mL0.10mol·L-1NaOH溶液中滴加0.10mol·L-1的一元弱酸HA溶液,溶液中 与
的关系如图所示。下列说法错误的是( )
A.25℃时,HA的电离常数为 B.a、b两点水的电离程度:a<b
C.b点时,加入的HA溶液的体积为10mL D.加水稀释c点溶液, 减小
二、非选择题(本题共4小题,共58分)
15.(14分)镓(Ga)是战略性物质。一种利用炼锌渣(主要含ZnO、CuO、 和一定量的 、
)为原料制备高纯镓的流程如下:
已知:ⅰ.电解制取镓时,溶液中的氯离子会影响镓的析出。
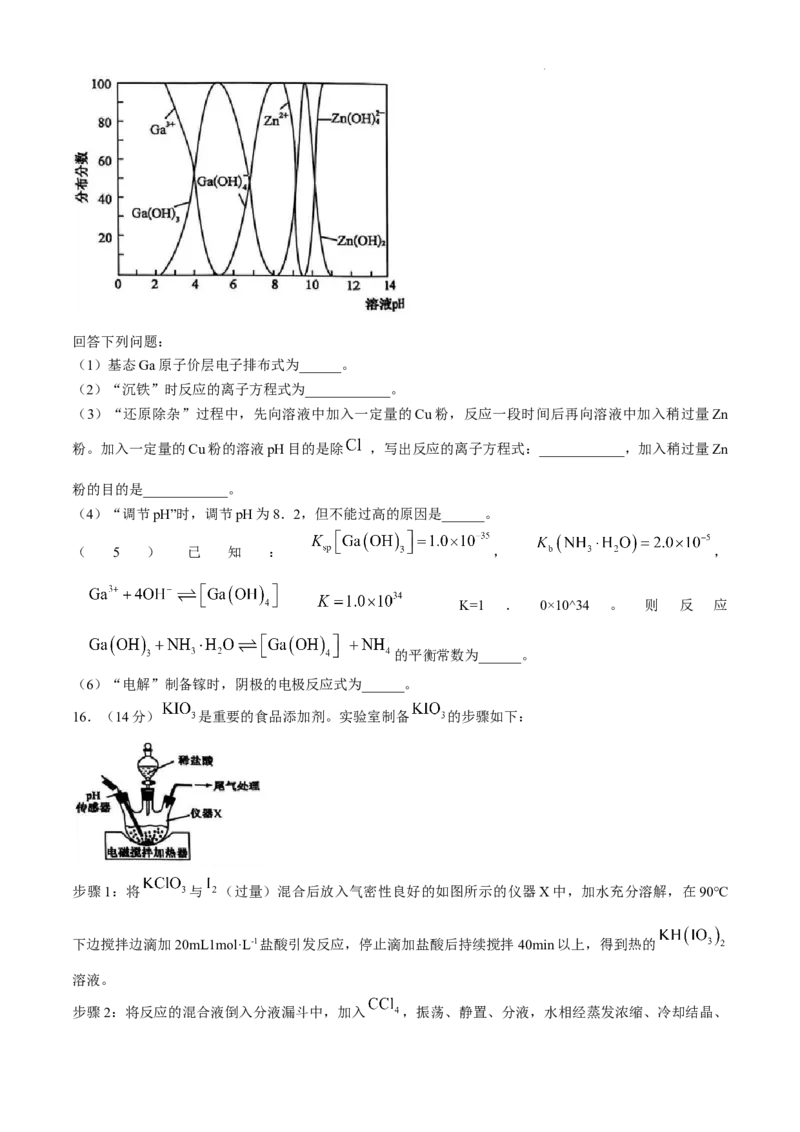
ⅱ. 与 的各物种的分布分数随pH的变化如图所示。
学科网(北京)股份有限公司回答下列问题:
(1)基态Ga原子价层电子排布式为______。
(2)“沉铁”时反应的离子方程式为____________。
(3)“还原除杂”过程中,先向溶液中加入一定量的Cu粉,反应一段时间后再向溶液中加入稍过量Zn
粉。加入一定量的Cu粉的溶液pH目的是除 ,写出反应的离子方程式:____________,加入稍过量Zn
粉的目的是____________。
(4)“调节pH”时,调节pH为8.2,但不能过高的原因是______。
( 5 ) 已 知 : , ,
K=1 . 0×10^34 。 则 反 应
的平衡常数为______。
(6)“电解”制备镓时,阴极的电极反应式为______。
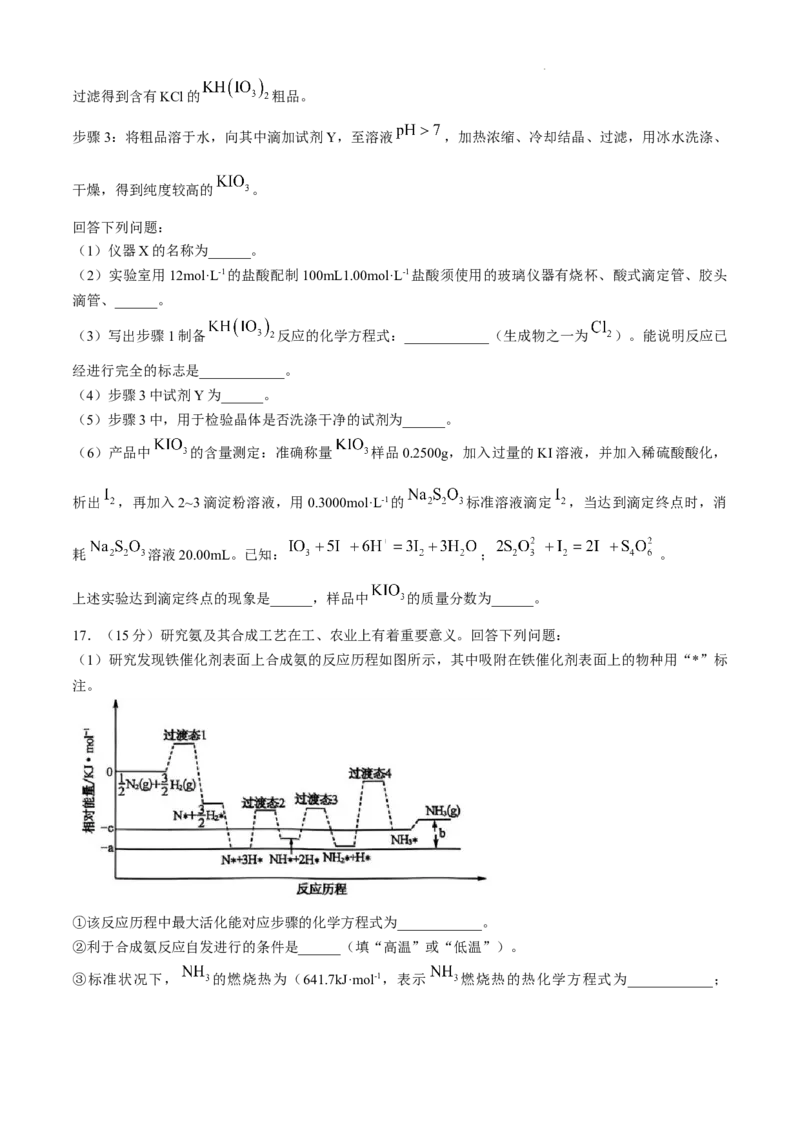
16.(14分) 是重要的食品添加剂。实验室制备 的步骤如下:
步骤1:将 与 (过量)混合后放入气密性良好的如图所示的仪器X中,加水充分溶解,在90℃
下边搅拌边滴加20mL1mol·L-1盐酸引发反应,停止滴加盐酸后持续搅拌40min以上,得到热的
溶液。
步骤2:将反应的混合液倒入分液漏斗中,加入 ,振荡、静置、分液,水相经蒸发浓缩、冷却结晶、
学科网(北京)股份有限公司过滤得到含有KCl的 粗品。
步骤3:将粗品溶于水,向其中滴加试剂Y,至溶液 ,加热浓缩、冷却结晶、过滤,用冰水洗涤、
干燥,得到纯度较高的 。
回答下列问题:
(1)仪器X的名称为______。
(2)实验室用12mol·L-1的盐酸配制100mL1.00mol·L-1盐酸须使用的玻璃仪器有烧杯、酸式滴定管、胶头
滴管、______。
(3)写出步骤1制备 反应的化学方程式:____________(生成物之一为 )。能说明反应已
经进行完全的标志是____________。
(4)步骤3中试剂Y为______。
(5)步骤3中,用于检验晶体是否洗涤干净的试剂为______。
(6)产品中 的含量测定:准确称量 样品0.2500g,加入过量的KI溶液,并加入稀硫酸酸化,
析出 ,再加入2~3滴淀粉溶液,用0.3000mol·L-1的 标准溶液滴定 ,当达到滴定终点时,消
耗 溶液20.00mL。已知: ; 。
上述实验达到滴定终点的现象是______,样品中 的质量分数为______。
17.(15分)研究氨及其合成工艺在工、农业上有着重要意义。回答下列问题:
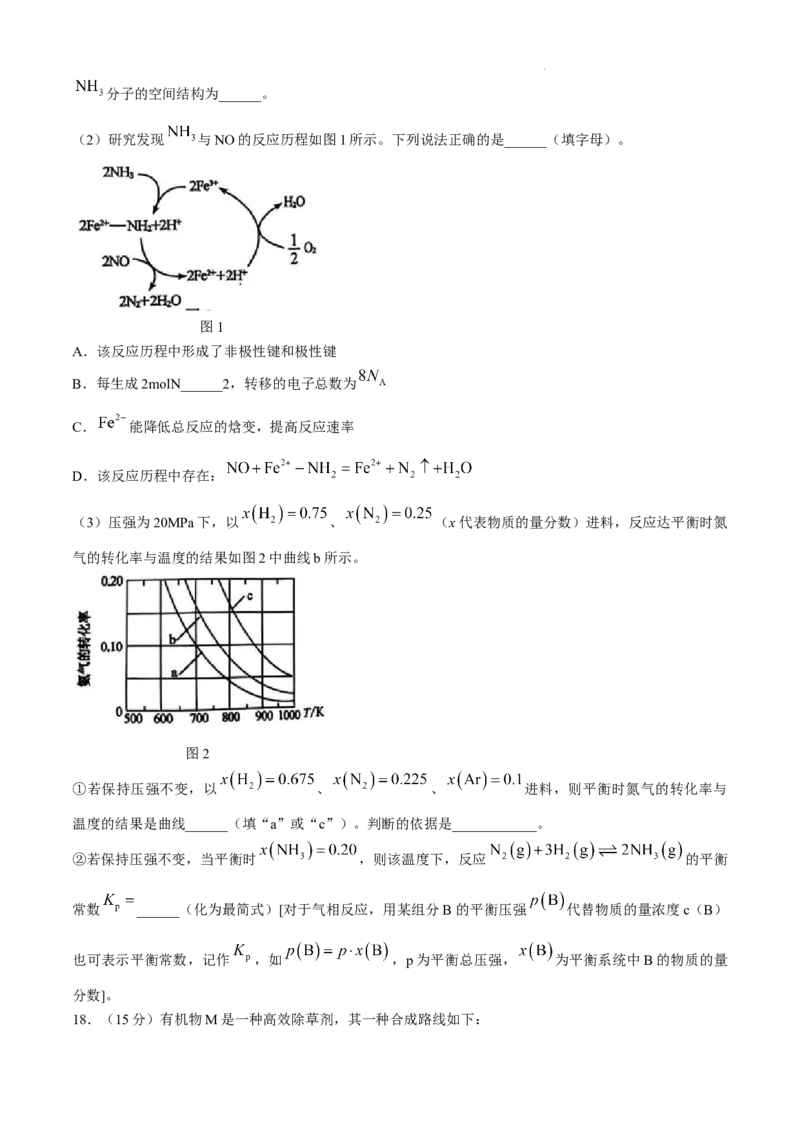
(1)研究发现铁催化剂表面上合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的物种用“*”标
注。
①该反应历程中最大活化能对应步骤的化学方程式为____________。
②利于合成氨反应自发进行的条件是______(填“高温”或“低温”)。
③标准状况下, 的燃烧热为(641.7kJ·mol-1,表示 燃烧热的热化学方程式为____________;
学科网(北京)股份有限公司分子的空间结构为______。
(2)研究发现 与NO的反应历程如图1所示。下列说法正确的是______(填字母)。
图1
A.该反应历程中形成了非极性键和极性键
B.每生成2molN______2,转移的电子总数为
C. 能降低总反应的焓变,提高反应速率
D.该反应历程中存在:
(3)压强为20MPa下,以 、 (x代表物质的量分数)进料,反应达平衡时氮
气的转化率与温度的结果如图2中曲线b所示。
图2
①若保持压强不变,以 、 、 进料,则平衡时氮气的转化率与
温度的结果是曲线______(填“a”或“c”)。判断的依据是____________。
②若保持压强不变,当平衡时 ,则该温度下,反应 的平衡
常数 ______(化为最简式)[对于气相反应,用某组分B的平衡压强 代替物质的量浓度c(B)
也可表示平衡常数,记作 ,如 ,p为平衡总压强, 为平衡系统中B的物质的量
分数]。
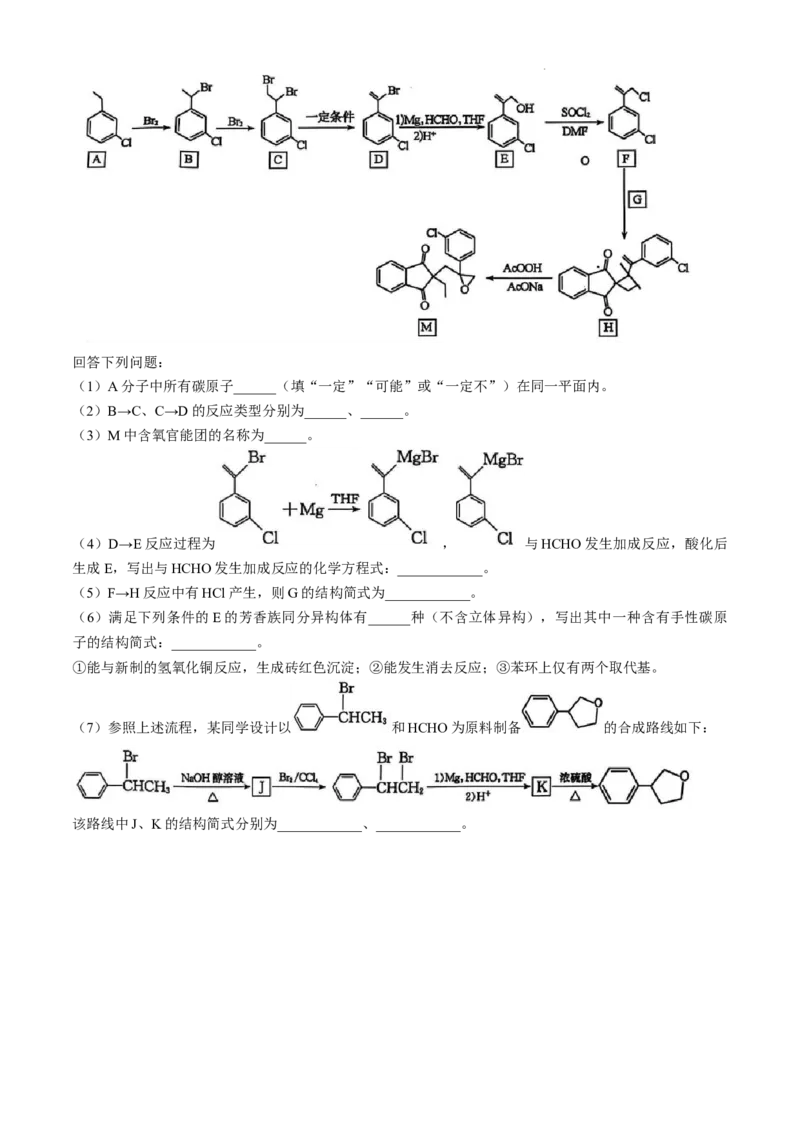
18.(15分)有机物M是一种高效除草剂,其一种合成路线如下:
学科网(北京)股份有限公司回答下列问题:
(1)A分子中所有碳原子______(填“一定”“可能”或“一定不”)在同一平面内。
(2)B→C、C→D的反应类型分别为______、______。
(3)M中含氧官能团的名称为______。
(4)D→E反应过程为 , 与HCHO发生加成反应,酸化后
生成E,写出与HCHO发生加成反应的化学方程式:____________。
(5)F→H反应中有HCl产生,则G的结构简式为____________。
(6)满足下列条件的E的芳香族同分异构体有______种(不含立体异构),写出其中一种含有手性碳原
子的结构简式:____________。
①能与新制的氢氧化铜反应,生成砖红色沉淀;②能发生消去反应;③苯环上仅有两个取代基。
(7)参照上述流程,某同学设计以 和HCHO为原料制备 的合成路线如下:
该路线中J、K的结构简式分别为____________、____________。
学科网(北京)股份有限公司2024~2025 学年第二学期高三开学质量检测卷•化学
参考答案、提示及评分细则
1.D 柠檬酸去除水垢,发生复分解反应,A项不符合题意;加入混凝剂聚合氯化铝,可使污水中细小悬
浮物聚集成大颗粒,B项不符合题意;用石膏作凝固剂做豆腐主要发生絮凝,C项不符合题意;黑火药爆
炸发生了氧化还原反应,D项符合题意。
2.C 含有10个中子的氧核素: ,A项错误;原子半径:Cl>C>H,因此该模型可表示甲烷,但不
能表示四氯化碳,B项错误; 能级电子云是哑铃形,C项正确;HCl为共价化合物,用电子式表示HCl
的形成过程为 ,D项错误。
3.B 制备流程不包含分液,B项符合题意。
4.A 不能与水反应,A项错误;硝酸铵受热分解生成氮气,B项正确; 具有还原性,能与酸
性高锰酸钾溶液和溴水反应,C项正确;磷酸与水分子间能形成氢键,D项正确。
5.C 1mol基态Cu原子中含未成对电子数为 ,A项错误;没有体积,无法计算,B项错误;由
得到 ,氯元素的化合价由+1 价下降到-1 价,则 1mol 参加反应转移 2mol 电子,C 项正确;
1molH₂O
分子中含氢键数目为 ,D项错误。
6.B 不拆开,A项错误;向 溶液中通入 : ,B.项正确;
与稀 溶液继续发生氧化还原反应,C项错误; 与盐酸反应,D项错误。
7.C Pt属于副族元素,A项错误;氢键不是化学键,B项错误;鸟嘌呤取代 与 形成配位键,C
项正确;身嘌呤分子中,C、N的杂化类型不完全相同,D项错误。
8.C 咔唑不属于苯的同系物,A项错误;苯环上的一溴代物有4种,B项错误; 分子间
存在氢键,其沸点高于 .C项正确;与强酸反应、与强碱不反应,D项错误。
9.A X的1s轨道半充满,说明X为H,Y的s能级电子数量是p能级的两倍,Y为C,M是地壳中含量
学科网(北京)股份有限公司最多的元素,M为O,原子序数:Y<Z<M,则Z为N,Q是纯碱中的一种元素,则Q为Na。简单离子
半径:M>Q,即 ,A项错误;O在五种元素中电负性最大,B项正确;在自然界存在碳、氧气、
氮气,C项正确;Y、Z、M分别为C、N、O,沸点: ,D项正确。
10.D根据单一变量原则,实验Ⅰ和Ⅱ催化剂比表面积不同,温度应该相同,则实验Ⅱ的反应温度为
280℃,A
项错误;对比反应Ⅰ和Ⅲ,温度升高,平衡时CO浓度升高,平衡逆向移动,说明 ,B项错误;化
学方程式为 ,实验Ⅲ达到平衡时,NO的浓度为 mol·L-1,,
C项错误;实验Ⅰ、Ⅱ催化剂比表面积不同,增大催化剂的比表面积,化学反应速率增大,但平衡转化率
不变,D项正确。
11.D 电极电势:a>b,A 项错误;工作时 由甲池移向乙池,B 项错误;甲室发生反应
,通电一段时间后甲区域的 pH减小,C项错误;阴极电极反应式:
,D项正确。
12.C 由晶胞可知,Mg原子在晶胞内,距离Mg原子最近的Fe原子为4个,A项错误;在晶胞中,Fe
原子位于顶点和面心,个数为 ,Mg原子在晶胞内,个数为 8,铁镁合金的化学式为
,B项错误;该合金的密度 g·cm-3,C项正确;晶胞中
Mg原子数为8,可储存 分子数为 ,Mg的物质的量为 2mol,储存的 的物质的量为
1mol,在标准状况下,体积为22.4L,D项错误。
13.B 将金属钠投入盛有医用酒精的烧杯中,钠优先与医用酒精中的水反应,无法检验乙醇分子中羟基
氢原子的活泼性,A项不能达到实验目的;0.1mol·L-1的醋酸溶液pH大于1,说明醋酸在溶液中发生部分
电离,则证明醋酸是弱电解质,B项能达到实验目的;硫代硫酸钠溶液与稀硫酸反应后所用试管中有硫单
质,硫无法溶于酒精,可先用 清洗,再用水清洗,C项不能达到实验目的;由于 不参与反应,加
入足量KCl溶液,颜色变化无法说明是移动产生,D项不能达到实验目的。
14. 时, ,可得: , , ,电离常
学科网(北京)股份有限公司数 ,A 项正确;由图可知 a 点溶液显碱性,主要溶质为
NaOH,b点溶液显中性,主要溶质为盐,碱抑制水的电离,盐水解促进水的电离,因此水的电离程度:
a