文档内容
高三化学参考答案
1-5.C D A B C 6-10 C B A D C 11-14 C D B C
15.(14分)(1) > (1分) Fe3+、Mn2+ (2分)
(2) 2Fe3++Ag S+4 Cl- 2Fe2++2[AgCl]- +S (2分) Cl-是为了与Ag S电
2 2 2
离出的Ag+结合生成[AgCl]-,使平衡正向移动,提高Ag S的浸出率;H+是为了抑制Fe3+水
2 2
解,防止生成Fe(OH) 沉淀(2分)
3
(3)2[AgCl]- +Fe=Fe2++2Ag+4Cl- (2分)、2Fe3++Fe=3Fe2+ (1分) Fe2+被氧气氧化
2
为Fe3+,Fe3+把Ag氧化为Ag+(2分)
(4)可将两种矿石中的锰元素同时提取到浸锰液中,得到MnSO ,同时将银元素和锰元
4
素分离开;生成的Fe3+还可以用于浸银,节约氧化剂(2分)
16.(14分)(每空2分)(1)与空气的接触面积增大,反应更加充分
(2)2CaSO 2CaO+2SO↑+O↑
4 2 2
(3) ①. SO+I +HO=3I—+SO +4H+ ②. 3I——2e—=I
2 2
(4)
(5) ①. I+I—=I ②. 偏小
2
17.(16分)(1) (2分)
(2) 90℃ ,防止 受热分解,以提高原料利用率 (2分)
(3) (2分)
(4)用滴定管A量取一定体积的上述II中混合液于锥形瓶中,加入淀粉溶液作指示剂,
用滴定管 B 量取一定体积的 0.1000mol/L 溶液进行滴定,当滴入最后半滴
溶液时,蓝色褪去且半分钟内颜色不复原,即达到滴定终点,记录标准液的体积。
(6分)
学科网(北京)股份有限公司(说明:本题需分析第II步发生反应: )
(5) 99.14%(4分)正确求出体积2分,产品纯度结果正确2分。
18.(14分)
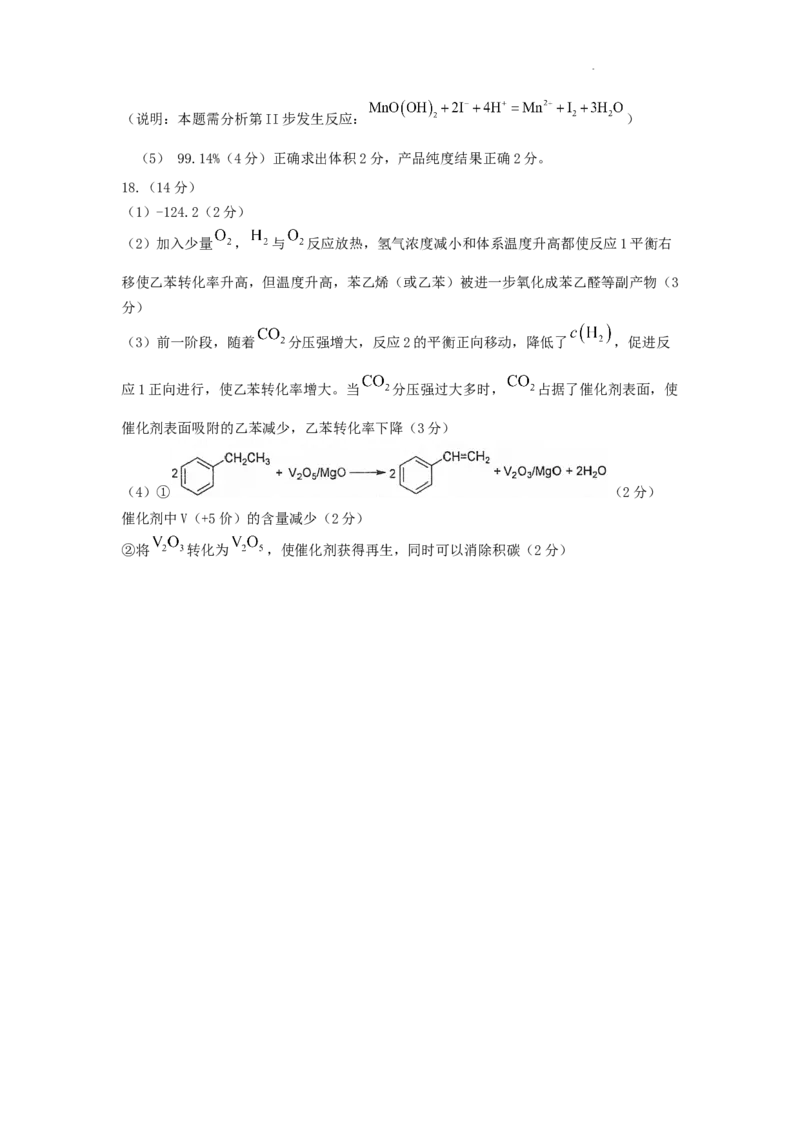
(1)-124.2(2分)
(2)加入少量 , 与 反应放热,氢气浓度减小和体系温度升高都使反应1平衡右
移使乙苯转化率升高,但温度升高,苯乙烯(或乙苯)被进一步氧化成苯乙醛等副产物(3
分)
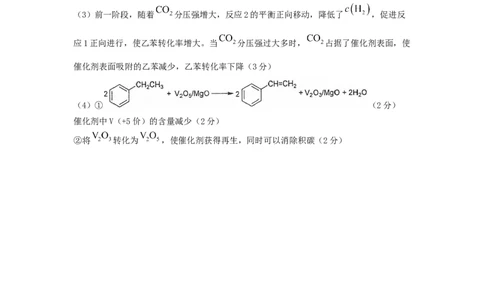
(3)前一阶段,随着 分压强增大,反应2的平衡正向移动,降低了 ,促进反
应1正向进行,使乙苯转化率增大。当 分压强过大多时, 占据了催化剂表面,使
催化剂表面吸附的乙苯减少,乙苯转化率下降(3分)
(4)① (2分)
催化剂中V(+5价)的含量减少(2分)
②将 转化为 ,使催化剂获得再生,同时可以消除积碳(2分)
学科网(北京)股份有限公司