文档内容
第三章 烃的衍生物
第一节 卤代烃
1.(2020·浙江绍兴市·诸暨中学高二期中)常温常压下为无色液体,而且密度大于水的是( )
①一氯甲烷 ②硝基苯 ③溴苯 ④四氯化碳 ⑤溴乙烷 ⑥乙酸乙酯
A.①⑥ B.②③④⑥ C.②③④⑤ D.①④⑤
【答案】C
【详解】
①一氯甲烷常温常压下为无色气体,密度比水小;②硝基苯常温常压下为无色具有苦杏仁味的液体,难溶
于水、密度比水大;③溴苯常温常压下为无色液体,难溶于水、密度比水大;④四氯化碳常温常压下为无
色液体,难溶于水、密度比水大;⑤溴乙烷常温常压下为无色液体,难溶于水、密度比水大;⑥乙酸乙酯
常温常压下为无色有香味的液体,难溶于水、密度比水小;则常温常压下为无色液体、且密度大于水的是
②③④⑤,答案选C。
2.(2019·大安市第六中学校高二期末)溴乙烷在某种条件下可生成乙烯或乙醇,下列说法正确的是
( )
A.生成乙烯的条件可以是热的氢氧化钾水溶液 B.生成乙醇的条件可以是热的氢氧化钾水溶液
C.生成乙烯的条件是加热 D.生成乙醇的条件可以是热的氢氧化钾醇溶液
【答案】B
【详解】
A.生成乙烯时,溴乙烷发生消去反应,所以条件可以是热的氢氧化钾醇溶液,A不正确;
B.生成乙醇时,溴乙烷发生水解反应,所以条件可以是热的氢氧化钾水溶液,B正确;
C.由上面分析可知,生成乙烯的条件是热的氢氧化钾醇溶液,C不正确;
D.由上面分析可知,生成乙醇的条件可以是热的氢氧化钾水溶液,D不正确;
故选B。
3.(2021·全国高一课时练习)下列化学反应中,属于取代反应的是( )
A.CH+2O CO+2H O
4 2 2 2
B.CHCHOH CH=CH ↑+H O
3 2 2 2 2C.CHCHBr+NaOH CHCHOH+NaBr
3 2 3 2
D.CHCH=CH+HCl CHCHCHCl
3 2 3 2 2
【答案】C
【分析】
有机物中的原子或原子团被其他原子或原子团所取代的反应叫做取代反应
【详解】
A.选项中的反应为甲烷的氧化反应,A不符合题意;
B.选项中的反应为乙醇的消去反应,B不符合题意;
C.选项中的反应为卤代烃的水解反应,属于取代反应,C符合题意;
D.选项中的反应为烯烃的加成反应,D不符合题意;
故答案选C。
4.2010年6月11日~7月12日,第19届世界杯足球赛在南非举行。当运动员肌肉受伤时,队医会随即
对准球员的受伤部位喷射药剂氯乙烷(化学式为C HCl,沸点为12.3℃),进行局部冷冻麻醉处理。下列
2 5
有关氯乙烷的说法错误的是
A.氯乙烷中的三种元素均处于化合态
B.氯乙烷中某些原子最外层未达到8电子稳定结构
C.氯乙烷用于冷冻麻醉与其沸点较低、易挥发吸热有关
D.1个C HCl分子含有24个电子
2 5
【答案】D
【解析】
【详解】
A、氯乙烷是化合物,化合物中的元素均处于化合态,故A正确;
B、氯乙烷(化学式为C HCl),氢原子与碳原子间形成1对共用电子对,氢原子最外层有2个电子,原
2 5
子最外层未达到8电子稳定结构,故B正确;
C、氯乙烷沸点较低、易挥发吸热,故可用于用于冷冻麻醉,故C正确;
D、碳原子核外电子数为6,氢原子核外电子数为1,氯原子核外电子数为17,所以1个C HCl分子含有
2 5
电子数为:2×6+1×5+17×1=34;故D错误;
故答案选D。
5.(2020·江苏徐州市·高二期中)为了检验某氯代烃中的氯元素,现进行如下操作,其中合理的是
A.取氯代烃少许,加入AgNO 溶液
3B.取氯代烃少许与NaOH水溶液共热,然后加入AgNO 溶液
3
C.取氯代烃少许与NaOH水溶液共热后,加入稀硝酸酸化,再加入AgNO 溶液
3
D.取氯代烃少许与NaOH水溶液共热后,加入稀盐酸酸化,再加入AgNO 溶液
3
【答案】C
【详解】
A.氯代烃中不存在Cl-,加入AgNO 溶液后,不发生反应,A不合理;
3
B.氯代烃与NaOH水溶液共热后发生水解,生成NaCl等,但由于溶液呈碱性,加入AgNO 溶液后,OH-
3
也会与Ag+反应生成白色沉淀,从而干扰Cl-的检验,B不合理;
C.氯代烃与NaOH水溶液共热后,加入稀硝酸酸化,将OH-转化为HO,从而排除OH-产生的干扰,再加
2
入AgNO 溶液,生成白色沉淀,则证明氯代烃中含有氯元素,C合理;
3
D.氯代烃与NaOH水溶液共热后,加入稀盐酸酸化,此时引入了Cl-,从而干扰氯代烃水解液中Cl-的检验,
D不合理;
故答案选C。
6.(2020·湖北高二期中)化学与生产生活、社会密切相关。下列说法中错误的是( )
A.天然气的主要成分是甲烷
B.75%医用酒精可有效消灭新型冠状病毒
C.用氟利昂做制冷剂会加剧雾霾天气的形成
D.用浸泡过高锰酸钾溶液的硅藻土保鲜水果,其作用是吸收水果释放出的乙烯
【答案】C
【详解】
A.天然气的主要成分是甲烷,故A正确;
B.75%医用酒精是有效的消毒剂,可以杀灭新型冠状病毒,故B正确;
C.氟利昂可导致臭氧空洞,与雾霾无关,故C错误;
D.乙烯为催熟剂,含有碳碳双键,可被高锰酸钾氧化,则用浸泡过高锰酸钾溶液的硅藻土吸收乙烯,降
低乙烯浓度,可利于保鲜水果,故D正确;
答案为C。
7.(2021·哈尔滨市·黑龙江实验中学高二期末)某有机物结构简式如图,下列叙述不正确的是( )
A.1mol该有机物在加热和催化剂作用下,最多能和4molH 反应
2
B.该有机物能使溴水褪色,也能使酸性KMnO 溶液褪色
4C.该有机物属于芳香烃,在一定条件下能通过加聚反应生成高分子化合物
D.该有机物在一定条件下能发生消去反应或取代反应
【答案】C
【详解】
A.1mol该有机物含有1mol苯环和1mol碳碳双键,在加热和催化剂作用下,最多能和4molH 反应,故A
2
不选;
B.该有机物含有碳碳双键,能使溴水褪色,也能使酸性KMnO 溶液褪色,故B不选;
4
C.该有机物含有碳元素、氢元素和氯元素,不属于芳香烃,有碳碳双键,但在一定条件下能通过加聚反
应生成高分子化合物,故C选;
D.该有机物含有氯原子,与氯原子相连碳原子的相邻碳原子上有氢原子,在一定条件下能发生消去反应,
氯原子也可以发生取代反应,故D不选;
故选:C。
8.(2021·湖北武汉市·高二期末)下列实验操作能达到目的的是
实验目的 实验操作
A 除去溴苯中的溴单质 加入NaOH溶液振荡,分液
B 除去乙烷中的乙烯 将混合气体通入酸性高锰酸钾溶液
C 除去乙酸乙酯中的乙酸 加入NaOH 溶液振荡,分液
D 检验溴乙烷与氢氧化钠醇溶液加热生成乙烯 将生成的气体通入酸性高锰酸钾溶液中观察颜色变化
【答案】A
【详解】
A.溴与NaOH溶液反应得到溴化钠、次溴酸钠和水,属于无机物,与溴苯互不相溶,通过分液实现分离,
故A项正确;
B.将乙烯通入酸性高锰酸钾溶液,会产生二氧化碳新杂质,故B项错误;
C.除去乙酸乙酯中的乙酸,应选用饱和碳酸钠溶液,故C项错误;
D.挥发出的乙醇,也能使酸性高锰酸钾溶液褪色,故D项错误;
故本题选A。
9.(2020·全国高三专题练习)用下列仪器或装置(图中夹持略)进行相应实验,不能达到实验目的的是
A B C D配制一定物
质的量浓度 检验浓硫酸与铜反应产生的 检验溴乙烷消去产物中的
分离酒精和水
的氯化钠溶 二氧化硫 乙烯
液
【答案】D
【解析】
【详解】
A.图示为配制一定量浓度溶液的转移操作,图示操作正确,故A 能达到实验目的;
B.浓硫酸和铜在加入条件下反应生成二氧化硫,二氧化硫具有漂白性,通入到品红溶液中,若品红褪色,
则证明生成二氧化硫,二氧化硫气体是大气污染物,不能排放到空气中,试管口用浸有氢氧化钠溶液的棉
花团吸收二氧化硫,图示正确,故B能达到实验目的;
C.溴乙烷在氢氧化钠醇溶液加热作用下发生消去反应生成乙烯,由于乙醇易挥发,制得的乙烯中含有乙
醇蒸汽,先通过水,使乙醇溶于水,在将气体通入酸性高锰酸钾溶液中,若酸性高锰酸钾溶液褪色,则可
以证明反应中产生乙烯,故C能达到实验目的;
D.乙醇和水任意比互溶,分液操作无法分离,故D不能达到实验目的;
答案选D。
10.(2020·甘谷县第四中学高三月考)如图装置可用于检验溴乙烷与氢氧化钠的醇溶液反应生成的乙烯,
下列说法不正确的是( )
A.该反应为消去反应
B.实验过程中可观察到酸性KMnO 溶液褪色
4
C.乙烯难溶于水,故此装置②可以省去D.可用溴水代替酸性KMnO 溶液
4
【答案】C
【详解】
A.溴乙烷在氢氧化钠的醇溶液中加热发生消去反应生成乙烯,故A正确;
B.乙烯能被高锰酸钾氧化,使酸性KMnO 溶液褪色,故B正确;
4
C.因乙醇、乙烯均使酸性高锰酸钾溶液褪色,干扰乙烯的检验,装置②是除去挥发出来的乙醇杂质的,
不能省去,故C错误;
D.乙烯与溴水发生加成反应,可用溴水代替酸性KMnO 溶液来检验乙烯,故D正确;
4
故选C 。
11.(2021·沙坪坝区·重庆八中高二期末)下列物质中,既能发生水解反应,又能发生加成反应,但不能
发生消去反应的是
A.(CH)CHCH Cl B.CH=CHC(CH )CHCl
3 2 2 2 3 2 2
C.CHCHFCH=CH D.CH=CHCHCHBr
3 2 2 2 2
【答案】B
【详解】
A.(CH)CHCH Cl,不含不饱和键,不能加成,卤代烃能水解,与-X相连碳的相邻碳上有氢原子,能消
3 2 2
去,故A错误;
B.CH=CHC(CH )CHCl含有双键,能加成,卤代烃能水解,与Cl相连碳的相邻碳上没有氢原子,不能
2 3 2 2
消去,故B正确;
C.CHCHFCH=CH 含有双键,能加成,卤代烃能水解,与F原子相连碳的相邻碳上有氢原子,能发生消
3 2
去反应,故C错误;
D.CH=CHCHCHBr含有双键,能加成,卤代烃能水解,与Br相连碳的相邻碳上有氢原子,能消去,故
2 2 2
D错误;
故选B。
12.(2020·江西宜春市·高安中学高二期末)有机物CH-CH=CH-Cl不能发生的反应有( )
3
①取代反应 ②加成反应 ③消去反应 ④使溴水褪色 ⑤使KMnO 酸性溶液褪色 ⑥与AgNO 溶
4 3
液生成白色沉淀 ⑦加聚反应
A.①②③④⑤⑥⑦ B.⑦ C.⑥ D.②
【答案】C
【详解】有机物CH-CH=CH-Cl中含有碳碳双键,可发生加成、加聚和氧化反应,则②④⑤⑦正确;含有-Cl,可发
3
生取代和消去反应,则①③正确;不能在溶液中电离出氯离子,则不能与AgNO 溶液生成白色沉淀,故⑥
3
错误,故选C。
【点睛】
本题的易错点为⑥,要注意CH-CH=CH-Cl不溶于水,不能电离出氯离子。
3
13.(2020·全国高一单元测试)下列有关氟氯烃的说法中不正确的是
A.氟氯烃是一类含氟和氯的卤代烃
B.氟氯烃的化学性质稳定,有毒
C.氟氯烃大多无色、无臭、无毒
D.在平流层中,氟氯烃在紫外线照射下分解产生的氯原子可引发损耗臭氧的循环反应
【答案】B
【解析】
【详解】
A.烃分子中1个或者多个氢原子被卤原子取代得到的产物为卤代烃,故A正确;
B.氟氯烃在紫外线照射下,分解产生氯原子从而引发损耗臭氧的循环反应,造成臭氧层空洞,使大量的
紫外线照向大地,伤害地球上的生物,但无毒,故B错误;
C.依据氟氯烃物理性质解答:大多数无色,无臭,无毒,故C正确;
D.在平流层,氟氯烃在紫外线照射下,分解产生氯原子可引发损耗O 的循环反应,故D正确;
3
故答案为B。
【点睛】
氟氯烃是一类含氟和氯的卤代烃,它化学性质稳定,大多无色、无臭、无毒,所以它被广泛应用于制冷业,
但是释放到空气中的氟氯烃,可以到达大气平流层,并且在紫外线作用下,分解产生氯原子,从而引发损
耗臭氧的循环反应,造成臭氧层空洞,使大量的紫外线照向大地,伤害地球上的生物。
14.(2020·江苏无锡市·高二期中)下列反应的有机产物只有一种的的是( )
A.CHCHCHCl在NaOH水溶液中加热
3 2 2
B.CHCH=CH 与HCl加成
3 2
C.CH=CH—CH=CH 与H 按1:1的物质的量之比进行反应
2 2 2
D.2—氯丁烷(CHCHCHClCH )与NaOH/乙醇溶液共热
3 2 3
【答案】A
【详解】
A.CHCHCHCl在NaOH水溶液中加热发生水解反应,生成CHCHCHOH,有机产物只有一种,故选
3 2 2 3 2 2A;
B.CHCH=CH 与HCl加成反应,生成CHCHCHCl或CHCHClCH ,有机产物有两种,故不选B;
3 2 3 2 2 3 3
C.CH=CH—CH=CH 与H 按1:1的物质的量之比进行反应,生成CHCHCH=CH 或CHCH=CHCH ,
2 2 2 3 2 2 3 3
有机产物有两种,故不选C;
D.2—氯丁烷(CHCHCHClCH )与NaOH/乙醇溶液共热发生消去反应,生成CHCHCH=CH 或
3 2 3 3 2 2
CHCH=CHCH ,有机产物有两种,故不选D;
3 3
选A。
15.(2021·平罗中学高二期末)制取1,2-二溴乙烷,以溴乙烷为原料,下列转化方案中最优的是
A.CHCHBr CHCHOH CH=CH CHBrCHBr
3 2 3 2 2 2 2 2
B.CHCHBr CHBrCHBr
3 2 2 2
C.CHCHBr CH=CH CHBrCH CHBrCHBr
3 2 2 2 2 3 2 2
D.CHCHBr CH=CH CHBrCHBr
3 2 2 2 2 2
【答案】D
【详解】
A.转化中发生三步转化,较复杂,消耗的试剂多,反应需要加热,故A不选;
B.发生取代反应的产物较多,引入杂质,且反应不易控制,故B不选;
C.转化中发生三步转化,较复杂,且最后一步转化为取代反应,产物不纯,故C不选;
D.发生消去、加成两步转化,节约原料、转化率高、操作简单、产物纯净,故D选;
故选D。
16.(2020·常州市第二中学高二期中)溴乙烷是卤代烃的代表,通过对溴乙烷的探究来掌握卤代烃的性质,
可以达到举一反三、触类旁通的效果。
I.已知:NaBr+HSO (浓) NaHSO+ HBr
2 4 4
CHCHOH+HBr CHCHBr+H O
3 2 3 2 2
溴乙烷的沸点38.4℃,实验室制备溴乙烷(CHCHBr)的装置和步骤如下:
3 2
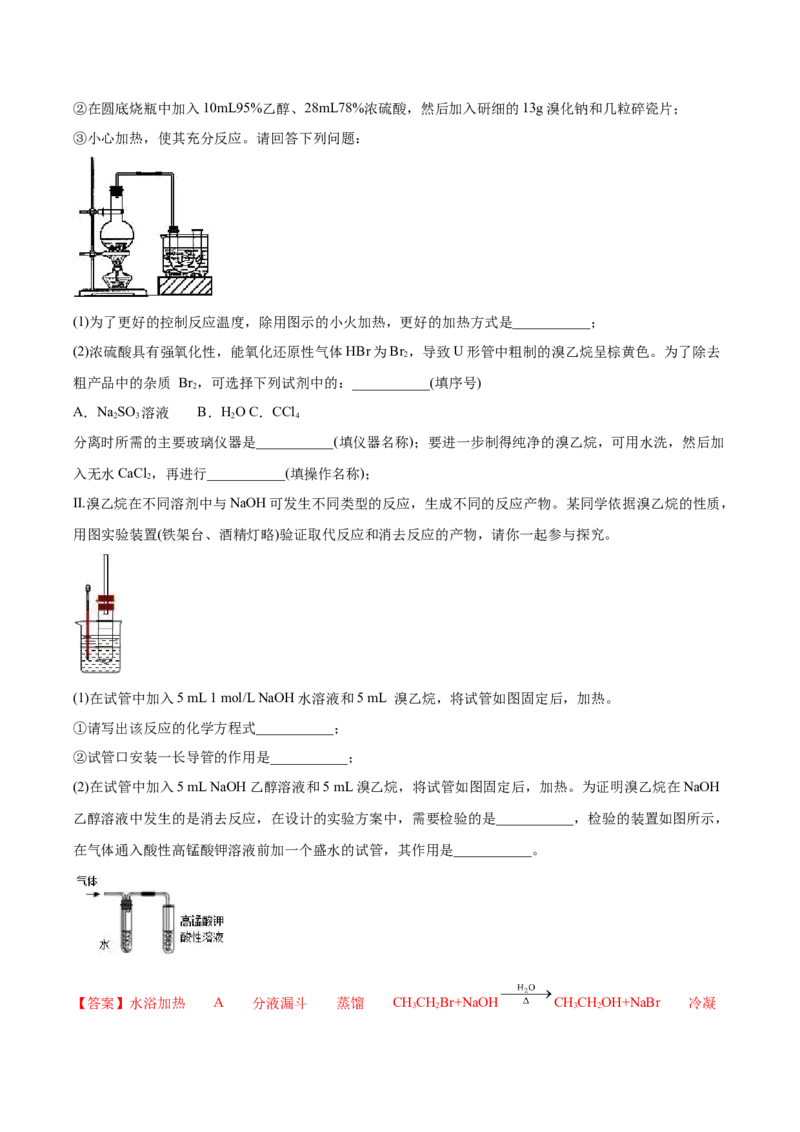
①检查装置的气密性,向装置图所示的 U 形管和大烧杯中加入冰水;②在圆底烧瓶中加入10mL95%乙醇、28mL78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;
③小心加热,使其充分反应。请回答下列问题:
(1)为了更好的控制反应温度,除用图示的小火加热,更好的加热方式是___________;
(2)浓硫酸具有强氧化性,能氧化还原性气体HBr为Br ,导致U形管中粗制的溴乙烷呈棕黄色。为了除去
2
粗产品中的杂质 Br ,可选择下列试剂中的:___________(填序号)
2
A.NaSO 溶液 B.HO C.CCl
2 3 2 4
分离时所需的主要玻璃仪器是___________(填仪器名称);要进一步制得纯净的溴乙烷,可用水洗,然后加
入无水CaCl ,再进行___________(填操作名称);
2
II.溴乙烷在不同溶剂中与NaOH可发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,
用图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。
(1)在试管中加入5 mL 1 mol/L NaOH水溶液和5 mL 溴乙烷,将试管如图固定后,加热。
①请写出该反应的化学方程式___________;
②试管口安装一长导管的作用是___________;
(2)在试管中加入5 mL NaOH乙醇溶液和5 mL溴乙烷,将试管如图固定后,加热。为证明溴乙烷在NaOH
乙醇溶液中发生的是消去反应,在设计的实验方案中,需要检验的是___________,检验的装置如图所示,
在气体通入酸性高锰酸钾溶液前加一个盛水的试管,其作用是___________。
【答案】水浴加热 A 分液漏斗 蒸馏 CHCHBr+NaOH CHCHOH+NaBr 冷凝
3 2 3 2回流减少溴乙烷的损失 乙烯 除去乙烯中混有的乙醇
【分析】
I.用水浴加热使烧瓶均匀受热,溴化钠、浓硫酸在烧瓶中反应产生HBr,HBr和乙醇在烧瓶中反应产生溴
乙烷,溴乙烷的沸点较低,挥发到U形管中用冰水冷凝得到液态的溴乙烷;
II.溴乙烷在NaOH水溶液中发生取代反应产生乙醇,在NaOH醇溶液中发生消去反应产生乙烯,可用溴
的水溶液、溴的四氯化碳溶液、或除去乙醇后通入酸性高锰酸钾溶液检验发生的是消去反应。
【详解】
I.(1)为了更好的控制温度,除用图示的小火加热外,最好用水浴加热的方法;
(2)在U型管内有Br :
2
A. Na SO 能与溴发生氧化还原反应,可除去溴,A项符合题意;
2 3
B. 溴在水中的溶解度小于在溴乙烷中的溶解度,无法加水除杂,B项不符合题意;
C. 溴和溴乙烷都能溶于四氯化碳,不能将二者分离,C项不符合题意;
答案选A;
加入NaSO 溶液反应,静置、分层、然后分液,使用的主要仪器是分液漏斗;
2 3
要进一步制得纯净的C HBr,可用水洗,分液后再加入无水CaCl ,利用沸点不同再进行蒸馏;
2 5 2
II.(1)①溴乙烷在NaOH水溶液中加热发生取代反应,反应的化学方程式为CHCHBr+NaOH
3 2
CHCHOH+NaBr;
3 2
②溴乙烷的沸点38.4℃,溴乙烷易挥发,用长导管进行冷凝回流减少溴乙烷的损失;
(2)溴乙烷在NaOH乙醇溶液中加热发生消去反应产生乙烯,因此为证明溴乙烷在NaOH乙醇溶液中发生的
是消去反应,需检验乙烯;
检验乙烯可根据其能使酸性高锰酸钾褪色的原理进行,但同时乙醇易挥发且能使酸性高锰酸钾褪色,故需
要除去乙烯中的乙醇,乙醇能溶于水,而乙烯不能溶于水,故在气体通入酸性高锰酸钾溶液前加一个盛水
的试管,其作用是除去乙烯中混有的乙醇。
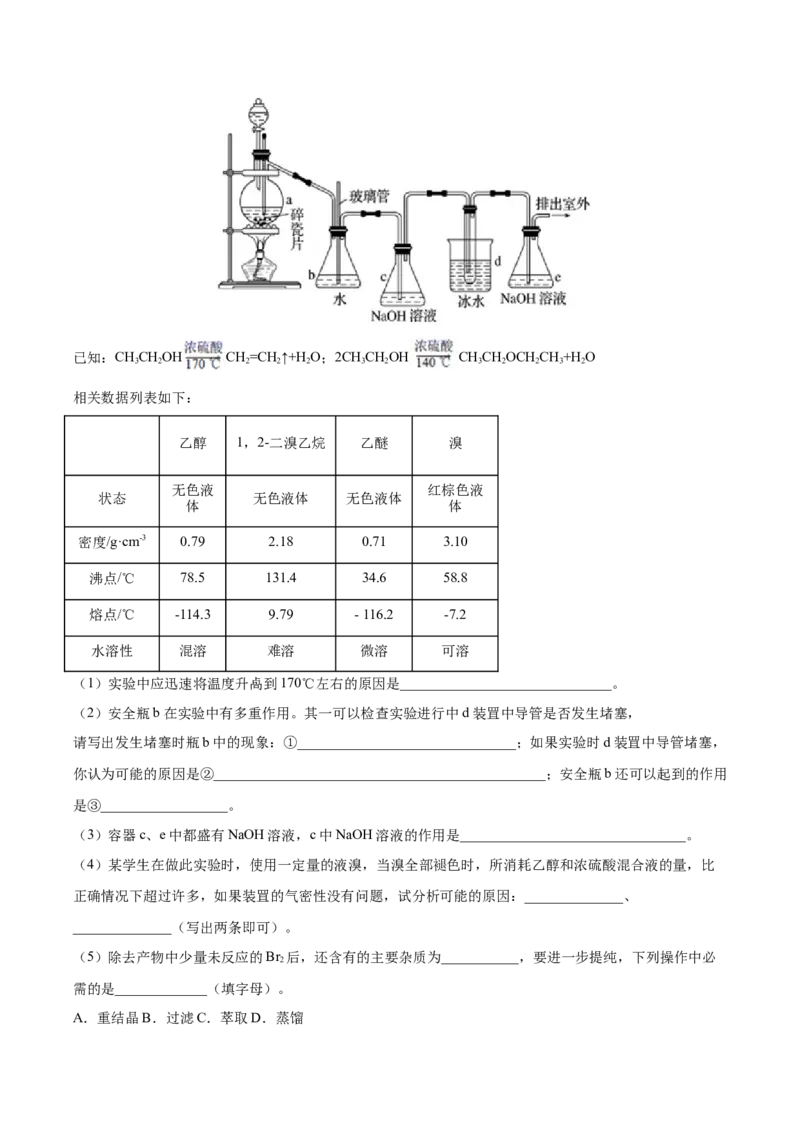
17.(2019·河北省曲阳县第一高级中学高二月考)1,2-二溴乙烷可作抗爆剂的添加剂。如图为实验室制
备1,2-二溴乙烷的装罝图, 图中分液制斗和烧瓶a中分别装有浓HSO 和无水乙醇,d装罝试管中装有
2 4
液溴。已知:CHCHOH CH=CH ↑+H O;2CHCHOH CHCHOCH CH+H O
3 2 2 2 2 3 2 3 2 2 3 2
相关数据列表如下:
乙醇 1,2-二溴乙烷 乙醚 溴
无色液 红棕色液
状态 无色液体 无色液体
体 体
密度/g·cm-3 0.79 2.18 0.71 3.10
沸点/℃ 78.5 131.4 34.6 58.8
熔点/℃ -114.3 9.79 - 116.2 -7.2
水溶性 混溶 难溶 微溶 可溶
(1)实验中应迅速将温度升卨到170℃左右的原因是______________________________。
(2)安全瓶b在实验中有多重作用。其一可以检查实验进行中d装罝中导管是否发生堵塞,
请写出发生堵塞时瓶b中的现象:①_______________________________;如果实验时d装罝中导管堵塞,
你认为可能的原因是②_______________________________________________;安全瓶b还可以起到的作用
是③__________________。
(3)容器c、e中都盛有NaOH溶液,c中NaOH溶液的作用是________________________________。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比
正确情况下超过许多,如果装罝的气密性没有问题,试分析可能的原因:______________、
______________(写出两条即可)。
(5)除去产物中少量未反应的Br 后,还含有的主要杂质为___________,要进一步提纯,下列操作中必
2
需的是_____________(填字母)。
A.重结晶B.过滤C.萃取D.蒸馏(6)实验中也可以撤去d装罝中盛冰水的烧杯,改为将冷水直接加入到d装罝的试管中,则 此时冷水除
了能起到冷却1,2-二溴乙烷的作用外,还可以起到的作用是____________________________。
【答案】减少副产物乙醚生成 b中长直玻璃管内液柱上升 过度冷却,产品1,2-二溴乙烷在装罝d
中凝固 防止倒吸 吸收乙烯气体中含有的CO、SO 等酸性气体 浓硫酸将部分乙醇氧化 发
2 2
生副反应生成乙醚;乙醇挥发;乙烯流速过快,未完全发生加成反应(写出两条即可) 乙醚 D
【答题空10】液封Br 和1,2-二溴乙烷,防止它们挥发
2
【解析】
(1)乙醇在浓硫酸140℃的条件下,发生分子内脱水,生成乙醚,实验中应迅速将温度升高到170℃左右
的原因是减少副产物乙醚生成;(2)根据大气压强原理,试管d发生堵塞时,b中压强的逐渐增大会导致
b中水面下降,玻璃管中的水柱上升,甚至溢出,故答案为b中长直玻璃管内有一段液柱上升。1,2-二溴
乙烷的凝固点9℃较低,不能过度冷却,过度冷却,就会在装置d中凝固造成堵塞。b装置导管短进长出,
可以防止倒吸;(3)由于浓硫酸具有强氧化性,能够氧化碳,同时被还原成具有刺激性气味的二氧化硫
气体,因此乙烯气体中混有CO、SO 等酸性气体,所以c中NaOH溶液作用是吸收乙烯气体中含有的
2 2
CO、SO 等酸性气体;(4)当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多
2 2
的原因可能是发生副反应生成乙醚;乙醇挥发;乙烯流速过快,未完全发生加成反应等;(5)1,2-二溴
乙烷与乙醚的沸点不同,两者均为有机物,互溶,用蒸馏的方法将它们分离,故选D;(6)溴易挥发,
在试管d中加入少量冰水可起到液封的作用,还可降低温度,减少挥发。
点睛:本题考查了乙醇制备1,2-二溴乙烷,掌握相关物质的基本化学性质。解题的关键是实验装置的正
确分析及反应产物的判断。