文档内容
3.4.1 难溶电解质的沉淀溶解平衡 练习(解析版)
一.选择题(共14小题)
1.25℃时CaCO 溶于水达饱和,其物质的量浓度为5.0×10﹣5mol•L﹣1,该温度下CaCO 的K 为(
3 3 sp
)
A.5.0×10﹣5 B.2.5×10﹣9 C.5.0×10﹣10 D.1.0×10﹣10
【答案】B
【解析】CaCO 溶于水达饱和,其物质的量浓度为5.0×10﹣5mol/L,CaCO 饱和溶液中c(Ca2+)=
3 3
c(CO 2﹣)=5.0×10﹣5mol•L﹣1,Ksp=5.0×10﹣5mol•L﹣1×5.0×10﹣5mol•L﹣1=2.5×10﹣9mol2/L2,故
3
选:B。
2.已知 相同温度下:K [Zn(OH) ]>K (ZnS),K (MgCO )>K [Mg(OH) ]; 电
sp 2 sp sp 3 sp 2
离出S①2﹣的能力:FeS>H S>CuS.则下列离子方程式错误的是( ) ②
2
A.将FeS加入稀盐酸中:FeS+2H+═Fe2++H S↑
2
B.向CuSO 溶液中通H S气体:Cu2++H S═CuS↓+2H+
4 2 2
C.将ZnCl 溶液和Na S溶液混合:Zn2++S2﹣+2H O═Zn(OH) ↓+H S↑
2 2 2 2 2
D.向少量Mg(HCO ) 溶液中加入足量NaOH溶液:Mg2++2HCO ﹣+4OH﹣═Mg(OH)
3 2 3
↓+2CO 2﹣+2H O
2 3 2
【答案】C
【解析】A.由 可知,电离出S2﹣的能力:FeS>H S,则FeS+2H+═H S↑+Fe2+,故A正确;
2 2
B.由 可知,②Cu2+易结合S2﹣,则Cu2++H S═CuS↓+2H+,故B正确;
2
C.因②溶解度Zn(OH) >ZnS,则Zn2++S2﹣+2H O═Zn(OH) ↓+H S↑不能发生,且ZnS不溶
2 2 2 2
于水,故C错误;
D.由 可知,Mg(OH) 更难溶,则碳酸氢镁与足量NaOH溶液反应生成碳酸钠、氢氧化镁、
2
水,离①子反应为Mg2++2HCO ﹣+4OH﹣═Mg(OH) ↓+2CO 2﹣+2H O,故D正确;故选:C。
3 2 3 2
3.某化学兴趣小组进行下列实验:
将0.1mol•L﹣1的MgCl 溶液和0.5mol•L﹣1的NaOH溶液等体积混合得到浊液
2
①取少量 中浊液,滴加0.1mol•L﹣1的FeCl 溶液,出现红褐色沉淀
3
②过滤 ①中浊液,取少量白色沉淀,滴加0.1mol•L﹣1的FeCl 溶液,白色沉淀变为红褐色沉淀
3
③另取①少量白色沉淀,滴加饱和NH
4
Cl溶液,沉淀溶解
④下列说法中错误的是( )
A.将 中浊液过滤,所得滤液中有微量的Mg2+存在
B.实验① 和 均能说明Fe(OH)
3
比Mg(OH)
2
难溶
② ③C. 中沉淀转化反应式为:3Mg(OH) (s)+2Fe3+(aq) 2Fe(OH) (s)+3Mg2+(aq)
2 3
D.③NH 4 Cl溶液中的NH 4 +水解可能是 中沉淀溶解的原因 ⇌
【答案】B ④
【解析】将0.1mol/LMgCl 溶液和0.5mol/LNaOH溶液等体积混合得到氢氧化镁悬浊液和氯化钠以
2
及剩余氢氧化钠的混合物,
A.将 中所得浊液氢氧化镁过滤,氢氧化镁存在沉淀溶解平衡:Mg(OH) Mg2++2OH﹣,所得
2
滤液中①含少量Mg2+,故A正确; ⇌
B.实验 中是因为剩余的氢氧化钠和氯化铁之间反应生成氢氧化铁的缘故,不能说明 Fe(OH)
3
比Mg(O②H) 难溶,故B错误;
2
C.氢氧化镁悬浊液中滴加氯化铁,白色沉淀变为红褐色沉淀,转化反应式为:3Mg(OH) (s)
2
+2Fe3+(aq) 2Fe(OH) (s)+3Mg2+(aq),故C正确;
3
D.氢氧化镁⇌存在沉淀溶解平衡:Mg(OH) Mg2++2OH﹣,加氯化铵,会和氢氧根离子之间反应,
2
所以平衡正向移动,沉淀溶解,故D正确;故⇌选:B。
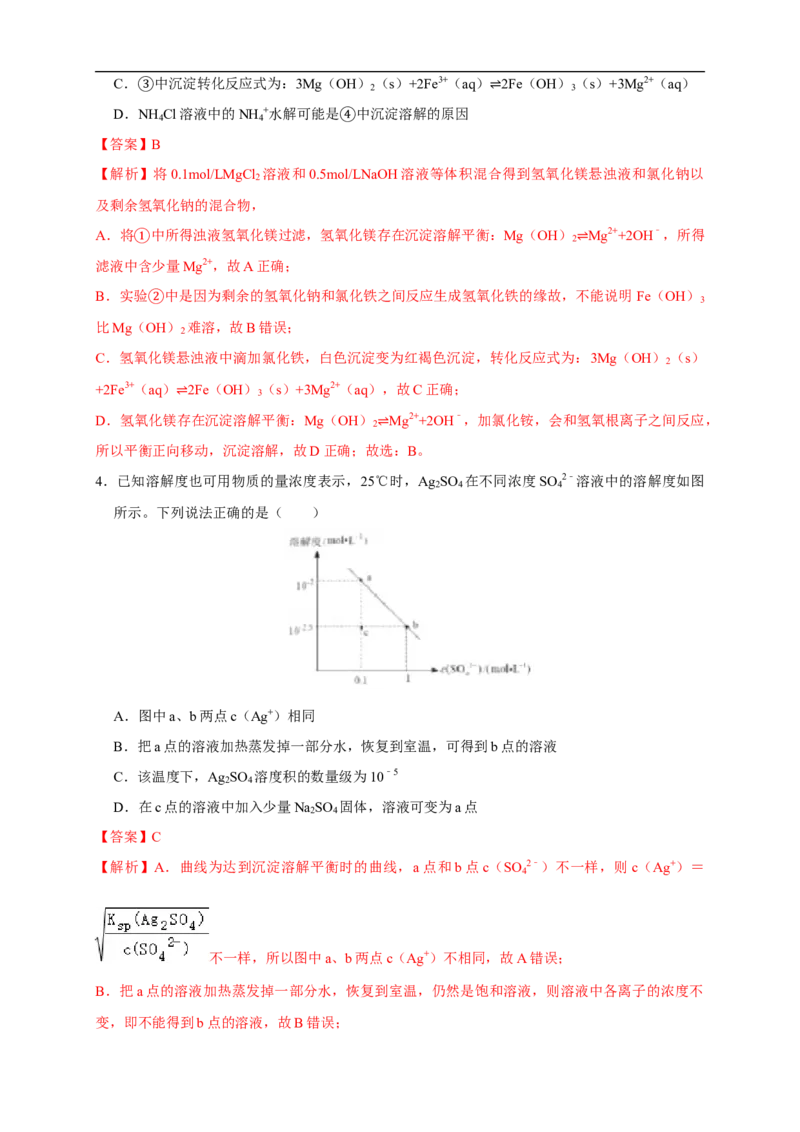
4.已知溶解度也可用物质的量浓度表示,25℃时,Ag SO 在不同浓度SO 2﹣溶液中的溶解度如图
2 4 4
所示。下列说法正确的是( )
A.图中a、b两点c(Ag+)相同
B.把a点的溶液加热蒸发掉一部分水,恢复到室温,可得到b点的溶液
C.该温度下,Ag SO 溶度积的数量级为10﹣5
2 4
D.在c点的溶液中加入少量Na SO 固体,溶液可变为a点
2 4
【答案】C
【解析】A.曲线为达到沉淀溶解平衡时的曲线,a点和b点c(SO 2﹣)不一样,则c(Ag+)=
4
不一样,所以图中a、b两点c(Ag+)不相同,故A错误;
B.把a点的溶液加热蒸发掉一部分水,恢复到室温,仍然是饱和溶液,则溶液中各离子的浓度不
变,即不能得到b点的溶液,故B错误;C.根据图象上相关数据,Ag SO (s) 2Ag+(aq)+SO 2﹣(aq),当c(SO 2﹣)=1mol/L时,
2 4 4 4
溶液中c(Ag+)=2×10﹣2.5mol/L,则K⇌=c2(Ag+)•c(SO 2﹣)=(2×10﹣2.5)2×1=4×10﹣5,则
sp 4
数量级为10﹣5,故C正确;
D.在c点的溶液是不饱和溶液,加入少量Na SO 固体,溶液中c(SO 2﹣)增大,c(Ag+)不变,
2 4 4
不可能从c点变为a点,故D错误。故选:C。
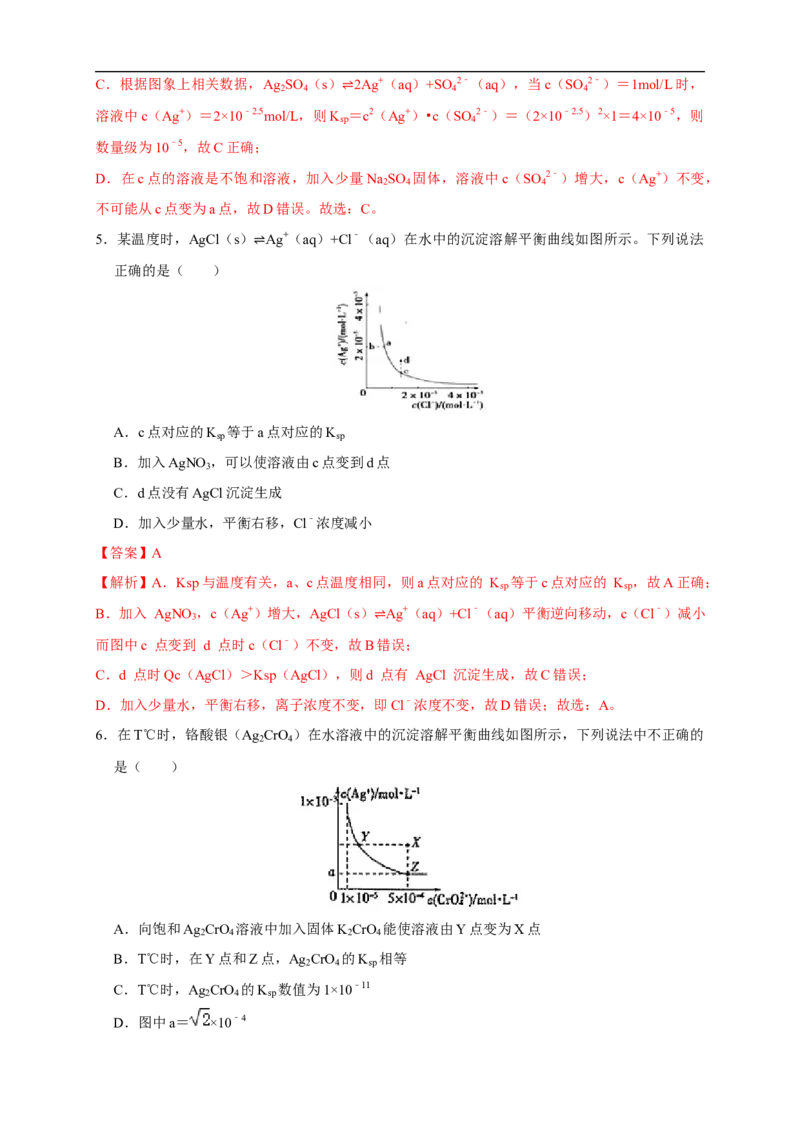
5.某温度时,AgCl(s) Ag+(aq)+Cl﹣(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法
正确的是( ) ⇌
A.c点对应的K 等于a点对应的K
sp sp
B.加入AgNO ,可以使溶液由c点变到d点
3
C.d点没有AgCl沉淀生成
D.加入少量水,平衡右移,Cl﹣浓度减小
【答案】A
【解析】A.Ksp与温度有关,a、c点温度相同,则a点对应的 K 等于c点对应的 K ,故A正确;
sp sp
B.加入 AgNO ,c(Ag+)增大,AgCl(s) Ag+(aq)+Cl﹣(aq)平衡逆向移动,c(Cl﹣)减小
3
而图中c 点变到 d 点时c(Cl﹣)不变,故B⇌错误;
C.d 点时Qc(AgCl)>Ksp(AgCl),则d 点有 AgCl 沉淀生成,故C错误;
D.加入少量水,平衡右移,离子浓度不变,即Cl﹣浓度不变,故D错误;故选:A。
6.在T℃时,铬酸银(Ag CrO )在水溶液中的沉淀溶解平衡曲线如图所示,下列说法中不正确的
2 4
是( )
A.向饱和Ag CrO 溶液中加入固体K CrO 能使溶液由Y点变为X点
2 4 2 4
B.T℃时,在Y点和Z点,Ag CrO 的K 相等
2 4 sp
C.T℃时,Ag CrO 的K 数值为1×10﹣11
2 4 sp
D.图中a= ×10﹣4【答案】A
【解析】A.在饱和 Ag CrO 溶液中加入 K CrO 仍为饱和溶液,点仍在曲线上,所以在饱和
2 4 2 4
Ag CrO 溶液中加入K CrO 不能使溶液由Y点变为X点,故A错误;
2 4 2 4
B.一定温度下溶度积是常数,随温度变化,不随浓度变化,所以t℃时,Y点和Z点时Ag CrO 的
2 4
K 相等,故B正确;
sp
C.曲线上的点是沉淀溶解平衡,Ag CrO 的沉淀溶剂平衡为:Ag CrO (s) 2Ag++CrO 2﹣,Ksp
2 4 2 4 4
=c2(Ag+)•c(CrO 2﹣)=(10﹣3)2×10﹣5=10﹣11,故C正确; ⇌
4
D.依据溶度积常数计算Ksp(Ag CrO )=c2(Ag+)•c(CrO 2﹣)=1×10﹣11,Z点时c(CrO 2
2 4 4 4
﹣)=5×10﹣4mol/L,则c(Ag+)2=2×10﹣8(mol/L)2,所以a= ×10﹣4,故D正确;故选:A。
7.已知20℃,K [Mg(OH) ]=1.6×10﹣11,K [Co(OH) ]=6.4×10﹣15,Co(OH) 为玫瑰红色
sp 2 sp 2 2
难溶物,某同学进行下列实验,依据上述实验操作及现象,下列说法错误的是( )
实验操作 现象
实验一 将镁条用砂纸打磨光亮后置 有无色气体和较多白色沉淀
于饱和氯化钠溶液中,滴加 产生,溶液变红色
几滴酚酞
实验二 取出镁条,将悬浊液加热 红色加深
实验三 冷却后滴加适量CoCl 溶液 部分白色难溶物变成玫瑰红
2
色难溶物
A.镁条和水发生置换反应生成H 和Mg(OH)
2 2
B.NaCl增大了Mg(OH) (s)在20℃水中的溶解度
2
C.Mg(OH) (s) Mg2+(aq)+2OH﹣(aq)△H>0
2
D.加入适量CoCl
2
溶⇌液后,c(Mg2+):c(Co2+)=2500:1
【答案】B
【解析】A.由实验一的现象知,镁条和水反应产生了H 和难溶物Mg(OH) ,故A正确;
2 2
B.氯化钠对Mg( OH) 在水中的溶解度无影响,故B错误;
2
C.由实验二加热悬浊液,红色更深,可知Mg( OH)
2(S)
在水中的溶解过程是吸热的,故C正确;
D.在Mg(OH) 饱和溶液中滴加 CoCl 溶液后,发生反应 Mg(OH) (s)+Co2+(aq) Co
2 2 2
(OH) (s)+Mg2+(aq),则c(Mg2+):c(Co2+)=[c(Mg2+)•c2(OH﹣)]:[c(Co2+)⇌•c2
2
(OH﹣)]=Ksp[Mg(OH) ]:Ksp[Co(OH) ]=2500:1,故D正确。故选:B。
2 2
8.一定温度下,AgCl(s) Ag+(aq)+Cl﹣(aq)体系中,c(Ag+)和c(Cl﹣)的关系如图所示.
下列说法错误的是( ⇌)A.a、b、c三点对应的K 相等
sp
B.d点的溶液为AgCl的不饱和溶液
C.AgCl在c点的溶解度比b点的大
D.AgCl溶于水形成的饱和溶液中,c(Ag+)=c(Cl﹣)
【答案】C
【解析】A.温度相同,溶度积相同,则a、b、c三点对应的K 相等,故A正确;
sp
B.d点c(Ag+)•c(Cl﹣)<K ,无固体析出,为不饱和溶液,故B正确
sp
C.增大c(Cl﹣),溶解平衡逆向移动,则AgCl在c点的溶解度比b点的小,故C错误;
D.饱和溶液中存在 AgCl(s) Ag+(aq)+Cl﹣(aq),则 AgCl溶于水形成的饱和溶液中,c
(Ag+)=c(Cl﹣),故D正确⇌;故选:C。
9.已知部分铅盐的溶度积如表,从溶度积角度分析,沉淀Pb2+时的最佳沉淀剂为( )
化合物 PbSO PbCO PbS PbCrO
4 3 4
K 1.8×10﹣8 7.4×10﹣14 8.0×10﹣28 2.8×10﹣13
sp
A.硫酸盐 B.碳酸盐 C.硫化物 D.铬酸盐
【答案】C
【解析】A.当沉淀剂为硫酸盐时,若 c(SO 2﹣)=0.1mol•L﹣1,则c(Pb2+)= =
4
mol•L﹣1=1.8×10﹣7mol•L﹣1;
B.当沉淀剂为碳酸盐时,若c(CO 2﹣)=0.1mol•L﹣1,则c(Pb2+)═ = =
3
mol•L﹣1=7.4×10﹣13mol•L﹣1;C.当沉淀剂为硫化物时,若 c(S2﹣)=0.1mol•L﹣1,则c(Pb2+)= =
mol•L﹣1=8.0×10﹣27mol•L﹣1;
D.当沉淀剂为铬酸盐时,若 c(CrO 2﹣)=0.1mol•L﹣1,则 c(Pb2+)= =
4
=2.8×10﹣12mol•L﹣1;
由上述推导可知,当阴离子浓度相同时,加入硫化物后,溶液中剩余的Pb2+浓度最小,故选:C。
10.常温下,K [Fe(OH) ]=4.0×10﹣38,在pH=4的Fe(OH) 饱和溶液中,c(Fe3+)为(
sp 3 3
)
A.1.0×10﹣8mol•L﹣1 B.4.0×10﹣8mol•L﹣1
C.1.0×10﹣26mol•L﹣1 D.1.3×10﹣28mol•L﹣1
【答案】B
【解析】pH=4的Fe(OH) 饱和溶液中,c(H+)=1×10﹣4mol/L,根据K =c(H+)•c(OH﹣)
3 w
=10﹣14,则 c(OH﹣)= = mol/L=1×10﹣10mol/L,根据 K [Fe(OH) ]=c
sp 3
(Fe3+)•c3(OH﹣)=4.0×10﹣38,c(Fe3+)= = mol/L=4.0×10﹣
8mol/L,故选:B。
11.25℃时,下列4种盐的溶度积常数(K )分别是如表,结合相关数据分析,下列说法错误的是
sp
( )
Ag SO (白色) Ag S(黑色) FeS(黑色) MnS(肉色)
2 4 2
1.4×10﹣5mol3•L﹣3 6.3×10﹣50mol3•L﹣3 3.3×10﹣18mol2•L﹣2 2.5×10﹣13mol2•L﹣2
A.除去某溶液中的Ag+用Na S溶液比Na SO 溶液效果好
2 2 4
B.25℃时,MnS的溶解度大于FeS的溶解度
C.向少量FeS悬浊液中加入足量饱和MnCl 溶液,沉淀颜色会由黑色变为肉色
2
D.向Ag S(s) 2Ag+(aq)+S2﹣(aq)平衡体系中加入少量Na S固体,溶液中c(Ag+)不
2 2
变 ⇌【答案】D
【解析】A.K (Ag S)<K (Ag SO ),除去某溶液中的Ag+用Na S溶液比Na SO 溶液效果
sp 2 sp 2 4 2 2 4
好,故A正确;
B.根据表中数据,25℃时,MnS的溶解度大于FeS的溶解度,故B正确;
C.向少量FeS悬浊液中,即FeS的饱和溶液,加入足量饱和MnCl 溶液,发生沉淀的转化,沉淀
2
颜色会由黑色变为肉色,故C正确;
D.向Ag S(s) 2Ag+(aq)+S2﹣(aq)平衡体系中加入少量Na S固体,溶液中c(S2﹣)增大,
2 2
平衡逆向移动,则⇌溶液中c(Ag+)减小,故D错误;故选:D。
12.当溶液中离子浓度小于1.0×10﹣5mol•L﹣1时,可视为该离子已完全除去,通过调节溶液 pH的
方法可以除去溶液中的某些杂质离子。常温下,某 0.1mol•L﹣1的NiSO 溶液中含有杂质Al3+和
4
Fe3+,欲将这两种杂质完全除去,需调节溶液pH的范围可以是(不考虑溶液体积变化,已知:
常温时,氢氧化镍 K =1×10﹣16、氢氧化铁 K =1×10﹣38、氢氧化铝 K =1×10﹣33 )
sp sp sp
( )
A.2~3 B.3~4 C.5~6 D.6~8
【答案】C
【解析】A、pH<3时,Al3+和Fe3+都不会生成沉淀,不能除去杂质,故A错误;
B、因pH>3时,Fe3+会生成沉淀;pH>5时,Al3+才会生成沉淀,所以pH=3~4,Al3+无法除去,
故B错误;
C、因pH<6时,Ni2+不会生成沉淀;pH>5时,Fe3+和Al3+都会生成沉淀,所以可以完全除去
NiSO 溶液中杂质Al3+和Fe3+,故C正确;
4
D、pH>6时,Ni2+、Fe3+、Al3+全部会生成沉淀,故D错误;故选:C。
13.取1mL 0.1mol•L﹣1AgNO 溶液进行如下实验(实验中所用试剂浓度均为0.1mol•L﹣1),下列
3
说法不正确的是( )
A.实验 白色沉淀是难溶的AgCl
B.若按① 顺序实验,能看到白色沉淀
C.若按②①顺序实验,能看到黑色沉淀
D.由实①验③说明AgI比AgCl更难溶
②【答案】B
【解析】A、AgNO 溶液中的Ag+和过量的NaCl溶液中的Cl﹣生成AgCl的白色沉淀,离子方程式
3
为:Ag++Cl﹣=AgCl↓,所以沉淀为难溶的AgCl,故A正确;
B、一般来说,溶解度小的沉淀转化为溶解度更小的沉淀容易实现,AgI的溶解度比AgCl小,所以
AgI不易生成AgCl,所以若按 顺序实验,看不到白色沉淀,故B错误;
C、2AgCl(s)+S2﹣(aq) A②g
2
S①(s)+2Cl﹣(aq),Ag
2
S比AgCl更难溶,溶解度更小,所以若
按 顺序实验,能看到黑⇌色沉淀,故C正确;
D、①一③般来说,溶解度小的沉淀转化为溶解度更小的沉淀容易实现,实验 的白色沉淀AgCl生成
了黄色的AgI沉淀,说明AgI比AgCl更难溶,故D正确;故选:B。 ②
14.向含有MgCO 固体的浊液中滴加少许浓盐酸(忽略体积变化),下列数值变小的是( )
3
A.c(Mg2+) B.K (MgCO ) C.c(H+) D.c(CO 2﹣)
sp 3 3
【答案】D
【解析】MgCO 固体的溶液中存在溶解平衡:MgCO (s) Mg2+(aq)+CO 2﹣(aq),加入少量
3 3 3
稀盐酸可与CO 2﹣促使溶解平衡正向移动,故溶液中c(CO⇌2﹣)减小,c(Mg2+)及c(H+)增大,
3 3
K (MgCO )只与温度有关,不变,只有D正确。故选:D。
sp 3
二.解答题(共4小题)
15.向湿法炼锌的电解液中同时加入Cu和CuSO ,可生成CuCl沉淀除去Cl﹣,反应
4
原理如下:
Cu(s)+Cu2++(aq) 2Cu+(aq)△H =ak•mol﹣l
1
Cl﹣(aq)+Cu+(aq)⇌CuCl(s)△H =bkJ•mol﹣l
2
(1)反应Cu(s)+Cu⇌2+(aq)+2Cl﹣(aq)═2CuCl(s)△H=_____。
物质 CuCl CuI Cul
2
K 1.7×10﹣7 1.3×10﹣12 ﹣
sp
颜色 白色 白色 金黄色
(2)实验测得电解液 pH 对溶液中残留(Cl﹣)的影响如图所示。当 pH=7时,溶液中 c
(Cu+)=_____。
(3)兴趣小组在CuCl 溶液中加入过量KI固体,观察到有白色沉淀生成。推测该白色沉淀中一
2
定含有的物质是_____,原因是_____。(已知:常温下 CuCl、CuI、CuI 的相关信息见上
2
表。)【答案】(1)(a+2b)kJ•mol﹣1;
(2)1.7×10﹣5mol•L﹣1;
(3)CuI;Cu2+与I﹣反应生成Cu+,因K (CuI)<K (CuCl),K 更小的CuI更容易产生沉淀。
sp sp sp
【解析】(1) Cu(s)+Cu2+(aq) 2Cu+(aq)△H =a kJ•mol﹣1, Cl﹣(aq)+Cu+(aq)
1
CuCl(s)△H①=bkJ•mol﹣1,结合盖斯⇌定律可知 + ×2得;Cu(s)②+Cu2+(aq)+2Cl﹣(aq)
2
⇌2CuCl(s)△H=(a+2b)kJ•mol﹣1, ① ②
⇌故答案为:(a+2b)kJ•mol﹣1;
(2)由图可知,pH=7时,﹣lgc(Cl﹣)=2,所以c(Cl﹣)=10﹣2mol•L﹣1,根据K (CuCl)
sp
=c(Cu+)c(Cl﹣),c(Cu+)= = =1.7×10﹣5mol•L﹣1,
故答案为:1.7×10﹣5mol•L﹣1;
(3)CuCl 溶液中加入过量KI固体,观察到有白色沉淀,因K (CuI)<K (CuCl),K 更小
2 sp sp sp
的CuI更容易产生沉淀,所以Cu2+与I﹣反应生成Cu+,I﹣+Cu+=CuI↓,
故答案为:CuI;Cu2+与I﹣反应生成Cu+,因K (CuI)<K (CuCl),K 更小的CuI更容易产生
sp sp sp
沉淀。
16.工业废水中常含有一定量的Cr O 2﹣和CrO 2﹣,它们会对人类及生态系统产生很大的伤害,必
2 7 4
须进行处理。常用的处理方法有两种。
方法 1:还原沉淀法。该法的工艺流程为:CrO Cr O Cr3+ Cr
2
(OH) ↓
3
(1)流程第 步存在平衡:2CrO 2﹣+2H+ Cr O 2﹣+H O,能说明第 步反应达平衡状态的是
4 2 7 2
_____。(填序①号) ⇌ ①
A.Cr O 2﹣和CrO 2﹣的浓度相同
2 7 4
B.2v(Cr O 2﹣)=v(CrO 2﹣)
2 7 4
C.溶液的颜色不变
(2)流程第 步生成的Cr(OH) 在溶液中存在以下沉淀溶解平衡:Cr(OH) (s) Cr3+
3 3
(aq)+3OH﹣③(aq)。常温下Cr(OH) 的溶度积K =10﹣32,当c(Cr3+)降至10﹣5mo⇌l/L时
3 sp溶液的pH为_____。
方法2:电解法
该法用Fe做电极电解含Cr O 2﹣的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr
2 7
(OH) 沉淀。请用电极反应方程式解释下列原因:
3
(3)用Fe做电极的原因是_____,在阴极附近溶液pH升高的原因是_____。
【答案】(1)C;
(2)5;
(3)Fe﹣2e﹣=Fe2+;2H++2e﹣=H ↑。
2
【解析】(1)对于平衡:2CrO 2﹣(黄色)+2H+ Cr O 2﹣(橙色)+H O,
4 2 7 2
A、各组分的浓度保持不变,而Cr O 2﹣和CrO 2﹣ ⇌的浓度相同,不能判定是否达平衡状态,故A错
2 7 4
误;
B、2v(Cr O 2﹣)=v(CrO 2﹣)不知道是正反应速率还是逆反应速率,不能证明正逆速率相等,
2 7 4
所以不是平衡状态,故B错误;
C、溶液的颜色不变,即有色离子浓度不会再不变,达到了化学平衡状态,故C正确;故选:C;
(2)常温 Cr(OH) 的溶度积 K =10﹣32,当 c(Cr3+)降至 10﹣5mol/L,则 c(OH﹣)=
3 sp
=10﹣9mol/L,c(H+)=10﹣5mol/L,溶液的pH为5,故答案为:5;
(3)在电解法除铬中,活性电极铁作阳极,所以阳极反应为:Fe﹣2e﹣═Fe2+,在阴极附近溶液
pH升高的原因是水电离产生的H+放电生成H :2H++2e﹣═H ↑;同时大量产生了OH﹣,产生Cr
2 2
(OH) 沉淀,故答案为:Fe﹣2e﹣=Fe2+;2H++2e﹣=H ↑。
3 2
17.已知:常温下,K [Fe(OH) ]=1.0×10﹣38,K [Al(OH) ]=1.0×10﹣34(为计算方便已作近
sp 3 sp 3
似处理。),本题中离子完全反应的标准:c(Fe3+)<1.0×10﹣5mol•L﹣1.在含Al3+、Fe3+的浓
度都均为0.2mol•L﹣1的溶液中加入稀氨水,请回答下列问题:
(1)Al3+跟氨水反应的离子方程式是_____。
(2)NH •H O的电离方程式是_____;其电离平衡常数表达式K ═_____。
3 2 b
(3)Fe(OH) 的溶度积常数表达式K [Fe(OH) ]=_____。
3 sp 3
(4)Fe3+完全沉淀的pH为_____;此时,Al3+沉淀的百分率为_____。
【答案】(1)Al3++3NH •H O═Al(OH) ↓+3NH +;
3 2 3 4
(2)NH •H O NH ++OH﹣; ;
3 2 4
(3)c3(OH﹣) ⇌ ×c(Fe3+);(3)3;50%。
【解析】(1)铝离子与氨水反应生成氢氧化铝沉淀和铵根离子,氨水为弱电解质,写化学式,离
子方程式为 Al3++3NH •H O═Al(OH) ↓+3NH +,故答案为:Al3++3NH •H O═Al(OH)
3 2 3 4 3 2
↓+3NH +;
3 4
(2)氨水为弱电解质,水溶液中部分电离,电离方程式为NH •H O NH ++OH﹣;电离平衡常数
3 2 4
⇌
表达式K = ,
b
故答案为:NH •H O NH ++OH﹣; ;
3 2 4
(3)根据 Fe(OH) ⇌ 的电离方程式,其溶度积常数表达式 K [Fe(OH) ]=c3(OH﹣)×c
3 sp 3
(Fe3+),
故答案为:c3(OH﹣)×c(Fe3+);
(4)根据 K [Fe(OH) ]及离子完全反应时 c(Fe3+)<1.0×10﹣5mol•L﹣1,c3(OH﹣)=
sp 3
=1.0×10﹣33,则 c(OH﹣)=1.0×10﹣11 mol•L﹣1,pH=﹣lg =3;根据
K [Al(OH) ]=1.0×10﹣34,此时溶液 c(Al3+)=0.1mol/L,Al3+沉淀的百分率=
sp 3
×100%=50%,
故答案为:3;50%。
18.工业废水中常含有一定量的Cr O 2﹣和CrO 2﹣,它们会对人类及生态系统产生很大危害,必须
2 7 4
进行处理。常用的处理方法有以下两种:
方法1:还原沉淀法。
该法的工艺流程为:CrO 2﹣ Cr O 2﹣ Cr3+ Cr(OH) ↓。
4 2 7 3
其中第 步存在平衡2CrO 2﹣(黄色)+2H+ Cr O 2﹣(橙色)+H O。
4 2 7 2
(1)若①平衡体系的pH=2,该溶液显_____色⇌。
(2)能说明第 步反应达平衡状态的是_____(填序号)。
A.Cr
2
O
7
2﹣和C①rO
4
2﹣的浓度相同
B.2v(Cr O 2﹣)=v(CrO 2﹣)
2 7 4
C.溶液的颜色不变(3)第 步中,还原1mol Cr O 2﹣离子,需要_____mol的FeSO •7H O。
2 7 4 2
(4)第②步生成的Cr(OH)
3
在溶液中存在以下沉淀溶解平衡:Cr(OH)
3
(s) Cr3+(aq)
+3OH﹣(③aq),常温下,Cr(OH) 的溶度积 K =c(Cr3+)•c3(OH﹣)=10⇌﹣32,要使c
3 sp
(Cr3+)降至10﹣5mol/L,溶液的pH应调至_____。
方法2:电解法。
该法用Fe做电极电解含Cr O 2﹣的酸性废水,随着电解的进行,在阴极附近溶液pH升高,产生
2 7
Cr(OH) 沉淀。
3
(5)用Fe做电极的原因为_____(用电极反应式解释)。
(6)在阴极附近溶液pH升高,溶液中同时生成的沉淀还有_____。
【答案】(1)橙;
(2)C;
(3)6;
(4)5;
(5)Fe﹣2e﹣=Fe2+,提供还原剂Fe2+;
(6)Fe(OH) 。
3
【解析】(1)溶液显酸性,c(H+)较大,上述平衡右移,该溶液显橙色,
故答案为:橙;
(2)A.Cr O 2﹣和CrO 2﹣的浓度相同时,反应不一定达到平衡状态,平衡时浓度不变,故A错误;
2 7 4
B.2v(Cr O 2﹣)=v(CrO 2﹣),没有标出正逆反应速率,无法判定反应是否达到平衡状态,故
2 7 4
B错误;
C.平衡时各物质的浓度不再改变,即溶液的颜色不再改变,可以判断反应达到平衡状态,故C正
确;
故答案为:C;
(3)由元素的化合价变化可知,还原1molCr O 2﹣离子,得到Cr3+,得到电子为2×(6﹣3)=
2 7
6mol,Fe2+被氧化为Fe3+,需要FeSO •7H O的物质的量为 =6mol,
4 2
故答案为:6;
(4)当c(Cr3+)=10﹣5mol/L时,溶液的c(OH﹣)= =10﹣9mol/L,c(H+)=
=10﹣5mol/L,pH=5,即要使c(Cr3+)降至10﹣5mol/L,溶液的pH应调至5,
故答案为:5;
(5)用Fe做阳极,发生氧化反应,失电子:Fe﹣2e﹣=Fe2+,产生的亚铁离子做还原剂,故答案为:Fe﹣2e﹣=Fe2+,提供还原剂Fe2+;
(6)溶液中氢离子在阴极得电子被还原为氢气,阴极极反应为:2H++2e﹣=H ↑,溶液酸性减弱,
2
溶液pH升高,亚铁离子被氧化为铁离子,酸性减弱,铁离子产生沉淀Fe(OH) ,
3
故答案为:Fe(OH) 。
3